疏肝健脾方药对非酒精性脂肪性肝病大鼠 Kup ffer细胞 SREBP-1c信号通路相关基因及蛋白表达的影响
2014-04-11杨钦河张玉佩徐拥建刘益臻杨雪松
韩 莉, 杨钦河, 张玉佩, 徐拥建, 刘益臻, 杨雪松, 金 玲
(1.暨南大学附属第一医院, 广东 广州 510632; 2.暨南大学医学院中医系, 广东 广州 510632; 3.暨南大学医学院组织学与胚胎学教研室, 广东 广州 510632)
[药 理]
疏肝健脾方药对非酒精性脂肪性肝病大鼠 Kup ffer细胞 SREBP-1c信号通路相关基因及蛋白表达的影响
韩 莉1, 杨钦河2*, 张玉佩2, 徐拥建2, 刘益臻2, 杨雪松3, 金 玲1
(1.暨南大学附属第一医院, 广东 广州 510632; 2.暨南大学医学院中医系, 广东 广州 510632; 3.暨南大学医学院组织学与胚胎学教研室, 广东 广州 510632)
目的 观 察 疏 肝 健 脾 方 药 对 非 酒 精 性 脂 肪 性 肝 病 ( NAFLD) 大 鼠 Kupffer细 胞 固 醇 调 节 元 件 结 合 蛋 白-1c(SREBP-1c) 信号通路相关基因及蛋白表达的影响及可能的机制。 方法 采用高脂饲料喂养复制大鼠 NAFLD模型,各药物干预组灌饲相应的疏肝健脾方药,8周后检测血液常规生化指标,观察肝组织病理形态改变;采用离体循环灌注Ⅳ型胶原酶法提取肝 脏 Kupffer细胞, Q-PCR及 Western blot法检 测 Kupffer细胞 SREBP-1c、 硬 脂酰辅酶 A去饱合酶-1 ( SCD-1) mRNA及蛋白 表 达 水 平。 结 果 模 型 组 大 鼠 肝 脏 脂 肪 蓄 积; 血 脂 及 Kupffer细 胞 SREBP-1c、 SCD-1 mRNA及蛋白表达水平较正常组均显著升高 ( P<0.01 ) ; 各药物干预组 Kupffer细胞 SREBP-1c、 SCD-1 mRNA及蛋白表达水平均有不同程度的下调,同时血脂及病理学改变也较模型组有不同程度的改善, 以疏肝组作用最为显著 (P<0.01) 。 结论 疏肝健脾方药可能是通过抑制 Kup ffer细胞 SREBP-1c/SCD-1 信号通路激活, 下调血清总胆固醇、 甘油三酯合成, 减少肝脏脂质沉积, 发挥抗 NAFLD作用。 可推测 SREBP-1c、 SCD-1 mRNA及蛋白可能是疏肝健脾方药抗NAFLD的有效作用靶点。
疏肝健脾方药; 非酒精性脂肪性肝病; 固醇调节元件结合蛋白-1c; 硬脂酰辅酶 A去饱和酶-1; Kup ffer细胞;大鼠
非 酒 精 性 脂 肪 性 肝 病 ( nonalcoholic fatty liver disease, NAFLD) 是一种与遗传-环境-代谢应激相关且无过量饮酒史、肝细胞脂肪变性和脂质贮积为特征的临床病理综合征,包括单纯性脂肪肝、非酒精 性 脂 肪 性 肝 炎 ( nonalcoholic steatohepatitis,NASH) 及 NASH相关肝纤维化、 肝硬化。 其发病非单一因素引起,可能与脂质代谢障碍、胰岛素抵抗、线粒体功能障碍、2型糖尿病、高血压和其他一些代谢症候群等密切相关[1-3]。 固醇调节 元件结合蛋白-1c( sterol regulatory element binding proteins-1c, SREBP-1c) 和 硬 脂 酰 辅 酶 A 去 饱 和 酶-1(stearyl-CoA desaturase-1, SCD-1 ) 是 参 与脂 肪 酸合成代谢过程的重要调控因子。 研究表明, NAFLD时肝脏 SREBP-1c可激活下游多种参与脂肪酸和甘油三酯合成酶的转录, 包括 SCD-1、 脂肪酸合成酶、乙酰辅酶A羧化酶等,导致脂肪酸合成增加,造成肝脏脂质蓄 积[4]。 本 课 题组前期研 究 发 现,疏肝健脾方药可显著改善 NAFLD大鼠肝脏脂质代谢紊乱, 减轻肝脏脂肪变性, 防治 NAFLD作用疗效确切[5-7]。 本 实 验 观 察 疏 肝 健 脾 方 药 对 NAFLD大鼠肝脏 Kupffer细胞 SREBP-1c/SCD-1 信号通路相关基因和蛋白表达的影响, 探讨其抗 NAFLD的干预作用机制。
1 材料
1.1 动物 雄性 SD大鼠, SPF级, 6 周龄, 体质量 (200 ±20) g, 广州中医药大学实验动物管理中心提供,动物生产许可证号: SCXK (粤) 2008-0020, 合格批号 0107792。
1.2 主要仪器与试剂 AU600 全自动生化分析仪(日本 Olympus公司) ; ELITE流式细 胞仪 ( 美国BECKMAN-COULTER公司); KDS200 双通道注射泵 (美国 KD Scientific公司); CFX Manager实时荧光定量 PCR仪 (美国 BIO-RAD公司)。 Trizol裂解液 (批号 D9108A)、 Quant cDNA第一链合成试剂盒 ( 批 号 DRR047A)、 SYBR Green 荧光 定 量PCR试剂盒 (批号 DRR820A)均购自日本 Takara公 司; SREBP-1c Antibody( 批 号 GR111569-1 )、SCD-1 Antibody( 批 号 GR91951-1 ) 均 购 自 美 国Abcam公司; 兔抗大鼠 Anti-Lysozyme(批号 Y-Bo-07J26C)购自武汉博士德生物技术有限公司; Ⅳ型胶原酶 ( 批号 C8160-100) 购自美国 GBICO公司; Nycodenz细胞分离液 (批号 1002424-1) 购自瑞典 Axis-shield 公司。
1.3 实验药材 方药组成及饮片剂量均参照 《方剂学》 教 材[8]。 疏 肝 方 药 ( 柴 胡 疏 肝 散: 柴 胡6 g, 川芎5 g, 枳壳 5 g, 陈皮 6 g, 白芍5 g, 香附5 g,炙甘草 3 g)、健脾方药 (参苓白术散:人参15 g, 白术 15 g, 茯苓 15 g,薏苡仁9 g, 砂仁 6 g,山药 15 g, 桔梗 6 g, 白扁豆 12 g, 莲子 9 g, 炙甘草 9 g)、 合方 (柴胡疏肝散与参苓白术散合用方)中药材均为深圳华润三九医药股份有限公司生产的免煎单味中药配方颗粒,购自暨南大学附属第一医院中药房。免煎中药配方颗粒按包装说明换算成实验所需的饮片剂量,溶于水制成水溶剂。其中疏肝方 含 生 药 量 0.96 g/mL; 健 脾 方 含 生 药 量3.00 g/mL; 合方含生药量 3.96 g/mL。
2 方法
2.1 动物分组及处理 将大鼠随机分为正常组、 模型组、 疏肝组、健脾组、合方组, 每组 15 只。NAFLD大鼠模型建立在本课题组以往的造模方法[9]的基础上加以改进, 建立 NAFLD大鼠模型。 除正常组大鼠给予基础饲料喂养外,其余各组大鼠均以高脂饲料 (基础饲料 88%,猪油10%, 胆固醇 1.5%,3 号 胆 盐 0.5%) 喂 养 造 模。 同 时 各 组 按10 mL/(kg体质量)给予相应的药物或蒸馏水灌胃。本课题组前期[10]已探讨不同疏肝健脾方药剂量对NAFLD大鼠的干预作用, 表明人临床等效剂量的3倍用量在改善 NAFLD大鼠肝功能,降低血脂、肝脂,减轻肝脏脂肪变性疗效更为显著。因此本实验采用成人临床等效剂量的3倍用量,疏肝组为9.6 g/(kg·d),健脾组为 30 g/(kg·d),合方组为39.6 g/(kg·d)。 每日上午 8 ∶00 灌胃 1 次,1周称体质量1次,根据体质量调整给药剂量,连续8 周。 各组动物分笼饲养于 22 ~26 ℃, 明暗各12 h的动物实验室内, 自由饮水进食。 实验期间观察大鼠毛色、体态、食欲、行为状态、大小便及对外界刺激的反应。
2.2 标本采集 第 8 周后, 禁食 12 h, 每组 8 ~9只大鼠 (注:因灌胃不当,正常组、模型组、健脾组及合方组大鼠各死亡1只)以 3%戊巴比妥钠按 0.1 mL/(kg体质量)腹腔麻醉, 腹主动脉采血,距离肝边缘 0.5 cm处取相同部位肝右叶组织若干,-80 ℃低温冰箱保存备用。 其余 6 只用以分离Kupffer细胞。
2.3 肝组织观察 距离肝边缘 0.5 cm处取相同部位肝右叶小块约 1.5 cm×1 cm×0.5 cm, 冰冻切片作油红O染色观察肝细胞内脂滴的分布情况。另若干小块以 10%中性甲醛溶液固定, 常规石蜡包埋, 作4μm连续切片行 HE染色, 光镜下观察大鼠肝脏脂肪变性情况。需要注意的是脂滴极易降解,因此取肝组织后应当日即行油红O染色。
2.4 血脂检测 采用全自动生化分析仪检测血清血清总胆固醇 (TC)、 甘油三酯 (TG)、 高密度脂蛋白 胆 固 醇 ( HDL-C)、 低 密 度 脂 蛋 白 胆 固 醇(LDL-C)水平。
2.5 Kupffer细胞分离及鉴定 采用离体循环灌注Ⅳ 型 胶 原 酶 法 提 取 Kupffer细 胞, 流 式 细 胞 术(flow cytometry, FCM) 鉴定细胞纯度, 具体分离与鉴定 方 法 详见本课 题 组 已 发 表 论 文[11], 不 再赘述。
2.6 Q-PCR法检测 Kupffer细胞 SREBP-1c、 SCD-1 mRNA表达水平 采用 Trizol裂解肝细胞, 提取总RNA,分光光度计检测总 RNA水平,然后逆转录为 cDNA。 引物设计依据 Genebank 采用 Primer 5.0软件以 GAPDH基因序列为内参照物, 由上海捷瑞生物工程有限公司合成, 引物序列见表 1。 PCR扩增采用25 μL反应体系,反应条件为90 ℃预变性,持 续 30 min; 95 ℃ 变 性, 持 续 5 s; GAPDH、 SREBP-1c、 SCD-1 均为 58 ℃, 退火 20 s; 60 ℃延伸, 持续 45 s, 39 个循环; 溶解曲线分析, 65 ~95 ℃, 持续 5 ~10 s。 反应完毕, 用 Opticon Monitor 3.1 软件处理结果, 设定正常组基因表达水平为 1。 公式 2-ΔΔCt=实验组目的基因表达相对于正常组 的 变 化 倍 数。 ΔΔCt=实 验 组 ( Ct目的基因-Ct内参基因) -空白组 (Ct目的基因-Ct内参其因)。

表1 引物序列Tab.1 Primer sequences
2.7 Western blot法检测 Kupffer细 胞 SREBP-1c、SCD-1 蛋白表达水平 每 5 ×106个细胞加入 1 mL RIPA裂 解 液 (含 PMSF) , 吹 打 混 匀 后,4 ℃,14 000 r/min,离心 8 min,取 上 清 BCA法 测 定 总蛋白浓度, 调整样品上样量终质量浓度为 50~80 μg/μL。 注意为避免蛋白降解, 全程都应在冰台上操作。 经 SDS-PAGE电泳分离蛋白, 然后转移至 PVDF膜上, 加 5%脱脂奶粉封闭液, 室温下平摇1 h; 洗膜, 加一抗稀释液4℃过夜孵育; 洗膜, 加二抗稀释液室温孵育1 h, 洗膜后, 进行化学发光反应。 用 Quantity One软件分析内参与目的蛋白的光密度值,统计分析。
2.8 统 计 学 处 理 计 量 资 料 以 均 数 ±标 准 差() 表 示, 采 用 SPSS 19.0 进 行 统 计 学 处 理,组间均数比较采用单因素方差分析,方差齐时用SNK ( Student-Newman-Keuls, 即 q检 验 ) 法 进 行组间两两比较, 方差不齐时用 Tamhane’s T2 检验,检验水准 P<0.05 表示差异具有统计学意义。
3 结果
3.1 动物一般状况 正常组大鼠毛色光泽,饮食、排泄物较正常,性情温顺,对外界刺激反应灵敏。模型组大鼠体毛略黄而干枯,体型肥胖,大便油腻感质略稀,对外界刺激反应迟钝,容易激惹。各用药组大鼠一般情况介于正常组和模型组大鼠之间。
3.2 肝组织病理学观察
3.2.1 油红 O染色结果 正常组大鼠肝细胞核呈淡蓝染色,少许肝细胞胞浆内可见散在的红染脂滴。模型组大鼠肝细胞肿胀,细胞核呈深蓝染色,细胞浆可见大量红色脂滴,少许肝细胞脂滴融合成大脂滴。各药物干预组大鼠肝细胞脂滴红染情况与模型组相比明显缩小和减少,其中以疏肝组大鼠肝细胞含脂滴量与正常组最为接近。 见图1。

图 1 各组大鼠肝组织病理变化 (油红 O染色 ×200)Fig.1 Histopathological changes of liver tissuesw ith oil red O staining in each group( ×200)
3.2.2 HE染色结果 正常组大鼠肝小叶轮廓清晰,肝窦结构正常,肝索以中央静脉为轴心呈放射状排列,肝细胞细胞质丰富呈红染,无空泡。模型组大鼠肝小叶轮廓欠清晰,肝索结构紊乱,肝细胞肿胀,胞内可见大小不等的空泡。各药物干预组大鼠肝组织病理改变较模型组有不同程度的改善,以疏肝组大鼠肝组织结构与正常组最为相似。见图2。

图 2 各组大鼠肝组织病理变化 (HE染色 ×200)Fig.2 H istopathological changes of liver tissues w ith HE staining in each group( ×200)
3.3 各组大鼠血脂比较 与正常组比较, 模型组大鼠血清 TC、TG、LDL-C水平显著升高 (P<0.01), HDL-C水平显著降低 (P<0.01);与模型组比较, 各药物干预组大鼠血清 TC、 LDL-C水平显著降低 (P<0.05, P<0.01), 疏肝组大鼠血清TG水平显著降低 (P<0.01),HDL-C水平显著升高 (P<0.01);各药物干预组间比较, 疏肝组大鼠血清 HDL-C水 平 明 显 高 于 健 脾 组 及 合 方 组(P<0.01), LDL-C水平明显低于健脾组及合方组(P<0.05, P<0.01)。 见表 2。
表2 各组大鼠血脂比较 ()Tab.2 Com parison of serum lipid in each group()

表2 各组大鼠血脂比较 ()Tab.2 Com parison of serum lipid in each group()
注: 与正常组比较,▲▲P<0.01; 与模型组比较,★P<0.05,★★P<0.01; 与健脾组比较,■P<0.05,■■P<0.01; 与合方组比较,●●P<0.01
组 别 动 物数 /只 TC/( mmol·L-1) TG/( mmol·L-1) HDL-C/( mmol·L-1) LDL-C/( mmol·L-1)正常组8 1.29 ±0.23 0.32 ±0.02 1.31 ±0.12 0.35 ±0.11模型组 8 3.84 ±1.06▲▲ 0.43 ±0.05▲▲ 0.85 ±0.11▲▲ 2.98 ±0.81▲▲疏肝组 9 2.26 ±0.60★ 0.30 ±0.06★★ 1.31 ±0.21★★■■●● 1.55 ±0.37★■●●健脾组 8 1.55 ±0.39★★ 0.36 ±0.09 1.01 ±0.15 0.91 ±0.40★★合方组 8 1.56 ±0.71★★ 0.35 ±0.06 0.96 ±0.21 0.93 ±0.21★★
3.4 Kupffer细胞分离及鉴定
3.4.1 细胞活性及产量 实验结果表明, 采用离体灌注Ⅳ型胶原酶、差速离心、密度梯度离心及选择性贴壁法成功分离大鼠 Kupffer细胞,其中每只大鼠肝脏可分离 Kupffer细胞 2.0 ×107~3.0 ×107个。 Typan blue染色鉴定两 细胞活 性均在 95% 以上。 见图 3, 图 4。

图 3 Kup ffer细胞分离Fig.3 Separation of Kup ffer cells

图 4 贴壁培养 3 h纯化后的 Kup ffer细胞 ( ×100)Fig.4 Kupffer cellswere purified by adherent culture for 3 h
3.4.2 FCM鉴定 Kupffer细胞纯度 M1 为低浓度标记峰标志, M1平行线起点左侧表示阴性细胞,起点右侧移位峰表示阳性细胞,起点左侧的高峰为IgG阴性对照峰。 Lysozyme抗体检测 Kupffer细胞,共检测细胞 1 ×104个, 其中表达 Lysozyme的细胞数是 9 121 个, 比例为 91.21%, 即 Kupffer细胞纯度为91.21%。 见图 5。

图 5 FCM 鉴定 Kup ffer细胞纯度Fig.5 The purity of Kupffer cellswas identificated by FCM
3.5 Kupffer细胞 SREBP-1c、 SCD-1 mRNA表达与正常组比较, 模型组 大鼠 Kupffer细胞 SREBP-1c、 SCD-1 mRNA表达水平显著升高 (P<0.01);与模型 组 比 较, 各药物干 预 组 大鼠 Kupffer细 胞SREBP-1c mRNA表达水平显著降低 ( P<0.01,P<0.05);各药物干预组组间比较,疏肝组大鼠Kupffer细胞 SREBP-1c mRNA表达水平明显低于合方组 (P<0.05), SCD-1 mRNA表达水平明显低于健脾组 (P<0.05)。提示 NAFLD大鼠 Kupffer细胞 SREBP-1c通路相关基因呈高表达,疏肝健脾方药可显著降低 NAFLD大鼠 Kupffer细胞 SREBP-1c通路相关基因表达水平,以疏肝组作用最为显著。见表3, 表4。
表 3 Kup ffer细 胞 SREBP-1cm RNA表 达 水平 (, n=6)Tab.3 Exp ression levels of SREBP-1cmRNA in Kupffer cells(, n=6)

表 3 Kup ffer细 胞 SREBP-1cm RNA表 达 水平 (, n=6)Tab.3 Exp ression levels of SREBP-1cmRNA in Kupffer cells(, n=6)
注: 与正常组比较,▲▲P<0.01; 与模型组比较,★P<0.05,★★P<0.01; 与合方组比较,●P<0.05①标 准差 计算公 式为 : S= ()1/2, 如 0.86= ( 0.692+0.542 )1/2, 下 同。②标准差计算公式为: 2-ΔΔCT+s和 2-ΔΔCT-s, S 为 ΔΔCT的标准偏差, 如 2-(0+0.86)=0.55
2-ΔΔCT SREBP-1c正常组 27.17 ±0.69 25.40 ±0.54 1.77 ±0.86① 0 ±0.86 1(0.55-1.82)组别 SREBP-1c Average.CT GAPDH Average.CT ΔCT SREBP-1c-GAPDH ΔΔCT ΔCT-ΔCT,Blank②模型组 24.51 ±0.57 25.67 ±0.59 -1.16 ±0.82 -2.93 ±0.82 7.62(4.32-13.45) ▲▲疏肝组 26.82 ±0.35 25.44 ±0.61 1.37 ±0.70 -0.40 ±0.70 1.32(0.81-2.14) ★★●健脾组 25.62 ±0.84 25.56 ±0.41 0.06 ±0.93 -1.71 ±0.93 3.27(1.72-6.23) ★合方组 25.08 ±0.52 25.47 ±0.26 -0.39 ±0.58 -2.16 ±0.58 4.47(2.99-6.68) ★
3.6 Kupffer细胞 SREBP-1c、 SCD-1 蛋白表达 与正常组比较, 模型组大鼠 Kupffer细胞 SREBP-1c、SCD-1 蛋白表达水平显著升高 (P<0.01); 与模型组比较,各药物干预组大鼠 Kupffer细胞 SREBP-1c、 SCD-1 蛋 白 表 达 显 著 降 低 P<0.01, P<0.05)。 各用药组组间比较无统计学意义 (P>0.05)。 见表 5, 图 6。
表 4 Kupffer细胞 SCD-1mRNA表达水平 (, n=6)Tab.4 Expression levels of SCD-1 m RNA in Kup ffer cells(, n=6)

表 4 Kupffer细胞 SCD-1mRNA表达水平 (, n=6)Tab.4 Expression levels of SCD-1 m RNA in Kup ffer cells(, n=6)
注: 与正常组比较,▲▲P<0.01; 与模型组比较,★P<0.05,★★P<0.01; 与健脾组比较,■P<0.05①标 准差 计算公 式为 : S= ()1/2, 如 1.07= ( 0.922+0.542 )1/2, 下 同。②标准差计算公式为: 2-ΔΔCT+s和 2-ΔΔCT-s, S 为 ΔΔCT的标准偏差, 如 2-(0+1.07)=0.48
2-ΔΔCT SCD-1 Rel.to control正常组 31.26 ±0.92 25.40 ±0.54 5.86 ±1.07① 0 ±1.07 1(0.48-2.10)组别 SCD-1 Average.CT GAPDH Average.CT ΔCT SCD-1-GAPDH ΔΔCT ΔCT-ΔCT,Blank②模型组 28.94 ±1.32 25.67 ±0.59 3.27 ±1.45 -2.59 ±1.45 6.02(2.20-16.45) ▲▲疏肝组 30.63 ±0.75 25.44 ±0.61 5.19 ±0.97 -0.67 ±0.97 1.59(0.81-3.12) ★★■健脾组 29.18 ±0.61 25.56 ±0.41 3.62 ±0.73 -2.24 ±0.73 4.72(2.85-7.84)合方组 29.76 ±0.86 25.47 ±0.26 4.29 ±0.90 -1.57 ±0.90 2.97(1.59-5.54) ★
表 5 Kup ffer细 胞 SREBP-1c信号通 路 相 关 蛋 白 表 达 水 平(, n=6)Tab.5 Expression levels of proteins involved in SREBP-1c signal pathway in Kup ffer cells(, n=6)

表 5 Kup ffer细 胞 SREBP-1c信号通 路 相 关 蛋 白 表 达 水 平(, n=6)Tab.5 Expression levels of proteins involved in SREBP-1c signal pathway in Kup ffer cells(, n=6)
注: 与正常组比较,*P<0.01; 与模型组比较,▲P<0.01,▲▲P<0.05
组 别 ( SREBP-1c/GAPDH) ( SCD-1/GAPDH)正常组0.41 ±0.12 0.73 ±0.18模型组 0.89 ±0.08* 2.04 ±0.11*疏肝组 0.66 ±0.07▲ 0.87 ±0.09▲健脾组 0.69 ±0.03▲ 1.44 ±0.22▲▲合方组 0.67 ±0.06▲ 0.80 ±0.06▲
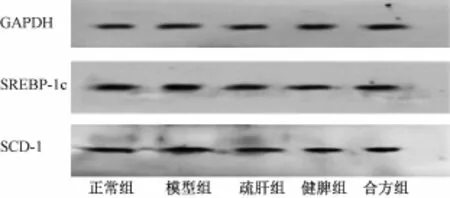
图 6 Kup ffer细胞 SREBP-1c、 SCD-1 蛋白灰度值比较Fig.6 Gray value of SREBP-1c and SCD-1 proteins in Kupffer cells
4 讨论
祖国医学无 “非酒精性脂肪肝” 病名,根据NAFLD的临床表现, 大多把其归属于癥瘕、 积聚、胁痛、痰证、瘀证等病证范畴。中医学认为本病的发生多因嗜食肥甘厚味,过度肥胖,或恣饮酒浆,或情志失调,或感受湿热疫毒,或久病年老体虚等引起,与肝、脾、肾三脏功能失调密切相关。现代医学对其发病机制的研究仍停留在假说层面,目前比较为人们所接受的假说是 1998 年 Day等[12]提出的 “二次打击学说”。 “初次打击” 主要是胰岛素抵抗和脂质代谢紊乱所致的肝细胞脂肪变性,引起肝脏脂质贮积,形成单纯性脂肪肝; “二次打击”主要为氧化应激、脂质过氧化、炎症性细胞因子释放等因素引起了脂肪性肝炎,进而发生炎症—坏死的恶性循环,最终形成脂肪性肝纤维化或肝硬化等严重的病理变化。
固醇调节元件结合蛋白 ( sterol regulatory element binding proteins, SREBPs) 属于螺旋-环-螺旋-亮氨酸锌指转录因子家族,在脂肪酸、甘油三酯及胆固醇合成代谢中具有中心调控地位[13]。 SREBP-1c是目前在哺乳动物体内发现的 SREBPs的 3 个亚型之一,在体内大多数组织中均有表达,以肝脏中表达较为丰富,主要负责调节脂肪酸和甘油三酯的代谢[14]。 在 NAFLD发生发展过程中, 通过调控转录因子 SREBPs, 进而调节肝脏脂质和葡萄糖平衡可能是 NAFLD的治疗关键[15],抑制 SREBP-1c可以逆转肝脏脂肪变性[16]。SCD-1 是一类催化饱和脂肪酸形成单不饱和脂肪酸的内质网跨膜蛋白亚型之一,与酶系催化饱和脂肪酸生成的棕榈油酰辅酶A和油酰辅酶A是体内各种脂质合成的底物,包括 TG、 胆固醇酯、 磷脂等。SCD-1 作为调节脂肪酸代谢的重要限速酶[17], 在脂肪酸合成代谢中起着重要的调节作用[18]。 研究 表明[19-20], NAFLD患者普遍存在肝脏 SCD-1 的激活, 肝脏脂肪百分比与 SCD-1 的激活呈正相关, 血清脂肪酸的水平亦高度 依 赖 于 SCD-1 的 激 活。 此 外 SCD-1 作 为SREBP-1c调控的下 游基因, 当 SREBP-1c转录因子与 SCD-1 的启动子结合后, 可上调 SCD-1 基因转录,最终导致脂质合成增加,肝脏内脂质蓄积,促进 NAFLD的发展[4,21]。 Kupffer细胞, 又称肝巨噬细胞, 约占体内巨噬细胞的 80% ~90%, 是肝脏防御系统主要成员,其最主要的生理功能是迅速吞噬和清除对人体有害的外源性颗粒及免疫活性物质。 Kupffer细胞与肝脏胆固醇和 TG的关系密切。NAFLD时, Kupffer细胞不仅影响着肝实质细胞脂质代谢的进行, 而且 Kupffer细胞本身也存在着脂质代谢障碍[22-23]。 Roth 等[23]给 予 SD大 鼠 高 脂 肪喂养后在电镜下观察到 Kupffer细胞内含有大量脂肪空泡。研究表明,当巨噬细胞脂肪酸增加,其中SCD的表达量会显著增加,抑制 SCD表达后, 巨噬细胞中脂肪酸水平下降[24], 而抑制肝脏 Kupffer细胞 活 性 可 减 弱 SREBP-1c的 激 活 及 其靶 基 因SCD-1蛋 白 表达 水 平, 导 致 肝 脏 脂 质 沉 积 形 成NAFLD[25]。 可 见 肝 脏 Kupffer细 胞 在 SREBP-1c/ SCD-1 信号通路激活引起脂质沉积过程中起着重要的作用。 目前对于 SREBP-1c/SCD-1 等脂质代谢相关信号通路的研究多着重于肝脏实质细胞中,对Kupffer细胞在该脂质代谢通路中的作用机制研究相对较少。 鉴于此, 本实 验从 Kupffer细胞入手,以 SREBP-1c/SCD-1 信号通路为切入点, 深入开展对 NAFLD脂质代谢紊乱机制及其防治研究。
本实验中血脂以及病理学观察结果表明,高脂饲料喂养 8 周建立大鼠 NAFLD模型存在明显的脂质代 谢 紊 乱, 可 能 与 模 型 组 大 鼠 Kupffer细 胞SREBP-1c、 SCD-1 mRNA及蛋白高度表达有关。 各药物干预组 Kupffer细胞 SREBP-1c、 SCD-1 mRNA及蛋白表达水平均有不同程度的下调,同时血脂及病理组织学改变也较模型组有不同程度地改善,证实疏肝健脾方药可能是通过抑制 NAFLD大鼠Kupffer细胞 SREBP-1c信号通路激活, 使 TC、TG合成减少, 发挥抗 NAFLD的药理作用。 SREBP-1c、 SCD-1 mRNA及蛋白可能是疏肝健脾方药抗NAFLD的有效作用靶点。
本课题组 前 期 研 究 表 明[6-7,26-28], 肝 郁 脾 虚 的病机贯穿于 NAFLD发病过程的始终, 确立以疏肝健脾法作为 NAFLD的基本治法。 肝郁脾虚证也是2010 年 12 月中华中医药学会脾胃病分会在制定的《非酒精性脂肪性肝病中医诊疗共识意见》[29]中提出的 NAFLD的四个基本证候之一。 从中医学证候学来看, 随着病程的进展, NAFLD可能或侧重于肝郁、或脾虚、或肝郁脾虚并重等病机的特点。因此本实验采用疏肝方、健脾方、合方分别干预高脂饮食诱导的 NAFLD大鼠, 旨在从中医病机角度揭示 8 周高脂饮食诱导的 NAFLD大鼠可能存在的病机特点。在本实验中观察到疏肝方药在改善血脂及病理组织学改变,下调 Kupffer细胞 SREBP-1c和SCD-1 mRNA水平明显优于健脾方和合方。 根据以方测证法,推测肝郁脾虚且以偏重肝郁可能是此阶段 NAFLD的中医基本病机之一。 随着 NAFLD的进一步发展,其病机又会发生怎样的变化,值得进一步研究。 此外, 疏肝健脾方药防治 NAFLD可能是多途径,多靶点,多环节不同药理作用的结果,详细机制仍有必要继续作进一步的探讨。
[ 1 ] Cohen JC, Horton JD, Hobbs H H.Human fatty liver disease: old questions and new insights[ J] .Science, 2011 , 332(6037): 1519-1523.
[ 2 ] Larter C Z, Chitturi S, Heydet D, etal.A fresh look at NASH pathogenesis.Part1: themetabolic movers[ J] .JGastroenterol Hepatol, 2010, 25(4) : 672-690.
[ 3 ] Polyzos S A, Kountouras J, Zavos C, et al.The role of adiponectin in the pathogenesis and treatmentof non-alcoholic fatty liver disease[ J] .Diabetes Obes Metab, 2010, 12 ( 5 ):365-383.
[ 4 ] Zhang C, Chen X, Zhu R M, et al.Endoplasmic reticulum stress is involved in hepatic SREBP-1c activation and lipid accumulation in fructose-fed mice[ J].Toxicol Lett, 2012, 212(3): 229-240.
[5] 杨钦河,顾常霖,陈同炎,等.疏肝健脾方药对非酒精性脂肪性肝病大鼠肝组织脂肪酸合成酶 mRNA及蛋白表达的影响[J].中华中医药杂志, 2011, 26(4): 843-846.
[6] 杨钦河,周迎春,郭桃美,等.不同治法方药对脂肪肝大鼠血脂作用的比 较研究 [J].新中医, 2004, 36 (5):74-75.
[ 7] 李玉权, 杨钦河.疏肝健脾法治疗非酒精性脂肪肝 35 例[J].中医杂志, 2007, 48(9): 824-825.
[ 8 ] 段富津.方剂学 [M].上海: 上海科学技术出版社, 1995:114-179.
[ 9 ] Yang Q H, Hu SP, Zhang Y P, et al.Effect of berberine on expressions of uncoupling protein-2 mRNA and protein of hepatic tissue in non-alcoholic fatty liver disease in rats[ J] .Chin J Integr Med, 2011, 17(3) : 205-211.
[10] 王文晶, 杨钦河, 冯高飞, 等.疏肝健脾方药对 NASH大鼠心脏舒张功能及炎症因子的影响[J].世界华人消化杂志, 2011, 19(25): 2615-2622.
[11] 冯高飞, 杨钦河, 王文晶, 等.NASH大鼠肝细胞和库普弗细胞同时分离及鉴 定[ J].广东医学, 2012, 33 (1 ):30-34.
[12 ] Day C P, James O F.Steatohepatitis: a tale of two“ hits”?[J] .Gastroenterology, 1998, 114(4) : 842-845.
[13 ] Goldstein JL, Debose-Boyd R A, Brown M S.Protein sensors formembrane sterols[J] .Cell, 2006, 124(1) : 35-46.
[14 ] Sato R.Sterolmetabolism and SREBP activation[ J].Arch Biochem Biophys, 2010, 501(2) : 177-181.
[15 ] Ahmed M H, Byrne C D.Modulation of sterol regulatory element binding proteins( SREBPs) as potential treatments for non-alcoholic fatty liver disease( NAFLD) [ J] .Drug Discov Today, 2007, 12(17/18) : 740-747.
[16 ] Vitto M F, Luz G, Luciano T F, etal.Reversion of steatosis by SREBP-1c antisense oligonucleotide did not improve hepatic in-sulin action in diet-induced obesitymice[J] .Horm Metab Res,2012, 44(12): 885-890.
[17] Stryjecki C, Roke K, Clarke S, et al.Enzymatic activity and genetic variation in SCD1 modulate the relationship between fatty acids and inflammation [ J].Mol Genet Metab, 2012, 105(3): 421-427.
[18] LIU X, Miyazaki M, Flowers M T, et al.Loss of stearoyl-CoA desaturase-1 attenuates adipocyte inflammation: effects of adipocyte-derived oleate[ J] .Arterioscler Thromb Vasc Biol, 2010,30(1): 31-38.
[19] Kotronen A, Seppanen-Laakso T, Westerbacka J, etal.Hepatic stearoyl-CoA desaturase( SCD) -1 activity and diacylglycerol but not ceramide concentrations are increased in the nonalcoholic human fatty liver[J] .Diabetes, 2009, 58(1) : 203-208.
[20] Petersson H, Lind L, Hulthe J, et al.Relationships between serum fatty acid composition and multiplemarkers of inflammation and endothelial function in an elderly population[ J] .Atherosclerosis, 2009, 203(1) : 298-303.
[21] Laplante M, Sabatini D M.mTORC1 activates SREBP-1c and uncouples lipogenesis from gluconeogenesis[ J] .Proc Natl Acad Sci USA, 2010, 107(8): 3281-3282.
[22] 朱明利, 施军平.枯否细胞活化在非酒精性脂肪性肝病发生和发展中的作用[ J].中华肝脏病杂志, 2012, 20(9):718-720.
[23] Roth B, Fkelund M, Fan B G, et al.Lipid deposition in Kupffer cells after parenteral fat nutrition in rats: a biochemical and ultrastructural study[ J] .Intensive Care Med, 1996, 22(11): 1224-1231.
[24] Wong B X, Kyle R A, Myhill PC, etal.Dyslipidemic diabetic serum increases lipid accumulation and expr ession of stearoyl-CoA desaturase in human macrophages[ J] .Lipids, 2011, 46(10): 931-41.
[25] 朱仁敏, 张 程, 陈 熙, 等.Kupffer细胞在果糖引起的非酒精性脂肪肝中的作用[ J].安徽医科大学学报, 2012,47(3): 257-260.
[26] 杨钦河, 谢 芳, 王凤珍, 等.不同治法方药对脂肪肝大鼠肝组织 NF-κBp65 及 Kupffer细胞 p38 MAPK蛋白表达的影响[J].广州中医药大学学报, 2009, 26(2): 141-146.
[27] 杨钦河, 凌家生, 平换换, 等.非酒精性脂肪肝的中医药防治研究思路与对策 [ J].中医杂志, 2007, 48 (8):746-748.
[28] 杨钦河, 欧 健, 孙升云, 等.疏肝健脾方药对非酒精性脂肪性肝病大鼠肝细胞 PI3K p85α蛋白表达的影响[J].广东药学院学报, 2009, 25(1): 62-67.
[29] 中华中医药学会脾胃病分会.非酒精性脂肪性肝病中医诊疗共识意见[J].北京中医药, 2011, 30(2): 83-86.
Effects of soothing liver and invigorating sp leen recipes on SREBP-1c signal pathway related genes and proteins in Kup ffer cells of nonalcoholic fatty liver disease rats
HAN Li1, YANG Qin-he2*, ZHANG Yu-pei2, XU Yong-jian2, LIU Yi-zhen2, YANG Xue-song3,JIN Ling1
(1.The First Affiliated Hospitalof Jinan University, Guangzhou 510632, China; 2.Departmentof Traditional ChineseMedicine, Medical Collegeof Jinan University, Guangzhou 510632, China; 3.Department of Histology and Embryology, Medical College of Jinan University, Guangzhou 510632, China)
AIM To explore effects of soothing liver and invigorating spleen recipes on sterol regulatory element binding proteins-1c(SREBP-1c) signal pathway related genes and proteins in Kupffer cells of nonalcoholic fatty liver disease( NAFLD) rats, and to study its possible preventive mechanism.METHODS The rats of NAFLDmodelwere induced by feeding a high-fat diet.The treatmentgroupswere given a gavage of soothing liver and invigorating spleen recipes.After treatment for 8 weeks, detecting routine blood biochemical indicator and liver tissue pathological changes, collagenase(TypeⅣ) was perfused to digest liver tissue with the circulation in vitro to separate Kupffer cells.Real-time Q-PCR and Western blotwere used to detect the expression levels of SREBP-1csignal pathway related genes and proteins.RESULTS The model group rats appeared hepatic fat accumulation obviously.Blood lipid and the expression levels of SREBP-1c, stearyl-CoA desaturase-1 ( SCD-1 ) genes and proteins in model group were higher than those in normal group.Compared with themodel group, SREBP-1c, SCD-1 genes and proteins decreased in all drug therapy groups.Levels of blood lipid and pathological changes showed different improvements, and the effect of soothing liver recipes was remarkable( P<0.01 ) .CONCLUSIONS Soothing liver and invigorating spleen recipes have good effect on NAFLD, which may be due to inhibiting the activation of SREBP-1c/SCD-1 in Kupffer cells, downing serum total cholesterol, triglyceride synthesis,reducing hepatic lipid deposition.SREBP-1c, SCD-1mRNA and proteinmay be effective targets for soothing liver and invigorating spleen recipes to treat NAFLD.
soothing liver and invigorating spleen recipes; nonalcoholic fatty liver disease; sterol regulatory element binding proteins-1c;stearyl-CoA desaturase-1; Kupffer cells; rats
R285.5
: A
: 1001-1528(2014)05-0885-08
10.3969/j.issn.1001-1528.2014.05.001
2013-06-12
国家自然科学基金资助项目 (81173216)
韩 莉 (1963—), 女, 医学硕士, 副主任医师, 主要从事中医药治疗代谢异常疾病及脂肪肝的临床疗效观察及研究工作。Tel: 13826120177, E-mail: hanli168@aliyun.com
*通信作者: 杨钦河 (1961—), 男, 医学博士, 教授, 博士生导师, 从事中西医结合防治慢性肝病及脂质代谢疾病研究工作。 Tel:(020) 85226197 , E-mail: tyangqh@jnu.edu.cn
