CT引导下肿瘤四维立体定位精确穿刺弓箭射频消融治疗肺癌
2014-04-08杨福奎陈德路
杨福奎,陈德路
射频消融是近年盛行的治疗原发和转移性肺癌的新技术。该方法疗效确切、创伤轻微、恢复快捷、生活质量高、可反复多次进行,具有光明的临床应用前景[1]。近年来,相关学者在提高肺癌射频消融疗效、降低并发症方面做了大量研究。肺癌准确定位穿刺、将肿瘤体积完全包容在射频消融灶内是提高疗效的基础,我们应用自行研制的“肿瘤四维立体定位精确穿刺弓箭”辅助肺癌定位穿刺,进行肺癌射频消融术,实现了肺癌穿刺一次准确到位,消融灶完全包容肺癌体积,疗效满意,现介绍如下。
1 资料与方法
1.1 一般资料
2010年5月至2012年6月,我们选择61例因心脏等重要器官功能不全、不能耐受手术或脏器功能正常而拒绝手术的中晚期原发性肺癌患者,共69个肿瘤(其中12个肿瘤直径>5 cm),在CT引导下,借助肿瘤四维立体定位精确穿刺弓箭辅助穿刺行肺癌射频消融术。其中男44例,女17例;年龄52~89岁,平均年龄(67.61±12.37)岁。术前检查包括血常规、肝肾功能、肿瘤标记物、T/B淋巴细胞亚群、X线胸片、胸部CT、肿瘤PET、腹部B超、骨扫描及头颅MRI。术前病理学明确诊断:腺癌28例,鳞癌25例,支气管肺胞癌3例,大细胞肺癌1例,腺鳞癌2例,未分型2例。术前发现骨转移15例,脑转移10例,肺内转移灶8例(同时行射频消融治疗)。接受射频消融的病灶直径1.00~11.60 cm,平均(3.54±2.01)cm。
1.2 方法
根据医院技术委员会和伦理委员会的批准文件(批文号:2010003),在患者及家属完全知情并签字同意的前提下,常规皮肤准备,术前禁食4~6 h,术前半小时予苯巴比妥或地西泮肌内注射,建立液体通路。手术区域常规消毒、铺巾,穿刺点局部麻醉,而后行穿刺和射频消融术。
1.2.1 肿瘤四维立体定位精确穿刺弓箭的结构和原理 示意图见图1。箭托可以带动箭杆绕半圆形穿刺弓移动;穿刺针尖端恒定位于穿刺弓圆心点(等中心点);箭杆可以带动穿刺针沿穿刺弓半径穿刺,并能够利用箭杆上的挡块将穿刺针尖端挡停在圆心点(等中心点);穿刺弓可以以固定螺丝A和B的连线(穿刺弓直径)为轴转动和锁止。借助以上结构,穿刺针的穿刺路径可以在以圆心为球心的半个球体的任意半径中随意选择,穿刺针尖端恒定被挡停在圆心点,其穿刺机械精度为1 mm。滑动x、y、z轴三方向滑块可以带动穿刺弓圆心在x、y、z轴三方向上移动(三维空间转移),各滑块滑动机械精度均为0.5 mm,弧形板可以与CT床板紧密结合,使x、y、z轴三方向滑块的坐标系与CT床坐标系融合。
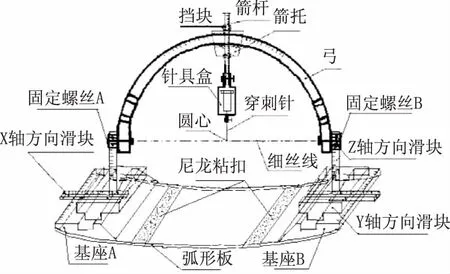
图1 肿瘤四维立体定位精确穿刺弓箭的结构、原理示意图
1.2.2 呼吸状态记录开关的原理和使用方法 示意图见图2。红外线发射器和接收器是点对点对应关系。使用时,先利用皮肤贴把红外线发射器固定在呼吸动度最大处的皮肤上,再调整红外线接收器的位置,使红外线接收器在固定体位下,患者平静呼吸的呼气末接收到红外线,光电开关接通,信号灯亮和蜂鸣器响,如果患者体位发生改变或呼吸状态不同,引起红外线移动距离超过2 mm,光电开关断开,声光信号中断。
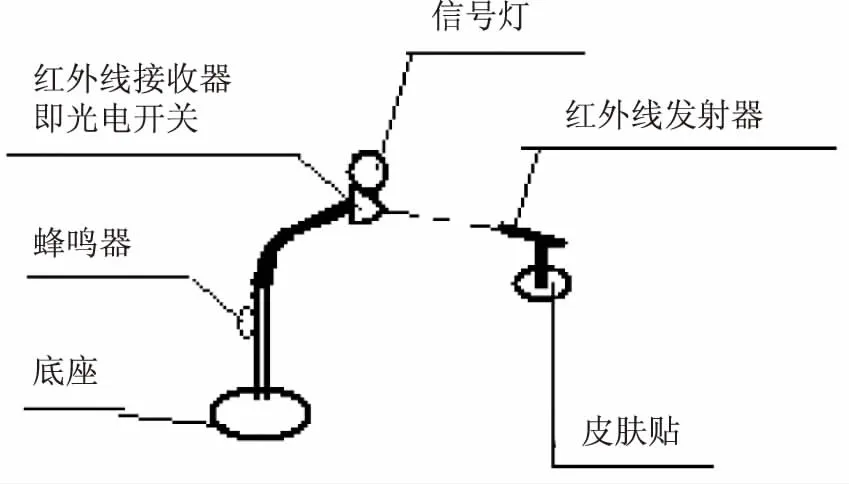
图2 呼吸状态记录开关原理图
1.2.3 选择固定患者体位、CT定位扫描、测量预穿刺点与皮肤标记点的位置关系 利用肿瘤四维立体定位精确穿刺弓箭的弧形板,把基座固定在CT床板上,使x、y、z轴三方向滑块的坐标系与CT床坐标系融合,再放置放射治疗固定患者体位用的负压袋,根据患者体位舒适稳定的要求和肺内肿瘤的位置,选择患者体位并用负压袋抽真空固定,与精确放射治疗的CT定位一样,粘贴直径1 mm的金属皮肤标记点,安装调整呼吸状态记录开关,在患者平静呼吸的呼气末信号灯亮蜂鸣器响,嘱咐患者看到信号灯亮或听到蜂鸣器响时屏气,进行3次屏气训练。在患者屏气状态下,采用Siemens somatom sensation 64 cardiac CT机,进行2 mm层厚CT定位扫描,图像导入CT影像工作站内的肿瘤放射治疗计划系统(tumor radiation therapy planning system,TPS),在肿瘤区(gross target volume, GTV)名目下勾画出肿瘤体积范围,根据肿瘤大小、预穿刺方向、锚状电极针打开后形成的球心与穿刺针尖端的距离,及锚状电极针形成的球心与肿瘤中心重合的要求,确定预穿刺点位置并测量预穿刺点与皮肤标记点在x、y、z轴三方向上的空间距离,见图3、图4。
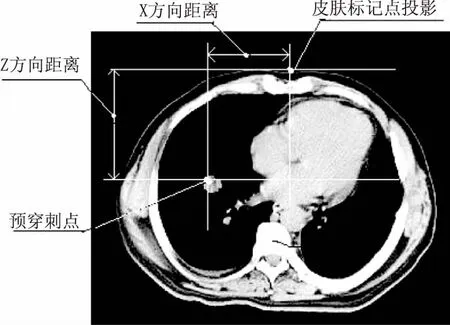
图3 TPS内测量预穿刺点与标记点在x、z方向距离
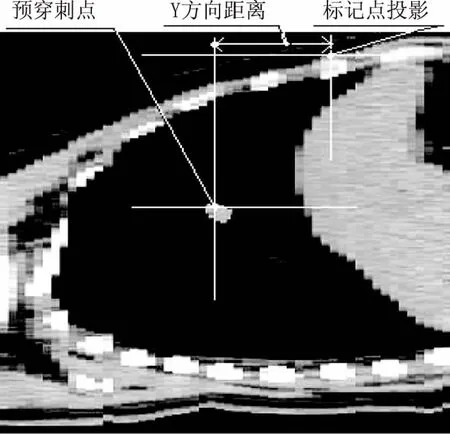
图4 TPS内测量预穿刺点与标记点在y方向距离
1.2.4 安装调整滑块和穿刺弓 通过移动x、y、z轴三方向滑块实现圆心(等中心)空间转移安装调整各滑块,x轴方向滑块和y轴方向滑块处于中间0刻度位置,z轴方向滑块处于最高点,安装穿刺弓,穿刺弓和箭杆都处于垂直0度位。根据肿瘤深度调整套针外露长度和针具盒与箭杆位置,使套针尖端位于圆心点,固定并记录箭杆上挡块的位置,移动x、y、z轴三方向滑块,使套针尖端位于皮肤标记点处(图5),记录x、y、z轴三方向滑块在此位置的数据。根据上述测量所得预穿刺点与皮肤标记点在三维空间内的距离数据,移动x、y、z轴三方向滑块,使弓圆心(等中心)位于预穿刺点(图6)。
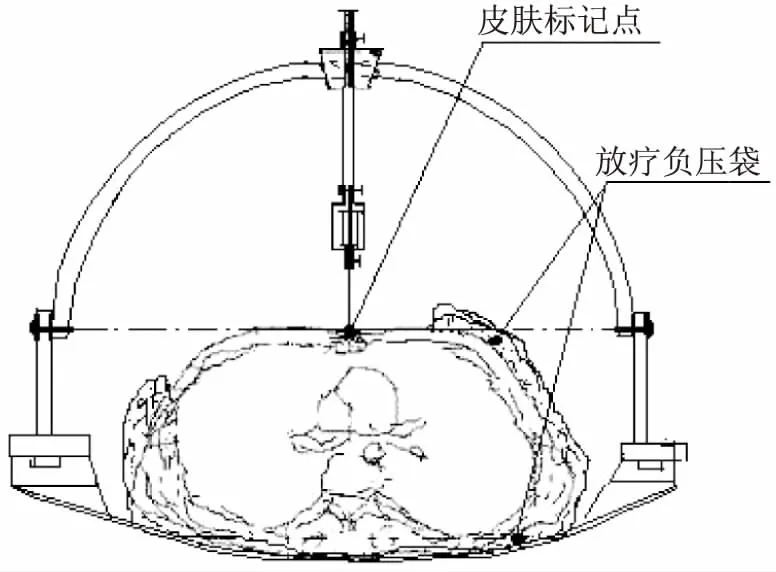
图5 坐标转移前皮肤标记点为等中心
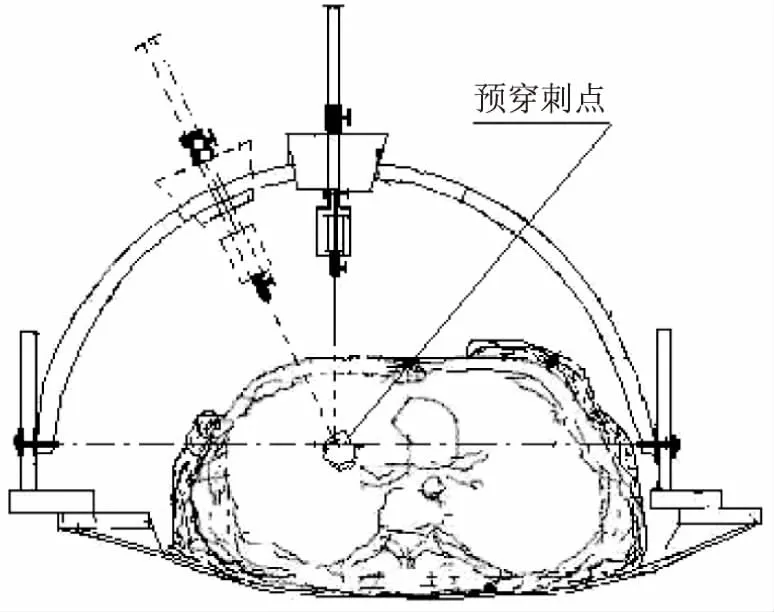
图6 坐标转移后预穿刺点为等中心
1.2.5 穿刺和实际消融灶验证 参考图像上肿瘤大小和在肺内的位置,避开肋骨、大血管、肺大泡等重要的组织和器官,选择最佳穿刺角度。根据选择的穿刺角度,调整并固定穿刺弓的倾斜角度(头足方向)和箭杆的倾斜角度(左右方向),常规皮肤消毒、麻醉,嘱咐患者听到蜂鸣器声或看到信号灯亮时屏气,医生在1~2 s时间内用手掌快速顶推箭杆直至被挡停,打开针具盒,撤去穿刺弓,通过穿刺套针针柄上的推进装置,根据预先计算的推进距离,将电极推出针壳,展开排成锚状阵列。嘱咐患者听到蜂鸣器声或见信号灯亮屏气,CT扫描验证细电极针形成的消融灶(图7),图像导入TPS内,在计划靶区(planning target volume,PTV)名目下勾画出细电极针形成的实际消融灶范围,在TPS的三维图像内观察实际消融灶是否完全包含肿瘤范围。如果肿瘤直径大于5 cm,在TPS内把肿瘤分割成若干个直径小于5 cm的小肿瘤并在GTV名目下分别进行勾画,分别命名为GTV1、GTV2……,各个小GTV之间可以有交叉重叠,但是其外缘必须紧密相连,包全肿瘤外缘,不得有漏空。标出各个小GTV的预穿刺点,分别按照独立小肿瘤逐个进行穿刺、实际消融灶验证,在PTV名目下勾画消融灶,分别命名为PTV1、PTV2……,最后在TPS的三维图像内进行叠加后的消融灶与肿瘤范围验证(图8)。
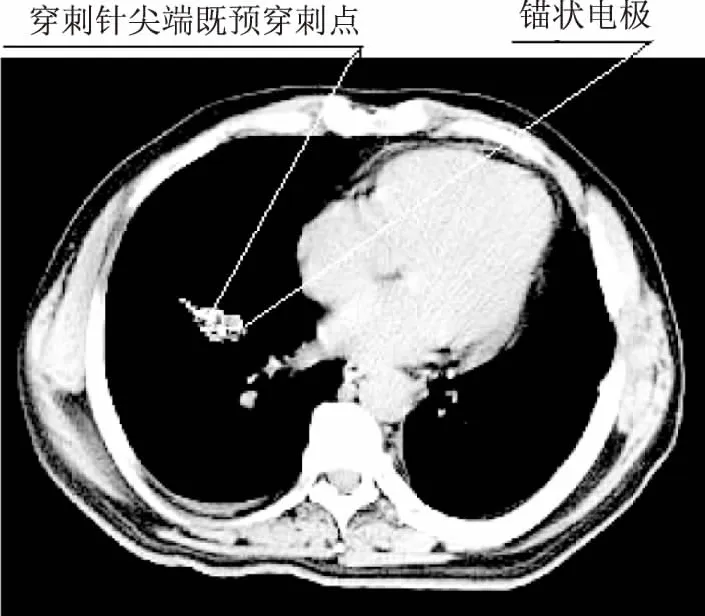
图7 锚状电极释放后效果图
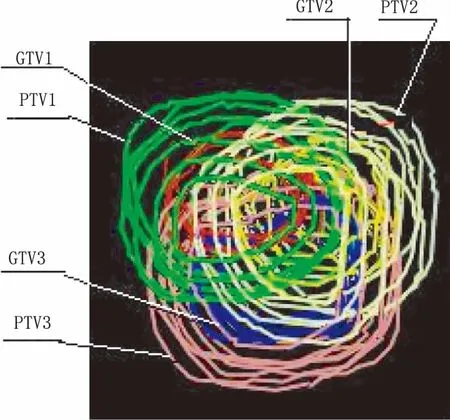
图8 较大肿瘤分割后在TPS内验证实际消融灶
1.2.6 射频消融 采用美国瑞达公司RITA1500X多极射频肿瘤消融仪,用电极套针经皮穿刺到肺内肿瘤,释放细电极针,根据肿瘤形状大小设计消融灶,再根据形成消融灶的直径采用相应消融程序,治疗靶温度90 ℃,射频输出功率70~150 W,多点位温度监测,确保完全消融肿瘤,不过度消融,避免碳化。消融时间15~125 min,平均消融时间(31.26±15.78)min。消融完毕冷却后收回射频针,针道消融,拔出穿刺针,包扎穿刺点。再进行扫描,观察病灶有无变化和气胸、出血等并发症,确保患者无异常时返回病房,静卧2 h,其他给予对症处理。
1.2.7 疗效判定标准 近期疗效采用实体瘤疗效评价标准(response evaluation criteria in solid tumors, RECIST),并增加肿瘤代谢显像(single position emission computed tomography, SPECT),指标包括:血清肿瘤标记物、胸部增强CT扫描(肿瘤大小以射频消融后5 min扫描结果为基准)。复查时间为1个月、3个月。
2 结果
2.1 定位穿刺结果
61例患者共69个肿瘤,其中有12个肿瘤直径>5 cm,将其在TPS内为分割成47个直径小于5 cm的肿瘤(体积有重叠),总共进行104个肿瘤定位穿刺和射频消融,定位穿刺均一次完成,无重复穿刺者。将CT定位图像及验证图像导入TPS,利用其精确放疗空间误差测量与计算方法,对穿刺套针尖端空间穿刺误差进行测量与计算,104个肿瘤套针尖端在空间内的穿刺误差1~4 mm,平均2.6 mm。在GTV名目下勾画肿瘤体积,在PTV名目下勾画细电极针形成的消融灶体积,本组GTV全部被PTV包含,即104个消融灶完全包含预消融肿瘤。
2.2 射频消融结果
术后1个月复查CT,病灶大小与原肿瘤相比变化不明显;但SPECT显示所有病灶完全无核素浓度。术后3个月复查CT,肿瘤缩小者82.6%(57/69),肿瘤无变化者17.4%(12/69),无肿瘤增大者;但有3例患者发现肺内转移灶,占4.92%(3/61)。SPECT显示消融灶均无核素浓度,发现3例肺内转移灶。
2.3 并发症
术中一般感觉局部发热,个别患者出汗甚至心率加快,无需特殊处理,3例患者出现剧烈咳嗽,经注水孔注入少量利多卡因缓解,4例患者出现少量气胸,3例患者出现轻度胸痛,无需特殊处理后缓解。
3 讨论
射频消融的原理是在肿瘤组织内施以一定频率的射频电流,产生高频率电磁波,组织内分子发生高速震荡产生摩擦,将射频能转化为热能,当温度达到90 ℃时可以有效地快速杀死局部肿瘤细胞,同时可使肿瘤周围正常组织凝固形成一个反应带,有利于防止肿瘤转移,治疗后的炎症反应可进一步导致肿瘤坏死[2]。肺部肿瘤周围的正常肺组织可通过肺部大血管的血液循环和呼气散热,因此正常肺组织实际起着绝缘的作用,使能量可以充分集中在病变部位;加之肺部肿瘤组织的血流量低,因此射频消融治疗肺部肿瘤是可行而有效的[3]。根据射频消融的原理,射频消融的范围(消融灶)必须完全包含所有肿瘤体积,由于细电极针释放后形成的是一个球形轮廓,其消融直径最大可达到5 cm,对于<5 cm的肿瘤,只要肿瘤中心和细电极针形成的球形轮廓中心重合,细电极针形成的消融灶就可以完全包含肿瘤体积。只有进行肿瘤精确定位和穿刺,才能实现上述两个中心的重合,避免消融灶与肿瘤之间出现偏移而不一致[4]。
肿瘤四维立体定位精确穿刺弓箭是利用肿瘤精确放射治疗的精确定位和等中心转移原理及GTV和PTV的勾画方法,实现肿瘤精确定位和穿刺,根据细电极针形成的球形轮廓中心与套针尖端的距离,利用TPS精确计算套针尖端的停留位置,为肿瘤中心和细电极针形成的球形轮廓中心重合提供了可靠数据。套针尖端在三维空间内的平均穿刺误差是2.6 mm,对于小于5 cm的肿瘤,该误差不会影响消融灶完全包含肿瘤体积。在TPS内把大于5 cm的肿瘤划分成为若干个小肿瘤,再按照独立肿瘤进行定位穿刺和射频消融,在PTV名目下逐个勾画出各个小射频消融灶,在三维图像内观察各个小消融灶的总体积是否包全肿瘤体积,如有遗漏,可以再次在GTV名目下勾画出遗漏的肿瘤体积,再次按照独立肿瘤进行定位穿刺和消融,这些过程可以确保所有肿瘤组织得到射频消融,特别是肿瘤外周生长活跃部分,必须完全包含在消融灶内。
肺内肿瘤的位置受呼吸运动影响较大,影响穿刺的准确性,进一步影响射频消融的效果,肺内肿瘤穿刺射频消融必须考虑呼吸运动的影响[5]。呼吸状态记录开关可以精确记录患者体位和呼吸状态,能够确保CT定位扫描时、穿刺过程、锚状电极针分布位置CT验证扫描时3个过程中,患者体位和呼吸状态一致,能够为肿瘤准确定位穿刺和布局细电极针及评估消融灶的安全性提供有力帮助,对于需要多肿瘤消融的患者,由于患者体位保持时间较长,容易发生体位改变,呼吸状态和体位的记录更为重要,只有患者呼吸状态和体位一致,才能保障肿瘤穿刺和消融灶的准确性和安全性。
肺内肿瘤是一个立体的体积,评估消融灶是否安全合理必须在三维图像内进行消融灶体积与肿瘤体积比较[6],TPS能够精确计算肿瘤体积和消融灶体积,可以准确、直观判断消融灶体积是否完全包含肿瘤体积,为肿瘤是否能够被完全消融提供可靠信息。TPS的三维图像能够为科学设计穿刺路径、避开重要的组织器官及判断消融灶是否包含重要组织器官提供帮助,结合肿瘤四维立体定位精确穿刺弓箭可以任意选择穿刺路径的特点,可以最大程度地减少穿刺和射频消融的并发症。总之,利用CT引导和肿瘤四维立体定位精确穿刺弓箭进行肺内肿瘤定位穿刺和射频消融,能够将肺内肿瘤所有体积完全消融,严重并发症少,安全有效。
参考文献:
[1] 方勇,倪旭东.射频消融术治疗肺部肿瘤的临床研究[J].中国临床医学,2012,19(6):619-621.
[2] Lanuti M,Sharma A,Willers H,et al.Radiofrequency ablation for stage I non-small cell lung cancer: management of locoregional recurrence[J].Ann Thorac Surg,2012,93(3):921-927.
[3] Sher DJ,Wee JO,Punglia RS.Cost-effectiveness analysis of stereotactic body radiotherapy and radiofrequency ablation for medically inoperable,early-stage non-small cell lung cancer[J].Int J Radiat Oncol Biol Phys,2011,81(5):e767-774.
[4] Baisi A,Raveglia F,De Simone M,et al.Recurrence after radiofrequency ablation for stage I non-small cell lung cancer[J].Ann Thorac Surg ,2012,94(5):1788-1792.
[5] 王纯,周红轩,张永良,等.CT导向肺穿刺标本检测的临床应用新价值[J].中国肿瘤外科杂志,2012,4(5):306-307.
[6] 杨雷,张临友,孙露,等.CT引导下肺癌射频消融治疗25例疗效分析[J].哈尔滨医科大学学报,2011,45(5):461-463.
