普萘洛尔联合噻吗洛尔滴眼液治疗婴幼儿血管瘤
2014-03-28林雀卿靖姜周少毅陈昆山李海波牛传强谭小云
林雀卿 张 靖姜 华 申 刚 周少毅 陈昆山 李海波 牛传强 谭小云
普萘洛尔联合噻吗洛尔滴眼液治疗婴幼儿血管瘤
林雀卿 张 靖∗姜 华 申 刚 周少毅 陈昆山 李海波 牛传强 谭小云
目的: 评价普萘洛尔联合噻吗洛尔滴眼液治疗婴幼儿血管瘤的临床疗效和安全性。方法:血管瘤患儿130例,普萘洛尔2 mg/(kg·d),分3次口服,皮损表面外搽噻吗洛尔滴眼液适量,日4次,治疗3个月。结果: 治疗8个月后随访,66例(49%)患者的瘤体缩小76%~100%,53例(42%)瘤体缩小51%~75%,10例(8%)瘤体缩小26%~50%,1例(1%)瘤体缩小<25%。治疗期间无严重不良反应。结论: 普萘洛尔联合噻吗洛尔滴眼液治疗婴幼儿血管瘤安全有效。
普萘洛尔; 噻吗洛尔; 婴幼儿血管瘤
婴幼儿血管瘤(infantile hemangioma,IH)是儿童常见具有血管内皮细胞异常增殖为特征的良性肿瘤,虽然大多可自行消退,但部分发展迅速,可出现感染、溃疡、坏死、出血,继发畸形、功能障碍等。自2008年Léauté-Labrèze等1医生发现口服普萘洛尔治疗婴幼儿血管瘤有效后,2010年Powell等2报道证实口服普萘洛尔疗效优于口服泼尼松,其不良反应也较泼尼松少。目前国内外皆有报道口服普萘洛尔治疗婴儿血管瘤可取得良好疗效,亦有报道使用噻吗洛尔滴眼液外搽浅表血管瘤也有一定疗效。3,4临床上经常可见到浅表及深部病灶同时存在,亦称为混合型血管瘤的患儿,使用单一方法治疗对于控制瘤体的增长无法达到满意的疗效,因此本实验联合二者应用治疗婴幼儿血管瘤,以期通过协同作用,提高疗效。
1 资料和方法
1.1 病例资料 2012年9月至2013年5月广州市妇女儿童医疗中心介入血管瘤专科病区收治血管瘤患儿130例,其中男58例,女72例;年龄20天至2岁。增生期(0~1岁)118例,消退期(1~2岁)12例。病灶位于颌面部76例,躯干及四肢24例,多发性血管瘤30例。
纳入标准 ①年龄≥1个月,表现为患处表面红斑,伴迅速生长史的混合型血管瘤(瘤体范围增大较迅速、伴隆起、与皮温增高),对不明显的皮下病灶以我院B超确诊血管瘤为标准;②未予治疗。
排除标准 普萘洛尔用药禁忌症:窦性心动过缓、心脏传导阻滞(二、三度房室传导阻滞)、重度或急性心力衰竭、心源性休克、支气管哮喘、肺炎、甲状腺功能低下、或肝肾功能不良等。先天性血管瘤(不消退型血管瘤及快速消退型血管瘤)。
1.2 方法
1.2.1 治疗前准备 血常规;脏器功能;凝血四项;甲状腺功五项;心电图;心脏彩超;测量患儿体重及生命体征;对治疗前瘤体进行测量评估记录;完善相关检查并排除口服普萘洛尔治疗禁忌症;对患儿家属交待治疗过程可能出现的疗效及不良反应,取得家属同意后予签署治疗知情同意书。
1.2.2 治疗方法 予普萘洛尔2 mg/(kg·d)治疗,分3次口服,首次服药在院观察并监测服药前后1 h、2 h及12 h内心率、血压、呼吸及观察有无不良反应。口服普萘洛尔药物治疗期间,瘤体表面红斑处予以噻吗洛尔滴眼液适量外擦,每日4次。在院观察12 h内上述监测指标大致正常,未出现心率<80次/分、血压<60/40 mmHg,无支气管痉挛、呼吸困难,无精神抑郁、反应迟钝、明显腹泻、恶心、倦怠等药物相关不良反应后,予以出院并继续治疗,由家属持续观察。
1.2.3 复查 初次用药后2周门诊复查,考虑普萘洛尔药物治疗安全性,予以生理性减量,即药物治疗期间维持首次用药剂量不予调整(单次口服剂量≤3.33 mg,患儿根据体重变化调整1次用药为单次口服剂量3.33 mg后不再变动)。噻吗洛尔滴眼液持续外搽血管瘤处,每日4~5次。每月复诊记录瘤体变化。
1.2.4 停止治疗指征 增生期血管瘤患儿(年龄为出生~8个月间)治疗时间至患儿年龄满8个月(包括早产儿纠正胎龄后);稳定期及消退期期间血管瘤患儿(年龄为8个月~2岁)治疗期为3个月。血管瘤瘤体无明显继续增大,部分患儿瘤体明显消退、颜色变淡可停药,停药后继续随访1个月,如无明显反弹则不再服药。停药时为避免突然停药引起的心脏超敏反应,又称普萘洛尔停药综合征(propranolol withdrawal syndrome),本研究分2周时间逐渐减量停药。考虑停药后易出现瘤体颜色加深情况,停药后患儿仍继续予以噻吗洛尔滴眼液适量外擦瘤体表面,每日4~5次,持续1~3个月,如瘤体表面颜色已明显变浅,予以停止。
1.2.5 疗效判定标准 采用Achauer等5分级标准评价疗效。I级(差):瘤体缩小<25%;II级(中):瘤体缩小26%~50%;III级(好):瘤体缩小51%~75%;IV级(优):瘤体缩小76%~100%。
2 结果
2.1 治疗结果 经过3~8个月随访,按疗效判定标准,结果为:I级1例(1%),II级10例(8%),III级53例(42%),IV级66例(49%)。所有患儿治疗后第1周内均可见瘤体不同程度缩小、皮温降低、颜色变浅。第2周均见瘤体张力有不同程度降低、瘤体体积、颜色进一步缩小变浅。开始治疗1个月内的患儿有127例(98%)表现为瘤体不同程度消退,有124例(96.2%)患儿瘤体表面颜色消退明显。2个月120例(93%)患儿瘤体表面颜色进一步消退(图1)。
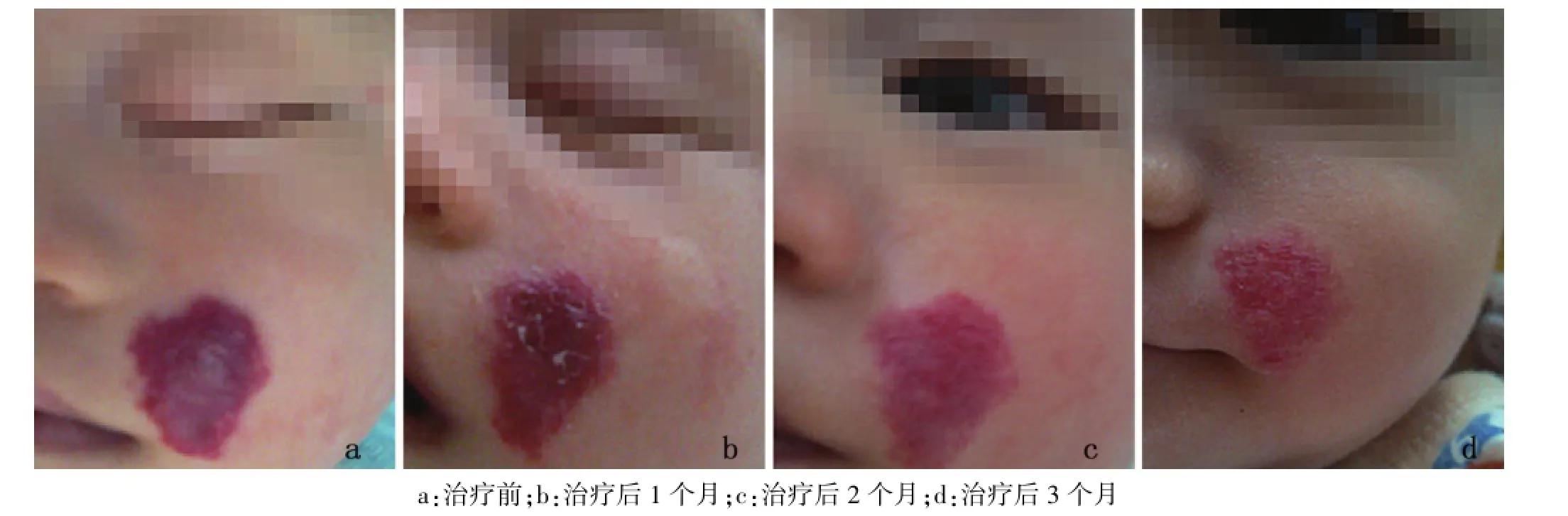
图1 面部血管瘤患儿治疗前后比较
130例患儿中有27例(21%)患儿停止治疗后1个月门诊复查发现肿物稍有增大,其中18例(14%)患儿血管瘤增大不明显,只予噻吗洛尔滴眼液持续外擦血管瘤处,每日4次。余9例(7%)患儿(6例颌面部,2例为胸壁,1例左上肢)。再次入院,在我科介入室全麻下行经导管动脉硬化栓塞术治疗,术后予普萘洛尔口服,用量仍为2 mg/kg·d,分每8 h 1次口服治疗,并予噻吗洛尔滴眼液持续外擦血管瘤处,每日4次,在院监测无明显不良反应后出院,持续治疗3个月后复查,病灶缩小明显、皮温降低、颜色变浅。
2.2 不良反应 ①心率减慢:有11例(8%)患儿在服药后12 h内熟睡状态下心率波动在70~80次/分,血压基本正常,患儿无明显不适,未予处理。②睡眠改变:有6例(4%)患儿服药后表现兴奋、睡眠减少,在持续服药后1个月症状可逐渐改善。③腹泻:有37例(29%)患儿出现不同程度腹泻,次数约在每日3~5次,每次量少。患儿无明显不适,部分患儿予以对症治疗并在持续服药后1个月症状可逐渐恢复正常。④其他:有6例(4%)患儿在治疗期间因上呼吸道、肺炎,家长自行停药1周,复诊时门诊医生评估后予以继续原方案治疗。本组病例未出现低血压、支气管痉挛、呼吸困难等严重不良反应,外擦噻吗洛尔滴眼液病灶及病灶周围均无出现红肿、皮疹、瘙痒等症状。
3 讨论
血管瘤在新生儿发病率为1.1%~2.6%,其中以早产儿和低体重儿更为常见。女性多于男性,比例约3∶1~5∶1。约60%发生于头颈部。病灶多位于皮下与皮下组织。Léauté-Labrèze等报道了应用普萘洛尔治疗婴儿血管瘤后,一系列相关研究相继报道。1,6,7有学者尝试用普萘洛尔治疗合并有溃疡形成的血管瘤,发现普萘洛尔对于血管瘤消退及溃疡愈合效果显著。8
糖皮质激素(以下简称激素)是以往公认的有效、安全一线药物,其临床应用已达30多年,该药物仅对增生期血管瘤有效,对稳定期、消退期及合并溃疡等并发症的血管瘤效果欠佳。此外,激素用药剂量较大,疗程长,患儿难于坚持服用,且不良反用相对较大,如库欣面容、生长延迟、夜间烦躁、多尿、多毛、鹅口疮和胃肠道不适等。因此临床应用受限。自发现普萘洛尔可用于治疗婴幼儿血管瘤开始,有一系列报道指出,普萘洛尔在血管瘤各个阶段皆有效9,10(分为早期的促进血管收缩作用、中期的抑制血管新生及晚期诱导血管内皮细胞凋亡)。在治疗剂量上尚无统一方案,自2008年至今国内外文献中,使用剂量范围大部分在1~3 mg/kg·d,分1~3次给药,治疗时间长约6~18个月。Lawley等11亦提出了“阶梯给药”方案。从药代动力学上来说,普萘洛尔给药后1~1.5 h达血药浓度峰值,药物半衰期为2~3 h,最佳给药时间为6 h,为提高顺应性,一般8~12 h给药1次。与本组病例相符。从结果来看,本组病例中服药1~2周内均有效,服药1个月内的患儿有127例(98%)表现为瘤体不同程度消退,停药后大部分患儿血管瘤瘤体已有明显缩小、颜色变浅、皮温降低表现。疗效显著,与国内外相关报道一致。
马来酸噻吗洛尔滴眼液原为眼科用药,为非选择性强效β受体阻断剂,作用强度为普萘洛尔8倍,无直接抑制心脏作用。因药物作用起效快、不良反应少、对瞳孔大小、对光反应及视力无影响,对组织刺激性小,对于噻吗洛尔滴眼液作为外用药来说有较大的安全性。以往在外用治疗上所使用的同位素敷贴治疗、冷冻治疗,因同位素敷贴本身含有射线的缘故,在治疗过程中亦容易留下色素沉着或减退,且若干年后患处易有萎缩、发育不良、皮肤敏感等不良反用;另外,冷冻治疗易使瘤体破溃,产生疤痕,近年来已逐渐被淘汰。自2010年Guo等4首次报道了噻吗洛尔滴眼液用于婴幼儿血管瘤的治疗,并取得满意疗效。而后Pope等12、Khunger等13、Tlougan等14多位学者均报道噻吗洛尔滴眼液在治疗婴幼儿浅表血管瘤的良好效果。该系列报道指出,噻吗洛尔滴眼液对于各期血管瘤均有效果,增生期疗效较消退期明显。Chambers等15对23例噻吗洛尔滴眼液治疗婴幼儿血管瘤作了2个月的回顾性分析,发现仅1例疗效较差,总体均取得良好疗效。但因数量较少、观察时间较短,仍有待大样本长期随访。
目前,尚未见有关口服普萘洛尔联合噻吗洛尔滴眼液治疗婴幼儿血管瘤的报道。本研究结果显示在联合治疗期间95%患儿均表现为瘤体不同程度缩小,瘤体缩小50%以上患儿占多数;减量停药后103例(79%)患儿无明显反弹增大,部分稍有瘤体增大的情况,仍可选用同为非选择性β受体阻断剂的噻吗洛尔滴眼液外擦,持续控制瘤体,使病灶缩小、皮温降低、颜色变浅。另外,在本研究过程中,均未出现口服普萘洛尔及外搽噻吗洛尔滴眼液的严重不良反应。
综上所述,普萘洛尔联合噻吗洛尔滴眼液治疗婴幼儿血管瘤,不仅明显提高了疗效性,治疗上更为安全、方便、费用低廉合理。本研究发现婴幼儿血管瘤的治疗具有多样性的选择,可针对不同时期的血管瘤选择合适的方法联合治疗,以有效控制瘤体,进一步缩短病程。
1 Léauté-Labrèze C,Dumas de la Roque E,Hubiche T,et al. Propranolol for severe hemangiomas of infancy.The New England Journal of Medicine,2008,358(24):2649-2651.
2 Powell J,Bertrand J,Ondrejchak S,et al.Propranolol vs prednisolone in the treatment of Infantil Hemangiomas:a retrospective comparative study.The 18th International Workshop on Vascular Anomalies,Brussels,2010.21-24.
3叶肖肖,金云波,林晓曦,等.外用马来酸噻吗洛尔治疗婴幼儿眼周浅表血管瘤的前瞻性研究.中华整形外科杂志,2012, 28(3):161-163.
4 Guo S,Ni N.Topical treatment for capillary hemangioma of the eyelid using beta-blocker solution.Arch Ophthalm01,2010,128 (2):255-256.
5 Achauer BM,Chang Cj,Vander Kam VM.Management of hemangioma of infancy:review of 245 patients.Plast Reconstr Surg,1997,99(5):1301-1308.
6 Manunza F,Syed S,Laguda B,et al.Propranolol for complicated infantile haemangiomas:a case series of 30 infants.Br J Dematol,2010,162(2):466-468.
7 Denoyelle F,Garabédian EN.Propranolol may become first-line treatment in obstructive subglottic infantile hemangiomas.Otolaryngology Head and Neck Surgery,2010,142(3):463-464.
8 Michel JL,Patural H.Response to oral propranolol therapy for ulcerated hemangiomas in infancy.Archives Pediatrie,2009,16 (12):1565-1568.
9 Annabi B,Lachambre MP,Plouffe K,et al.Propranolol adrenergic blockade inhibits human brain endothelial cells tubulogenesis and matrix metalloproteinase-9 secretion.Pharmacol Res, 2009,60(5):438-445.
10 Itinteang T,Brasch HD,Tan ST,et al.Expression of components of the renin-angiotensin system in proliferating infantile laemangioma my account for propranolol-induced acceleratedinvolution.Plast Reconstr Aesthet Surg,2011,64(6):759-765.
11 Lawley L,Siegfried E.Propranolol treatment for hemangiomas of infancey:risks and recommendations.Pediatr Dermatol, 2009,26(5):610-614.
12 Pope E,Chak K,ttakandiyil A.Topical timolol gel for infantile hemangiomast U pilot study.Arch Dermatol,2010,146(5):564-565.
13 Khunger N,Pahwa M.Dramatic response to topical timolol lotion of a large hemifacial infantile haemangioma associated with PHACE syndrome.Br J Dermatol,2011,164(4):886-888.
14 Tlougan BE,Gonzalez ME,Orlow SJ.Abortive segmental perineal hemangioma.Dermatol Online,2011,17(10):8.
15 Chambers CB,Katowitz WR,Katowitz JA,et al.A controlled study Of yopical 0.25%yimolol maleate gel for the treatment of cutaneous infantile capillary hemangiomas.Ophthal Plast Reconstr Surg,2012,28(2):103-106.
(收稿:2013-12-04 修回:2014-08-08)
The therapeutic effects of propranolol combined with timolol eye drops in the treatment of infantile hemangioma
LIN Que-qing,ZHANG Jing,JIANG Hua,et al.Guangzhou Women and Children’s Medical Center,Guangzhou,510120
Objective:To assess the efficacy and safety of propranolol combined with timolol eye drops in the treatment of infantile hemangioma(IH).Methods:One hundred and thirty patients were treated with oral propranolol 2 mg/(kg·d),3 times a day and topical timolol eye drops,4 times a day for 3 months.Results: The size of tumors was reduced by 26%~50%in 66(49%)patients,by 51%~75%in 53(42%)patients, by 26%~50%in 10(8%)patients and by 1%in one(1%)patient.There were no obvious adverse reactions.Conclusion:Propranolol combined with timolol eye drops is effective and safe in the treatment of IH.
propranolo;timolol;infantile hemangioma
广东省医学科学技术研究基金课题(编号:A2012504)
广州市妇女儿童医疗中心,510120
∗通信作者
