放疗同步应用洛铂治疗中晚期食管癌的临床观察
2014-03-27田大龙喻志冲王贺芳
田大龙,刘 辉,喻志冲,李 华,王贺芳
(盐城市第一人民医院放疗科,江苏 盐城 224006)
近20年来,基于美国放射肿瘤协作组(radiation therapy oncology group,RTOG)随机Ⅲ期试验结果,同步放化疗成为了美国和欧洲等国家的局部/区域食管癌非手术治疗的标准方案[1]。顺铂+5-氟尿嘧啶(5-fluorouracil,5-FU)联合放疗是治疗中晚期食管癌的标准方案[2-3],其不仅可以改善近期疗效,减少局部未控与复发,而且能提高远期生存率。顺铂虽然价格较低但毒性反应较大,部分患者不能耐受,进而使治疗时间延长,限制了其临床应用。因此需要继续探索新的有效、低毒性铂类药物治疗食管癌。洛铂是德国ASAT公司研制的第三代铂类抗肿瘤药物,洛铂单药治疗食管鳞癌的Ⅱ期临床研究中,28%(5/18)获得部分缓解(partial response,PR),提示对食管鳞癌疗效明显[4]。本研究对78例病理证实为鳞癌的中晚期食管癌患者进行洛铂+5-FU化疗联合放疗方案与顺铂+5-FU化疗联合放疗方案治疗的临床观察,现报道如下。
1 资料与方法
1.1一般资料 选择盐城市第一人民医院2006年10月至2008年12月收治的病理证实为鳞癌的中晚期食管癌患者78例。纳入标准:初治,病理证实为食管鳞状细胞癌,并有客观可测量病灶;以CT影像根据美国癌症研究联合会分期[5]为Ⅱ~Ⅳ期;年龄40~70岁;Karnofsky评分≥70分;X线片显示无食管瘘及食管穿孔征象,无活动性食管出血;血常规、肝肾功能、心电图基本正常;无化疗禁忌证;无严重药物过敏史;无严重器官功能障碍。78例患者中,男51例、女27例,年龄38~70岁,中位年龄56.6岁,依据随机数字表法分为两组:试验组40例,采用洛铂+5-FU+放疗;对照组38例,采用顺铂+5-FU+放疗。患者及家属知情同意。两组患者的性别、年龄、病变部位等一般资料比较差异无统计学意义(P>0.05),具有可比性(表1)。
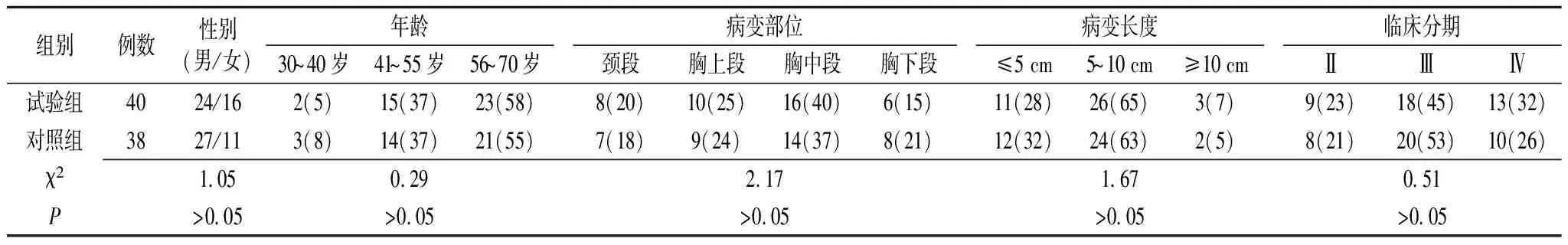
表1 两组中晚期食管癌患者一般资料的比较 [例(%)]
试验组:采用洛铂+5-氟尿嘧啶+放疗;对照组:采用顺铂+5-氟尿嘧啶+放疗
1.2治疗方法 放疗应用瑞典医科达公司生产的Precise直线加速器6兆高能量X线,根据CT、食管吞钡片所见肿瘤实际侵犯范围设野,上下界为超过病变两端3~4 cm,两野对穿等中心放疗,野内同时包括区域淋巴结,每次2 Gy,每周5次,肿瘤总剂量:60~66 Gy。化疗在放疗的第1日开始,试验组给予洛铂(海南亚洲制药生产)联合5-FU(上海旭东海普药业生产)方案化疗,于放疗开始的第1日、第29日静脉滴注洛铂35 mg/m2,于第1~5日、第29~33日静脉滴注5-FU 500 mg/m2;对照组于第1~5日、第29~33日给予顺铂(江苏豪森药业生产) 20 mg/m2静脉滴注,第1~5日、第29~33日给予5-FU 500 mg/m2静脉滴注。每4周为1个周期,共2个周期。每2周复查食管吞钡片,给予阿扎司琼、格拉司琼止吐,每周复查血常规。出现骨髓抑制后给予人粒细胞集落刺激因子处理。
1.3疗效评价
1.3.1近期疗效评价标准 放疗结束及结束后1~2个月,根据食管造影结果评价近期疗效。近期疗效评价按照WHO实体瘤评价标准[6],完全缓解:所有临床指标显示肿瘤完全消失持续至少4周;部分缓解:肿瘤缩小超过50%,持续超过至少4周;进展:肿瘤增大超过25%以上或出现新病灶;稳定:肿瘤缩小不足50%,或增大不超过25%,无新病灶出现,维持4周以上,但未达部分缓解,或虽有增加但未达进展。总有效率=(完全缓解+部分缓解)例数/总例数×100%。
1.3.2毒性反应评价标准 毒性反应评价按照WHO抗癌药物急性与亚急性毒性表现和分级标准[6]及RTOG急性放射损伤标准[7]进行观察记录,分为0~Ⅳ度(表2、3)。
1.4统计学方法 应用SPSS 13.0软件行统计学分析,生存率比较采用Log-rank检验,计数资料比较采用χ2检验,等级资料比较采用秩和检验,P<0.05为差异有统计学意义。

表2 抗肿瘤药物毒性反应分级标准

表3 RTOG急性放射损伤标准
RTOG:美国放射肿瘤协作组
2 结 果
2.1两组中晚期食管癌患者近期临床疗效的比较 治疗后2个月内试验组总有效率为87.5%(35/40),对照组总有效率为68.4%(26/38),试验组临床疗效显著优于对照组,差异有统计学意义(u=2.365,P<0.05)(表4)。
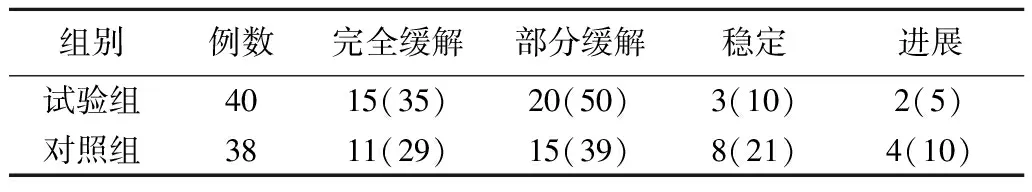
表4 两组中晚期食管癌患者近期临床疗效的比较 [例(%)]
试验组:采用洛铂+5-氟尿嘧啶+放疗;对照组:采用顺铂+5-氟尿嘧啶+放疗
2.2两组中晚期食管癌患者生存率的比较 试验组1年、2年、3年生存率分别为75%(30/40)、55%(22/40)、35%(14/40),对照组分别为65.8%(25/38)、39.5%(15/38)、21.1%(8/38),两组生存率比较差异有统计学意义(χ2=4.026,P=0.045)(图1)。
2.3两组中晚期食管癌患者毒性反应的比较 试验组恶心、呕吐发生率均显著低于对照组(P<0.05),但血小板减少发生率显著高于对照组(P<0.05);两组白细胞减少及放射性食管炎发生率比较差异无统计学意义(P>0.05)。全部毒性反应均可以耐受,对症处理后未影响治疗(表5)。
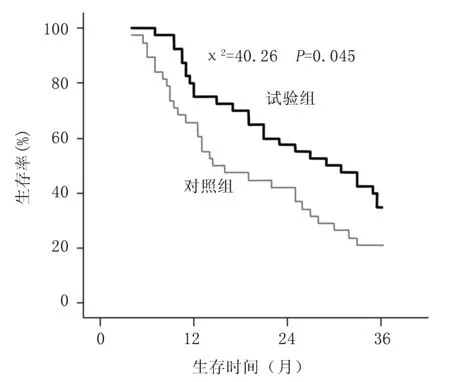
图1 两组中晚期食管癌患者治疗后生存率曲线比较
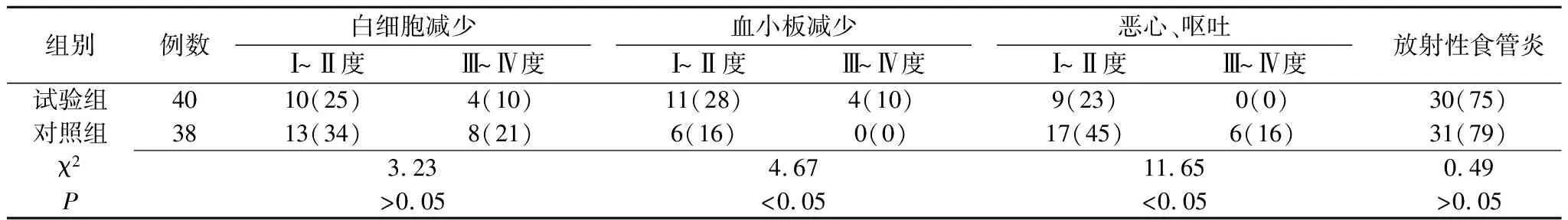
表5 两组中晚期食管癌患者治疗后毒性反应的比较 [例(%)]
试验组:采用洛铂+5-氟尿嘧啶+放疗;对照组:采用顺铂+5-氟尿嘧啶+放疗
3 讨 论
放疗是中晚期食管癌的主要治疗手段,但单纯放疗疗效很差,主要死亡原因为局部未控、复发和远处转移[8]。放化疗联合可产生疗效相加或协同作用,且化疗对远处转移的治疗作用可弥补放疗的局限性。RTOG-8501随机临床试验推动了同期放化疗应用于食管癌治疗。顺铂+5-FU联合放疗治疗中晚期食管癌的疗效确切且稳定,但顺铂毒性反应较大,部分患者使用后生活质量较差。洛铂是德国ASAT公司研制的第三代铂类抗肿瘤药物,国外文献报道其与顺铂、卡铂作用相当或更好,但肾毒性和消化道反应较轻[9]。
本研究结果显示,试验组总有效率高于对照组(87.5% vs 68.4%)(P<0.05),试验组1年、2年、3年生存率均高于对照组(P=0.045),提示试验组方案较对照组可提高生存率。
从毒性反应上看,主要为急性放射性食管炎、消化道反应、骨髓抑制。试验组、对照组急性放射性食管炎的发生率分别为75%、79%,与李巧巧等[10]报道的结果相似。但本研究中主要为Ⅰ~Ⅱ度,未发现Ⅲ度以上放射性食管炎的发生,严重放射性食管炎的发生率低于预期估计。所有患者在积极应用激素、抗生素和局部麻醉药等治疗后症状即可停止。试验组较对照组未能显著降低急性放射性食管炎的发生率,试验组恶心、呕吐发生率显著低于对照组,且试验组未出现Ⅲ度以上恶心、呕吐,对照组Ⅲ度以上出现6例,所有患者在给予格拉司琼、阿扎司琼等对症处理后明显缓解,提示洛铂消化道反应显著低于顺铂,结果与国外文献报道[9]相同。两组患者白细胞减少发生率比较差异无统计学意义,当白细胞低于4.0×109/L,给予重组人粒细胞集落刺激因子处理后白细胞均升至正常范围内。而且持续时间短,未出现中性粒细胞减少性发热和出血。血小板减少为洛铂的剂量限制性毒性[11],与肌酐清除有关。试验组血小板减少发生率为37.5%,低于杨柳青等[12]报道的45.5%。其中,Ⅲ度血小板减少发生率为10%,无Ⅳ度血小板下降发生,试验组显著高于对照组。当血小板低于100×109/L时,使用重组人血小板生成素或白细胞介素11对症治疗;当血小板低于50×109/L时,给予输注血小板悬液。未发现其他明显毒性反应。全部患者均能耐受毒性反应,按计划顺利完成放疗和两疗程化疗。两组中均未出现因为严重难以耐受毒性反应而终止治疗的患者,也没有出现治疗相关性死亡的病例。
综上所述,洛铂+5-FU联合放疗治疗中晚期食管癌疗效肯定、安全,可以显著提高有效率、生存率,为中晚期食管癌的患者提供了一种新的选择。若同期放化疗时采用三维适形放疗,且对化疗方案进行更加合理化的改进,预期应能取得更好的疗效。由于洛铂在国内上市不久,还需进一步累积病例和进行长期的临床观察,以确定放疗及药物对患者的最佳剂量,以及最佳的放化疗联合方案。
[1] Herskovic A,Martz-Mclo JR,Al-sarraf M,etal.Combined chenotherapy and radiotherapy compared with radiotherapy alone in patients with esophageal cancer[J].N Engl J Med,1992,326(24):1593-1598.
[2] 田大龙.中晚期食管癌放疗和联合化疗112例的随机研究[J].中国临床医学,2000,7(4):409-410.
[3] 吴剑,戴慧,翁欣然,等.小剂量顺铂对中晚期食管癌放疗增敏食管癌放疗增敏作用的近期疗效观察[J].中国肿瘤临床,2006,33(13):768-770.
[4] Schmoll HJ,Kohne CH,Papageorion E,etal.Single agent lobaplatin is active in patients with esophageal squamous cell carcinoma:a phase Ⅱ evaluation[J].Proc Am Soc Clin Oncol,1995,14:483.
[5] 刘明,李彩英,万欣,等.304例放疗为主的食管癌CT分期研究[J].中华放射肿瘤学杂志,2004,13(1):18-20.
[6] 孙燕,周际昌.临床肿瘤内科手册[M].4版.北京:人民卫生出版社,2003:106-107,274-276.
[7] 殷蔚伯,余子豪,徐国镇,等.肿瘤放射治疗学[M].4版.北京:中国协和医科大学出版社,2008:1350-1351.
[8] Brenner B,Ilson DH,Minsky BD.Treatment of localized esophageal cancer[J].Semin Oncol,2004,31(4):554-565.
[9] Mckeage MJ.Lobaplatin:a new antitumour platinum drug[J].Expert Opin Investing Drugs,2001,10(1):119-128.
[10] 李巧巧,胡永红,刘孟忠,等.放疗同期多西紫杉醇和顺铂化疗不能手术食管癌的疗效观察[J].中华放射肿瘤学杂志,2009,18(5):279-382.
[11] 刘秀峰.洛铂的临床研究进展[J].临床肿瘤学杂志,2006,11(7):549-552.
[12] 杨柳青,秦叔逵,钱军,等.洛铂联合醛氢叶酸、氟尿嘧啶治疗晚期食管癌的多中心Ⅱ期临床研究[J].临床肿瘤学杂志,2006,11(12):895-897.
