玉米芯废液中纯化L阿拉伯糖的研究
2014-03-23,,,
, , ,
(福建师范大学生命科学学院,福建福州 350108)
玉米芯废液是提取过木糖之后的副产品,是较为丰富而廉价的可利用资源,所以采用玉米芯废液的成本远小于玉米芯原料。玉米皮经稀硫酸水解后得到了以L- 阿拉伯糖、木糖和葡萄糖为主要成分的水解液[1]。L- 阿拉伯糖属于五碳醛糖,以L- 阿拉伯聚糖、L- 阿拉伯糖基本聚糖、L- 阿拉伯糖基半乳糖体及类似于高等植物半纤维的形式存在[2]。L- 阿拉伯糖是一种新型的无热量功能性糖,对传统糖类的吸收有竞争性阻断作用[3]。L- 阿拉伯糖是一种重要的医药中间体,可用来合成抗癌、抗病毒和治疗心血管疾病的药物[4 - 5]。其最显著的作用是抑制人体小肠内蔗糖酶的活性,降低蔗糖的分解,从而调节人体对蔗糖的过量吸收并抑制新脂肪的形成。其在减肥,控制糖尿病等方面的应用前景很好[6 - 7]。然而自然界中阿拉伯糖含量较低,尤以玉米芯、甜菜根等植物中含量较高[1]。但是L- 阿拉伯糖的纯度达到一定的级别方可作为食品食用,所以研究L- 阿拉伯糖的提取及分离纯化有重要意义。常见的提取方法包括水酸提取法、碱提取法[8 - 9]、酶提取法[10]、微生物发酵法[11]、化学合成法[12]及高压蒸汽法[13]等。现对提取过木糖醇的玉米芯废液用酸解法得到含L- 阿拉伯糖混合液,再通过旋转蒸发浓缩、活性炭脱色、无水乙醇去无机盐离子并采用响应面分析法得到较纯的L- 阿拉伯糖晶体的最佳条件[14]。该方法简便、效率高。
1 材料与方法
1. 1 材料与仪器
提取木糖醇后的玉米芯废液 河南某生物公司;L- 阿拉伯糖标准品 国药集团化学试剂有限公司。
4. 00%、5. 00%、6. 00%的浓硫酸、活性炭、氢氧化钠、盐酸、冰醋酸、三氯化铁 国药集团化学试剂有限公司;3,5 - 二羟基甲苯 北京鼎国昌盛生物技术有限公司。
电子天平 精确度0. 0001g,上海精密仪器公司;手掌式离心机 海门其林贝尔制造公司;电热鼓风干燥箱 福建裕华化玻有限公司;紫外分光光度计、THZ - C恒温振荡器 江苏省太仓市实验设备厂;HJ - 6多头加热磁力旋转器 常州国华电器有限公司。
1. 2 实验方法
1. 2. 1 显色剂的制备 参考文献[15],A:称取3,5 - 二羟基甲苯适量,用盐酸 - 冰醋酸(1∶ 3)的混合液溶解,配成浓度为0. 1 %的3,5 - 二羟基甲苯溶液;B:配1mol·L-1的三氯化铁溶液。临用前,取A溶液99mL与B溶液1mL混合,摇匀,即得3,5 - 二羟基甲苯三氯化铁显色剂。
1. 2. 2 酸解法提取L- 阿拉伯糖
1. 2. 2. 1L- 阿拉伯糖的提取 取提取过木糖醇的玉米芯废液30mL,加入5. 00%硫酸300mL,95. 00℃水浴2. 00h[16]。抽滤,取其滤液,用旋转蒸发仪将滤液浓缩至30mL转移至烧杯中。在80. 00℃水浴中预热5min,将烧杯取出,加入液体体积1%的活性炭,搅拌脱色约10 ~ 15min。往脱色后的浓缩液中加入其4倍体积的无水乙醇进行低温结晶,静置过夜。次日,将上述的无水乙醇用吸管吸干,再将其在56℃的烘箱内烘干。向烘干后的固体里加入100mL的无水乙醇除去其中的无机盐离子。最后除去无水乙醇即得到粗的L- 阿拉伯糖。
1. 2. 2. 2 标准曲线的绘制 分别吸取2、4、6、8mL的L- 阿拉伯糖对照品(54. 120μg·mL-1)置于容量瓶中,补加蒸馏水稀释到10mL,配成浓度分别为10. 824、21. 648、32. 472、43. 296μg·mL-1的对照品溶液。吸取上述对照品溶液1mL,加入3,5 - 2二羟基甲苯三氯化铁显色剂4mL,充分混匀,置沸水浴中加热30min后迅速放入冰水中冷却到室温,在665nm处测定吸收度。以对照品浓度为横坐标,吸收度为纵坐标绘制工作曲线。
1. 2. 2. 3 实验样品中L- 阿拉伯糖含量的测定 取0. 005g粗提的阿拉伯糖样品,配制成500μg·mL-1的母液,再稀释成所需的浓度(100、200、400μg·mL-1)。精密吸取上述对照品溶液1mL,加入3,5 - 2二羟基甲苯三氯化铁显色剂4mL,充分混匀,置沸水浴中加热30min 后迅速放入冰水中冷却到室温,在665nm处测定吸收度。根据标准曲线计算出样品中L- 阿拉伯糖的含量。
1. 2. 3 酸解法分离纯化L- 阿拉伯糖条件的优化
1. 2. 3. 1 硫酸水解玉米芯工业废液中L- 阿拉伯糖的单因素预实验 通过单因素预实验,确定硫酸浓度、硫酸用量、水解时间、水解温度并进行单因素实验。
1. 2. 3. 2 硫酸浓度对L- 阿拉伯糖含量的影响 准确量取5份玉米芯工业废液5mL,硫酸∶ 玉米芯废液为10. 00∶ 1,温度为90. 00℃,水解时间为2. 50h,考察不同硫酸浓度对玉米皮中L- 阿拉伯糖含量的影响。
1. 2. 3. 3 硫酸∶ 玉米芯废液对L- 阿拉伯糖含量的影响 准确量取5份玉米芯工业废液5mL,硫酸浓度为5. 00%,温度为90. 00℃,水解时间为2. 50h,计算不同硫酸∶ 玉米芯废液对玉米皮中L- 阿拉伯糖水解含量的影响。
1. 2. 3. 4 水解温度对L- 阿拉伯糖含量的影响 准确量取5份玉米芯工业废液5mL,硫酸浓度为5. 00%,硫酸∶ 玉米芯废液为10∶ 1,水解时间2. 50h,考察不同水解温度对玉米皮中L- 阿拉伯糖水解含量的影响情况。
1. 2. 3. 5 水解时间对L- 阿拉伯糖含量的影响 准确量取5份玉米芯工业废液5mL,硫酸浓度为5. 00%,温度为90. 00℃,硫酸∶ 玉米芯废液为10. 00∶ 1,不同水解时间为1. 00、1. 50、2. 00、2. 50、3. 00h对玉米皮中L- 阿拉伯糖水解含量的影响。
1. 2. 4 应用响应面分析法优化L- 阿拉伯糖的分离纯化条件 应用Design - Expert. 8. 05b响应面分析软件提供的模型,设硫酸浓度(A)、硫酸∶ 玉米芯废液(B)、水解温度(C)、水解时间(D)4个因素为自变量,L- 阿拉伯糖水解得率为响应值,设计四因素三水平的实验,并根据单因素实验结果选定三因素的零水平和波动区。实验因素与水平的取值表见表1。
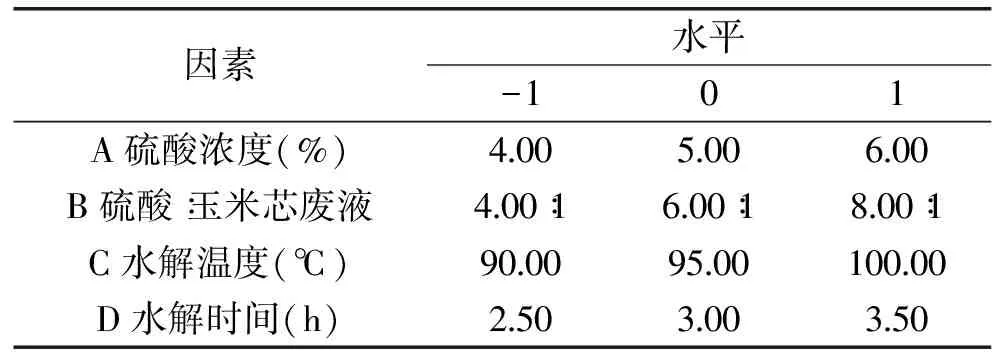
表1 响应面因素水平编码表Table 1 Factors and levels of response surface test
2 结果与分析
2. 1 实验样品中L - 阿拉伯糖含量标准曲线
以对照品浓度为横坐标,吸光度为纵坐标绘制工作曲线。回归方程为y=0. 0242x+0. 0035,R2为0. 9984,在10. 824 ~ 54. 120μg·mL-1范围内呈线形关系。
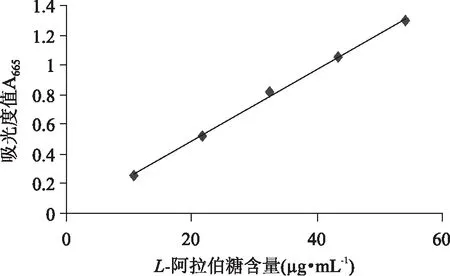
图1 L - 阿拉伯糖含量标准曲线Fig. 1 Standard curve of L - arabinose content
2. 2 硫酸浓度对L - 阿拉伯糖含量的影响
图2为不同硫酸浓度对玉米皮中L- 阿拉伯糖含量的影响。当硫酸浓度为5. 00%时,L- 阿拉伯糖水解后含量达到最大值12. 97μg·mL-1,再增大硫酸浓度,L- 阿拉伯糖的含量不再增加反而下降。这可能是因为在高温下增大酸的浓度加剧了其他副反应的发生,比如玉米芯废液中残留的部分木糖脱水生成了糠醛[5]。随硫酸浓度的提高,水解液的颜色变深,这给活性炭脱色处理带来难度。
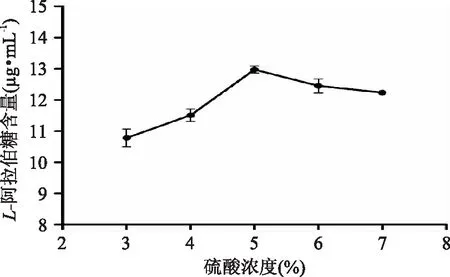
图2 硫酸浓度对L - 阿拉伯糖纯化的影响Fig. 2 Effect of sulfuric acid concentration on the L - arabinose purification
2. 3 硫酸用量对玉米芯废液中L - 阿拉伯糖含量的影响
不同的硫酸用量对玉米皮中L- 阿拉伯糖水解后含量的影响如图3所示。当硫酸用量为玉米芯工业废液体积的6倍时水解程度达到最高,继续增大硫酸用量L- 阿拉伯糖的含量反而下降。如图3所示,硫酸∶ 玉米芯废液为4. 00∶ 1时,原料可能未能被充分被浸泡,很大一部分玉米芯废液未能参与酸解反应,因而L- 阿拉伯糖含量较低。硫酸∶ 玉米芯废液增大至6. 00∶ 1,含量迅速上升,达到最大值。硫酸:玉米芯废液继续增加,L- 阿拉伯糖含量反而减小。
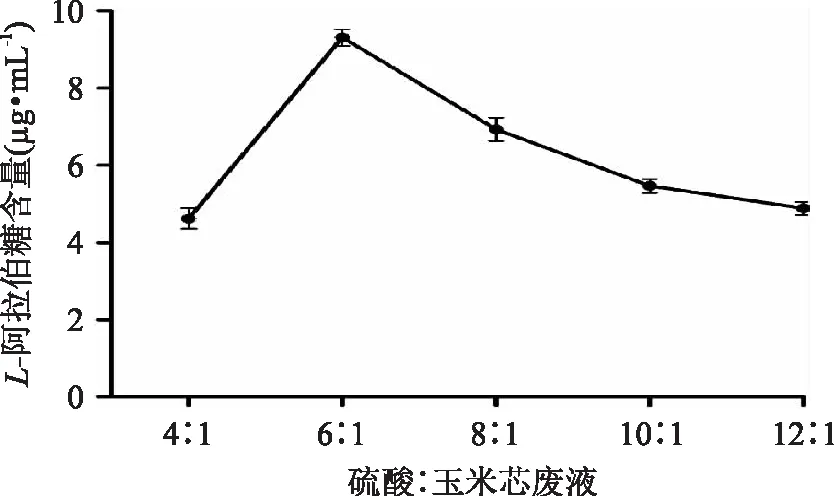
图3 硫酸∶ 玉米芯废液对L - 阿拉伯糖纯化的影响Fig. 3 Effect of sulfuric acid:corncob waste on the L - arabinose purification
2. 4 水解温度对L - 阿拉伯糖含量的影响
不同水解温度对玉米皮中L- 阿拉伯糖水解后含量的影响情况如图4所示:温度升高有利于加速玉米芯废液酸解生成单糖,L- 阿拉伯糖含量也随之增高,当温度达到95. 00℃时,L- 阿拉伯糖含量基本达到最大值;在100. 00℃时L- 阿拉伯糖含量有下降的趋势,这可能是在高温和酸催化下,部分玉米芯废液酸解产生其他副产物(木糖脱水生成了糠醛)。因此,选取反应温度95. 00℃为最佳水解温度。
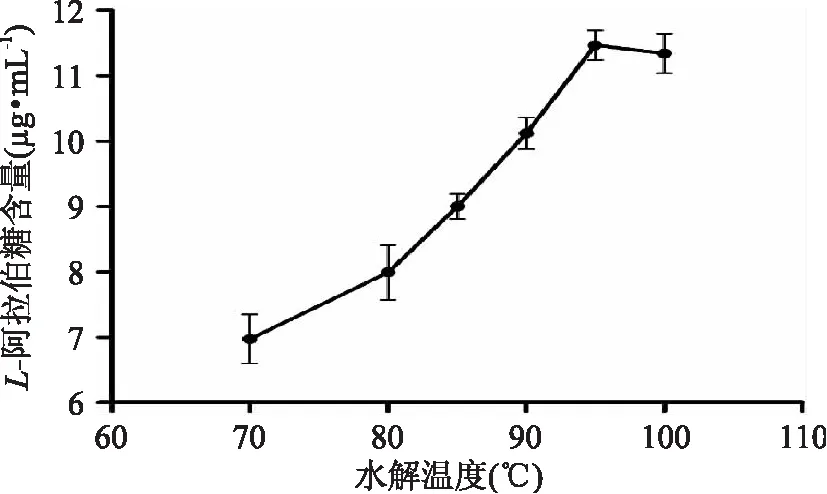
图4 水解温度对L - 阿拉伯糖纯化的影响Fig. 4 Effect of hydrolysis temperature on the L - arabinose purification
2. 5 水解时间对L - 阿拉伯糖含量的影响
不同水解时间为1. 00、1. 50、2. 00、2. 50、3. 00h时对玉米芯废液中L- 阿拉伯糖水解后含量的影响如图5所示。L- 阿拉伯糖含量随着水解时间的增加呈现先增后减的趋势,3. 00h时L- 阿拉伯糖含量达到最大值。随着时间的增加,会使酸解液颜色更深,对于下面的脱色更难,所以选择3. 00h作为最佳酸解时间。水解时间为2. 50h和3. 00h时,测量误差较大,可能原因是水解时间的增加,使得酸解更彻底,使得玉米芯废液中残留的部分木糖脱水生成了糠醛[5],在测定L- 阿拉伯糖含量时造成较大的误差。
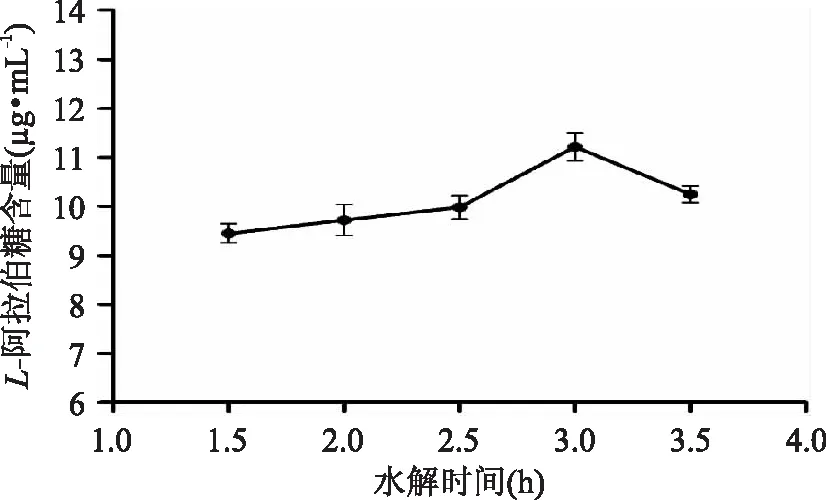
图5 水解时间对阿拉伯糖纯化的影响Fig. 5 Effect of hydrolysis time on the L - arabinose purification
2. 6 响应面实验结果分析
2. 6. 1 实验结果 Box - Benhnken四因素三水平实验所得L- 阿拉伯糖含量见表2,模型共设29个实验,其中16、18、20、21、24号实验为中心实验,其余的为析因实验。析因实验构成三维定点,中心实验为区域的中心,重复五次中心实验以估计误差。
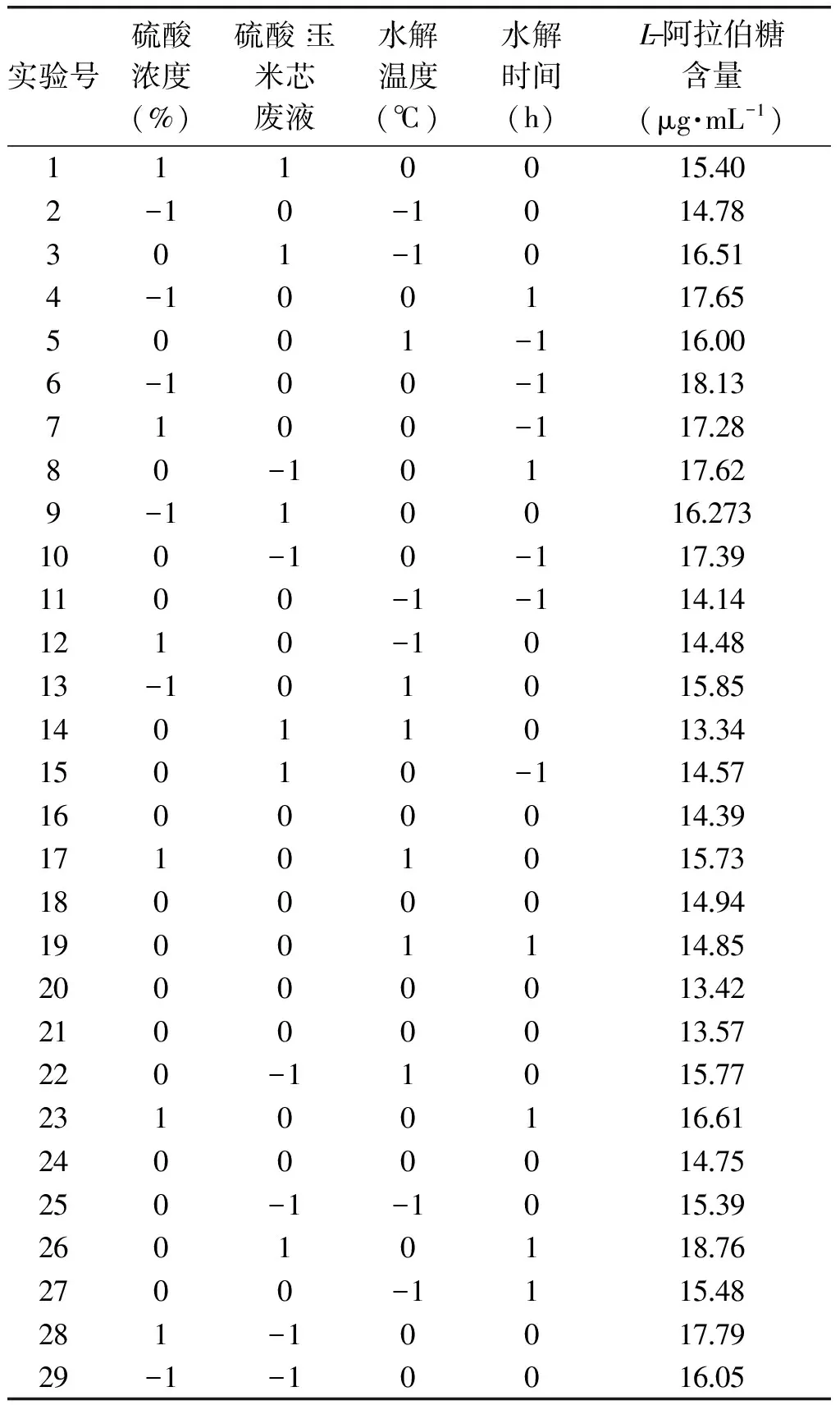
表2 响应面实验设计及结果Table 2 The response surface experimental design and results
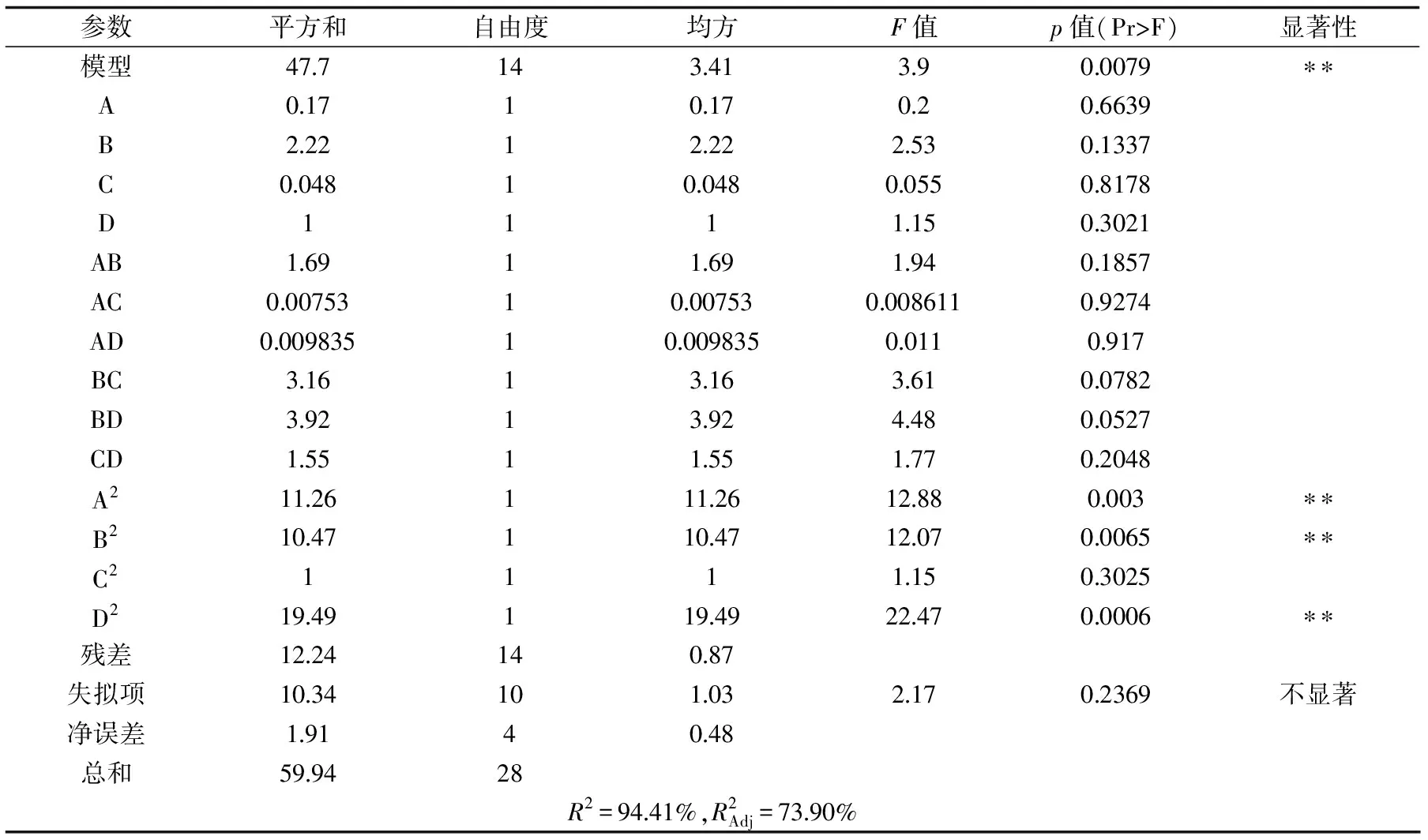
表3 回归分析结果Table 3 The results of regression analysis
注:*差异性显著(p<0. 05),* *差异性极显著(p<0. 01)。
2. 6. 2 模型建立 利用Design - Expert8. 0. 5b软件对实验结果进行多元拟合,得到硫酸浓度(A)、硫酸:玉米芯废液(B)、水解温度(C)、水解时间(D)二次多项回归方程:L- 阿拉伯糖含量=14. 22 - 0. 12A - 0. 43B+0. 063C+0. 29D - 0. 65AB+0. 043AC - 0. 050AD -0. 89BC+0. 99BD - 0. 62CD+1. 32A2+1. 17B2- 0. 39C2+1. 63D2
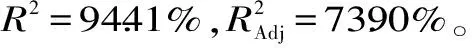
2. 6. 4 响应面分析 为了更直观地反映四个因素之间的相互作用对提取含量的影响,做出两两自变量为坐标的3D图。由图6可知,L- 阿拉伯糖提取量曲线呈现出先上升到平缓稳定再到略有下降的状态。 随着硫酸浓度(A)的升高与硫酸∶ 玉米芯废液(B)增加,提取量上升。当硫酸浓度、硫酸∶ 玉米芯废液分别增大到一定程度时,提取量(Y)趋于饱和,响应曲面变平缓,随后若再同时增大硫酸浓度、硫酸∶ 玉米芯废液时,提取量会略有下降。因此,最佳取值点应取在L- 阿拉伯糖提取量最高点,即L- 阿拉伯糖提取量不再显著增高的坐标点处。图7 ~ 图11反映出的结果与图6类似。但是图9中水解温度的变化对L- 阿拉伯糖提取量交互影响不大。图6 - 图11可得各因素的交互作用不显著。通过计算本实验的回归方程,可得到四个因素的最佳作用值。
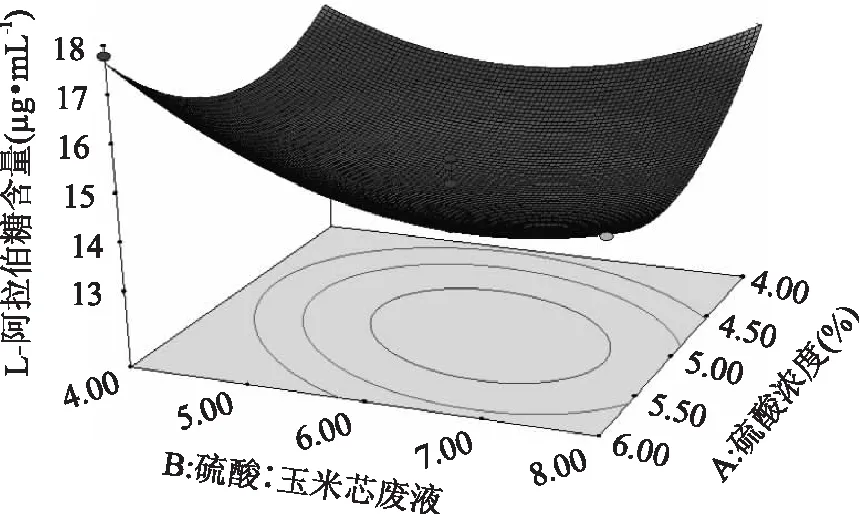
图6 硫酸浓度与硫酸∶ 玉米芯废液交互作用对L - 阿拉伯糖提取量影响的响应面等高线图Fig. 6 Response surface contour map for concentration of sulfuric acid and sulfuric acid∶ corncobwaste interaction on L - arabinose extraction
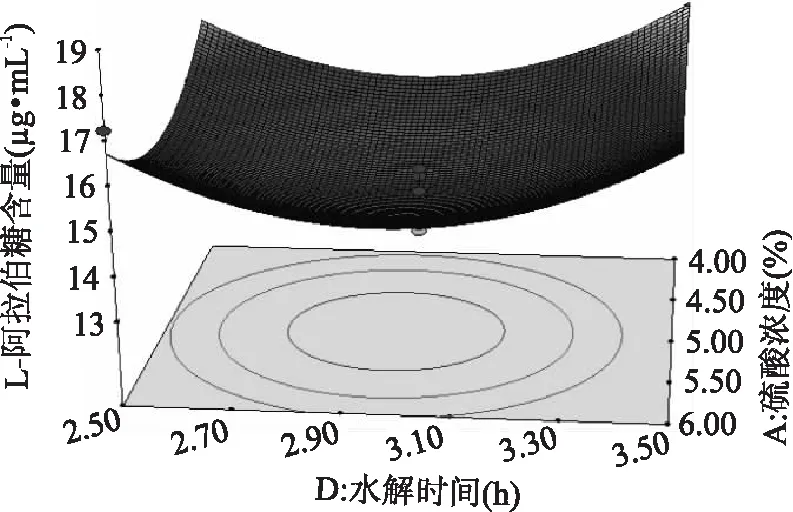
图7 硫酸浓度与水解时间交互作用对L - 阿拉伯糖提取量影响的响应面等高线图Fig. 7 Response surface contour map for concentration of sulfuric acid and hydrolysis time interaction on L - arabinose extraction
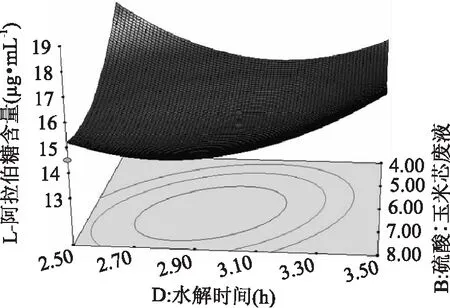
图8 硫酸∶ 玉米芯废液与水解时间交互作用对L - 阿拉伯糖提取量影响的响应面等高线图Fig. 8 Response surface contour map for sulfuric acid∶ corncob waste and hydrolysis time interaction on L - arabinose extraction
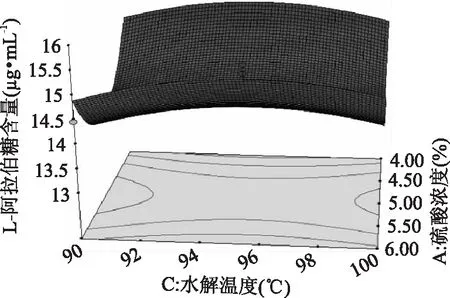
图9 硫酸浓度与水解温度交互作用对L - 阿拉伯糖提取量影响的响应面等高线图Fig. 9 Response surface contour map for concentration of sulfuric acid and hydrolysis temperature interaction on L - arabinose extraction
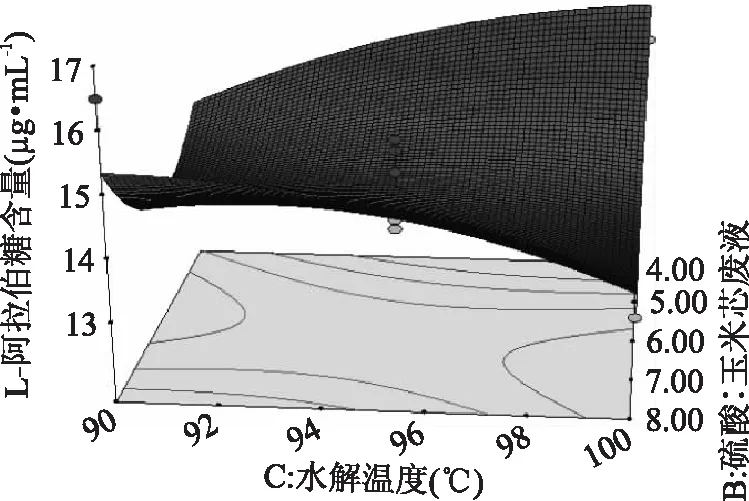
图10 硫酸:玉米芯废液与水解温度交互作用对L - 阿拉伯糖提取量影响的响应面等高线图Fig. 10 Response surface contour map for sulfuric acid∶ corncob waste and hydrolysis temperature interaction on L - arabinose extraction
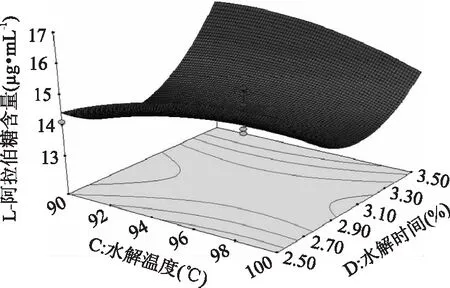
图11 水解时间与水解温度交互作用对L - 阿拉伯糖提取量影响的响应面等高线图Fig. 11 Response surface contour map for hydrolysis time and hydrolysis temperature interaction on L - arabinose extraction
为了确定各因素的最优值,利用软件分析得L- 阿拉伯糖的含量最高的实验条件如表3所示:
我们通过Design - Expert. 8. 05软件分析,最佳的分离纯化工艺是硫酸浓度6. 00%,硫酸∶ 玉米芯废液4. 01∶ 1,水解温度100. 00℃,水解时间2. 50h,阿拉伯糖的含量可达21. 25μg·mL-1。为了检验响应面分析法的可行性,采用得到的最佳提取条件进行L- 阿拉伯糖的含量提取的验证实验,同时考虑到实际操作和生产的便利,以硫酸浓度6. 00%、硫酸∶ 玉米芯废液4. 00∶ 1、水解时间2. 50h、水解温度100. 00℃为最佳。3次平行实验得到的实际平均提取含量为20. 86μg·mL-1,与理论值相差1. 84%。因此,响应面法对L- 阿拉伯糖含量提取条件的优化是可行的,得到的L- 阿拉伯糖提取条件具有实际应用价值。
3 结论
根据响应面分析可知,影响从玉米芯工业废液中分离制备L- 阿拉伯糖的显著工艺条件为:水解温度、水解时间、硫酸浓度,硫酸与玉米芯工业废液的体积比。最后确定的最佳工艺条件为水解温度100. 00℃,纾解时间2. 50h,硫酸浓度6. 00%,硫酸与玉米芯工业废液的体积比4. 00∶ 1,此时L- 阿拉伯糖的含量为20. 86μg·mL-1。此次探讨的工艺对玉米芯工业废液中制备L- 阿拉伯糖的提取率和纯度有显著提高。从玉米芯废液中提取L- 阿拉伯糖的得率达到20. 86μg·mL-1对于开拓L- 阿拉伯糖的市场有很大前景,并对其作用机理的研究也有一定的推动作用。
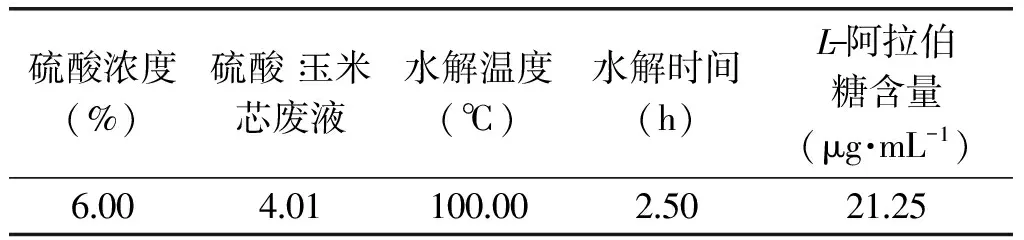
表3 响应面分析获得的最佳纯化工艺条件Table 3 The best purification process conditions obtained from response surface analysis
[1]魏承厚,雷光鸿,张帆,等. 资源化利用磷酸制备D - 木糖和L- 阿拉伯糖的研究[J]. 轻工科技:制糖工程与技术,2014,2:25 - 27.
[2]Forsman J,Leino R.L- Pentoses in biological and medicinal applications[J]. Chemical Reviews,2011,111:3334 - 3357.
[3]周春丽,刘华,李玉萍. 功能性五碳糖的生产及应用研究[J]. 食品工业,2013,34(5):195 - 198.
[4]Helanto M,Kiviharju K,Granström T,etal. Biotechnological production of l - ribose from L - arabinose[J]. Applied Microbiology and Biotechnology,2009,83(1):77 - 83.
[5]陈军,王元春. 蔗髓制备木糖、L- 阿拉伯糖的工艺优化[J].食品科技,2011,36(11):237 - 240.
[6]周俊,徐畅,浦佳. 微生物酶解法产生阿拉伯糖 - 菌种筛选与初步鉴定[J]. 氨基酸和生物资源,2010,32(4):73 - 76.
[7]桂堂辉,何成新,李赐玉.L- 阿拉伯糖对降低高糖高脂喂养小鼠体重增长速率的影响[J]. 广西植物,2010,3(2):280 - 283.
[8]苏会波,林海龙. 新资源食品L- 阿拉伯糖的制备、功能、应用和市场现状[J]. 食品工业科技,2014,35(7):368 - 372.
[9]李雪雁,王丹,胡朝霞,等. 玉米芯酸法提取木糖的工艺改进[J]. 食品工业科技,2009,30(6):263 - 265.
[10]詹伊婧,徐铮,许露,等.L- 核糖的生产研究进展[J]. 生物加工工程,2013,11(5):74 - 78.
[11]邹鸿菲,张泽生,郑敏. 微生物分离玉米皮水解液中L- 阿拉伯糖的研究[J]. 食品工业科技,2012,33(12):214 - 220.
[12]Kim K S,Moon C W,Park J,etal. Enantiopure synthesis of carbohydrates mediated by oxyselenenylation of 3,4 - dihydro - 2H- pyran[J]. J Chem Soc Perkin Trans,2000,1(9):1341 - 1343.
[13]Toeda K,Kawabata Y. Production of L - arabinose from corn hull and beet pulp by high pressure steaming[J]. Journal of the Japanese Society for Food Science and Technology,2002,49(8):551 - 554.
[14]李令平,周娟,邱学良. 玉米皮酸解提取L- 阿拉伯糖的工艺研究[J]. 中国食品添加剂开发应用,2009,6:139 - 142.
[15]王晓雷,徐梦丹. 黄芪多糖中阿拉伯糖含量的测定[J]. 中成药,2003,25(11):925 - 926.
[16]梁智. 浅析L- 阿拉伯糖化学[J]广西轻工业,2011,4:4 - 5.
