脉脂康胶囊制备工艺研究
2014-03-20张留记屠万倩孙丹丹
周 丽,张留记,屠万倩,孙丹丹
(1.河南中医学院2011 级硕士研究生,河南 郑州450008;2.河南省中医药研究院,河南郑州450004)
近年来,随着人民生活水平的提高,高脂血症的发病率逐年上升,且有患者年轻化的趋势[1]。脉脂康胶囊为河南省中医药研究院附属医院制剂室研制品种,由人参、川芎、当归、山楂、制何首乌等5 味中药组成。全方标本兼治,通补结合,具有益气补血[2]、活血化瘀[3-4]、健脾化积[5]、降脂通便[6-7]等功能,适用于高脂血症人群,对动脉粥样硬化、冠心病等心血管疾病具有较好的预防保健作用。本研究根据文献资料所报道的各药味有效成分的特性及相关药理作用,设计实验,以期优选出脉脂康胶囊的最佳提取工艺。
1 药品、试剂与仪器
人参皂苷Rb1对照品(批号110704 -200318)、人参皂苷Re 对照品(批号110754 -200421,含量测定用对照品)、人参皂苷Rg1对照品(批号110703-200323,含量测定用对照品)、2,3,5,4'-四羟基二苯乙烯-2-O-β-D 葡萄糖苷对照品(批号110844 -200404,含量测定用对照品),均购自中国药品生物制品检验所。甲醇、乙腈均为色谱纯,均购自德国Merck 公司;其他试剂均为分析纯;蒸馏水购自郑州市大成蒸馏水厂;重蒸水为自制。Waters 2695 高效液相色谱仪(2996 紫外检测器,Empower Ⅱ色谱工作站软件),美国Waters 公司产品;恒温水浴锅,北京中兴伟业仪器有限公司产品;GT -350W 超声波提取器,济宁科技超声电子有限公司产品;日本岛津LIBROR-160DPT 万分之一天平,产地日本;Mettler Toledo 十万分之一天平,产地瑞士;DZTW 调温电热套,北京永光明医疗仪器厂产品;挥发油提取器,上海玻璃仪器厂产品;DL-1 万用电炉,北京中兴伟业仪器有限公司产品;101 -2 电热恒温鼓风干燥箱,上海市实验仪器厂产品。
2 方法与结果
2.1 山楂、人参乙醇提取工艺的考察
2.1.1 乙醇提取工艺条件正交试验法优选
在乙醇提取工艺研究中,选取乙醇浓度、乙醇用量、提取时间、提取次数4 个主要影响因素,每个因素选择3 个水平,按照L9(34)表进行正交试验。见表1。以人参皂苷Rb1、Rg1和Re 为测定指标优选最佳提取工艺。

表1 乙醇提取工艺因素水平表
按处方比例称取山楂和人参,采用L9(34)正交试验表,按各试验号参数进行实验,提取液过滤,滤液浓缩至无醇味,转移至100 mL 量瓶中,加水稀释至刻度,即得1 ~9 号乙醇提取液。
2.1.2 乙醇提取液中人参皂苷Rb1、Rg1和Re 的含量测定
色谱条件:色谱柱为美国热电Hypersil C18ODS填料柱(4.6 mm×250 mm,5 μm);流动相为乙腈—水溶液系统,梯度洗脱,梯度洗脱程序见表2;体积流量1.0 mL/min;检测波长203 nm;柱温40 ℃;理论塔板数按人参皂苷Rg1峰计算应不低于3 000。对照品和供试品色谱图见图1、图2。

表2 梯度洗脱时间程序
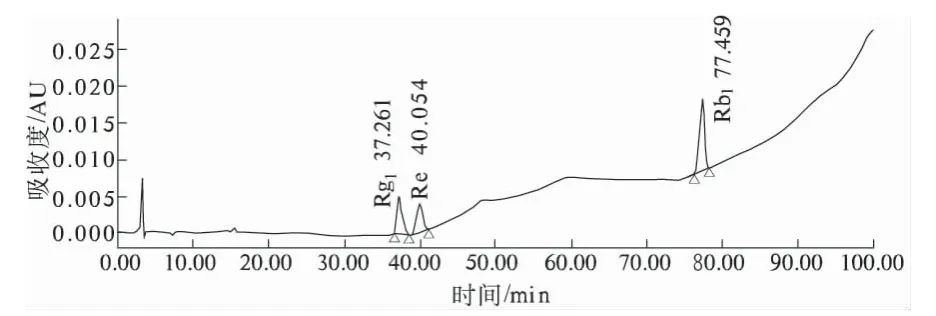
图1 人参皂苷(Rg1、Re、Rb1)对照品HPLC 图
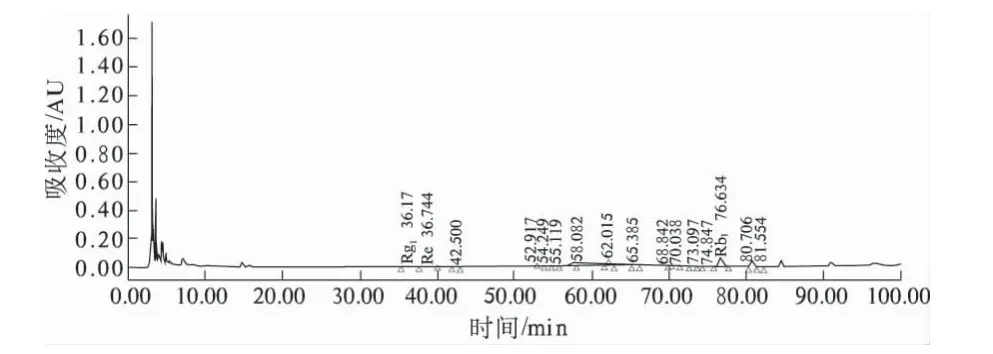
图2 人参乙醇提取供试品HPLC 图
对照品溶液的制备:精密称取人参皂苷Rb1、Rg1、Re 对照品2.9,1.39,1.10 mg,置5 mL 量瓶中,加甲醇溶解并定容至刻度,摇匀,制成每毫升含人参皂苷Rb10.580 mg、Rg10.278 mg、Re 0.220 mg 的混合溶液,即得。
标准曲线:精密吸取对照品溶液2,5,10,15,20 μL,分别注入液相色谱仪,按上述色谱条件测定人参皂苷Rb1、Rg1、Re 的吸收峰峰面积积分值,以进样量为横坐标(X),以峰面积积分值为纵坐标(Y),进行回归处理,结果见下表3。

表3 人参皂苷Rb1、Rg1、Re 线性范围考察
供试品溶液的制备及测定:分别精密吸取2.1.1项下1 ~9 号乙醇提取液各20 mL;用乙酸乙酯振摇提取4 次,每次20 mL;弃去乙酸乙酯液,水层用水饱和正丁醇振摇提取4 次,每次20 mL;合并正丁醇液;用体积分数40%的氨试液充分洗涤2 次,每次30 mL;弃去氨液;正丁醇液蒸干;残渣加甲醇溶解,移至5 mL 量瓶中;加甲醇稀释至刻度,摇匀,用0.45 μm 的微孔滤膜滤过,即得。精密吸取各供试品溶液10 μL 注入液相色谱仪,按照上述色谱条件进行测定,并计算提取液中人参皂苷Rb1、Rg1和Re的总含量,结果见表4。
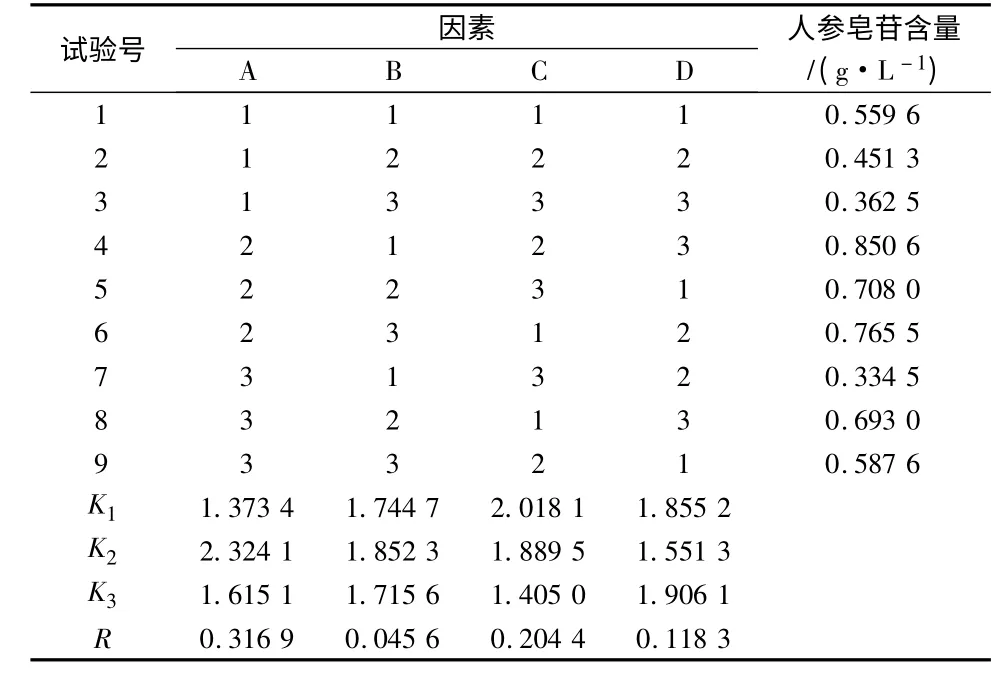
表4 乙醇提取正交试验设计和人参总皂苷含量测定结果
根据上表可知,因素B 的极差R 值最小,以B列为误差列,对正交试验结果进行方差分析,结果见表5。

表5 乙醇提取正交试验方差分析表
结果:由试验结果的直观分析和方差分析可知,在乙醇提取过程中对人参皂苷总含量影响因素的大小顺序为A >C >D >B,因素A、C 对试验结果均有显著性影响。根据正交试验结果,选取显著因素A、C的最佳水平,得到最佳工艺水平A2C1。次要因素B、D 均取第一水平,故山楂、人参乙醇提取的最佳条件为A2B1C1D1,即:山楂和人参用5 倍量750 g/L 乙醇,加热回流0.5 h 即可。
2.2 制何首乌等药材水提工艺的优选
以煎液中2,3,5,4'-四羟基二苯乙烯-2-O-β-D葡萄糖苷(以下简称二苯乙烯苷)含量为控制指标,采用L9(34)正交试验,对煎煮工艺的煎煮次数、煎煮时间、加水量和浸泡时间等主要影响因素进行考察,优选最佳工艺参数。
2.2.1 水煎煮工艺条件正交试验因素水平表见表6。
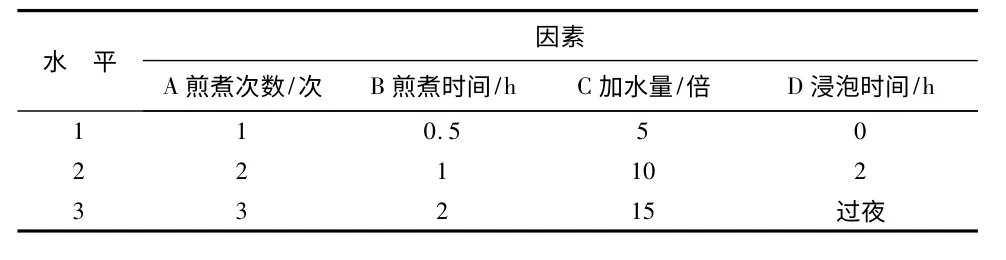
表6 煎煮工艺因素水平表
按脉脂康胶囊处方比例,称取人参、川芎、当归、山楂、制何首乌,川芎和当归加水蒸馏挥发油,人参、山楂按2.1.2 项下乙醇提取工艺方法进行提取,其药渣与制何首乌混合,采用L9(34)正交试验表,按各试验号参数进行实验,煎液滤过,合并,浓缩至约200 mL,完全转移至250 mL 量瓶中,加水至刻度,摇匀,即得1 ~9 号水煎提取液。
2.2.2 提取液中二苯乙烯苷的含量测定
色谱条件:色谱柱为美国热电Hypersil C18ODS填料柱(4.6 mm×250 mm,5 μm);流动相为乙腈—水(20∶80),体积流量1.0 mL/min;检测波长320 nm;柱温40 ℃;理论塔板数按二苯乙烯苷峰计算应不低于2 000。对照品和供试品色谱图见图3、图4。
对照品溶液的制备:精密称取二苯乙烯苷对照品2.665 mg,置50 mL 量瓶中,加甲醇溶解并定容至刻度,摇匀,制成每毫升含0.053 3 mg 的溶液,即得。
标准曲线:精密吸取对照品溶液2,4,6,8,10,12 μL,分别注入液相色谱仪,按上述色谱条件测定二苯乙烯苷吸收峰峰面积积分值,以进样量为横坐标(X),以峰面积积分为纵坐标(Y),进行回归处理。回归方程为Y =3.63 ×106X -3.79 ×104,r =0.999 8。结果提示:二苯乙烯苷在0. 106 6 ~0.629 6 μg 范围内,进样量与峰面积积分值呈良好的线性关系。
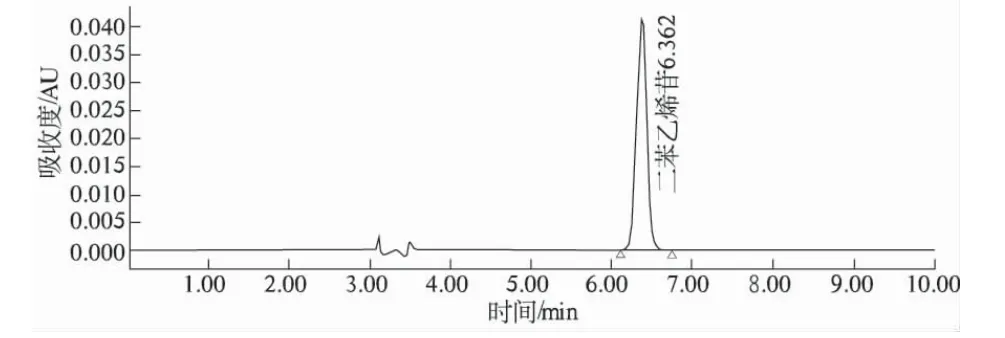
图3 二苯乙烯苷对照品HPLC 图
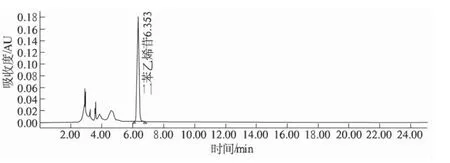
图4 供试品HPLC 图
供试品溶液的制备及测定:精密吸取2.2.1 项下1 ~9 号水煎煮正交实验提取液各5 mL,置25 mL量瓶中,缓缓滴加950 g/L 乙醇,振摇,稀释至刻度,静置,滤过,取续滤液,用0.45 μm 的微孔滤膜滤过,即得。精密吸取各供试品溶液2 μL,注入液相色谱仪,按照上述2.2.2 项下色谱条件进行测定计算提取液中二苯乙烯苷的含量。结果见表7。

表7 正交试验设计和二苯乙烯苷含量测定结果
由表7 可知,因素D 的极差R 值最小,以D 列做误差列,对正交试验结果进行方差分析,结果见表8。

表8 方差分析表
由表8 可知:对试验结果进行直观分析和统计分析,水煎煮提取过程中对二苯乙烯苷含量影响因素大小顺序依次为:B >A >C >D,其中因素B、A 对试验结果均有显著性影响。根据正交试验结果可知,最佳工艺条件为B3A2。影响因素C、D 对试验结果影响较小,不呈显著性,为节约生产成本、加快提取效率,加水量和浸泡时间均选择最低水平,即C、D 均取1 水平。因此,通过综合考虑,得到煎煮提取最佳工艺为:B3A2C1D1,即何首乌等药材加5 倍量水,不需浸泡,直接煎煮2 次,每次2 h。
2.3 浓缩干燥工艺考察
2.3.1 不同浓缩干燥方式样品的制备
按脉脂康胶囊处方比例,称取相同质量的药材2 份,分别按照优选出的最佳提取工艺进行提取。取1 份将乙醇提取液和水煎液混合浓缩至稠膏状,干燥;另一份乙醇提取液和水煎液分别浓缩至稠膏状,分别烘干后混合。
2.3.2 人参皂苷含量测定对比
色谱条件和对照品溶液的制备:按2.1.2 项下方法。
供试品溶液的制备及测定:分别取混合浓缩和单独浓缩的干膏适量,分别粉碎成细粉;取3 g 左右,精密称定,置索氏提取器中,用乙酸乙酯提取至无色,滤纸筒挥干溶剂,再用甲醇提取至无色,甲醇提取液蒸干;加20 mL 水溶解,用水饱和正丁醇每次20 mL 振摇提取5 次,合并正丁醇液;用体积分数40%的氨试液洗涤2 次,每次30 mL,弃去氨液,正丁醇液水浴蒸干;残渣用甲醇溶解至5 mL 的量瓶中,摇匀,用0.45 μm 的微孔滤膜滤过,即得。精密吸取供试品溶液30 μL,进行测定,计算混合浓缩和单独浓缩后混合的粉末中人参总皂苷的含量,结果见表9。结果表明:不同的浓缩干燥工艺对人参皂苷含量影响较大,混合浓缩干燥工艺的人参皂苷转移率明显低于单独浓缩方式。
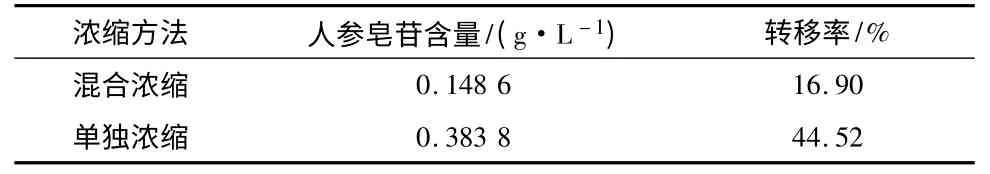
表9 干燥方式对人参总皂苷含量的结果对比
3 讨 论
3.1 工艺路线的拟定
脉脂康胶囊处方中的川芎、当归含有较多挥发油[8-9],应先蒸馏提取挥发油。人参中的主要活性成分人参皂苷类成分[10]。山楂中的主要活性成分总黄酮和有机酸等,均为脂溶性物质,乙醇溶解度较好,应先采用乙醇提取。制何首乌中的主要活性成分为二苯乙烯苷等苯乙醇苷类成分,易溶于水。制何首乌可与川芎、当归蒸馏挥发油后的药渣及人参、山楂乙醇提取后的药渣混合,采用加水煎煮的方法进行提取。乙醇和水煎煮提取液浓缩干燥后,粉碎,混匀,将挥发油喷于干燥粉末中,密封过夜,再低温烘干。
3.2 最佳提取工艺的确定
通过正交试验对山楂和人参的乙醇提取工艺、制何首乌等药材的水煎煮工艺分别进行优选,得出的最佳提取工艺参数为:山楂和人参加5 倍量的750 g/L 乙醇,加热回流提取1 次,0.5 h;何首乌等药材加10 倍量的水,不需浸泡,煎煮2 次,每次2 h。
3.3 不同浓缩干燥方式的比较
在浓缩干燥工艺方式研究中,主要考察了浓缩方式及出膏率。结果显示:混合浓缩对人参皂苷等有效成分的保留明显低于单独浓缩,应选择单独浓缩的方式;浓缩方式对出膏率无影响。通过本研究,确定了脉脂康胶囊的最佳制备工艺,对拟定的生产工艺进行3 批中试生产验证,结果证明所优选的生产工艺简单稳定,适合工业化生产。脉脂康胶囊工艺改进后,可减小服药量,并保证临床用药的安全有效性。
[1]王艳宁,张迪. 阿伐他汀片与辛伐他汀片治疗混合性高脂血症的成本效果分析[J]. 医学信息,2008,21(2):258 -260.
[2]张前进. 人参的化学成分和药理活性[J]. 光明中医,2011,26(2):368 -369.
[3]王雪梅.当归有效成分及其药理作用的研究进展[J].甘肃中医,2009,22(11):50 -51.
[4]李秋怡,干国平,刘焱文.川芎的化学成分及药理研究进展[J].时珍国医国药,2006,17(7):1298 -1299.
[5]王春雷,芦柏震,侯桂兰. 山楂的化学成分、药理作用及临床应用[J].海峡药学,2010,22(3):75 -78.
[6]李贵海,孙敬勇.山楂降血脂有效成分的实验研究[J].中草药,2002,33(1):50 -52.
[7]张印发. 何首乌的药理作用研究[J]. 中国现代医生,2007,45(15):149 -151.
[8]叶璟.川芎有效成分的提取技术[J]. 中国高新技术企业,2009,126:55 -56.
[9]袁久荣,容蓉,杨东.当归饮片挥发油成分的研究[J].中国中药杂志,1998,23(10):601 -603.
[10]唐斌,程绪,刘江,等.人参皂苷药理作用研究进展[J].西南军医,2005,7(3):45 -47.
