2010-2014年高考氧化还原反应试题研究
2014-03-18罗华平衷明华
罗华平 衷明华
(韩山师范学院,广东 潮州 521041)
1.广东省2010—2014年高考理综化学氧化还原反应试题考点分布

表 广东省2010—2014年高考理综化学氧化还原反应试题考点分布
从历年的广东高考试题来看,氧化还原反应的知识是很重要的,很少的试题会单独考察氧化还原反应的知识(除2012年选择题9),它以综合题为主,贯穿于各个选择题(离子共存、阿伏伽德罗常数、元素周期律、基本实验和变形实验、原电池、电解池、有机化学基础)工艺流程图、实验大题等试题中。从2010—2014的在单选题中来看,氧化还原反应在离子共存、阿伏伽德罗常数的考察中更受高考命题人的青睐;而氧化还原反应知识点在双选题中全部是基本实验和变形实验的考察,但在大题目当中考察氧化还原反应知识的形式比较灵活多变。这就要求学生要能够真正掌握氧化还原反应的知识点,并且能够灵活应用。
2.高考试题分析
2.1 离子共存
在高考中常见氧化剂和还原剂一般用来判断离子共存的问题。氧化剂与还原剂在一起能发生氧化还原反应,导致离子不能大量共存。
例:(2010广东卷第7题)能在溶液中大量共存的一组离子是( )。
A.NH4+、Ag+、PO43—、Cl—
B.Fe3+、H+、I—、HCO3—
C.K+、Na+、NO3—、MnO4—
D.Al3+、Mg2+、SO42—、CO32—
解析:B项中Fe3+是氧化剂,I—是还原剂,能发生氧化还原反应,所以不能大量共存。
2.2 阿伏伽德罗常数
高考中氧化还原反应与阿伏伽德罗常数的知识点结合,让学生计算电子的转移数或得失电子总数。
电子转移数=得电子总数=失电子总数
失电子数=(还原剂)变价原子个数×化合价变化值
得电子数=(氧化剂)变价原子个数×化合价变化值
例:(2011广东A卷第9题)设nA为阿伏伽德罗常数的数值,下列说法正确的是( )。
A.常温下,23gNO2含有nA个氧原子
B.1L 0.1mol·L-1的氨水含有0.1nA个OH―
C.常温常压下,22.4L CCl4含有nA个CCl4分子
D.1mol Fe2+与足量的H2O2溶液反应,转移2nA个电子
解析:D项1mol Fe元素化合价从+2到+3转移为nA个电子
2.3 元素周期表
在高考中一般利用元素在周期表的位置用来判断氧化剂或还原性强弱。
例:(2014广东卷第23题)甲~辛等元素在周期表中的相对位置如下图。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )。
A.金属性:甲>乙>丁
B.原子半径:辛>己>戊

图 甲~辛等元素在周期表中的相对位置
C.丙与庚的原子核外电子数相差13
D.乙的单质在空气中燃烧生成只含离子键的化合物
解析:同周期从左到右金属性逐渐减弱,同主族从上到下金属性逐渐增强,所以甲<乙,A项错误。
2.4 基本实验和变形实验
基本实验和变形实验考察氧化还原反应的形式比较多样,有根据实验原理现象判断氧化性还原性的强弱、常见氧化剂还原剂的性质实验等。
例1:(2014广东卷第22题)下列实验操作、现象和结论均正确的是( )。

表 实验操作、现象和结论
解析:D项中Fe3+氧化剂,I2是氧化产物,根据根据氧化还原反应的方向判断氧化性:氧化剂>氧化产物,所以氧化性:Fe3+>I2
例2:(2012广东卷第12题)下列陈述正确并且有因果关系的是( )。

表 陈述Ⅰ,陈述Ⅱ
2.5 非选择题
非选择题当中考察氧化还原反应知识的形式比较灵活多变,一般与能量变化、电化学知识、化学平衡有很强的关联性,考察内容氧化还原反应的基本概念(判断氧化剂、还原剂、氧化产物、还原产物)、双线桥、单线桥(标明电子转移的方向和数目)、比较氧化性(或还原性)的强弱、配平简单的氧化还原反应方程式、利用电子得失守恒、电荷守恒进行计算、根据信息或综合运用以上原理和方法写出氧化还原反应。
例1:(2010广东卷第33题部分试题)某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
反应Cl2+Na2SO3+2NaOH===2NaCl+Na2SO4+H2O中的还原剂为____。
解析:S元素的价态是从+4→+6,失去电子的反应物为还原剂,所以是Na2SO3。
例2:(2014广东卷第33题部分试题)H2O2是一种绿色氧化还原试剂,在化学研究中应用广泛。
①写出本实验H2O2分解反应方程式并标明电子转移的方向和数目:____。
解析:该反应得失电子的元素都是O,从-1到0,从-1到-2;得电子总数=失电子总数=失电子数=(氧化剂)变价原子个数×化合价变化值=2xe—则有:
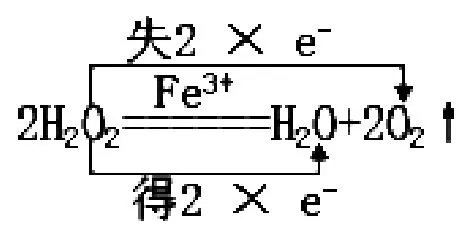
3.高考趋势分析
未来高考中氧化还原反应仍是重点考察内容,它会与离子共存、阿伏伽德罗常数、元素周期律、基础实验、能量变化、电化学知识有很强的关联性,和它们一起进行综合考察的可能性较大。
4.考生对策
近几年的高考题中,关于氧化还原反应概念的题目虽然较多,但考察的都是基础知识。在非选择题中通常考察氧化剂、还原剂的判断,氧化性、还原性的强弱比较,简单的氧化还原反应的配平。复习时应对概念的准确理解为目的,不要在技巧型氧化还原反应计算和复杂的氧化还原反应配平上浪费时间。
