藻类生物吸附剂应用于处理水中重金属离子研究进展
2014-03-18王金扣马腾腾王志峰陈俊生
王金扣 马腾腾 肖 琳 谢 盈 王志峰 陈俊生 李 敏
(1.放射性地质与勘探技术国防重点学科实验室,东华理工大学,江西 南昌 330013;2.化学生物与材料科学学院,东华理工大学,江西 南昌 330013)
重金属污染已经越来越成为全球性关注的问题,主要是因为重金属具有高毒性、在人体内和食物链中的高生物富集性、非生物降解性及最有可能对人类致癌性。铅、汞、铬、砷、镉、锌、铜和镍是地表水和工业废水中最常见的污染物。这些出现在水中的重金属对人类及其他生物造成巨大的威胁,因此有效地去除受污染的水中的这些重金属离子显得至关重要。目前传统的处理技术如沉淀、吸附、还原、凝固、膜过滤,人们都可以接受,但是也有缺点,特别是不能处理受污染的水中重金属离子浓度范围从几毫克到几百毫克每升[1]。
生物吸附以其操作简单、运行成本低、无二次污染及高效率处理低浓度重金属的特点,成为人们关注的焦点。生物吸附现象被发现于20世纪70年代,在核电站排出的废水里发现几种藻类中出现放射性元素及重金属离子的富集。近年来实验室进行的研究表明,生物吸附去除水中重金属离子是一个很有前途的和具有成本效益的技术解决方案[2]。
生物吸附所使用的吸附材料包括微生物生物量(细菌、古细菌、蓝细菌、丝状真菌和酵母,微藻类),海藻(微藻类),工业废物(发酵和食品废物,活性和厌氧污泥,等等),农业废物(水果废物、蔬菜废物、稻草、麦麸、菜粕、大豆皮,等等),自然界中的残留物(植物残留、锯末、树叶、杂草、水藓等)和其他材料(壳聚糖、纤维素等)。近年来有关藻类用于处理水中重金属离子污染的报道越来越多,藻类生物吸附剂的应用逐渐成为人们的关注[2]。
海藻属于一种种类繁多的微生物,从单细胞到多细胞组织分布在不同的水体和陆地环境中[3]。藻类由于多糖和蛋白质或脂质表面的存在而具有好的吸附污染物的能力,细胞壁含有一些功能基团,如氨基、羟基、羧基和硫酸等。常常利用死去的藻类生物质应用于工业废水处理,减少有害的有机和无机污染物,不需要营养,可以暴露于高毒性的环境中[4]。以微藻类的死亡形式来充当有效的生物吸附剂,容易培养,具有良好的收益、更好的效率和更高的表面面积[5]。
一、藻类生物吸附剂的种类
在各种有关生物吸附剂的报道文献中,海洋藻类生物质因其高吸附性、低成本、可再生性、来源丰富的特性,被确定为一种有前途的生物吸附剂[6]。
海藻依据其完全独立的进化途径可以分为几个子组:“褐色途径”褐藻(褐藻门),“红色途径”红藻(红藻门)和“绿色途径”包括绿藻(绿藻门)、苔藓、蕨类植物和一些植物。它们的区别主要是在于细胞壁,也是生物吸附发生的地方[7]。
褐藻的细胞壁通常包含三种成分:纤维素(如支撑结构),海藻酸,与钠、钾、镁、钙轻金属和多糖(如硫酸盐)混合在一起的聚合物(如甘露糖醛酸和古洛糖醛酸)[7]。海藻酸和一些硫酸多糖(如褐藻糖胶)是褐藻(褐藻门)细胞壁很重要的组成成分。据报道海藻酸盐和硫酸盐是褐藻中主要的活跃组份[8][9]。绿藻的细胞壁中主要有纤维素和高蛋白质含量结合的多糖。这些化合物包含官能团如氨基、羧基、硫酸和羟基,在生物吸附中起着重要的作用。红藻的细胞壁含有纤维素,但它们的生物吸附能力主要是因为有由半乳糖体组成的硫酸多糖的存在。
在过去的二十年里,生物吸附的研究都集中在褐藻去除重金属[10][11][12][13][14][15][16]。最近的研究已经逐渐投入到绿藻[17][18][19]和红藻的生物吸附中[20]。
1.1 褐藻类生物吸附剂
褐藻是研究最广泛的藻类生物质。它们吸附铅、铜、镉、锌、镍、铬、铀和金等重金属离子的性能已经被广泛地研究。褐藻能有效去除剧毒金属离子,如铅和铬。一般来说,所有吸附重金属离子研究类型的褐藻的最大的生物吸附量都相当高。褐藻对铅的最大生物吸附能力可以高达1.37mmol/g,大部分的吸着剂的最大生物吸附可以在0.8mmol/g以上[7][9][21][22]。Sargassum muticum吸附铬(Cr)的最大生物吸附量更是高至3.77mmol/g[23]。褐藻对铜也显示出较好的去除能力,最大生物吸附能力从0.80mmol/g到1.66mmol/g不等[7][9][11][13][24][25][26]。对于同一种的褐藻类生物吸附剂,去除重金属能力的顺序:铅>铜>镍>镉>锌。在各种褐藻类生物吸附剂中,马尾藻类海草似乎可以显现出更好地吸附金属的能力。褐藻类生物吸附剂的性能也是三种藻类生物吸附剂(褐藻、绿藻、红藻)中最好的[9]。
褐藻也可以积累稀有金属和放射性金属。褐藻去除稀有金属Au(III)似乎相当成功,吸附能力也可达0.376mmol/g[27]。马尾藻类海草fluitans(褐藻)可以成功地去除贫铀UO2(II),并且最大吸附能力高于1.59mmol/g[28]。
1.2 绿藻和红藻类生物吸附剂
最近几年有更多的研究已经报道了绿藻和红藻类生物吸附剂吸附重金属的性能。重金属的研究包括:对于铅、铜、镉、锌和铬的吸附性能。
绿藻类生物吸附剂对重金属也具有较好的去除能力。绿藻类石莼属海藻去除Pb(II)的最大生物吸附能力在最适pH为5.0时高达1.46mmol/g,较低最大生物吸附能力的Caulerpa lentillifera对Pb(II)的去除能力也有0.13mmol/g[9][29]。Ulva lactuca显示出对Ni(II)具有很大的去除能力,在最适pH为4.5时最大生物吸附能力可达1.14mmol/g[19]。Romera的研究中表明,绿藻对Zn(II)具有一定的去除能力,Codium vermilara和Spirogyra insignis在最适pH为6.0时对Zn(II)的最大生物吸附量可以达到0.36mmol/g、0.32mmol/g[7]。在各种绿藻类生物吸附剂中,石莼属海藻显现出对各种金属都有较好的去除能力,去除Cu(II)的最大生物吸附能力在最适pH为5.0时也有0.75mmol/g[9],去除Cd(II)时在最适pH=5.5的最大生物吸附能力为0.58mmol/g[9],在去除镉时对于不同价态的镉离子也显现出不同的去除能力,在最适pH为2时去除Cr(VI)的最大生物吸附量有0.58mmol/g,吸附Cr(III)时在最适pH为4.5的最大生物吸附能力更是高达1.02mmol/g[30]。
红藻类生物吸附剂相对于褐藻类生物吸附剂和绿藻类生物吸附剂而言,对于重金属的吸附能力显得没有那么强。红藻类中Chondrus crispus在最适pH为4.0时对Pb(II)的最大生物吸附能力较高的也只有0.98mmol/g[7],其他种类的大部分吸附剂的最大生物吸附能力同样的也都处于较低水平,较弱的低至0.14mmol/g[20]。对于Cu(II)的吸附能力,大部分红藻类生物吸附剂的最大生物吸附量都在0.5mmol/g左右[7][9][31],吸附Cd(II)、Zn(II)、Ni(II)重金属离子的能力也处于较弱[7][9][20]。然而Ibrahim发现Galaxaura oblongata在最适pH为5.0时对Cr(III)的最大生物吸附能力竟然高达2.02mmol/g,比绿藻类生物吸附剂的吸附能力还要高出好多[20]。Romera的研究显示,Chondrus crispus对Pb(II)、Cu(II)、Cd(II)、Zn(II)、Ni(II)重金属离子同时具有较高的最大生物吸附量[9]。红藻类生物吸附剂可以成功去除金属钴,对Co(II)也表现出较高的生物吸附能力,Carallina mediterranea在最适pH为5.0时的最大生物吸附量也高达1.29mmol/g[20]。
然而,许多的研究报道中表明,绿藻和红藻类生物吸附剂对于重金属离子的生物吸附能力都远低于褐藻类生物吸附剂。
二、生物吸附动力学
重金属的生物吸附是独立的新陈代谢过程,它通常发生迅速,特别是对金属阳离子的吸收。
大多数金属阳离子的吸收发生在开始的20-60分钟内,接着是一个相对缓慢的吸收过程。重金属阳离子的吸附平衡通常在2-6小时内即可达到[20][29][32],这是远远高于活性碳和金属氧化物/氢氧化物类型吸附剂。如图1所示,即是典型的生物吸附动力学特征[33]。
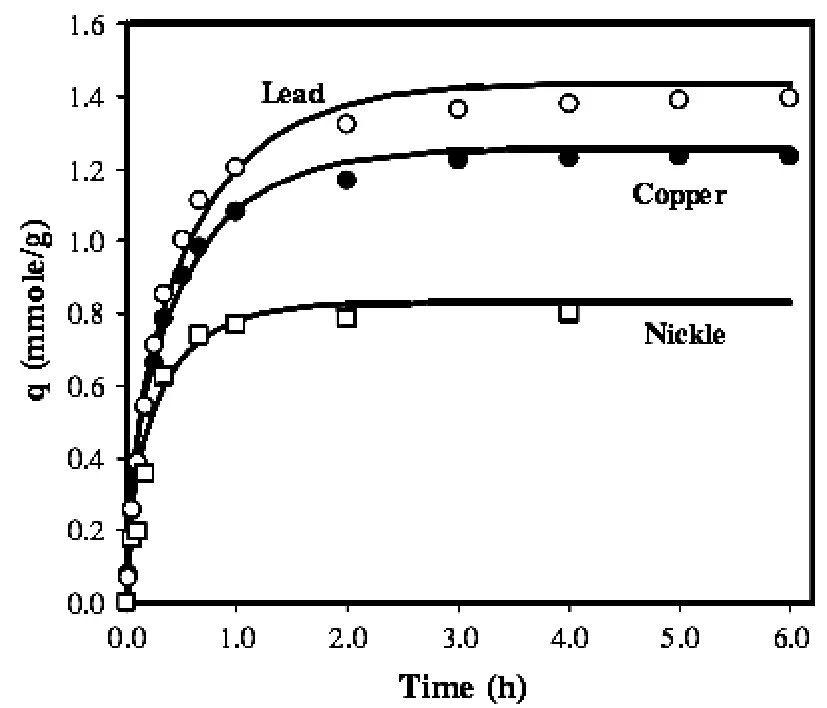
图1 马尾藻属海藻生物吸附重金属离子铅、铜、镍的吸附动力学曲线
然而,生物吸附剂对于阴离子污染物的去除(如六价铬)远低于阳离子污染物。通常,生物吸附剂处理阴离子污染物时需要超过半天到几天的时间才可达到生物吸附平衡。如Chen and Yang[33]的研究中表明,当经过化学改性的马尾藻属海藻完全吸附六价铬达到生物吸附平衡时,时间长达20h。
三、生物吸附平衡
生物吸附平衡是高度依赖于水化学及重金属离子和生物吸附剂的性质。在pH值处于较高的时候(如pH值为4-6以上),生物吸附剂容易吸附较高的金属阳离子。如图2所示[34]。
然而,生物吸附剂去除重金属阴离子时,在较低的pH值可以更好地进行。Lim[34]的研究中表明,离子强度在生物吸附过程中起着重要的作用。如图3所示[34]。
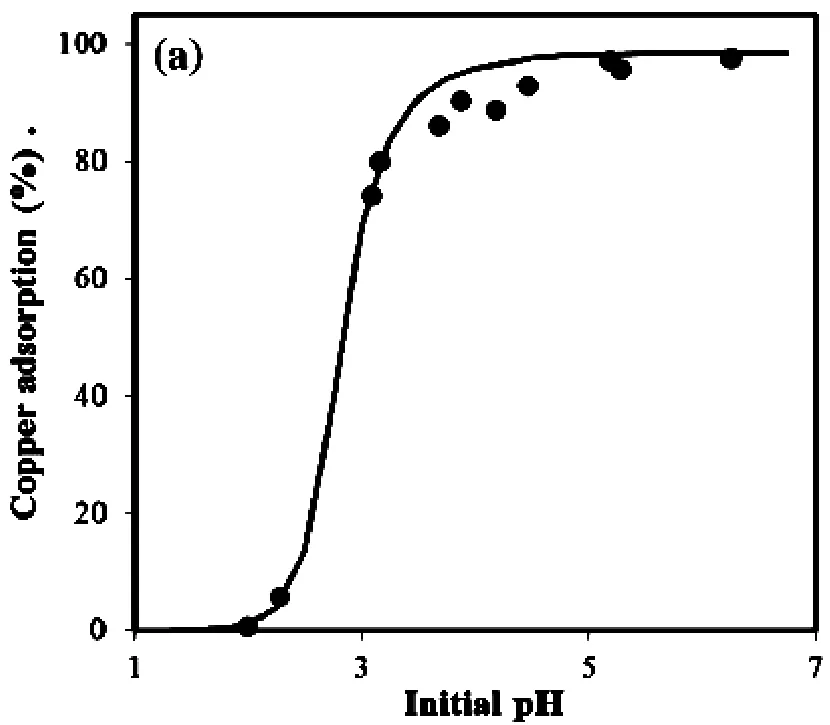
图2 pH对生物吸附剂吸附铜离子的吸附率的影响
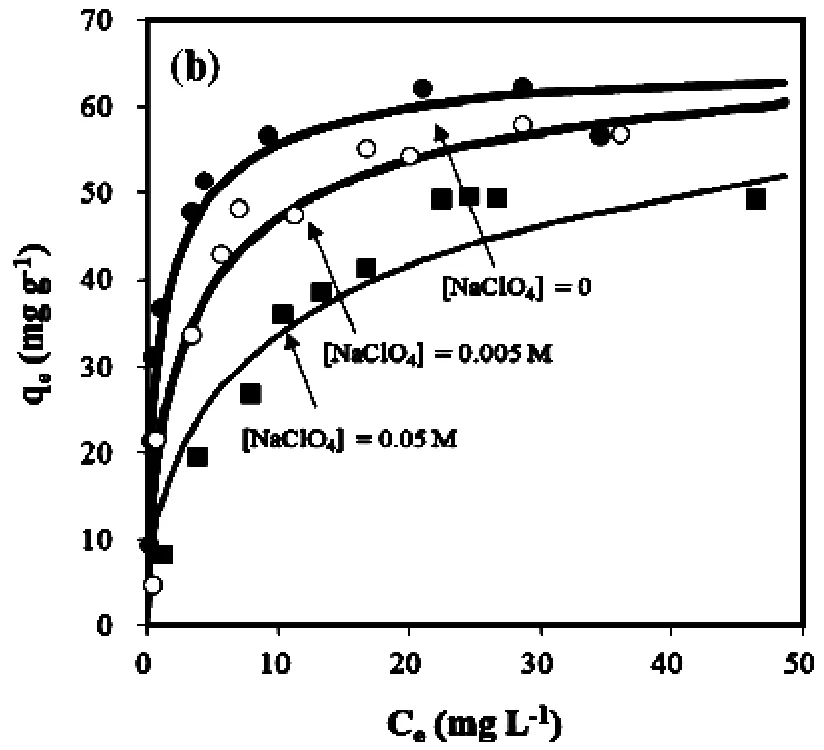
图3 离子强度对生物吸附量的影响
离子强度高时会导致重金属的生物吸附量降低,这主要是因为由于离子强度的存在,轻金属和重金属的官能团之间表现出竞争吸附。应该注意的是,当离子强度较高的时候,活性碳和金属氧化物对金属的吸附将会增加,这主要是由于压缩双电层(EDL)的作用影响[1]。
四、生物吸附金属的化学机制
金属离子的去除通过不活跃的、非活性的生物质来实行,是在金属离子和生物质之间具有高度关联性的金属吸附的基础上来实现的。复杂的自然机制如图4[35]所示。
海藻的基础生化结构对其生物吸附的过程起着至关重要的作用。更具体地说,海藻的生物吸附性能得益于细胞壁成分的性能,如海藻酸和褐藻糖胶,主要负责重金属螯合。通常情况下,褐藻、红藻和许多绿色藻类的藻细胞壁是由一个纤维骨架和一个无定形的嵌入基质组成的。最常见的纤维骨架材料通常是纤维素。褐藻的嵌入基质是海藻酸或海藻酸盐(海藻盐)和硫酸多糖(褐藻糖胶),红藻的嵌入基质是海藻酸或海藻酸盐(海藻盐)和硫酸半乳糖体。
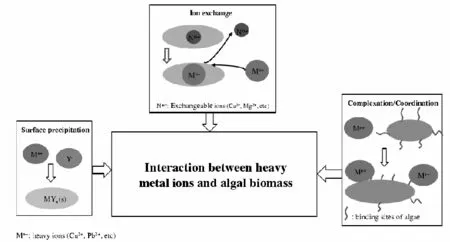
图4 重金属离子生物吸附过程的机制
褐藻和绿藻中高效出现的关键功能基团,如羧基、羟基、硫酸盐、磷酸盐、和胺类基团,在结合金属时发挥着主导的作用[9][36]。其中,羧基基团在pKa~5.0时是金属结合最重要的,褐藻糖胶的磺酸基团则是第二重要[10]。
为了研究各种官能团的存在及其与重金属络合的生物吸附过程,利用了光谱技术,如FT-IR和 XPS[33][37]。Zheng试图为了进一步更好地解释生物吸附的机制,采用了X射线吸收精细结构光谱和量子化学计算工具的科学手段[38]。
离子交换机制被发现在来源于海水环境的生物吸附剂中发挥着主导作用。离子交换发生在重金属和轻金属之间的(主要是Ca2+和Mg2+,单化合价Na+和K+都不能导致强烈的交键产生[25][33]。
褐藻的海藻酸盐,是存在于细胞壁和细胞间的物质,对二价阳离子(如Pb2+,Cu2+,Cd2+,和Zn2+),具有较高的吸收。此外,配位或络合物的形成也在海藻酸和硫酸多糖(褐藻糖胶)与重金属结合时被观察到[10]。据报道,金属离子和海藻酸或褐藻糖胶的亲和力与立体化学的影响相关。较大的离子可能更好地适应一个有两个远距离功能性基团的结合位点,如亲和力序列Pb2+>Cu2+>Cd2+>Zn2+>Ni2+>Ca2+>Mg2+。红藻中的硫酸多糖(半乳糖体)也被发现是主要负责金属离子络合的形成[7]。
XPS和红外光谱技术已经被广泛用于研究生物吸附剂官能团和金属离子之间的相互作用。褐藻生物吸附一些常见的重金属后的结合能值如表1[37]所示。
此外,生物质中在生物吸附重金属时发挥着主导作用的典型官能团的红外光谱波段如表2[33]所示。

表2 不同官能团的FT-IR特征吸收峰
五、结论与展望
藻类生物吸附剂因其高吸附性、低成本、可再生性、来源丰富的特性越来越受到人们的关注。近年来有关藻类生物吸附剂应用的报道也越来越多。藻类生物吸附剂逐渐被确定为一种有前途的生物吸附剂,是公认的生物吸附去除水中重金属离子的高成本效益技术解决方案。藻类生物吸附剂尤其突出的优点就是来源丰富,海洋藻类的产量每年多达百万吨,材料的获取容易便捷,成本更是廉价。根据文献中报道可知藻类生物吸附剂的吸附量也相当可观,特别是可以处理水中重金属离子范围几毫克到几百毫克每升的污染水,在污水治理和控制方面展现出巨大的作用,尤其是对放射性元素的去除,更是给人类的健康带来了保证。
可是,大量的研究都是在实验室中进行,应用到实际生活及生产中还有待进一步地大量研究。根据实验室中研究出的各种藻类生物吸附剂的性能,作出比较,筛选出最优的一类,考虑到实际中的应用及生产,再进行性能条件的进一步优化,让藻类生物吸附剂较好地实现实际应用及生产,由此带来的经济效益和社会效应将是相当大的,前景相当可观。
[1]He J,Chen J P.A comprehensive review on biosorption of heavy metals by algal biomass:Materials,performances,chemistry,and modeling simulation tools[J].Bioresource technology,2014,160:67-78.
[2]Sheng,P.X.,Ting,Y.-P.,Chen,J.P.,2007.Biosorption of heavy metal ions(Pb,Cu,and Cd)from aqueous solutions by the marine alga Sargassum sp.in single-and multiple-metal systems.Ind.Eng.Chem.Res.46(8),2438-2444.
[3]Sisca OL,Novie F,Felycia ES,Jaka S,Suryadi I(2009)Studies on potential applications of biomass for the separation of heavy metals from water and wastewater:review.Biochem Eng J 44:19-41.
[4]Crist HR,Oberholser K,Shank N,Nguyen M(1981)Nature of bonding between metallic ions and algal cell walls.Environ Sci Technol 15:1212-1217.
[5]Azza MAA,Nabila SA,Hany HAG,Rizka KA(2013)Biosorption of cadmium and lead from aqueous solution by fresh water alga Anabaena sphaerica biomass.J Advanc Res 4:367-374.
[6]Chen,J.P.,2012.Decontamination of Heavy Metals:Processes,Mechanisms,and Applications.CRC Press/Taylor and Francis Group.
[7]Romera,E.,González,F.,Ballester,A.,Blázquez,M.L.,Muoz,J.A.,2007.Comparative study of biosorption of heavy metals using different types of algae.Bioresour.Technol.98(17),3344-3353.
[8]Chen,J.P.,Hong,L.,Wu,S.,Wang,L.,2002.Elucidation of interactions between metal ions and Ca alginate-based ion-exchange resin by spectroscopic analysis and modeling simulation.Langmuir 18(24),9413-9421.
[9]Sheng,P.X.,Ting,Y.-P.,Chen,J.P.,Hong,L.,2004.Sorption of lead,copper,cadmium,zinc,and nickel by marine algal biomass:characterization of biosorptive capacity and investigation of mechanisms.J.Colloid Interface Sci.275(1),131-141.
[10]Davis,T.A.,Volesky,B.,Mucci,A.,2003.A review of the biochemistry of heavy metal biosorption by brown algae.Water Res.37(18),4311-4330.
[11]Davis,T.A.,Volesky,B.,Vieira,R.H.S.F.,2000.Sargassum seaweed as biosorbent for heavy metals.Water Res.34(17),4270-4278.
[12]Figueira,M.M.,Volesky,B.,Ciminelli,V.S.T.,Roddick,F.A.,2000.Biosorption of metals in brown seaweed biomass.Water Res.34(1),196-204.
[13]Kleinübing,S.J.,da Silva,E.A.,da Silva,M.G.C.,Guibal,E.,2011.Equilibrium of Cu(II)and Ni(II)biosorption by marine alga Sargassum filipendula in a dynamic system:competitiveness and selectivity.Bioresour.Technol.102(7),4610-4617.
[14]Lodeiro,P.,Cordero,B.,Barriada,J.L.,Herrero,R.,Sastre de Vicente,M.E.,2005.Biosorption of cadmium by biomass of brown marine macroalgae.Bioresour.Technol.96(16),1796-1803.
[15]Luna,A.S.,Costa,A.L.H.,da Costa,A.C.A.,Henriques,C.A.,2010.Competitive biosorption of cadmium(II)and zinc(II)ions from binary systems by Sargassum filipendula.Bioresour.Technol.101(14),5104-5111.
[16]Yu,Q.,Matheickal,J.T.,Yin,P.,Kaewsarn,P.,1999.Heavy metal uptake capacities of common marine macro algal biomass.Water Res.33(6),1534-1537.
[17]Deng,L.,Zhang,Y.,Qin,J.,Wang,X.,Zhu,X.,2009.Biosorption of Cr(VI)from aqueous solutions by nonliving green algae Cladophora albida.Miner.Eng.22(4),372-377.
[18]Wan Maznah,W.O.,Al-Fawwaz,A.T.,Surif,M.,2012.Biosorption of copper and zinc by immobilised and free algal biomass,and the effects of metal biosorption on the growth and cellular structure of Chlorella sp.and Chlamydomonas sp.isolated from rivers in Penang,Malaysia.J.Environ.Sci.24(8),1386-1393.
[19]Zakhama,S.,Dhaouadi,H.,M’Henni,F.,2011.Nonlinear modelisation of heavy metal removal from aqueous solution using Ulva lactuca algae.Bioresour.Technol.102(2),786-796.
[20]Ibrahim,W.M.,2011.Biosorption of heavy metal ions from aqueous solution by red macroalgae.J.Hazard.Mater.192(3),1827-1835.
[21]Holan,Z.R.,Volesky,B.,1994.Biosorption of lead and nickel by biomass of marine algae.Biotechnol.Bioeng.43(11),1001-1009.
[22]Jalali,R.,Ghafourian,H.,Asef,Y.,Davarpanah,S.J.,Sepehr,S.,2002.Removal and recovery of lead using nonliving biomass of marine algae.J.Hazard.Mater.92(3),253-262.
[23]González Bermúdez,Y.,Rodríguez Rico,I.L.,Guibal,E.,Calero de Hoces,M.,MartínLara,M..,2012.Biosorption of hexavalent chromium from aqueous solution by Sargassum muticum brown alga.Application of statistical design for process optimization.Chem.Eng.J.183,68-76.
[24]Mata,Y.N.,Blázquez,M.L.,Ballester,A.,González,F.,Muoz,J.A.,2008.Characterization of the biosorption of cadmium,lead and copper with the brown alga Fucus vesiculosus.J.Hazard.Mater.158(2-3),316-323.
[25]Ahmady-Asbchin,S.,Andrès,Y.,Gérente,C.,Cloirec,P.L.,2008.Biosorption of Cu(II)from aqueous solution by Fucus serratus:surface characterization and sorption mechanisms.Bioresour.Technol.99(14),6150-6155.
[26]Karthikeyan,S.,Balasubramanian,R.,Iyer,C.S.P.,2007.Evaluation of the marine algae Ulva fasciata and Sargassum sp.for the biosorption of Cu(II)from aqueous solutions.Bioresour.Technol.98(2),452-455.
[27]Mata,Y.N.,Torres,E.,Blázquez,M.L.,Ballester,A.,González,F.,Muoz,J.A.,2009b.Gold(III)biosorption and bioreduction with the brown alga Fucus vesiculosus.J.Hazard.Mater.166(2-3),612-618.
[28]Yang,J.,Volesky,B.,1999.Biosorption of uranium on Sargassum biomass.Water Res.33(15),3357-3363.
[29]Pavasant,P.,Apiratikul,R.,Sungkhum,V.,Suthiparinyanont,P.,Wattanachira,S.,Marhaba,T.F.,2006.Biosorption of Cu2+,Cd2+,Pb2+,and Zn2+using dried marine green macroalga Caulerpa lentillifera.Bioresour.Technol.97(18),2321-2329.
[30]Murphy,V.,Hughes,H.,McLoughlin,P.,2008.Comparative study of chromium biosorption by red,green and brown seaweed biomass.Chemosphere 70(6),1128-1134.
[31]Vilar,V.J.P.,Botelho,C.M.S.,Boaventura,R.A.R.,2008.Copper removal by algae Gelidium,agar extraction algal waste and granulated algal waste:kinetics and equilibrium.Bioresour.Technol.99(4),750-762.
[32]Vijayaraghavan,K.,Yun,Y.-S.,2008.Bacterial biosorbents and biosorption.Biotechnol.Adv.26(3),266-291.
[33]Chen,J.P.,Yang,L.,2005.Chemical modification of Sargassum sp.for prevention of organic leaching and enhancement of uptake during metal biosorption.Ind.Eng.Chem.Res.44(26),9931-9942.
[34]Lim,S.-F.,Zheng,Y.-M.,Zou,S.-W.,Chen,J.P.,2008.Characterization of copper adsorption onto an alginate encapsulated magnetic sorbent by a combined FT-IR,XPS,and mathematical modeling study.Environ.Sci.Technol.42(7),2551-2556.
[35]Sud,D.,Mahajan,G.,Kaur,M.P.,2008.Agricultural waste material as potential adsorbent for sequestering heavy metal ions from aqueous solutions-a review.Bioresour.Technol.99(14),6017-6027.
[36]Gupta,V.K.,Rastogi,A.,2008.Equilibrium and kinetic modelling of cadmium(II)biosorption by nonliving algal biomass Oedogonium sp.from aqueous phase.J.Hazard.Mater.153(1-2),759-766.
[37]Yang,F.,Liu,H.,Qu,J.,Paul Chen,J.,2011.Preparation and characterization of chitosan encapsulated Sargassum sp.biosorbent for nickel ions sorption.Bioresour.Technol.102(3),2821-2828.
[38]Zheng,Y.M.,Liu,T.,Jiang,J.W.,Yang,L.,Fan,Y.P.,Wee,A.T.S.,Chen,J.P.,2011.Characterization of hexavalent chromium interaction with Sargassum by X-ray absorption fine structure spectroscopy,X-ray photoelectron spectroscopy and quantum chemistry calculation.J.Colloid Interface Sci.356(2),741-748.
