吗替麦考酚酯对比环磷酰胺治疗狼疮性肾炎的有效性和安全性的系统评价Δ
2014-03-09卢克鹏林立敏金砚杰宋洪涛南京军区福州总医院药学科福州350025沈阳药科大学药学院沈阳006福建医科大学药学院福州350025
刘 倩,张 晶,卢克鹏,2,林立敏,2,金砚杰,3,宋洪涛#(.南京军区福州总医院药学科,福州 350025;2.沈阳药科大学药学院,沈阳 006;3.福建医科大学药学院,福州 350025)
狼疮性肾炎(LN)是系统性红斑狼疮累及肾脏所引起的一种免疫复合物性肾炎,是系统性红斑狼疮主要的死亡原因。对于LN 积极地给予糖皮质激素和免疫抑制剂治疗已成为共识,但采用何种免疫抑制剂仍存在异议。糖皮质激素联合环磷酰胺(CYC)是目前治疗LN推荐的一线方案。但是,该方案不良反应较严重,患者耐受性较差。吗替麦考酚酯(MMF)为一种新型免疫抑制剂,但由于其价格昂贵,并且各个临床研究报道的治疗LN的有效性与安全性的结论相互矛盾[1-2],故在一定程度上限制了其应用。
此前,关于MMF治疗LN已有一些Meta分析:殷蕾等[3]纳入11项随机对照试验(RCT),但纳入文献质量偏低,且疗效指标只有缓解率、复发率、死亡率,不够全面;徐云芬等[4]纳入16篇文献,大部分文献质量偏低,Jadad评分为1分;沈琪等[5]纳入37 项RCT,但只评价了CYC 的有效性和安全性;而Kamanamool N[1]和Touma Z[2]均存在文献检索不全的情况。鉴于前述Meta分析存在的不足,笔者全面地对已发表的RCT文献进行Meta分析,系统评价了MMF对比CYC治疗LN的有效性和安全性,以为临床治疗提供循证参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1 纳入标准 必须同时符合:RCT 或半随机对照试验(qRCT),语种限定为中文和英文;试验组患者给予MMF或与强的松龙联合使用,对照组患者给予CYC或与强的松龙联合使用;所有患者诊断符合美国风湿病协会系统性红斑狼疮诊断标准[6],肾穿刺活检病理符合Lee氏分级Ⅲ~Ⅴ型;疗程≥6个月。
1.1.2 排除标准 试验组与对照组均给予MMF治疗的研究。
1.1.3 结局指标 ①有效性指标:缓解率、完全缓解率、死亡率、发展为终末期肾病发生率(ESRD)、血清肌酐变化、尿蛋白变化、肾小球滤过率变化、补体C3及C4浓度的变化、系统性红斑狼疮疾病活动度(SLEDAI)评分的变化。②安全性指标:胃肠道不良反应发生率、白细胞减少(白细胞<3.5×109L-1)发生率、月经不调发生率。
1.2 文献检索
计算机检索PubMed、Medline、Cochrane图书馆、EMBase、中国期刊全文数据库(CNKI)、中文科技期刊数据库、万方数据库,检索时限均从建库起至2013 年12 月。英文检索词包括:“Mycophenolate Mofetil”“Mycophenolic acid”“Mycophenolate Sodium Enteric-coated Tablets”“Cellcept”“MMF”“MPA”“cyclophosphamide”“CYC”“lupus nephritis”“glomerulonephritis LN”“randomized controlled trial”“controlled clinical trial”“randomized、placebo”;中文检索词包括:“吗替麦考酚酯”“霉酚酸吗啉乙酯”“麦考酚酸酯”“霉酚酸酯”“麦考酚钠肠溶片”“骁悉”“环磷酰胺”“狼疮性肾炎”。
1.3 资料提取
由两位研究者独立对最终纳入研究的RCT进行有效的数据提取并进行交叉核对,如意见不一致时通过讨论或征求第三方研究者的意见解决。数据提取包括:研究题目、发表时间等基本资料,患者数量、病情程度,给药剂量、使用疗程,随访时间,不良反应发生率,等等。
1.4 质量评价
采用“Cochrane Reviewer’Handbook”4.2.3 RCT 4 条质量评价标准对纳入的文献进行质量评价:1)随机方法是否正确;2)是否进行分配隐藏、方法是否正确;3)有无失访或退出,如有失访或退出时,原因是否描述清楚;4)是否采用意向性治疗分析。如果所有4条质量评价标准均完全满足,则该研究存在偏倚的可能性最小(A级);如果其中任何1条或多条质量评价标准仅为部分满足,即不清楚,则该研究存在偏倚的可能性为中等(B级);如果其中任何1条或多条质量评价标准完全不满足,即未采用或不正确,则该研究存在偏倚的可能性为高度(C级)。
1.5 统计学方法
采用Rev Man 5.0 统计软件进行Meta 分析。首先对纳入文献进行临床异质性评价,必要时采用亚组分析或者描述性分析。采用Q检验判断统计学异质性,检验水准为α=0.10。无统计学异质性(P>0.1 且I2<50%)的研究采用固定效应模型进行合并分析;反之(P≤0.1 且I2≥50%),在寻找异质性的原因后采用随机效应模型进行合并分析。对分类变量采用比值比(OR)、连续变量采用均数差(MD)及其95%可信区间(CI)表示合并效应量。必要时进行敏感性分析。
2 结果
2.1 纳入研究基本信息
共检索出1 244 篇文献,通过阅读文题和摘要,排除会议报道、个案、综述、重复发表的文献后得到43篇文献,进一步阅读全文,最终纳入9 篇(项)RCT[7-15],合计846 例患者。纳入研究基本信息详见表1。

表1 纳入研究基本信息Tab 1 General characteristics of included studies
2.2 纳入研究方法学质量评价结果
纳入研究方法学质量评价结果详见表2。
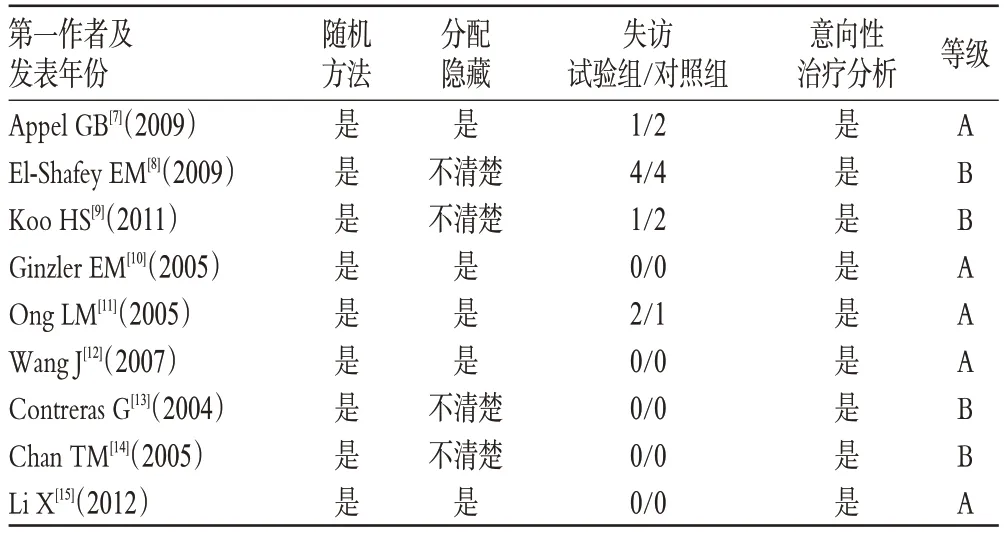
表2 纳入研究方法学质量评价结果Tab 2 Quality evaluation of the included studies
2.3 Meta分析结果
2.3.1 缓解率 7 篇文献报道了缓解率[8-10,12,14-15],共426 例患者,研究结果间无统计学异质性(P=0.54,I2=0),采用固定效应模型分析,详见图1。Meta 分析结果显示,MMF 联合糖皮质激素治疗LN 缓解率显著高于CYC 联合糖皮质激素[RR=1.72,95%CI(1.12,2.62),P=0.01]。
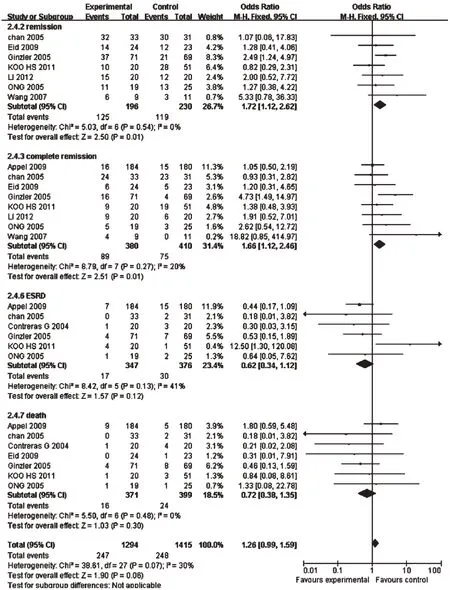
图1 两组患者缓解率、完全缓解率、死亡率、ESRD发生率的Meta分析森林图Fig 1 Forest plot of Meta-analysis of remission rate,complete remission rate,the incidence of death and ESRD rate in 2 groups
2.3.2 完全缓解率 8 篇文献报道了完全缓解率[7-12,14-15],共790例患者,研究结果间无统计学异质性(P=0.27,I2=20%),采用固定效应模型分析,详见图1。Meta分析结果显示,MMF联合糖皮质激素治疗LN完全缓解率显著高于CYC联合糖皮质激素[RR=1.66,95%CI(1.12,2.42),P=0.01]。
2.3.3 死亡率 7篇文献报道了死亡率[7-11,13-14],共770例患者,研究结果间无统计学异质性(P=0.48,I2=0),采用固定效应模型分析,详见图1。Meta 分析结果显示,两组死亡率比较差异无统计学意义[RR=0.72,95%CI(0.38,1.35),P=0.30]。
2.3.4 ESRD发生率 6篇文献报道了ESRD发生率[7,9-11,13-14],共723 例患者,研究结果间无统计学异质性(P=0.13,I2=41%),采用固定效应模型分析,详见图1。Meta分析研究结果显示,两组患者ESRD 发生率比较差异无统计学意义[RR=0.62,95%CI(0.34,1.12),P=0.12]。
2.3.5 肾功能指标 ①24 h 尿蛋白变化量。3 篇文献报道了24 h尿蛋白变化量[8,10,12],共199 例患者,研究结果间无统计学异质性(P=0.15,I2=48%),采用固定效应模型分析,详见图2。Meta 分析结果显示,两组比较差异无统计学意义[MD=-0.24,95%CI(-0.85,0.38),P=0.45]。②血清肌酐。3篇文献报道了血清肌酐[8,10,12],共199例患者,研究结果间无统计学异质性(P=0.77,I2=0),采用固定效应模型分析,详见图2。Meta 分析结果显示,两组比较差异无统计学意义[MD=-0.02,95%CI(-0.19,0.15),P=0.81]。③肾小球滤过率。1篇文献报道了肾小球滤过率[8],共39例患者,研究结果间无统计学异质性(P=0.33),采用固定效应模型分析,详见图2。Meta 分析结果显示,两组比较差异无统计学意义[MD=9.36,95%CI(-9.45,28.17),P=0.33]。
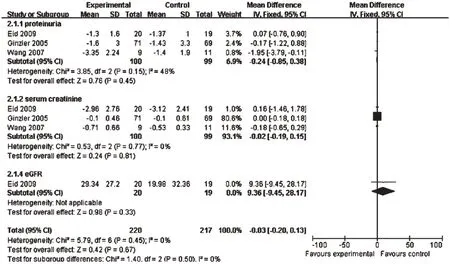
图2 两组患者肾功能指标的Meta分析森林图Fig 2 Forest plot of Meta-analysis of renal function indicators in 2 groups
2.3.6 LN活动指标 ①补体C3浓度。3篇文献报道了补体C3浓度的变化[8,10-11],共203 例患者,研究结果间无统计学异质性(P=0.21,I2=36%),采用固定效应模型分析,详见图3。Meta分析结果显示,两组比较差异无统计学意义[MD=6.52,95%CI(-1.57,14.61),P=0.11]。②补体C4浓度。3篇文献报道了补体C4浓度的变化[8,10-11],共203 例患者,研究结果间无统计学异质性(P=0.19,I2=39%),采用固定效应模型分析,详见图3。Meta分析结果显示,两组比较差异无统计学意义[MD=-1.15,95%CI(-4.85,2.56),P=0.54]。③SLEDAI 评分。1 篇文献报道了SLEDAI 评分[11],共24 例患者,研究结果间无统计学异质性(P=0.89,I2=36%),采用固定效应模型分析,详见图3。Meta分析结果显示,两组比较差异无统计学意义[MD=-0.4,95%CI(-6.12,5.32),P=0.89]。
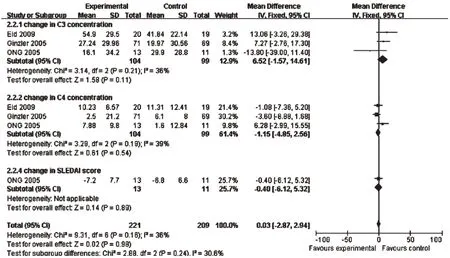
图3 两组患者LN活动指标的Meta分析森林图Fig 3 Forest plot of Meta-analysis of lupus nephritis indicators in 2 groups
2.3.7 胃肠道不良反应发生率 5 篇文献报道了胃肠道不良反应的发生率[7-8,10,12,14],共635例患者,研究结果间无统计学异质性(P=0.11,I2=47%),采用固定效应模型分析,详见图4。Meta 分析结果显示,两组比较差异无统计学意义[RR=1.01,95%CI(0.72,1.41),P=0.97]。
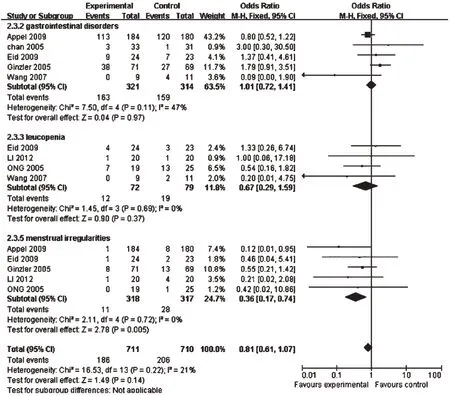
图4 两组患者安全性指标的Meta分析森林图Fig 4 Forest plot of Meta-analysis of safety indicators in 2 groups
2.3.8 白细胞减少发生率 4 篇文献报道了白细胞减少发生率[8,11-12,15],共151 例患者,研究结果间无统计学异质性(P=0.69,I2=0),采用固定效应模型分析,详见图4。Meta 分析结果显示,两组比较差异无统计学意义[RR=0.67,95%CI(0.29,1.59),P=0.37]。
2.3.9 月经不调发生率 5 篇文献报道了月经不调发生率[7-8,10-11,15],共635 例患者,研究结果间无统计学异质性(P=0.72,I2=0),采用固定效应模型分析,详见图4。Meta 分析结果显示,两组比较差异有统计学意义[RR=0.36,95%CI(0.17,0.74),P=0.005]。
3 讨论
本研究纳入9篇(项)RCT,合计846例患者。采用Meta分析的方法比较了MMF 与CYC 两组患者的有效性与安全性。结果,MMF 组患者缓解率和完全缓解率均显著高于CYC 组,ESRD发生率显著低于CYC组,差异有统计学意义;两组患者死亡率比较差异无统计学意义。此结论与Touma Z[2]等的研究结果不同:MMF 组与CYC 组缓解率、完全缓解率无显著性差异,MMF组ESRD发生率较CYC组显著下降。造成差异的原因可能是由于Touma Z等只纳入诱导疗法治疗LN的RCT,而笔者纳入诱导疗法和维持疗法治疗LN 的RCT。殷蕾[3]等的Meta分析提示:MMF组患者总有效率和完全缓解率高于CYC组,差异有统计学意义,但两组患者复发率比较差异无统计学意义,CYC组患者死亡率高于MMF组。上述结论均与本研究结果不一致,分析原因可能是由于:(1)LN 本身疾病进展缓慢,纳入的RCT随访时限不一,存在随访时间较短尚未观察到LN 患者死亡的情况。(2)殷雷等纳入文献的检索时限为1966-2007年,未纳入2007年之后发表的RCT,报道相对陈旧。
MMF联合糖皮质激素治疗LN和CYC联合糖皮质激素治疗LN的疗效可能存在种族差异,Isenberg D[16]等研究认为亚洲黄种人群对MMF 和CYC 反应相近,但黑种人及西班牙人对MMF反应较差,而拉丁美洲人对MMF反应较好。Ginzler EM等[10]人根据黑种人需要更大剂量的MMF 的理论,给予受试者MMF 的剂量为3 g/d,其纳入患者中56%为黑人(MMF 组43人,CYC 组36 人),该项研究可能会造成结果偏倚。剔除Ginzler 的研究进行Meta 分析结果发现异质性消失但有效性不变。
随着LN患者生存率的显著提高,对长期用药的安全性提出了更高要求。本研究结果显示,MMF组胃肠道不良反应发生率高于CYC 组、白细胞减少发生率低于CYC 组,但差异无统计学意义。MMF组月经不调的发生率显著低于CYC组,提示当患者为未生育女性时,选择MMF 安全性更好。感染是LN 患者治疗过程中最常见及严重的并发症,在LN 的治疗过程中如何预防和避免感染显得特别重要。由于各个研究中对感染的定义不同,造成结果存在较大异质性,因此本研究并未对感染进行Meta分析。
本研究的局限性:(1)本研究纳入的RCT样本较小且为单中心研究,部分研究失访率较高存在失访偏倚,这在一定程度上影响本Meta 分析结果的可靠性;(2)本研究纳入的RCT 随访时间普遍较短,未能明确MMF 与CYC 对LN 患者死亡率及ESRD 的影响;(3)LN 的疾病进展程度与治疗效果密切相关,因为纳入RCT 的患者基本情况不一,未能进行详细的分层分析。
综上所述,MMF治疗LN的疗效优于CYC,安全性与CYC相当。由于纳入研究质量不高、样本量较小,此结论尚需高质量、大样本且长时间随访的RCT进一步验证。
[1]Kamanamool N,McEvoy M,Attia J,et al.Efficacy and Adverse Events of Mycophenolate Mofetil Versus Cyclophosphamide for Induction Therapy of Lupus Nephritis Systematic Review and Meta-Analysis[J].Medicine:Bal-timore,2010,89(4):227.
[2]Touma Z,Gladman DD,Urowitz MB,et al.Mycophenolate Mofetil for Induction Treatment of Lupus Nephritis:A Systematic Review and Metaanalysis[J].J Rheumatol,2011,38(1):69.
[3]殷蕾,周纬,金燕樑,等.环磷酰胺与霉酚酸酯治疗狼疮性肾炎疗效比较的系统评价[J].临床儿科杂志,2008,26(1):69.
[4]徐云芬.霉酚酸酯在狼疮性肾炎诱导及维持治疗中疗效的系统评价和Meta分析[D].杭州:浙江大学,2010.
[5]沈琪,杨彤,黄献文.环磷酰胺治疗增殖性狼疮肾炎的Meta分析[J].中国循证儿科杂志,2011,6(1):11.
[6]Hochberg MC.Updating the American College of Rheumatology revised criteria for the classification of systemiclupus erythematosus[J].Arthritis Rheum,1997,40(9):17.
[7]Appel GB,Contreras G,Dooley MA,et al.Mycophenolate Mofetil versus Cyclophosphamide for Induction Treatment of Lupus Nephritis[J].J Am Soc Nephrol,2009,20(5):1 103.
[8]El-Shafey EM,Abdou SH,Shareef MM,et al.Is mycopheolate mofetil superior to pulse intravenous cyclophosphamide for induction therapy of proliferative lupus nephritis in Egyptian patients?[J].Clin Exp Nephrol,2010,14(3):214.
[9]Koo HS,Kim YC,Lee SW,et al.The effects of cyclophosphamide and mycophenolate on end-stage renal disease and death of lupus nephritis[J].Lupus,2011,20(13):1 442.
[10]Ginzler EM,Dooley MA,Aranow C,et al.Mycophenolate mofetil or intravenous cyclophosphamide for lupus nephritis[J].N Engl J Med,2005,353(21):2 219.
[11]Ong LM,Hooi LS,Lim TO,et al.Randomized controlled trial of pulse intravenous cyclophosphamide versus mycophenolate mofetil in the induction therapy of proliferative lupus nephritis[J].Nephrology(Carlton),2005,10(5):504.
[12]Wang J,Hu W,Xie H,et al.Induction therapies for class IV lupus nephritis with non-inflammatory necrotizing vasculopathy:mycophenolate mofetil or intravenous cyclophosphamide[J].Lupus,2007,16(9):707.
[13]Contreras G,Pardo V,Leclercq B,et al.Sequential therapies for proliferative lupus nephritis[J].N Engl J Med,2004,350:971.
[14]Chan TM,Tse KC,Tang CS,et al.Long-term study of mycophenolate mofetil as continuous induction and maintenance treatment for diffuse proliferative lupus nephritis[J].J Am Soc Nephrol,2005,16(4):1 076.
[15]Li X,Ren H,Zhang Q,et al.Mycophenolate mofetil or tacrolimus compared with intravenous cyclophosphamide in the induction treatment for active lupus nephritis[J].Nephrol Dial Transplant,2012,27(4):1 467.
[16]Isenberg D,Appel GB,Contreras G,et al.Influence of race/ethnicity on response to lupus nephritis treatment:the ALMS study[J].Rheumatology:Oxford,2010,49(1):128.
