柴胡桂枝颗粒质量标准研究
2014-03-09王婵林广黄志权周永强粟华生
王婵,林广,黄志权,周永强,粟华生
·炮制制剂·
柴胡桂枝颗粒质量标准研究
王婵,林广,黄志权,周永强,粟华生
目的:建立柴胡桂枝颗粒质量标准。方法:采用薄层色谱法对处方中的君药柴胡进行定性鉴别;采用高效液相色谱法,色谱柱为Welch Ultimate XB-C18(250×4.6 mm,5 μm),流动相为甲醇-0.1%磷酸(47:53),流速1.0 mL.min-1,检测波长280 nm,柱温25℃,对处方中黄芩的有效成分黄芩苷进行含量测定。结果:本品中柴胡定性鉴别薄层色谱特征明显,专属性强;有效成分黄芩苷含量测定专属性强,稳定性、重复性好,平均回收率为100.15%,RSD为1.22%(n=6)。结论:该方法简便、准确、重复性好,可作为柴胡桂枝颗粒的质量控制。
柴胡桂枝颗粒;质量标准;薄层色谱法;含量测定
柴胡桂枝颗粒由柴胡、桂枝、黄芩、白芍、人参等九味中药组成,具有和解少阳,发散表邪的功能。主治少阳证兼有太阳表证,症见发热微恶寒、肢节烦痛,微呕,心下支结,外证未去者,亦可用肝胃不和之胃疼[1]。中药配方颗粒是应用现代制药技术将传统中药饮片经过提取、浓缩、干燥、制粒、包装而成的颗粒状剂型,具有应用灵活、携带方便、质量可控、不需煎煮等优点[2]。随着生活水平的日益提高,人们对中药免煎颗粒的需求量不断增长,因此提高对中药配方颗粒的质量控制至关重要。有关柴胡桂枝颗粒药理作用研究的报道较多,但对其质量控制方面的报道较少。为了保证药品的安全性、有效性及质量可控性,本研究对处方中的君药柴胡进行了薄层色谱鉴别,并采用高效液相色谱法对黄芩中的黄芩苷进行了含量测定。结果表明,本法操作简便,稳定性、重现性好,精密度高,测定结果准确,可作为柴胡桂枝颗粒的质量控制。
1 仪器与试药
Agilent 1260高效液相色谱仪(美国Agilent公司);GR-202分析天平(日本);昆山KQ-500DE超声波清洗仪(昆山市超声仪器有限公司);卡玛薄层摄像系统(Reportstar-5);预制硅胶G薄层板(青岛海洋化工有限公司)。
黄芩苷对照品(批号:MUST-11101403,含量测定用,成都曼思特生物科技有限公司);柴胡对照药材(批号:120992-201108,中国食品药品检定研究院);甲醇(FIRSH)为色谱纯,水为超纯水,其他试剂均为分析纯;柴胡桂枝颗粒(批号:A090283-01、A091015-01、A100364-02和A101035-01,培力(南宁)药业有限公司)。
2 方法与结果
2.1 柴胡鉴别
取本品5.0 g,加热水30 mL使溶解,放冷,用水饱和正丁醇振摇提取2次,每次25 mL,合并正丁醇液,用氨试液洗涤2次,每次30 mL,正丁醇液蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。另取柴胡对照药材0.5 g,加水50 mL,加热回流1 h,滤过,滤液置水浴上蒸至约30 mL,放冷,自“用水饱和正丁醇振摇提取2次”起同供试品溶液方法制成对照药材溶液。再取缺柴胡药材的阴性样品5.0 g,同供试品溶液方法制成阴性样品溶液。照薄层色谱法(中国药典2010年版一部附录Ⅵ B)试验,吸取上述供试品溶液及阴性样品溶液各5 μL,对照药材溶液10 μL,分别点于同一硅胶G薄层板上,以乙酸乙酯-乙醇-水(8:2:1)为展开剂,展开,取出,晾干,喷以2 %对二甲氨基苯甲醛的40 %硫酸溶液,60℃加热至斑点显色清晰,日光及紫外光灯(365 nm)下检视。供试品色谱中,在与柴胡对照药材色谱相应的位置上,显相同颜色的主斑点,结果见图1。
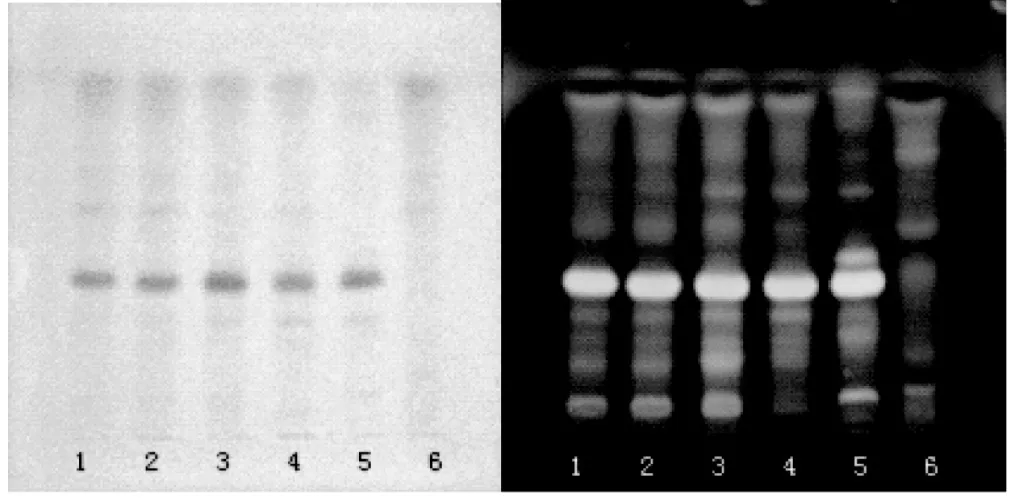
图1 柴胡薄层鉴别色谱图
2.2 黄芩苷含量测定
2.2.1 色谱条件 色谱柱为Welch Ultimate XB-C18,250×4.6 mm,5 μm;以甲醇-0.1%磷酸(47:53)为流动相;检测波长为280 nm;流速1.0 mL.min-1;柱温25℃。理论塔板数按黄芩苷峰计算应不低于3000。
2.2.2 对照品溶液的制备 取黄芩苷对照品适量,精密称定,加甲醇制成每1 mL含30 mg的溶液,即得。2.2.3 供试品溶液的制备 取本品适量,研细,取约0.2 g,精密称定,置具塞锥形瓶中,精密加入70%乙醇50 mL,称定重量,超声处理(功率500 W,频率40 kHz)30 min,取出,放冷,称重,用70 %乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.2.4 阴性样品溶液的制备 取缺黄芩药材的柴胡桂枝汤配方颗粒阴性样品,研细,取约0.2 g,精密称定,置具塞锥形瓶中,精密加入70 %乙醇50 mL,称定重量,超声处理(功率500 W,频率40 kHz)30 min,取出,放冷,称重,用70 %乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.2.5 专属性考察 分别吸取对照品溶液、供试品溶液、阴性样品溶液各10 μL进样。在“2.2.1色谱条件”下,供试品中黄芩苷色谱峰与对照品色谱峰保留时间一致,并与其他共存成分最小分离度为1.76(大于1.5),理论塔板数为10258(大于3000),主峰与杂质峰达到基线分离,且阴性样品在相应的位置没有色谱峰干扰,说明本方法专属性良好。色谱图见图2、图3、图4。
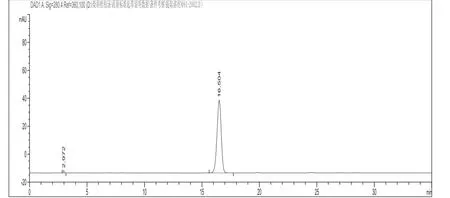
图2 黄芩苷对照品色谱图
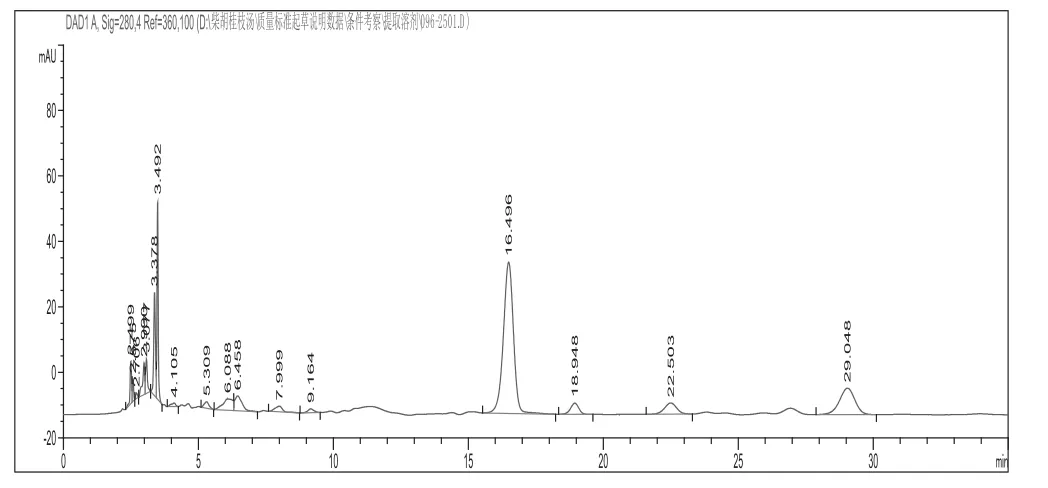
图3 供试品色谱图
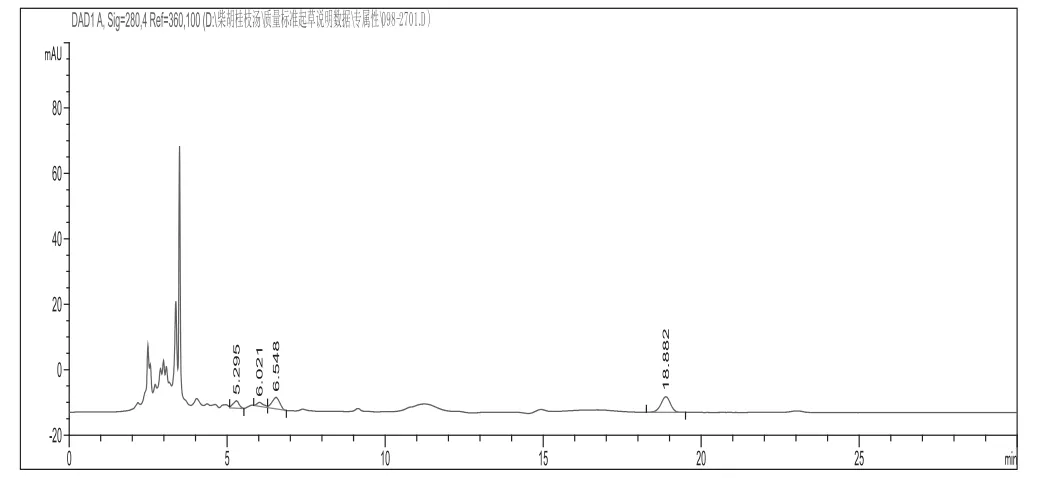
图4 阴性样品色谱图
2.2.6 线性关系考察 取黄芩苷对照品7.62 mg,置25 mL的量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得(浓度为0.3048 mg.mL-1),精密量取上述对照品溶液0.20、0.50、1.0、2.0、4.0 mL分别置10 mL的量瓶中,加甲醇稀释至刻度,摇匀,作为线1~线5,取0.3048 mg.mL-1的对照品溶液作为线6。分别精密吸取上述对照品溶液各10 μL,注入液相色谱仪进行测定。按上述色谱条件测得峰面积积分值,以进样量(μg)为横坐标,峰面积积分值为纵坐标,黄芩苷对照品的回归方程:Y=2615.5136X+21.6848, R² = 0.9999。结果表明:黄芩苷在0.06096~3.048 μg范围内时,黄芩苷进样量与峰面积呈良好的线性关系。
2.2.7 精密度试验 精密吸取黄芩苷对照品溶液(浓度为60.96 μg.mL-1)10 μL,重复进样6次,测定峰面积,结果表明,黄芩苷峰面积的RSD(%)值为0.07 %,小于2.0 %,说明仪器精密度良好。
2.2.8 稳定性试验 取同一供试品溶液,分别于0 h、3 h、5 h、7 h、9 h进样,依法测定,结果黄芩苷峰面积的RSD(%)值为0.20 %,说明供试品溶液在9 h稳定。
2.2.9 重复性试验 取同一批样品,研细,取6份,每份约0.2 g,精密称定,按“2.2.3供试品溶液的制备”项方法制得供试品溶液,精密吸取供试品溶液各10 μL进样,测定峰面积并计算黄芩苷含量。结果黄芩苷的平均含量为6.4194 mg.g-1,含量的RSD(%)值为0.39 %,说明重复性良好。
2.2.10 中间精密度试验 取同一批样品,研细,取12份,每份约0.2 g,精密称定,按“2.2.3供试品溶液的制备”项方法制得供试品溶液,精密吸取供试品溶液各10 μL分别在不同时间注入两台不同液相色谱仪(每台测6份),测定峰面积并计算黄芩苷含量。结果黄芩苷的平均含量为6.32 mg.g-1,黄芩苷含量的RSD(%)值为1.83%,说明中间精密度良好。
2.2.11 加样回收率试验 取同一批已知含量的样品(含量为6.4194 mg.g-1),研细,取6份,每份约0.1 g,精密称定,置具塞锥形瓶中,分别精密加入黄芩苷对照品溶液(浓度为0.3048 mg.mL-1)2.0 mL,水浴蒸干溶剂,按供试品溶液的制备方法制得供试品溶液,进样测定,计算回收率,结果见表1。

表1 黄芩苷加样回收率试验结果
结果表明,黄芩苷回收率在95%~105%之间,RSD(%)值小于2.0%,说明本方法回收率良好。
2.2.12 样品含量测定 取本品三批各约0.2 g,精密称定,照“2.2.3供试品溶液的制备”制得供试品溶液,在“2.2.1色谱条件”下进样测定,结果见表2。
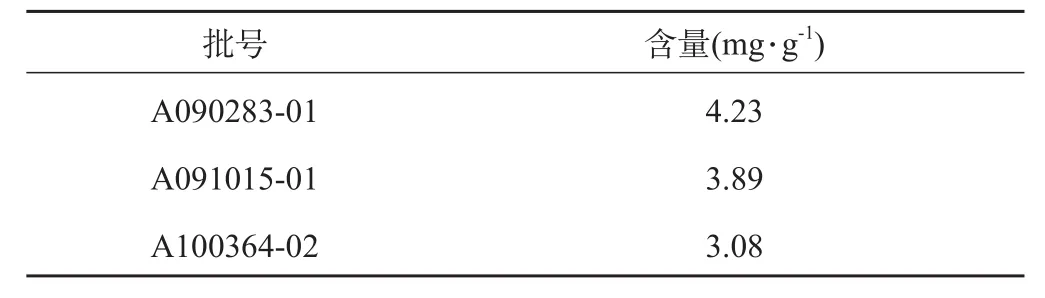
表2 柴胡桂枝颗粒含量测定结果
3 讨论
根据柴胡桂枝颗粒的组方原则与方解,柴胡、桂枝为君药,黄芩、白芍为臣药,本研究按照处方的君臣佐使优先顺序首先对君药“柴胡”进行了薄层鉴别研究,并建立了其薄层色谱定性鉴别方法,结果薄层色谱斑点清晰,阴性无干扰,专属性强,重现性好。
在含量测定研究中,曾对君药“桂枝”中的桂皮醛进行过含量测定的研究,供试品溶液的制备方法采用的是与《中国药典》2010版【桂枝】的含量测定项的方法:用甲醇进行超声处理;流动相为:乙腈-0.1%冰醋酸(33:67),检测波长为290nm。但经计算得到产品中桂皮醛含量约为0.007%,含量较低,不仅进行准确定量难度较大,而且意义不大,因此未选择其作为含测指标。在黄芩苷含量测定中,参考2010版《中国药典》一部【黄芩】含量测定项的流动相[3],使用甲醇-0.1%磷酸(47:53)作为流动相,结果黄芩苷峰与杂质峰分离效果较好,因此确定选用该流动相。在黄芩苷提取条件的考察中,分别对甲醇、70%甲醇、50%甲醇、乙醇、70%乙醇、稀乙醇等提取溶剂进行了比较,结果用70%甲醇和70%乙醇作为提取溶剂时,测得含量较高且无明显差异,但考虑到甲醇的毒性,因此选择70%乙醇作为提取溶剂。除此之外,还考察了提取方式(超声处理、加热回流、浸泡处理),超声处理时间(15 min、30 min、45 min),溶剂用量(25 mL、50 mL、100 mL)对黄芩苷含量的影响,结果以50 mL超声处理30 min提取的黄芩苷含量较高。文中建立的定性、定量方法准确、可行,可有效控制柴胡桂枝颗粒的质量。
[1] 段富津主编.方剂学[M].上海:上海科技出版社,1995.
[2] 刘志勤.中药配方颗粒利弊浅析[J].实用中医药杂志,2007, 28(8):722.
[3] 国家药典委员会.中国药典一部[S].北京:中国医药科技出版社,2010 :282.
(责任编辑:陈思敏)
Study on the quality standard of Chaihuguizhi Granules
WANG Chan, LING Guang, HUANG Zhi-quan, ZHOU Yongqiang, LI Hua-sheng//(Pura (Nanning) Pharmaceutical Co., Ltd., Nannin 530000, Guangxi)
Objective:To establish the quality standard of Chaihuguizhi Granules.Method:TLC was used to identify Chaihu in the prescription. HPLC method was used to carry out the determination. Welch Ultimate XB-C18column(250×4.6mm,5 μm) was used, and mobile phase was methanol-0.1% phosphoric acid(47:53). The fow rate was 1.0 mL.min-1,and detection wavelength was 280 nm. The column temperature was set at 25℃.Result:TLC Chromatogram were clear without the interference of the blank control. The average recovery of Baicalin in Scutellariae Radix were 100.15% with RSD of 1.22% ( n=6).Conclusion:The methods of identifcation and quantifcation are convenient, accurate and reproducibility. They can be used effectively for the quality control of Chaihuguizhi Granules.
ChaihuguizhiGranules; quality standard; TLC; content determination
R 283
A
1674-926X(2014)01-007-03
培力(南宁)药业有限公司,广西 南宁 530000
Tel:+86 771 321 8026 转 8008 Mol:+86 14795662929
2013-05-02
