槲皮素异戊烯基修饰及清除自由基活性研究
2014-03-01董华强陈链杰张英慧佛山科学技术学院食品与园艺学院广东佛山528231
李 梅,董华强,陈链杰,张英慧(佛山科学技术学院,食品与园艺学院,广东佛山528231)
槲皮素异戊烯基修饰及清除自由基活性研究
李 梅,董华强,陈链杰,张英慧
(佛山科学技术学院,食品与园艺学院,广东佛山528231)
目的:对槲皮素分子进行异戊烯化结构修饰,探索槲皮素异戊烯基修饰的最佳条件以及修饰产物的抗氧化活性。方法:以槲皮素、溴代异戊烯基为原料,采用威廉姆逊成醚法合成槲皮素异戊烯基修饰物,采用邻苯三酚自氧化法、DPPH法、Fenton反应法检测修饰产物体外对超氧阴离子自由基、DPPH自由基、羟自由基的清除作用。结果:槲皮素异戊烯基修饰的最佳反应条件为槲皮素与异戊烯基溴的比例为1∶1,在催化剂无水碳酸钾的作用下,60℃水浴冷凝逆流反应8h,经柱层析分离获得异戊烯基修饰物,HPLC检测产物出峰时间较槲皮素晚,获得的产物可能有两种,峰面积为48.9%。槲皮素经异戊烯基化修饰后,所得产物对羟自由基的清除率显著增加;低浓度时对超氧阴离子自由基的清除能力也增强,但对DPPH自由基的清除率低于槲皮素。结论:对槲皮素进行异戊烯基修饰,所得的异戊烯基修饰物是生物活性比槲皮素更高的新型活性化合物。
槲皮素,异戊烯化修饰,自由基,清除
自由基是人体正常代谢过程中的产物,具有高度的化学活性,可对机体产生毒害,生命活动的代谢过程中不断产生各种氧自由基,是产生疾病的主要原因之一。从中草药活性成分中寻找和开发具有较强清除自由基作用的低毒抗氧化剂已成为人们研究的热点[1]。槲皮素(quercetin,3,3’,4’,5,7-五羟基黄酮,结构见图1)是含量最为丰富的黄酮类化合物之一,具有广泛的抗肿瘤、抗血小板、抗氧化等药理作用,但该化合物含有多个极性基团羟基,亲脂性弱,同时由于羟基在分子间形成氢键,晶格能较高,亲水性也很差(槲皮素在水中溶解度为7μg/mL),导致其生物利用度低,大大限制了其临床应用[2-5],因此,槲皮素及其衍生物的合成及生物活性研究越来越受到人们的关注。近年来,学者们利用槲皮素分子中的活性基团——羟基,合成了一系列的槲皮素衍生物,期望改善槲皮素的药物性能[6-9]。异戊烯黄酮类化合物是黄酮类化合物中独特的一类。研究表明,异戊烯基的存在极大的增长了该类化合物的亲脂性,使得化合物分子能够强烈的亲和生物膜,进而可引起相关生物活性的显著提高[10-11]。对槲皮素进行异戊烯基修饰,可能会合成新的具有较高生物活性的物质。
本研究拟对槲皮素分子进行异戊烯化结构修饰,并对槲皮素及其异戊烯基化修饰物的抗氧化能力进行比较,为寻找新型、高效、低毒的槲皮素修饰物提供初步的实验依据。
1 材料与方法
1.1 材料与仪器
槲皮素(95%)、异戊烯基溴(90%) 国药集团化学试剂有限公司;其他试剂 均为市售分析纯。
2690高效液相色谱仪 美国Waters公司;722可见分光光度计 上海菁华科技仪器有限公司。
1.2 实验方法
1.2.1 槲皮素异戊烯基修饰物的冷凝逆流合成 利用异戊烯基溴取代槲皮素中某一位置的H原子,从而发生直接异戊烯基化的取代反应。合成路线如图1所示[12]。
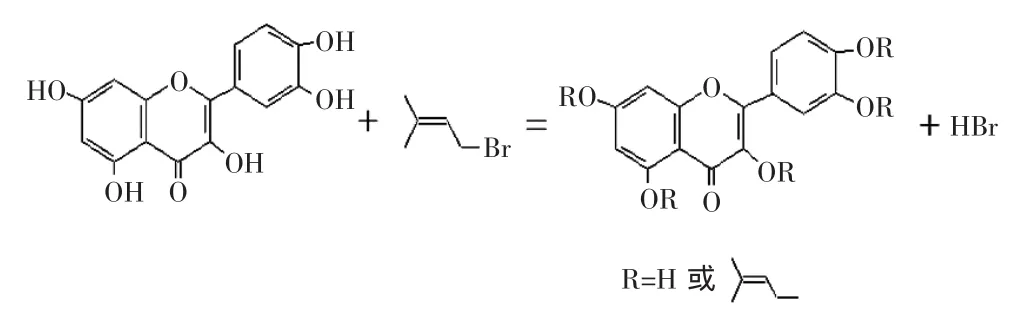
图1 槲皮素异戊烯基修饰物合成路线图Fig.1 Synthetic roadmap of quercetin isopentenyl modifier
按照以上路线图,准确称量(0.302g,1mmol)的槲皮素,50mL丙酮溶解,加入少量无水碳酸钾(催化剂),0℃冰浴条件下加入与槲皮素相应摩尔比例(1∶1、1∶2、1∶3)的异戊烯溴丙酮溶液,振荡均匀后,于58~62℃下冷凝逆流(密封、避光)4~16h,利用薄层层析法(TLC)跟踪反应进程。反应完成后滤去碳酸钾,用丙酮润洗旋转蒸发,蒸干产物用乙醚/乙酸乙酯萃取,浓缩,经柱层析分离(二氯甲烷∶乙酸乙酯=4∶1),得黄褐色固体,即槲皮素异戊烯基修饰物。用高效液相色谱法(色谱条件,色谱柱:C18(250nm×416nm,5滋m)反相液相色谱柱;流动相:甲醇(色谱纯);流速:1mL/min;检测波长:360nm;柱温:25℃;进样量:10滋L。检测器:UV)测定峰值,对比底物槲皮素与反应后的异戊烯基修饰产物的出峰时间和峰值差异。
1.2.2 槲皮素及其异戊烯基化修饰物抗氧化活性测定 以槲皮素为对照,研究不同浓度的槲皮素异戊烯基化修饰物对不同体系自由基的清除能力。
1.2.2.1 对羟自由基的清除作用 比色法测定Fenton反应生成的羟自由基,在各试管中加入不同浓度的槲皮素、槲皮素异戊烯基修饰物0.5mL,再依次加入9mmol/L Fe2+溶液0.5mL、9mmol/L水杨酸-乙醇溶液0.5mL,最后加入9.1mmol/L H2O25mL启动Fenton反应,摇匀后在510nm测量不同浓度下的吸光度为A1。取0.5mL蒸馏水取代9mmol/L Fe2+溶液测定吸光度为A2。取0.5mL蒸馏水代替不同浓度样液测吸光度为A3。
1.2.2.2 对超氧阴离子自由基的清除作用 采用邻苯三酚自氧化法测定不同浓度的槲皮素、槲皮素异戊烯基修饰物对超氧阴离子自由基的清除作用。于试管中加入相应试剂,25℃恒温预热20min,取混合液3mL于比色皿中加入45mmol/L邻苯三酚(用0.01mol/L HCl配成)0.1mL,摇匀反应4min后在波长325nm处测定吸光度值,其中,A1为9mL pH8磷酸盐缓冲液+1mL样液+0.1mL 45mmol/L邻苯三酚时的吸光度;A2为9mL pH8磷酸盐缓冲液+1mL样液时的吸光度;A3为9mL pH8磷酸盐缓冲液+1mL蒸馏水+0.1mL 45mmol/L邻苯三酚时的吸光度。
1.2.2.3 对DPPH自由基的清除作用 比色法测定槲皮素及其异戊烯基修饰物对DPPH·的清除作用:DPPH用95%乙醇配制0.0001mol/L溶液,于试管中加入相应试剂,25℃恒温预热30min,在波长517nm下测定吸光度。其中,A1为5mL DPPH溶液+0.5mL样液时的吸光度;A2为5mL 95%的乙醇+0.5mL样液时的吸光度;A3为5mL DPPH溶液+0.5mL蒸馏水的吸光度。
1.2.2.4 自由基清除率P(%)的计算 以上各体系测定所得的吸光度为A1、A2和A3代入以下公式,计算不同浓度的槲皮素及槲皮素异戊烯基化修饰物对不同体系自由基的清除能力。
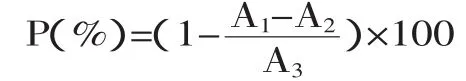
1.3 数据处理
实验数据利用Excel进行整理,利用DPS统计软件进行统计分析。
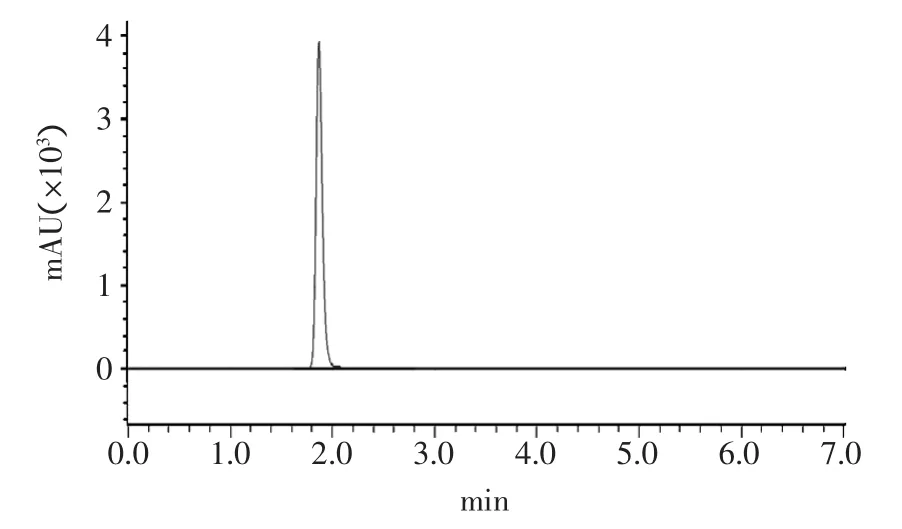
图2 反应物槲皮素色谱图Fig.2 Chromatogram of reactants quercetin
2 结果与分析
2.1 槲皮素异戊烯基修饰物的合成
由于槲皮素分子中存在着五个羟基官能团,即存在多个反应位点,导致反应的选择性差,合成的产物可能是单取代反应产物,也可能是多取代反应产物,将槲皮素与异戊烯基溴按(1∶2,1∶3)的比例于58~62℃下冷凝逆流反应4~16h后,发现反应产物经薄层层析法监测,斑点复杂,重现性差,意味着反应选择性差,副产物多,而两者按1∶1的比例合成时,TLC监测的斑点集中少数几个点,且重现性较好,推测由于槲皮素分子结构中有5个羟基酸性各不相同,反应活性也不相同,在弱碱(K2CO3)存在条件下,可能是苷原上的酚羟基选择性的连接异戊烯基,从而得到较高产率的单一或几种衍生物。实验还发现,槲皮素与异戊烯基溴1∶1的比例,有催化剂无水碳酸钾作用条件下,在60℃水浴下反应8h后得槲皮素异戊烯基修饰产物的数量最多。该产物经柱层析分离,获得纯度较高的单取代异戊烯基修饰产物。

图3 合成后产物色谱图Fig.3 Chromatogram of synthetic product
由图3可知,反应产物主要有两种物质,保留时间分别为4.387min和4.782min,尤其是后一种产物的峰面积占48.9%。产物的保留时间比槲皮素的出峰时间1.877min晚2.51min和2.905min,可以得出:第一,保留时间不同,组分不同,两种产物是不同于反应物槲皮素的新物质;第二,高效液相所用柱子为C18反相液相色谱柱,出峰时间越晚,极性越小,因此,可推测4.387min和4.782min出峰的新物质极性比1.877min出峰的反应物槲皮素极性小,符合产物特性。
2.2 槲皮素及其异戊烯基修饰物的抗氧化活性
2.2.1 槲皮素及槲皮素异戊烯基化修饰物对羟自由基的清除能力 羟基自由基是最活泼的自由基,也是毒性最大的自由基,它可与活细胞中的任何分子发生反应而造成损害,且反应速度快,能杀死红细胞,降解DNA、细胞膜和多糖化合物,许多由它所致的有害效应在加入羟自由基的清除剂后会明显降低,所以羟自由基清除率是评价物质对自由基的清除效果的最常用的指标之一。槲皮素是一种天然强氧化剂,大量研究表明,槲皮素的酯类衍生物和金属配合物具有比槲皮素更强的抗氧化活性[13-14]。从图4可知,槲皮素和异戊烯基修饰物都具有较强的清除羟基自由基的活性,随着浓度的增大,两者清除羟基自由基的活性均急剧增加,呈一定的量效关系。槲皮素异戊烯基修饰物的清除活性明显强于槲皮素,样液浓度同为40μmol/L时,异戊烯基修饰物对羟自由基的清除率已经达到87.41%,而槲皮素对羟自由基的清除率不足50%,说明对槲皮素进行异戊烯基修饰后,其对羟自由基的清除能力会大大提高。
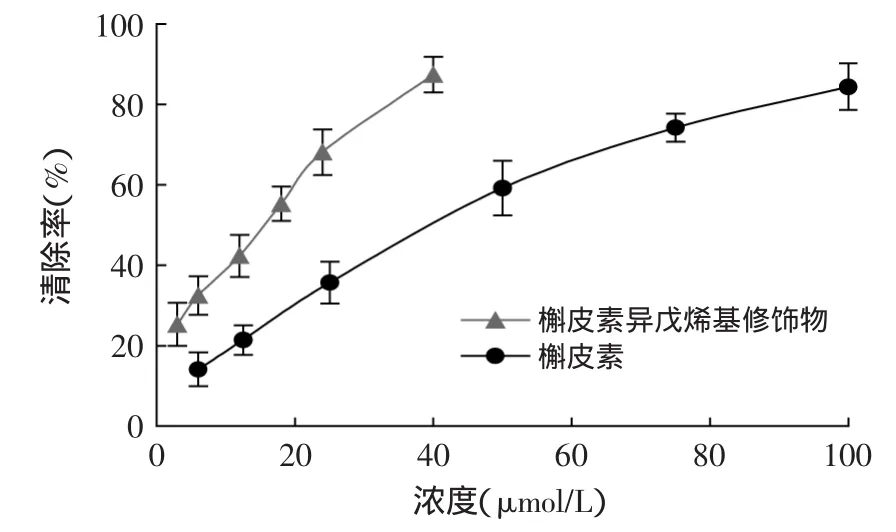
图4 槲皮素及其异戊烯基化修饰物对羟自由基的清除率Fig.4 Scawenging activities of quercetin and quercetin prenylation modification to·OH
2.2.2 槲皮素及槲皮素异戊烯基化修饰物对超氧阴离子自由基的清除能力 生物体内氧化还原反应中,大致有2%~5%的氧会产生超氧阴离子自由基,超氧阴离子自由基的毒性是机体发生氧中毒的主要原因,表现在使核酸链断裂、多糖解聚和不饱和脂肪酸过氧化作用,进而造成遗传突变、膜损伤、酶系失活、线粒体氧化磷酸化作用改变等一系列变化。
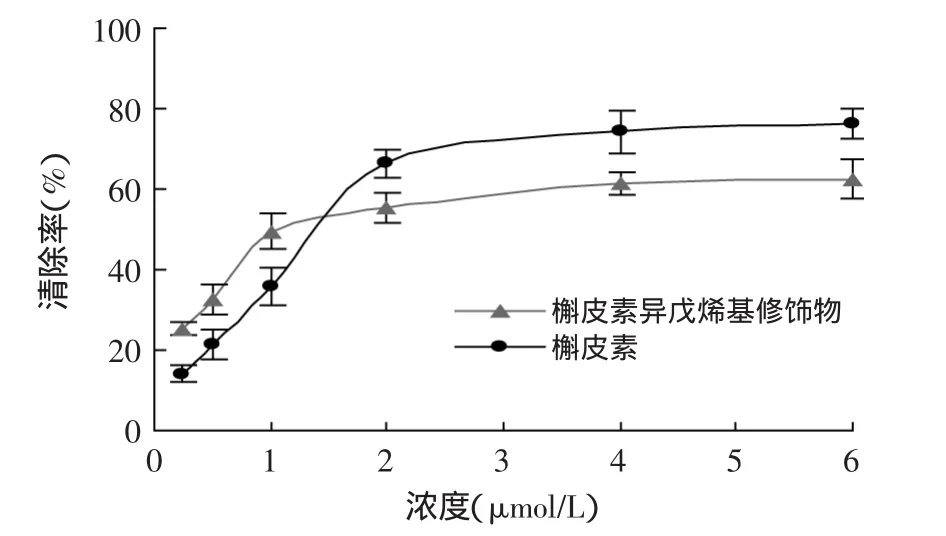
图5 槲皮素及其异戊烯基化修饰物对超氧阴离子的清除率Fig.5 Scawenging activities of quercetin and quercetin prenylation modification to O2-·
不同浓度的槲皮素及槲皮素异戊烯基修饰物对O2-·的清除率见图5,槲皮素和槲皮素异戊烯基修饰物都具有较强的清除O2-·的作用,随着浓度的增加,清除率也呈明显上升趋势,呈现量-效关系。在低浓度时(0.25~1.5μmol/L),槲皮素异戊烯基修饰物的清除率高于槲皮素(p<0.05),在高浓度时(1.50~6.0μmol/L),槲皮素高于槲皮素异戊烯基修饰物(p<0.05),这与对羟自由基的清除作用表现不同,槲皮素钼配合物也有相似表现[15],这可能是因为槲皮素及槲皮素异戊烯基修饰物对O2-·和·OH反应的活性部位和作用机制存在差异,具体的机理尚需进一步的研究。
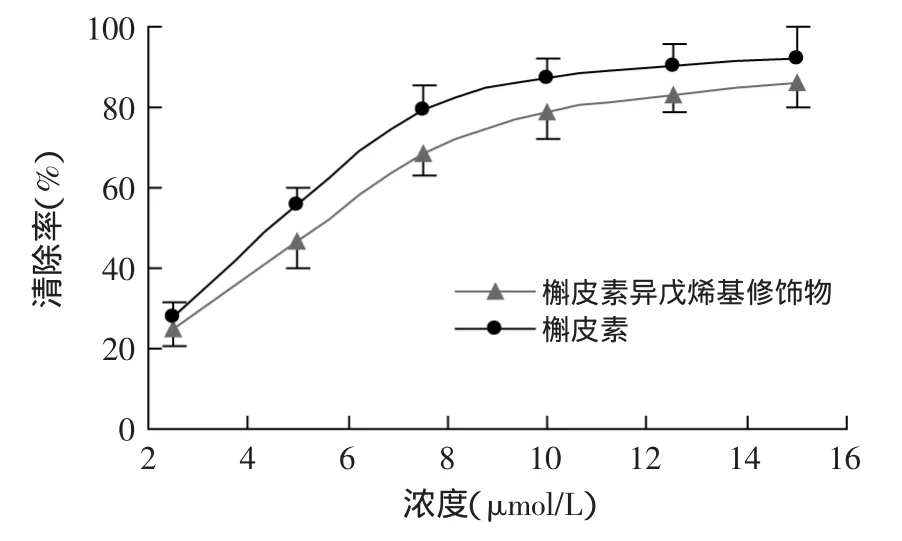
图6 槲皮素及其异戊烯基化修饰物对DPPH·的清除率Fig.6 Scawenging activities of quercetin and quercetin prenylation modification to DPPH·
2.2.3 槲皮素及槲皮素异戊烯基化修饰物对DPPH·的清除能力 DPPH·在有机溶剂中是一种稳定的自由基,在517nm处对光有较强的吸收,当有自由基消除剂存在时,其孤电子被配对,吸收消失或减弱。因此,可通过检测自由基的清除情况,来评价某物质的氧化能力。自由基清除率越大,物质的抗氧化能力越强。
实验结果表明(图6),槲皮素及槲皮素异戊烯基化修饰物均有较强的清除DPPH自由基的能力,且随样液浓度的增加而增加,相比,槲皮素对DPPH自由基的清除能力更强,但两者无显著差异,槲皮素进行异戊烯基修饰后,并不能增强其对DPPH自由基的清除活性。
2.3 槲皮素及其异戊烯基化修饰物对不同体系自由基清除率的比较
以清除自由基达到稳定态50%清除率所需加入槲皮素或槲皮素异戊烯基修饰物的量为IC50(μmol/L),用以表示其抗氧化能力。IC50值越小,达到50%自由基清除率所需的抗氧化剂越少,表明其抗氧化能力越强。从表1可以看出,槲皮素对超氧阴离子自由基的清除能力最强,其次是DPPH自由基,对羟自由基的清除能力最弱,经异戊烯基修饰后,产物对羟自由基的IC50为15.27μmol/L,远小于槲皮素的39.53μmol/L,低浓度时,异戊烯基修饰物对超氧阴离子自由基的清除能力也较槲皮素更强,但对DPPH·的清除能力较槲皮素减弱,具体原因尚待进一步的研究。

表1 槲皮素及槲皮素异戊烯基化修饰物体外清除自由基IC50(μmol/L)Table 1 Quercetin and quercetin isopentenyl modification to different free radicals scavenging IC50(μmol/L)
3 结论
3.1 本实验对槲皮素分子进行异戊烯化结构修饰,探索出槲皮素异戊烯基修饰产物的最佳条件:槲皮素反应物与异戊烯基溴的比例为1∶1,在催化剂无水碳酸钾的作用下,60℃水浴冷凝逆流反应8h。经柱层析分离可获得纯度较高,可能包含两种成分的异戊烯基修饰物。
3.2 槲皮素具有较强的体外抗氧化活性,对其结构进行异戊烯基化修饰,所得的异戊烯基化修饰物的体外抗氧化活性会显著增强,表现为对羟自由基的清除率较槲皮素显著增加;低浓度时对超氧阴离子自由基的清除能力也较槲皮素强,但对DPPH自由基的清除率低于槲皮素。
3.3 对槲皮素进行异戊烯基修饰,获得的槲皮素异戊烯基修饰物可能是生物活性比槲皮素更高的新型活性化合物,具体合成产物的结构及其食用和药用价值有待进一步的研究。
[1]虞跃.近年来我国中草药活性成分结构修饰及类似物合成的研究进展[J].时珍国医国药,2006,17(6):1079-1080.
[2]王艳芳,王新华,朱宇同.槲皮素药理作用研究进展[J].天然产物研究与开发,2003,15(2):171-173.
[3]Boots AW,Haenen GRMM,Bast A.Health effects of quercetin:from antioxidantto nutraceutical[J].European Journal of Pharmacology,2008,585:325-337.
[4]彭游,付小兰,陶春元,等.槲皮素化学修饰与体内转运过程研究进展[J].天然产物研究与开发,2012,24:398-405.
[5]Zhou J,Wang L F,Wang J Y,et al.Antioxidative and antitumour activities of solid quercetin metal(11)complexes[J].Transition Metal Chemistry,2001,26:57-63.
[6]陈慧娟.槲皮素-钼配合物的结构表征及生物活性研究[D].郑州:郑州大学,2010.
[7]郭瑞霞,李力更,霍长虹,等.槲皮素甲基化衍生物的半合成及构效关系[J].中草药,2013,44(3):359-369.
[8]辜艳.水溶性槲皮素衍生物的合成[D].南京:南京理工大学,2013.
[9]魏素梅.槲皮素衍生物的合成研究[D].济南:山东师范大学,2009.
[10]于令军.异戊烯基黄铜类化合物的合成方法及雌激素样活性研究[D].杭州:浙江大学,2004.
[11]陈积常,黄初升,刘红星,等.具有生物活性的异戊烯基及香叶基黄酮类化合物[J].化学技术与开发,2013,42(1):12-17.
[12]张毅.多穗柯黄酮异戊烯改性及性质研究[D].广州:华南理工大学,2011.
[13]朱玮,翟广玉,樊卫华,等.槲皮素酯类衍生物的研究进展[J].化学与黏合,2011,22(6):67-71,79.
[14]吴春,黄梅桂,车春波.槲皮素-锌(Ⅱ)配合物清除自由基的活性研究[J].食品工业科技,2010,31(1):128-129,247.
[15]贾小燕,李文杰,柴保臣.槲皮素-钼配合物的抗氧化作用[J].郑州大学学报:医学版,2008,43(3):588-591.
Study on quercetin isopentenyl modification and free radical scavenging activity
LI Mei,DONG Hua-qiang,CHEN Lian-jie,ZHANG Ying-hui
(College of Food and Horticulture,Foshan University,Foshan 528231,China)
Objective:The best conditions of synthesizing quercetin isopentenyl modifier and the antioxidant activity of modified products were discovered.Methods:The Williamson forming ether method was adopted to synthesizing quercetin isopentenyl modifier with quercetin and prenyl bromide as raw reactants.Moreover,the scavenging effects of modified products in vitro on superoxide anion(by pyrogallol autoxidation method),DPPH radical and hydroxyl radicals(by Fenton reaction method)were evaluated.Results:The optimal reaction conditions to synthesize quercetin modifier were quercetin and prenyl bromide ratio of 1∶1,the catalyst role of anhydrous potassium carbonate,60℃ water bath reflux condensation reaction 8h,separated by column chromatography to obtain modifications.HPLC retention times of the product detected later than quercetin,the product obtained may have two,peak area 48.9%.Quercetin by isopentenyl modification,the resulting products on hydroxyl radical and superoxide anion scavenging rate was significantly increased,but the removal of the DPPH radical was lower than that of quercetin.Conclusion:After quercetin was modified by isopentenyl,the resulting product was a new active compounds which have higher biological activity than quercetin.
quercetin;prenylation modification;free radicals;scavenging
TS201.2
A
1002-0306(2014)14-0084-04
10.13386/j.issn1002-0306.2014.14.009
2013-09-24
李梅(1973-),女,副教授,研究方向:食品安全。
国家自然科学基金项目(31071537);佛山科学技术学院校级重点课题。
