某低品位复杂铝土矿中高岭石与一水硬铝石的分离方法问题研究
2014-02-26周海波李玉茹黄宝贵
杨 静 周海波 李玉茹 王 悦 黄宝贵
(长沙矿冶研究院有限责任公司,长沙 410012)
0 引言
工业上用于冶炼铝的含铝矿物主要是铝土矿,且其物质相态组成多以三水铝石(Al2O3·3H2O)、高岭石(Al2O3·2SiO2·2H2O)和一水硬铝石(Al2O3·H2O)等为主。但不同共生组合关系的铝土矿的具体分布率,却存在着较大的地域性差异。例如,国外的铝土矿多为三水铝石或三水铝石-一水软铝石型矿物;只有俄罗斯、希腊等少数国家是比较单一的一水硬铝石型矿物。我国的铝土矿则主要是以一水硬铝石-高岭石型矿物存在[1],至于三水铝石型矿物,除广西个别地区有工业储量者外,一般分布都很少[2]。在对铝土矿进行化学物相分析时,目前通用的传统方法是用稀碱或稀酸溶液浸取分离三水铝石、稀HF溶液浸取分离高岭石,并于滤渣中测定一水硬铝石[1,3-4]。
上述相态分离方法程序模式虽然已被公认[1-4],但也存在有一定的局限性。例如,当笔者将其用于伴生矿物比较复杂的铝土矿中高岭石与一水硬铝石的分离测定时,屡见不稳定的异常结果,且多为前者偏低、后者偏高。由于对其产生的原因似仍未引起人们的注意,所以本文拟通过实验研究予以查明,并提出解决问题的方法。
1 实验部分
1.1 主要参比物料和试剂
高岭石(精矿,含Al2O337.15%,纯度94.05%);一水硬铝石(精矿,含Al2O368.48%,纯度80.57%);钠长石(精矿,含Na2O 8.33%,纯度70.41%);钾长石(GBW03116,含K2O 9.60,纯度56.87%);钾长石(精矿,含K2O 10.11%,纯度59.89%)和铁质角闪石(尾矿,铁镁硅酸盐矿物约70%;组成不固定,含FeO,MgO,SiO2比较高,Al2O3<1%,主要伴生矿物为游离石英等)。
NaOH(10 g/L)-EDTA(5 g/L)溶液;HF(5+95)溶液;H2SO4(12 mol/L)溶液,NaOH和Na2O2等(均为分析纯试剂)。
1.2 实验方法
1.2.1 传统方法要点
试样经50 mL NaOH(10 g/L)- EDTA(5 g/L)溶液沸水浴浸取20 min溶解三水铝石,滤渣用30 mL HF(5+95)溶液沸水浴浸取15 min以分离高岭石,于余渣中测定一水硬铝石之Al2O3量[1,3-4]。
1.2.2 分离测定一水硬铝石的推荐方法模式
准确称取0.1~0.3 g(精确至0.000 1 g)试样(粒度<0.074 mm)于小瓷坩埚中,并将其置于500 ℃马弗炉中焙烧2 h,取出冷却至室温,将试样移入150 mL烧杯中,加入30 mL刚煮沸的H2SO4(12 mol/L)溶液,立即置于沸水浴上加热浸取2 h(常搅拌),取下流水冷却至室温,搅拌下缓慢加水稀释至约100 mL,冷却后用慢速滤纸(加适量纸浆)过滤,并将沉淀定量移入滤纸上,用HCl(3+97)溶液洗净烧杯,洗沉淀6~8次,再用热水洗2~3次后,将滤纸和沉淀一起移入银坩埚中,干燥、灼烧炭化后取出冷却,加4~6 g NaOH,并于电炉上加热至刚熔化,取下稍冷,加入0.5~0.6 g Na2O2,送入已升温至近300 ℃的马弗炉中,继续升温至约650 ℃,并保持10~15 min,取出冷却、水浸出、加入HCl(1+1)溶液酸化、氨水分离Ca(Ⅱ)、Mg(Ⅱ),用氟盐取代-EDTA容量法测定一水硬铝石等之Al2O3量。
通过对钠(钾)长石中Al2O3量干扰的校正,按下式计算出一水硬铝石中Al2O3的含量结果:


2 实验结果与问题讨论
2.1 问题产生的原因
物质组成分析表明,所检铝土矿原矿石的品位较低,故其相伴脉石矿物共生组合关系具有一定的复杂性(表1)。载体矿物中以高岭石和一水硬铝石为主,三水铝石比较少。脉石类矿物中除游离石英外,就是各种硅酸盐矿物,如钠长石(Na[AlSi3O8])、铁质角闪石(组成不固定,所含成分主要为铁(Ⅱ)、镁、钙等的硅酸盐矿物)以及很少量的钾长石(K[AlSi3O8])等;同时也伴生有少量赤铁矿等。

表1 原矿石主要成分分析结果 Table 1 Results of main component analysis for raw ore /%
关于相伴矿物共生组合关系复杂性的问题,很显然,对于共存有如上所述的脉石类矿物的铝土矿而言,似也称不上有多么复杂。但问题就是实践过程中却屡见难予解释的异常现象。例如,当用传统的选择性溶剂(HF溶液)浸出高岭石而与一水硬铝石分离时,不易获得稳定结果的问题就亟待解决。因此,首先对HF溶液浸出渣物质组成的性质进行了研究:将留于浸出渣中的沉淀物过滤,用水洗涤干净,将盛有沉淀物的滤纸展开,置于110 ℃烘箱中烘干后,进行XRD分析。图1结果证明,其中除已知的一水硬铝石被富集外,游离硅也明显被富集,同时尚存在有少量未完全溶解的钠长石、铁质角闪石、赤铁矿等,物质组成构架除高岭石和三水铝石已不复存在、铁质角闪石和钠长石已明显减少之外,基本上与原矿石相似。但令人费解的是其中却增添了新的相态(NaMgAlF6·xH2O)。对这一反应结果的进一步研究表明, 其原因主要是在用HF溶液浸取分离高岭石的反应过程中,由于伴生的钠长石、铁质角闪石等矿物的大部分都同步被溶解,故其Na+,Mg2+等离子与Al3+一起进入浸出液之中,并与已经存在的F-反应,旋即形成了NaMgAlF6·xH2O次生沉淀,且其与一水硬铝石一并留于余渣中而被误测,乃引起检测结果不稳定的主要原因。

图1 HF溶液分离高岭石后余渣的X射线衍射图谱Figure 1 XRD Spectrum of the residue after kaolinite was separated using HF solution.
2.2 分离高岭石的选择性溶剂的再筛选问题
上述实验已经指出,对同时存在有含钠、镁等脉石类矿物的铝土矿进行物相分析时,因Na+,Mg2+,F-以及Al3+等离子的不相容性,故不宜引用HF溶液作为高岭石的选择性溶剂。因此,必须另行筛选。文献中分离高岭石的选择性溶剂只有三种[3,5-6],其中最早者是用H2SO4(11.5 mol/L)溶液沸水浴浸取经500 ℃预焙烧的试样以分离高岭石(包括三水铝石),并于余渣中测定一水硬铝石之Al2O3量(%)[5]。此法后经验证并给予了充分肯定的同时,另外又提出可用NH4F-HNO3溶液替代之[6]。但二者似仍未见有用于生产实践的报道[1-4],而获得普遍推广者,只有蒋月瑾等推荐的用HF(5%)溶液选择溶解高岭石的方法[3]。
上述三种方法中有两个是含F-的,显然,适于本文所需者,唯H2SO4溶液可供选择。因此,笔者对其进行了验证实验,结果指出,H2SO4溶液作为高岭石矿物相的选择性溶剂,并使之与一水硬铝石分离的方法,从首次推荐[5]到系统研究与优化定型[6]等,虽多侧重于理论方面,但其所提出的分离条件参数与操作程序模式等,基本上都是可以直接引用的。因此,本文仅对其在具体样品检测实践中的适应性问题进行了探讨。
2.2.1 基本条件验证实验
当初推荐该方法者指出,试样必须预焙烧脱水方可使高岭石矿物在H2SO4热溶液中完全分解而与一水硬铝石分离;同时指出,脱水条件是500 ℃焙 烧至恒重;在沸水浴上进行溶解反应[H2SO4(11.5 mol/L)溶液预煮沸后使用]时间为4 h,于余渣中测定一水硬铝石之Al2O3量[5]。嗣后其他作者的验证也肯定了500 ℃预焙烧脱水的实验条件,并指出,采用H2SO4(12 mol/L)溶液可以加快浸出反应的速度(高岭石的浸出率:1.5 h接近90%,2 h可达98%)[6]。但对于脱水时间规定为500 ℃焙烧至恒重的操作程序,似显有点模糊,因为实际操作中并不易执行(过于麻烦)。所以笔者特对此做了进一步考查。表2结果指出,参比物料和检测样品在500 ℃马弗炉中预焙烧1.5 h,基本上都可以接近或达到恒重。为了便于操作,检测样品预焙烧脱水的时间均规定为2 h。
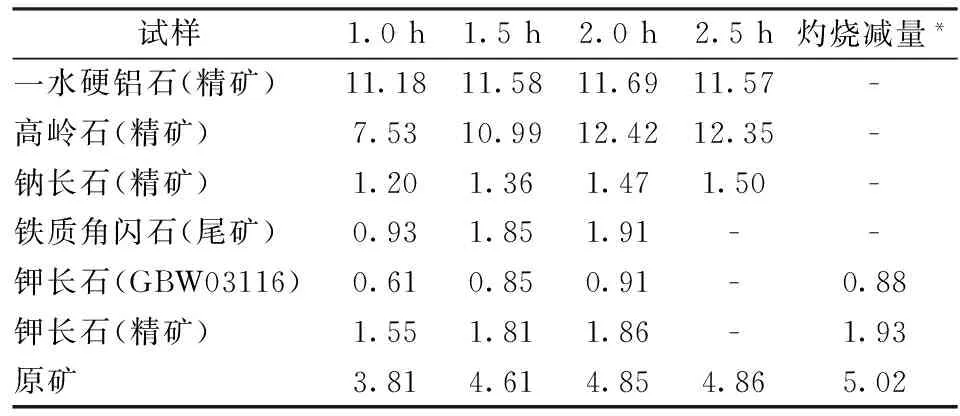
表2 试样500 ℃焙烧恒重与时间关系的实验结果 Table 2 Experimental results for studying the relation between sample constant weight and roasting time at the roasting temperature of 500 ℃ /%
*为常法测得之烧失量。
对于H2SO4溶液浸出反应效果的验证结果指出,与文献报道也基本一致:用12 mol/L预沸腾的H2SO4溶液,旋即于沸水浴上进行浸出(常搅拌)2 h,高岭石的浸出率>98% Al2O3,一水硬铝石的溶失率<1%(0.52%~0.54% Al2O3)。此值在一般工艺过程物料检测中或一水硬铝石分布率较低时,似可不予考虑。
2.2.2 钠(钾)长石中Al2O3干扰的校正问题
鉴于所检物料中伴生有干扰传统分相方法的钠长石等矿物,所以特推荐了H2SO4法[5-6]。但本法却存在有另一类共生成分干扰的问题。为寻找校正这种源自钠长石以及可能存在的少量钾长石矿物中所含之Al2O3量的干扰,对其在H2SO4溶液浸取高岭石矿物相反应过程中的走向问题,进行了研究。从检测H2SO4溶液浸出过高岭石之后的余渣中所得之Na2O(K2O)量结果与TNa2O(TK2O)量对比得知,在该浸出反应过程中,钠长石和钾长石矿物虽也均参与了反应,但其却都只是部分溶解。所以对余存于一水硬铝石滤渣中的钠长石及钾长石矿物中Al2O3量的干扰,都必须进行校正。然而,由于对赋存于长石矿物中的Al2O3量干扰一水硬铝石测定进行直接校正的方法,目前却不易找到。因此,笔者借助于化学物相分析中寻找共存矿物特征性成分的研究[7-8],推荐其所含之 Na2O和K2O作为特征性成分,并根据矿物的物质组成式(Na2O·Al2O3·6SiO2和K2O·Al2O3·6SiO2)将Na2O和K2O量转换为Al2O3量之后即可准确校正之。
当然,用Na2O和K2O作为长石的特征性成分,首先必须准确测定出其含量。但上述实验已指出,Na2O(K2O)在H2SO4溶液浸出反应过程中并非单一走向,为充分利用样品中TNa2O(TK2O)量的检测结果,尚应对双走向的Na2O(K2O)量转换归一。因此,同时推荐了对反应过程中Na2O(K2O)量溶失率(%)进行校正的具体操作程序。表3是根据钠长石和钾长石参比物料及部分检测样品等在H2SO4溶液浸出反应过程中Na2O和K2O的溶失率测定结果的平均值(Na2O为5.87%,K2O为3.82%),并将其作为溶失率的换算系数,这样就只需通过样品中的TNa2O和TK2O量,而无需对产物中的余Na2O和余K2O再进行测定,即可计算出二者在余渣中的分别含量;继而根据钠长石及钾长石的物质组成式转换为Al2O3的分别含量予以校正之(1.2.2节)。同时尚应指出,由于实际检测样品中伴生的钾长石矿物很少,所以K2O的含量自然也很低。表3结果证明,K2O在H2SO4溶液浸出反应过程中的溶失率仅3.82%,故在1.2.2节检测结果的校正计算中,省略K2值项,而直接以TK2O量计之,不会有明显影响。
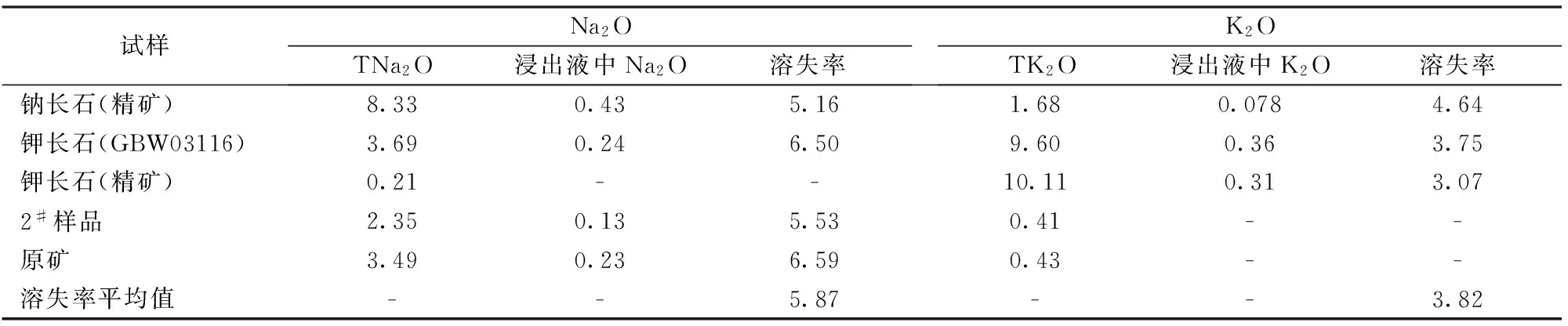
表3 长石Na2O和K2O在H2SO4浸出反应过程中溶失率的测定结果 Table 3 Determination results of the dissolving-loss rate for feldspar Na2O and K2O in the H2SO4 leaching reaction /%
2.2.3 样品中一水硬铝石的测定
按1.2.2节所述程序操作对生产样品中的一水硬铝石进行分离测定,表4指出,本法结果低于传统方法(HF)法[1],但其应比较接近实际值,因XRD分析结果表明,经HF溶液分离出高岭石之后,在一水硬铝石的待测滤渣中存在有明显的外来含铝物质(NaMgAlF6·xH2O),故其应属偏高结果。
表4 样品中一水硬铝石的测定结果
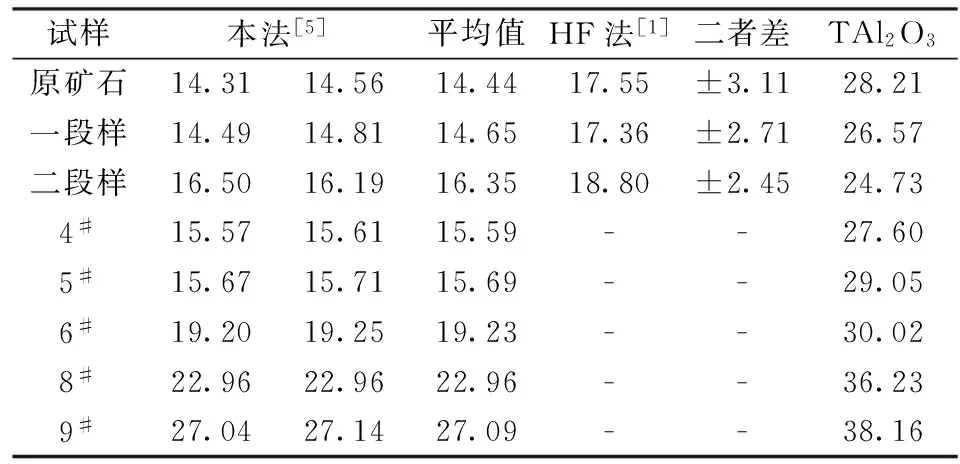
Table 4 Determination results of disporite in the samples /%
3 结语
研究查明,由于共存的Na+,Mg2+,Al3+和F-的不相容性(形成NaMgAlF6·xH2O次生沉淀,且其与一水硬铝石一并留于浸出渣之中而直接被误测),所以在对共存有含钠和含镁等脉石类矿物的铝土矿中的一水硬铝石进行测定时,不宜引用传统的选择性溶剂(HF溶液)使其与高岭石分离的操作程序。
验证实验指出,对所述铝土矿进行化学物相分析时,引用H2SO4溶液作选择性溶剂,分离出高岭石(包括三水铝石)之后,于余渣中测定一水铝石的方法可获得比较满意的结果。同时对存在的部分未溶长石矿物中Al2O3量干扰的问题,提出了有效的校正方法:推荐Na2O(K2O)作长石矿物的特征性成分,根据TNa2O和TK2O含量,通过长石矿物的物质组成式(Na2O·Al2O3·6SiO2和K2O·Al2O3·6SiO2)计算出Al2O3量校正之。
[1] 张惠斌,主编.矿石和工业产品化学物相分析[M].北京:冶金工业出版社,1992:39-47.
[2] 柳建春,黄宝贵.红土型铝土矿中三水铝石的分离方法研究[J].岩矿测试,1995,14(3):161-165.
[3] 蒋月瑾,康永莉.一九八○年全国岩矿分析经验交流会论文集[M].北京:地质出版社,1980:516-518.
[4] 龚美菱.相态分析与地质找矿[M].北京:地质出版社,2007:11-13.
[5] В. В.多利伏-多布洛沃尔斯基,Ю.В.克利门科,著.矿石物相分析[M].陈树元,唐肖玫,译.北京:冶金工业出版社,1956:129-133.
[6] Масленицкий Н Н,Федорова М Н,Милнер Р С, Будникова Н А. Химический фазовый Аналиэ Алюминиевого Сыръя и неметаллческх Полеэных Ископаемых[M].Москва:“НЕДРА”,1983:61-77.
[7] 黄宝贵,曹文涛.榴辉岩中绿辉石的测定方法研究[J].岩矿测试,1998,17(4):249-253.
[8] 黄宝贵.我国化学物相分析的进展[J].分析化学,1999,27(12):1454-1461.
