胰腺癌体部伽玛刀治疗的剂量学研究
2014-02-08奇康静波李建国李启亮
朱 奇康静波李建国李启亮
胰腺癌体部伽玛刀治疗的剂量学研究
朱 奇①康静波①李建国①李启亮①
目的:比较并分析OUR-QGD型体部伽玛刀(γ-SBRT)与三维适形放射治疗(3D-CRT)在胰腺癌治疗计划中剂量学数据,为胰腺癌放射治疗技术的选择提供依据。方法:分别对10例胰腺癌患者(胰头癌、胰体尾癌各5例)制定体部伽玛刀及三维适形放射治疗计划,处方剂量均要求50 Gy剂量曲线包绕肿瘤计划靶体积(PTV)。比较两种PTV的适形指数和均匀指数,根据剂量体积直方图(DVH)显示的结果计算靶区剂量和危险器官(OARs)照射剂量。结果:3D-CRT计划的均匀指数好于γ-SBRT,两者适形度近似。γ-SBRT计划中靶区剂量明显高于3D-CRT,且OARs受照射剂量较低。结论:γ-SBRT治疗胰腺癌明显提高靶区照射剂量,更好的保护靶区周边正常组织,可以作为治疗胰腺癌安全有效的放射治疗技术。
胰腺癌;体部伽玛刀;三维适形放疗
胰腺癌是消化系统常见的恶性肿瘤之一,近年来发病率在世界及国内大中城市呈明显增高趋势。由于胰腺解剖位置深且隐蔽,发病早期缺少特异性症状,极易侵犯周围脏器和发生转移,多数患者确诊时已属中晚期,手术切除率往往不足20%[1-2]。因此,放射治疗等非手术治疗在胰腺癌治疗中起着重要的作用,但由于其所处的位置,前方有胃、横结肠覆盖,且胰头被十二指肠包绕,放射剂量受到胃肠道耐受剂量的限制,胰腺癌放射敏感性较低,导致常规放射治疗效果不佳[3]。
随着放射治疗技术的发展,出现了三维适形放疗和体部伽玛刀等放射治疗方法。如何选择合理的放射技术以实现最大限度提高靶区照射剂量,同时减少正常组织的损伤是胰腺癌放射治疗的关键。
本研究通过比较OUR-QGD型体部伽玛刀(γ-ray stereotactic body radiation therapy,γ-SBRT)与三维适形放射治疗(Three dimensional conformalradiation therapy,3D-CRT)在胰腺癌治疗计划中剂量学数据,为临床治疗放射技术的选择提供依据。
1 资料与方法
1.1 一般资料
选择10例经病理学或PET/CT、肿瘤标志物(CA-199等)检查明确诊断的胰腺癌患者,其中胰头癌5例,胰体、尾癌5例,肿瘤直径≤5 cm,肿瘤病灶形状规则。
1.2 仪器设备
γ-SBRT的立体定向伽玛射线全身治疗计划系统(wTPS99),3D-CRT计划系统(AccuSoft-WB V3.0)为对照系统。
1.3 治疗方法
(1)CT模拟定位。按照要求通过真空袋对患者进行塑形并固定体位,均选取仰卧位。将定位框架(N形定位标尺)安放在靶区位置,保证病灶处于框架范围内,患者在平静呼吸下进行CT薄层(3~5 mm)扫描并增强,扫描范围自膈顶上至右肾下极,获得定位图像。
(2)靶区及危险器官的勾画。将定位图像分别传输至wTPS99及AccuSoft-WB治疗计划系统,勾画出肿瘤靶区(gross tumor volume,GTV),临床靶区(clinical target volume,CTV)和危险器官(organs at risk,OARs),OARs主要包括胃、小肠(十二指肠)、脊髓以及肾脏。
(3)计划设计。γ-SBR治疗计划根据肿瘤计划靶体积(PTV)的形状及大小,选择适当的靶点,在轴位图像上进行单靶点或多靶点拟合(采用较少靶点,尽量选用小号准直器),调整靶点的位置分布和各自权重,尽量达到适形、均匀的剂量分布。3D-CRT采用10MV-X射线,4~6个共面或非共面野进行设野。射野原则: ①尽量避开OARs;②射野边平行于靶区的长轴;③入射面到靶中心距离短;④与相邻射野夹角大。处方剂量均要求50 Gy剂量曲线包绕肿瘤PTV。
(4)计划比较。对两种计划在靶区剂量分布、适形指数(CI)、均匀性指数(HI)及剂量体积直方图(DVH)等方面的差异进行比较。其中CI值:CI=(Vt.ref/ VT)×(Vt.ref/Vref),Vt为靶体积,Vt.ref为参考等剂量线所包绕的靶区体积,Vref为参考等剂量线所包绕的所有区域的体积;HI值:HI=D5/D95,D5和D95分别代表5%和95%体积的PTV受照射的剂量。CI的范围介于0和1之间,值越大表示适形度越好。HI越低,靶区剂量均匀性越好。Coverage值:指处方等剂量曲线覆盖病灶体积百分数。
1.4 统计学方法
利用SPSS18统计软件处理。计量资料结果以均值±标准差(x±s)表示,统计方法采用t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 靶区内剂量分布
γ-SBRT计划中靶区内最高剂量(High Dose)、最低剂量(Low Dose)及平均剂量(Mean Dose)均明显高于3D-CRT计划对应值,见表1。
表1 γ-SBRT与3D-CRT靶区剂量比较±s, Gy)

表1 γ-SBRT与3D-CRT靶区剂量比较±s, Gy)
?
2.2 γ-SBRT计划中OARs受量比较
γ-SBRT治疗计划中OARs受量明显低于3D-CRT,见表2。
表2 γ-SBRT与3D-CRT计划危险器官受量比较(±s, Gy)

表2 γ-SBRT与3D-CRT计划危险器官受量比较(±s, Gy)
?
2.3 γ-SBRT与3D-CRT计划中的CI、HI及Coverage值比较
γ-SBRT与3D-CRT计划中CI、Coverage值相比,无统计学差异,γ-SBRT计划HI高于3D-CRT,见表3。
表3 γ-SBRT与3D-CRT计划CI与HI比较(±s, Gy)
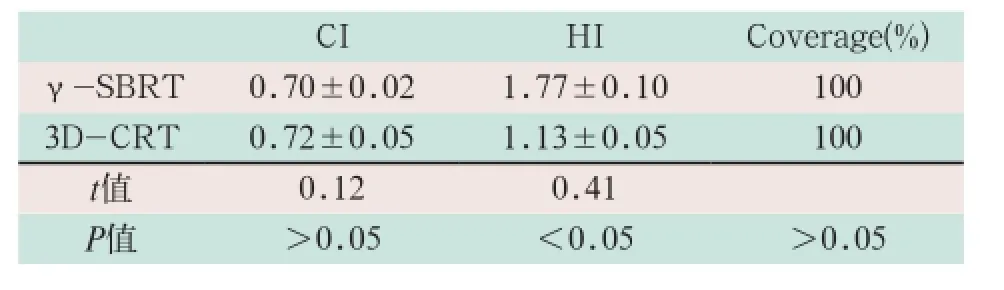
表3 γ-SBRT与3D-CRT计划CI与HI比较(±s, Gy)
?
3 讨论
由于胰腺癌早期缺乏典型临床表现,待明确诊断时往往已属晚期,手术切除率为10%~20%,其中50%~60%为局部晚期胰腺癌[4]。该病病程短、进展快及病死率高为其发病特点,中位生存期在6个月左右,5年生存率仅为2%~3%[5-6]。
放射治疗是胰腺癌重要的治疗手段,随着放疗设备和放射技术的发展,针对胰腺癌的临床治疗也有了很大的发展[7]。就理论而言,只要给予足够的放射剂量,肿瘤是完全可以控制的,但是临床实践中很难做到这一点,原因是肿瘤周围正常组织的放射耐受剂量限制了肿瘤部位的照射剂量[8]。如何找到一种放射治疗方法可以达到肿瘤区域尽可能高的照射剂量,同时使肿瘤周围正常组织受到尽可能少的照射剂量,是放射治疗技术发展的首要任务。
3D-CRT是一种使得高剂量区分布的形状在三维方向上与病变靶区形状一致的放射治疗技术。该技术可使靶区获得高剂量照射,而对靶区外正常组织受照射剂量减少,从而有效提高肿瘤局部控制率,减少放射治疗的并发症[9]。γ-SBRT是立体定向放射治疗的一种特例,是利用立体定向等中心技术把放射线聚焦在病灶,使高剂量区分布的形状在三维方向上与靶区形状一致,最大限度地将放射线剂量集中于病变区域,而使周围正常组织减少或避免不必要的照射,提高局部控制率。伽玛刀治疗胰腺癌的优势在于高度精确性,既能保证胰腺获得高剂量照射,边缘剂量达40~50 Gy,且十二指肠受量控制在40 Gy以下,有效避免十二指肠放射性损伤[10-11]。
本研究对于优化后的γ-SBRT计划与3D-CRT计划进行了比较分析,结果显示,γ-SBRT靶区剂量明显高于3D-CRT,γ-SBRT计划中最高剂量和最低剂量相差较3D-CRT大,说明剂量落差大,体现“刀”的剂量学分布。肿瘤靶区邻近OARs受量均在耐受范围内:脊髓≤40 Gy,十二指肠、结肠≤40 Gy,50%肝脏体积受照射剂量≤30 Gy,30%双肾体积受照射剂量≤20 Gy,其中γ-SBRT计划中OARs受照射剂量明显低于3D-CRT计划。基于以上γ-SBRT计划与3D-CRT计划分布特点,结合DVH图和剂量分布曲线图,计算出CI值及HI值。其中γ-SBRT计划与3D-CRT计划比较CI无明显差异,提示γ-SBRT计划的适形度与3D-CRT相似,说明采用较少靶点,尽量选用小号准直器的方法进行单靶点或多靶点拟合,可获得较为理想的适形度。两者的HI值比较有统计学差异,即3D-CRT计划中HI值低于γ-SBRT计划,说明3D-CRT靶区剂量分布更加均匀,而γ-SBRT剂量梯度大。这是因为γ-SBRT采用旋转聚焦及填充式的治疗方法,形成“洋葱皮样”包裹的剂量线[12]。而3D-CRT治疗设备采用多个共面或非共面照射野对靶区照射,形成的高剂量区范围较大,故剂量均匀[13]。γ-SBRT突破了“靶区内剂量分布要求均匀”的传统放射治疗原则,形成“刀”的剂量学概念,靶区中心高剂量更利于杀灭肿瘤中心乏氧细胞和静止期细胞[14-15]。
本研究表明,对于胰腺癌病灶(≤5 cm)的放射治疗,γ-SBRT治疗明显提高靶区照射剂量,更好的保护靶区周边正常组织,在剂量分布及OARs的保护上优于3D-CRT,可以作为治疗胰腺癌的安全有效的放射治疗技术。
[1]Evans DB,Crane CH,Charnsangavej C,et al.The added value of multidisciplinary care for patients with pancreatic cancer[J].Ann Surg Oncol,2008,15(8):2078-2080.
[2]智永宏,齐广珍.胰头癌早期诊断和治疗127例[J].肿瘤研究与临床,2012,23(12):842-843.
[3]朱奇,康静波,聂青,等.康莱特联合体部伽玛刀治疗局部晚期胰腺癌28例[J].中国肿瘤,2013,22(11):931-934.
[4]韩华正,章迎凤.三维适形放疗联合吉西他滨化疗治疗局部晚期胰腺癌28例[J].肿瘤研究与临床,2010, 22(2):124-125.
[5]Cress RD,Yin D,Clarke L,et al.Survival among patients with adenocarci-noma of the pancreas:a population-based study(United States)[J].Cancer Causes Control,2006,17(4):403-409.
[6]沈泽天,武新虎,李兵,等.射波刀治疗局部晚期胰腺癌的临床疗效[J].中国癌症杂志,2012,22(8):589-594.
[7]Das P,Wolff RA,Abbruzzese JL,et al.Concurrent capecitabine and upper abdominal radiation therapy is well tolerated[J].Radiat Oncol,2006, 1:41.
[8]夏廷毅,康静波.体部肿瘤伽玛刀治疗学[M].人民卫生出版社,2010:171-182.
[9]殷蔚伯.肿瘤放射治疗学[M].中国协和医科大学出版社,2008:149-156.
[10]潘德键,王标,周锡建,等.健择单药联合伽玛刀治疗18例晚期胰腺癌疗效观察[J].中国肿瘤,2007,16(9): 741-743.
[11]夏廷毅,于勇,孙庆选,等.全身γ刀治疗胰腺癌75例临床结果分析[J].中国肿瘤,2006,15(8):518-520.
[12]高宏,郎红娟,于得全,等.三维适形照射与体部γ-刀照射剂量学的比较与研究[J].现代肿瘤医学,2010,18(11):2246-2248.
[13]Berber B,Sanabria JR,Braun K,et a1.Emerging role of stereotactic body radiotherapy in the treatment of pancreatic cancer[J].Expert Rev Anticancer Ther,2013,32(5):481-487.
[14]姚锦章,郭日开,陈勇.旋转式伽玛刀的辐射剂量学[J].原子能科学技术,1998,32(5):427-432.
[15]Wulf J,Guckenberger M,Haedinger U,et al.Stereotactic radiotherapy of primary liver cancer and hepatic metastases[J].Acts Oncol, 2006,45(7):838-847.
Dosimetry studies on body gamma knife treatment of pancreatic cancer
/
ZHU Qi, KANG Jing-bo, LI Jian-guo, et al//
China Medical Equipment,2014,11(11):33-35.
Objective: To compare the dosimetry data of OUR-QGD Body gamma knife and Three dimensional conformal Radiation Therapy in pancreatic cancer treatment plan, and to provide evidence for the selection of the radiotherapy technique about pancreatic cancer. Methods: 10 patients with pancreatic cancer, including 5 cases of pancreatic head carcinoma, 5 cases of pancreatic body carcinoma and pancreatic tail carcinoma, ten patients formulate body gamma knife and three-dimensional conformal radiotherapy plan respectively. Prescribed dose requirements 50Gy PTV dose curve surrounding the tumors. To compare conformal index and homogeneity index of planning target volume of two kinds of radiation technology. According to the Dose Volume Histogram,calculate the exposure dose of target organs and organs at risk. Results: The homogeneity index of 3D-CRT were better than those of γ-SBRT, the conformal index of 3D-CRT and γ-SBRT were approximate. At the same time plan target dose of γ-SBRT was significantly higher than that of 3D-CRT and OARs dosage is lower. Conclusion: γ-SBRT obviously improve the target dose of treatment plan about pancreatic cancer, protect normal tissues surrounding the target areas. It can be used as a safe and effective radiotherapy technique in pancreatic cancer treatment.
Pancreatic cancer; Body gamma knife; Three dimensional conformal radiotherapy
10.3969/J.ISSN.1672-8270.2014.11.012
1672-8270(2014)11-0033-03
R735.9
A

朱奇,男,(1978- ),硕士,主治医师。海军总医院肿瘤放射治疗中心,从事恶性肿瘤体部伽玛刀治疗及研究。
2014-02-19
①海军总医院肿瘤放射治疗中心 北京 100048
[First-author’s address]Department of Radiotherapy, Navy General Hospital, Beijing 100048, China.
