抗氧化剂茶多酚反相微乳液的制备
2014-01-18孙静静刘建华王仲妮王正武
孙静静,刘建华,2,王仲妮,王正武,*
(1.上海交通大学农业与生物学院,上海 200240;2.宜宾学院化学与化工学院,江苏 宜宾 644000;3.山东师范大学化学化工与材料科学学院,山东 济南 250014)
抗氧化剂茶多酚反相微乳液的制备
孙静静1,刘建华1,2,王仲妮3,王正武1,*
(1.上海交通大学农业与生物学院,上海 200240;2.宜宾学院化学与化工学院,江苏 宜宾 644000;3.山东师范大学化学化工与材料科学学院,山东 济南 250014)
制备茶多酚在亚油酸-水-乙醇体系的反相微乳液,使其成功地添加到亚油酸中,并研究该微乳液体系的相形为、电导率、粒径分布、流变及抗氧化能力等特性。结果表明:当油相亚油酸质量分数大于24% 时,可形成油包水型微乳液。该微乳液体系粒径均一,表现为剪切变稀的流变特征,且具有温度触变性。过氧化值测试结果表明:相比空白微乳液,水相添加0.01 g/mL茶多酚对亚油酸氧化的抑制率为68.32%,添加0.1 g/mL茶多酚对亚油酸氧化的抑制率为92.42%。
亚油酸;茶多酚;反相微乳液;抗氧化剂
亚油酸是一种必需脂肪酸,与其他脂肪酸一起以甘油酯的形式存在于动植物油脂中, 是功能性多不饱和脂肪酸中被最早认识的一种[1]。亚油酸具有降低血清胆固醇水平的作用,对高甘油三酯病人有明显的疗效[2],故将其应用于保健食品已成为近年来研究的重点。但由于亚油酸结构上存在不饱和键而在空气中易发生自氧化转变为反式亚油酸,故在其贮存中需要添加一定的抗氧化剂。目前油脂业主要使用人工合成的油溶性抗氧化剂,如丁基羟基茴香醚(3(2)-tert-butyl-4-hydroxyanisole,BHA)、2,6-二叔丁基-4-甲基苯酚(butylated hydroxytoluene,BHT)、特丁基对苯二酚(tertiary butylhydroquinone,TBHQ)和没食子酸丙酯(propyl gallate,PG)[3]及一些天然油溶性抗氧化剂,如VE。
茶多酚(tea polyphenols,TP)是茶叶中所含有的一类多羟基酚类化合物的总称,包括儿茶素类(黄烷醇类)、花色苷类、黄酮类、黄酮醇类和酚酸类等。其中儿茶素类化合物为茶多酚的主体成分,约占茶多酚总量的65%~80%[4]。茶多酚是一种高效无毒的自由基清除剂,同时,又是国家批准使用的食品天然抗氧化剂[5],其抗氧化活力不但强于常用的合成抗氧化剂如BHA、BHT和天然抗氧化剂VE、VC、β-胡萝卜素等,而且与VE、VC等具有较好的协同效应[4]。有关它对油脂的抗氧化性研究已有很多报道,但由于茶多酚受自身分子结构限制,水溶性好而脂溶性差,影响了抗氧化效果和油脂外观,从而限制了它在油脂体系的应用和发展[6]。目前解决茶多酚不能在油脂中溶解的方法主要有溶剂法、乳化法和分子修饰法,前两种方法得到的产品脂溶性不稳定,长期放置会使茶多酚析出[7],分子修饰法修改后的茶多酚衍生品的安全性还不确定。
微乳液是一种透明的、各向同性的、热力学稳定的体系。通常由油相、水相、表面活性剂及助表面活性剂等构成。非脂溶性的物质可以通过反相微乳液的方法来提高其在油脂中的溶解度。传统的方式是首先将物质溶解于水,然后作为水相添加到微乳液中。考虑到以上情况,利用反向微乳液来增加茶多酚在油脂中的溶解是一个简单而有效的方法,反相微乳液法不但不会改变茶多酚的结构,而且缓释作用可以进一步增强其抗氧化效果。
本实验选用亚油酸作为油相,同时发挥表面活性剂的作用,乙醇作为助表面活性剂,制备亚油酸-水-乙醇反相微乳液并包封茶多酚,对该微乳液体系进行表征并研究茶多酚对油相(亚油酸)的抗氧化效果。
1 材料与方法
1.1 材料与试剂
亚油酸 国药集团化学试剂有限公司;茶多酚西安一禾生物技术有限公司。
1.2 仪器与设备
AL204电子天平 梅特勒-托利多仪器(上海)有限公司;DF-Ⅱ集热式磁力加热搅拌器 上海比朗仪器有限公司;DDS-11A数显电导率仪 上海雷磁仪器厂;DK-8D电热恒温水槽 上海精宏仪器设备有限公司;Zetasizer Nano S纳米粒度分析仪 马尔文仪器有限公司;AR-G2流变仪 美国TA公司;摩尔超纯水机 重庆摩尔水处理设备有限公司。
1.3 方法
1.3.1 相图绘制
固定亚油酸和水的质量之和为2 g,分别称取亚油酸与水的质量比为19∶1、18∶2、17∶3、16∶4、15∶5、14∶6、13∶7、12∶8、11∶9、10∶10、9∶11、8∶12、7∶13、6∶14、5∶15、4∶16、3∶17、2∶18、1∶19的混合液体,对每一组混合物,逐滴滴加乙醇直到体系由混浊变澄清。记录下加入的乙醇的质量,分别计算亚油酸、水和乙醇在临界点的质量分数,用Origin8.0软件画出微乳液的三元相图。
1.3.2 电导率的测定
电导法普遍应用于确定微乳液类型[8]。应用电导率法来区分微乳液类型时,通常测定电导率与水相质量分数的关系。而考虑到本微乳液体系的特殊性(亚油酸同时作为油相和表面活性剂),结合已有的近似微乳液体系电导率的研究经验[9],本实验采取测定电导率与油相质量分数的关系来区分微乳液类型。分别配制水和乙醇的比例为1∶4和1∶7的二元溶液,恒温在25 ℃条件下,磁力搅拌下逐渐增加油相,每次滴加后,充分搅拌均匀约5 min再读数,同时记录所加入亚油酸的质量,从而绘制出电导率随油相质量分数的变化曲线,直至体系由澄清变混浊。
1.3.3 微乳液粒径和多分散度的测定
1.3.3.1 不同配方条件下微乳液粒径分布
采用动态光散射法测定,4.0 mW He-Ne激光器,633 nm波长。将准备好的待测样品置于清洁的通用式插入样品池中,25 ℃条件下测定微乳液的粒径和多分散度(polydispersity index,PDI)。判断是否形成稳定的纳米微乳液。总质量固定2 g的条件下,测定不同水-油比例下的微乳液粒径,3 次测量取平均值,测定粒径的微乳样品的配方见表1。配方A、B、C固定乙醇质量分数为50%,水-亚油酸质量比分别为1∶1、1∶2和1∶3。A、D、E固定亚油酸质量分数为25%,水-亚油酸质量比分别为1∶1.0、1∶1.5和1∶2。

表1 微乳液配方Table 1 Formulation of microemulsion
1.3.3.2 微乳液的粒径稳定性测试
配制空白微乳液和与之具有相同三相比例的茶多酚微乳液(水相以0.1 g/mL茶多酚水溶液替代),相同的测试条件下,测定茶多酚微乳液和空白微乳液的粒径及多分散指数随时间的变化。
1.3.3.3 茶多酚对微乳液粒径的影响
通过测试包封了不同质量浓度茶多酚微乳液的粒径和多分散指数来考察茶多酚的添加对微乳液粒径的影响。本实验选取6 个质量浓度:0、0.2、0.4、0.6、0.8、1.0 g/mL,测试每种质量浓度的茶多酚微乳液的粒径和PDI,探究茶多酚的加载对微乳液粒径的影响。
1.3.4 微乳液流变性测定
1.3.4.1 阶段性流动测试
流变特性通过AR-G2旋转流变仪测定。测量转子选用锥板,直径40 mm、锥角1°、间距23 øm,测量温度(25±0.1) ℃,刮去椎板周围挤出样品(避免边缘效应)后,开始测量。采用阶段性流动测试法(stepped flow test)测定微乳液的表观黏度(η)与剪切速率(γ)的关系,剪切速率范围为0.1~1 000 s-1。
1.3.4.2 温度扫描
相同的测试条件下,固定剪切速率为100 s-1,以5 ℃/min的升温速率,测定微乳液的表观黏度(η)与温度(T)的关系,温度扫描范围为10~60 ℃。
1.3.4.3 触变性
相同的测试条件下,分别测定微乳液的剪切触变性:表观黏度(η)随剪切速率(γ)上升(0.1~1 000 s-1)和下降(1 000~0.1 s-1)的变化。以及温度触变性:表观黏度(η)随温度(T)上升(10~60 ℃)和下降(60~10 ℃)的变化。
1.3.5 茶多酚对微乳液(亚油酸)的抗氧化效果
配制亚油酸乙醇溶液、空白微乳液、包封了茶多酚的微乳液a和b共4 个样品,室温放置。分别测定新鲜配制的和放置45 d后样品的过氧化值(peroxide value,POV),测试方法按照国标GB/T 5009.37—2003《食用植物油卫生标准的分析方法》执行,计算茶多酚对微乳液氧化的抑制率。

式中:X样品表示微乳液a、b的过氧化值;X空白表示空白微乳液的过氧化值。
1.4 数据处理
所有实验最少重复3 次,所有数据绘图用Origin 8软件处理。用SAS软件进行方差分析,P<0.05为差异显著。
2 结果与分析
2.1 微乳液各组分的选择
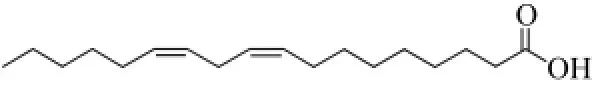
图1 亚油酸结构示意图Fig.1 Structural formula of linoleic acid
本实验旨在将茶多酚应用于亚油酸的抗氧化,因此选择亚油酸为该微乳液体系的油相。由于亚油酸(图1)中的碳氢链是亲油基团,羧基在水中能电离,是亲水基团,因此亚油酸也可用作表面活性剂。亚油酸的亲油性很高、亲水性弱,降低界面张力的效果并不十分理想,因此在体系中添加乙醇做为助表面活性剂。
2.2 亚油酸-水-乙醇相图的绘制
亚油酸-水-乙醇微乳液体系在(25±1) ℃条件下的相图如图2所示,图中各成分含量均以质量分数表示。图2中空白区域(I区)为微乳液区,阴影区域(E区)为乳状液区。
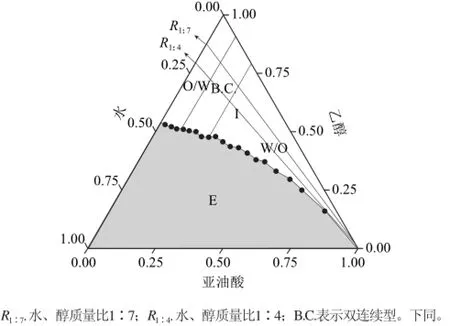
图2 亚油酸-水-乙醇微乳液体系三相图(25℃)Fig.2 Phase diagram of linoleic acid/water/ethanol microemulsion system at 25 ℃
2.3 微乳液类型的区分
由于不同形态的微乳液导电机理不同,可用电导法对微乳液区域进行区分[10]。电导率的测量是识别微乳液类型的经典方法[11]。普通W/O和O/W微乳液具有明显的电导特征差异:W/O型微乳液具有类似油的低电导特性;而O/W型微乳液因为水是连续相,决定了它具有水的高电导特性;当达到双连续结构,即发生相转变时,因为双连续相是油、水同时成为连续相的结构,电导率有明显的突变,因而常被用来指示微乳液的转相[12-13]。图3为三元相图(图2)中水相(水)与助表面活性剂(乙醇)质量比为1∶7和1∶4时,电导率与亚油酸质量分数的关系图。由图3可知,两种水-醇比条件下,电导率变化趋势相同:随着亚油酸质量分数的增加,电导率先增加后减小。根据W/O和O/W微乳液的电导特征差异,结合电导率曲线的变化规律,可以确定,在亚油酸质量分数小于12%时,为O/W微乳液,电导率比较高且随着油相质量分数的增加而增加,即O/W微乳液粒子的增多使得微乳液的导电能力增强[14]。而后在亚油酸质量分数12%~24%时,电导率呈缓慢降低的趋势,说明体系发生了相转变,成为双连续型,这是由于导电的O/W微乳液粒子的持续增加和相互交联形成网络结构导致的。水、醇质量比为1∶7的微乳液体系,双连续型(B.C.)结构形成范围(8%~23%)略大于水、醇质量比为1∶4的微乳液体系(12%~24%),这可能是由于助表面活性剂(乙醇)的增加有利于双连续型微乳的形成。当亚油酸质量分数在24%~70%时,电导率呈线性降低,说明了随油相的不断增加,体系转变为W/O型微乳液,连续相转变为油相,从而电导率迅速降低。亚油酸质量分数>70%时,电导率缓慢降低,几乎降为0,这是由于油相对W/O型微乳液的稀释作用导致的。

图3 不同水-醇比条件下微乳液电导率与油相质量分数的关系(25℃)Fig.3 Conductivity of the microemulsion at 25 ℃ as a function of the mass fraction of linoleic acid at different water/ethanol values
2.4 微乳液粒径和多分散度
2.4.1 微乳液各组分质量分数对粒径的影响
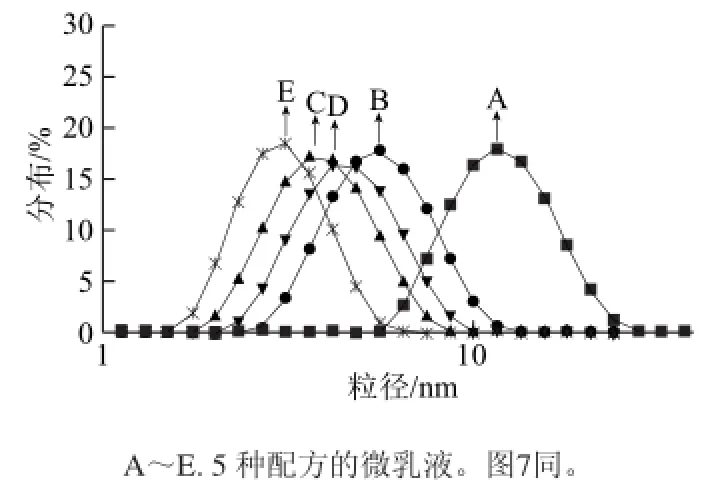
图4 不同配方的微乳液的粒径分布(25℃)Fig.4 Particle size distribution of microemulsion with different formulations at 25 ℃
配制不同配方的W/O型微乳液A~E(表1),测定5 种配方微乳液的粒径分布如图4所示。微乳液是油相、表面活性剂和水相之间的一种微妙的平衡状态。微乳液中任何组成含量的改变都可能影响微乳液的结构、粒径大小及物理化学性质[15]。由图4可知,对于固定乙醇质量分数为50%的微乳液A、B和C,随水相质量分数从25.0%降到12.5%,微乳液的粒径从12.35 nm降到3.683 nm。对于固定亚油酸质量分数为25%的微乳液A、C和E,随水相质量分数从25%降到12.5%,微乳液的粒径从12.35 nm降到3.06 nm。在这两种情况下,微乳液的粒径均随水相质量分数的增加而增大。从整体来看,微乳液E、C、D、B、A的粒径依次增大,而它们的水相质量分数也是依次增大的(12.5%、12.5%、17.0%、17.0%、25.0%),以上分析可以说明该微乳液体系的粒径随水相质量分数的增加而增大。原因是随着水相质量分数的增大,W/O微乳液中的分散粒子增多,分散的水相在油连续相中的扩散和聚集导致微乳液滴粒径增大。对于微乳液E和C及D和B,它们水相质量分数相同,分别为12.5%和17.0%。在这种情况下,粒径大小为:微乳液E(油相质量分数25%)<微乳液C(油相质量分数37.5%);微乳液D(油相质量分数25%)<微乳液B(油相质量分数33%),即油相质量分数低的微乳液粒径偏小,原因可能是,水相质量分数相同的情况下,油相质量分数越低则助表面活性剂比例越高。在一定范围内,含有较高质量浓度的助表面活性剂可进一步降低界面张力,有利于微乳的形成,从而使分散相的粒径变小。
2.4.2 茶多酚对微乳液粒径的影响

图5 25℃条件下空白微乳液和茶多酚微乳液的PDI(a)及粒径(b)随时间的变化Fig.5 Changes in mean particle size (b) and PDI (a) of the empty microemulsion and tea polyphenol-loaded microemulsion at 25 ℃
平均粒径及多分散度是考察微乳液稳定性及粒径均一性的重要参数。随着微乳液粒径的减小,微乳液中分散粒子的相互作用增大,微乳液将更加稳定[16]。由图5可知,新鲜配制(第1天)的空白微乳液粒径为14.99 nm,多分散指数为0.06。包埋了茶多酚的微乳液粒径为9.383 nm,多分散指数为0.134。在水相中包封茶多酚后微乳液粒径减小,多分散指数增大。为进一步探究茶多酚的质量浓度对微乳液粒径及多分散指数的影响,进而测定了包封不同质量浓度的茶多酚的微乳液的粒径和多分散指数,结果如图6所示。随茶多酚质量浓度的增加,微乳液的粒径逐渐变小,当茶多酚由0.0 g/mL增加到0.6 g/mL,粒径迅速由13 nm降低至10 nm,而后再增加茶多酚的质量浓度,粒径变化不大。这是由于茶多酚增溶到微乳液液滴球型的内核里,提高了水相的极性,使得其与表面活性剂极性基团之间的吸引力增大,从而导致微乳液粒径变小。但茶多酚提高水相的极性的作用有一定的限度,因此达到一定质量浓度后,继续增加茶多酚的质量浓度对粒径影响不大。微乳液中加入茶多酚后,PDI值增大,且随茶多酚质量浓度的增大而增大,原因是茶多酚是一种混合物,茶多酚质量浓度越高,微乳液组成越复杂,体系混乱度增加,液滴尺寸向非均匀性发展,多分散指数增大。

图6 茶多酚质量浓度对微乳液粒径的影响(25℃)Fig.6 Effects of different concentrations of tea polyphenol solutions on mean particle size of microemulsion at 25 ℃
微乳液的物理稳定性可以由粒径大小变化来表征[17]。由图5可知,在测试的40 d内,空白微乳液的粒径基本保持不变,在12.5~15.0 nm范围内有微小的波动。而包埋了茶多酚的微乳液粒径在40 d内从9 nm逐渐增大到14 nm。对于该微乳液体系,亚油酸同时承担了油相和表面活性剂的作用,而亚油酸作为表面活性剂亲水性比较弱,由表面活性剂亚油酸和助表面活性剂乙醇构成的界面膜比较薄弱,随着时间的推移,茶多酚穿透界面膜及水相分子扩散的可能性增加,微乳液滴间的聚合导致粒径逐渐增大,稳定性下降。空白微乳液和茶多酚微乳液的多分散指数在40 d内变化均不大。
2.5 微乳液的流变特性
流变学方法已经成为一种常用的、有效的微乳液表征方法。通过对流变参数的测定,不仅可以掌握微乳液体系的流变性质,还可以了解到其内部微观结构的稳态和动态信息[18]。
2.5.1 不同配方的微乳液阶段性流变特性

图7 不同配方的微乳液的流变特性(25℃)Fig.7 Viscosity of empty microemulsion with different formulas as a function of shear rates at 25 ℃
图7 为25 ℃条件下不同配方(表1)的微乳液的表观黏度(η)与剪切速率(γ)的双对数关系图。在剪切速率小于10 s-1时,黏度变化幅度较大,规律不明显,原因是低剪切速率下测试的黏度误差较大,但整体上表现为随剪切速率增大而迅速降低的趋势。当剪切速率大于10 s-1后,黏度随着剪切速率的增加呈规律性的降低,表现为假塑性流体的特征。当剪切速率进入较高速阶段(100~1 000 s-1)微乳液的黏度基本无变化,达到恒定的最低值,表现为牛顿流体的流变特征。
剪切变稀是微乳液流体的共同特性,也是食品分散系所需的特性,因为黏度降低有利于制备过程的进行。剪切过程,可使流体组织排列更加有序,有利于延长或改善功能因子的缓释时间[19]。
从图7中A、B、C 3 种微乳液的流变曲线还可以看出,微乳液的黏度随着水相质量分数的增加而增加。黏度在很大程度上取决于分散的粒子之间的相互作用,是说明微乳液体系结构变化的一个重要参数。一般认为,W/O型微乳液的黏度随含水量的增加而增加。原因是在低水量时,微乳液中的水滴分散在连续的油相中,这些液滴间的作用力很小,所以黏度比较低,随着水量的增加,分散在连续的油相中水滴增多,液滴之间的碰撞和相互作用增强,黏度随之增大。而C与D相比,C的水相质量分数小于D,黏度却高于D,原因可能是C含的乙醇百分比较高,对微乳液起到了稀释作用,使得黏度降低。D的黏度高于E同样说明了乙醇的稀释作用使得微乳液的黏度降低。
2.5.2 茶多酚的添加对微乳液流变性的影响
为探究茶多酚的添加对微乳液流变性的影响,配制了如表2所示3 种样品,测定3 种微乳液样品的流变曲线见图8。

表2 微乳液样品的配方表Table 2 Formulation of samples

图8 空白微乳液及茶多酚微乳液的流变特性(25℃)Fig.8 Viscosity of empty microemulsion and tea-polyphenol-loaded microemulsion as a function of shear rates at 25 ℃
由图8可知,加载0.01 g/mL茶多酚之后,微乳液a的黏度略有下降,原因可能是茶多酚的加入导致微乳液滴粒径变小,液滴之间距离增大,相互作用减小,从而黏度减小。然而加载0.10 g/mL茶多酚的微乳液b黏度较空白略有升高。原因可能是在分散相质量一定的情况下,当粒径减小到一定程度,分散相液滴数量的显著增加导致液滴之间的相互作用增加,使得黏度升高,且该影响程度强于体系粒径变小对黏度的影响。另外茶多酚具有较大的分子质量,所以随溶液中茶多酚质量浓度的提高,水相的黏度会逐渐增大,这影响了表面活性剂和水相之间氢键的形成及界面膜的流动性,也可导致黏度的增加。3 种微乳液的流变曲线基本重合,说明茶多酚的加入对微乳液的流变影响并不大。
2.5.3 温度对微乳液黏度的影响

图9 空白微乳液和茶多酚微乳液的表观黏度随温度的变化Fig.9 Viscosity of empty microemulsion and tea-polyphenol-loaded microemulsion as a function of temperature
由图9可知,微乳液的表观黏度与温度关系密切,在10~60 ℃温度范围内,微乳液的表观黏度随温度的升高而降低,表现出受热变稀的特点。原因是虽然微乳液是热力学稳定体系,但温度的升高增加了体系的自由能,微乳液中各成分分子间的距离加大,引力减小,相互作用力减小,导致微乳液的黏度降低。
2.5.4 微乳液的触变性
触变性是物质的一个重要的依时特性,包括剪切触变性和温度触变性,表明了流体的黏度与剪切速率、剪切历史或受热历史的关系[20]。
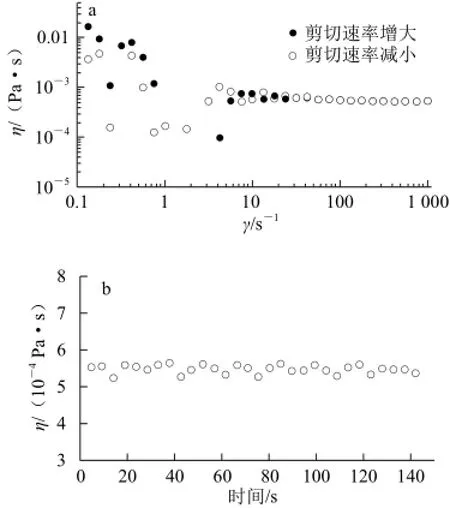
图10 空白微乳液的触变性(a)和恒定剪切速率条件下的黏度(b)Fig.10 Shear thixotropy (a) and viscosity (b) at constant shear rate of empty microemulsion
由图10剪切触变性的测试结果显示,黏度随剪切速率增大和减小的变化曲线基本重合,且在恒定剪切速率(100 s-1)下,该微乳液体系的黏度随时间基本恒定。因此该微乳液体系不具备剪切触变性。

图11 空白微乳液及茶多酚微乳液的温度触变性Fig.11 Temperature thixotropy of empty microemulsion and teapolyphenol-loaded microemulsion
图11 的温度扫描曲线显示,空白微乳液及茶多酚微乳液a和b的黏度曲线在加热和冷却过程中不能重合,呈现明显的温度滞后环。说明了该微乳液体系具有温度触变性。
2.5.5 茶多酚对微乳液的抗氧化效果
为测试微乳液中的茶多酚对亚油酸的抗氧化效果,配制了表2所示的3 种样品及亚油酸-乙醇溶液(25%亚油酸+75%乙醇)共4 种样品。分别于刚配制好和室温放置45 d后测得POV值,结果如图12所示,新鲜配制的4 种样品过氧化值基本相同,茶多酚微乳液a和b的POV较空白微乳液值无显著差异(P>0.05)。室温45 d后,茶多酚微乳液a和b的POV较空白微乳液显著降低(P<0.000 1)。水相添加0.01 g/mL茶多酚对微乳液氧化的抑制率为68.32%,添加0.1 g/mL茶多酚对微乳液氧化的抑制率为92.42%,4 种样品的POV:空白微乳液>亚油酸-乙醇溶液>茶多酚微乳液a>茶多酚微乳液b。可见茶多酚对亚油酸的氧化有很好的抑制作用,反相微乳液法是一种理想的将茶多酚应用于亚油酸的抗氧化剂方法。

图12 室温储存45 d后样品的过氧化值Fig.12 POV values of samples with different formulas after storage at ambient temperature for 45 days
3 结 论
通过三元相图法,在亚油酸同时作为油相和表面活性剂的条件下,制备了亚油酸-水-乙醇油包水型微乳液,结果显示,该微乳液粒径随水相质量分数的增加而增大,随茶多酚质量浓度的增加而减小;阶段性流动测试显示,该微乳液体系在低剪切速率范围内呈现剪切变稀的特征,在高剪切速率范围内表现为牛顿流体;触变性测试表明该微乳液具有温度触变性,无剪切触变性。通过反相微乳液法将茶多酚包封于亚油酸中,大大提高茶多酚在亚油酸中的溶解度,很好地抑制了亚油酸的氧化。另外,茶多酚卓越的功效也增加了体系的功能活性。因此通过反相微乳液法向食用油中加入茶多酚,能阻止和延缓不饱和脂肪酸的自动氧化分解,防止油脂的变质腐败,同时强化油脂的功能性。
[1] CHOQUE B, CATHELINE D, RIOUX V, et al. Linoleic acid: between doubts and certainties[J]. Biochimie, 2014, 96: 14-21.
[2] 张春娥, 张惠, 刘楚怡, 等. 亚油酸的研究进展[J]. 粮油加工, 2010(5): 18-21.
[3] 傅竹生, 蒋晓翠. 油溶性茶多酚在食品工业中的应用[N/OL]. 中国食品报, 2013-3-25(6). http://news.cntrades.com/show-172986.html.
[4] 朱桂勤, 李建科. 茶多酚的功能研究进展[J]. 食品研究与开发, 2005, 26(1): 33-35.
[5] 陈留记, 杨贤强, 张锡林. 乳化剂对茶多酚和脂溶性茶多酚抗亚油酸及其乳化体系氧化作用的影响注[J]. 中国粮油学报, 2003, 18(1): 61-64.
[6] 严梅荣, 王丹丹, 冷媛媛. 脂溶性茶多酚对共轭亚油酸的抗氧化性研究[J]. 中国粮油学报, 2007, 22(1): 83-86.
[7] 旷英姿, 马全红, 顾宁. 脂溶性茶多酚的制备与表征[J]. 食品科技, 2005, 30(7): 53-56.
[8] 周芳霞, 侯万国, 李历历. 一种无表面活性剂微乳液的相行为研究[J].湖南科技学院学报, 2013, 34(4): 43-46.
[9] XU Jie, YIN Aaolin, ZHAO Jikuan, et al. Surfactant-free microemulsion composed of oleic acid, n-propanol, and H2O[J]. The Journal of Physical Chemistry B, 2013, 117: 450-456.
[10] WANG J L, WANG Z W, LIU F, et al. Preparation and in vitro release test of insulin loaded W/O microemulsion[J]. Journal of Dispersion Science and Technology, 2008, 29: 756-762.
[11] 薛美玲, 张积树. 微乳液变型及W/O型导电机理的研究[J]. 青岛化工学院学报, 1998, 2(1): 21-26.
[12] 郑敏, 刘峰, 刘杨, 等. 鱼油微乳液的制备与特性研究[J]. 食品与药品, 2011(1): 23-24.
[13] BAUDUIN P, TOURAUD D, KUNZ W, et al. The influence of structure and composition of a reverse SDS microemulsion on enzymatic activities and electrical conductivities[J]. Journal of Colloid and Interface Science, 2005, 292(1): 244-254.
[14] 张佩华, 梅子, 傅玉颖. 微乳的稳定性研究[J]. 食品工业科技, 2014, 35(7): 73-79.
[15] SHARMA G, WILSON K, WALLE C F, et al. Microemulsions for oral delivery of insulin: design, development and evaluation in streptozotocin induced diabetic rats[J]. European Journal of Pharmaceutics and Biopharmaceutics, 2010, 76: 159-169.
[16] BERA A, KUMAR T, OJHA K, et al. Screening of microemulsion properties for application in enhanced oil recovery[J]. Fuel, 2014, 121: 198-207.
[17] 徐胜男. 油包水微乳液的制备及特性研究[D]. 无锡: 江南大学, 2011.
[18] ACHARYA D P, HARTLEY P G. Progress in microemulsion characterization[J]. Current Opinion in Colloid and Interface Science, 2012, 17: 274-280.
[19] 刘峰, 催莉, 耿岩玲, 等. 核桃油微乳液的制备及抗氧化活性研究[J].山东科学, 2013, 26(3): 26-30.
[20] 方波. 化工流变学[M]. 北京: 中国纺织出版社, 2010.
Preparation of Inverse Microemulsion Loaded with Tea Polyphenols
SUN Jing-jing1, LIU Jian-hua1,2, WANG Zhong-ni3, WANG Zheng-wu1,*
(1. School of Agriculture and Biology, Shanghai Jiaotong University, Shanghai 200240, China; 2. College of Chemistry and Chemical Engineering, Yibin University, Yibin 644000, China; 3. College of Chemistry, Chemical Engineering and Materials Science, Shandong Normal University, Jinan 250014, China)
Water in oil (W/O) microemulison (ME) of linoleic acid/ethanol/H2O to envelop tea polyphenols was prepared. The ternary phase diagram, electrical conductivity, particle size, rheological behavior and oxidation resistance ability of the microemulison were investigated. The results showed that the W/O microemulsion was for med when linoleic content was above 24%. This ME, characterized as pseudoplastic and temperature thixotropy, had an uniform particle size. It was found by determining peroxide value that compared with the blank, the inhibition rates of linoleic acid oxidation for microemulsion with adding 0.01 and 0.1mg/mL tea polyphenols were 68.32% and 92.42%, respectively.
linoleic acid; tea polyphenols; inverse microemulsion; antioxidant
TS225.6;TS202.3
A
1002-6630(2014)13-0008-07
10.7506/spkx1002-6630-201413002
2014-06-15
国家自然科学基金面上项目(21276154;31171642;31271933)
孙静静(1990—),女,硕士研究生,研究方向为功能性食品。E-mail:sjj15261596307@sjtu.edu.cn
*通信作者:王正武(1961—),男,教授,博士,研究方向为功能性食品。E-mail:zhengwuwang@sjtu.edu.cn
