超高效液相色谱-二极管阵列检测器法快速测定保健食品中违法添加的14种性功能药物
2014-01-18耿庆光刘海静朱小红
林 芳,李 涛*,耿庆光,刘海静,朱小红,王 松
(陕西省食品药品检验所,陕西 西安 710061)
超高效液相色谱-二极管阵列检测器法快速测定保健食品中违法添加的14种性功能药物
林 芳,李 涛*,耿庆光,刘海静,朱小红,王 松
(陕西省食品药品检验所,陕西 西安 710061)
建立超高效液相色谱-二极管阵列检测器检测方法同时、快速测定抗疲劳类及增强免疫力类保健食品中违法添加的14种性功能类化学药物(那红地那非、红地那非、伐地那非、羟基豪莫西地那非、枸橼酸西地那非、豪莫西地那非、氨基他达拉非、他达拉非、硫代艾地那非、伪伐地那非、那莫西地那非、康力龙、丙酸睾酮、苯丙酸诺龙)。采用ZORBAX SB-C18色谱柱,流动相A:乙腈-甲醇(90∶10,V/V),B:0.7%三乙胺溶液(pH 2.8),梯度洗脱,流速0.35 mL/min。采集230 nm波长处的色谱图进行初筛和定量。根据14种药物的光谱特征建立光谱库,确证检出化合物。结果表明:14种性功能药物在15.0 min内可有效分离,在8~80 μg/mL的线性范围内相关系数均大于0.999 5,平均回收率为90.1%~106.5%,相对标准偏差为0.7%~4.9%,检测限为2~3 ng。该方法简便、快速、灵敏度高且重复性好,可作为检测抗疲劳类及增强免疫力类保健食品中违法添加化学药物的快速测定方法。
保健食品;性功能药物;违法添加;快速测定;超高效液相色谱-二极管阵列检测器
近年来,随着经济的发展和生活节奏的加快,越来越多的人出现易疲劳、免疫力低下等问题,长期处于亚健康状态。保健食品作为一种新兴的功能性食品,常宣称含有天然、有机、中草药成分,具备免疫调节等功能,拥有越来越广泛的服用人群。同时,一些不法商家为了增加疗效、牟取暴利,在部分抗疲劳、增强免疫力产品中添加了可促进疗效的性功能化学药物。这类药物,如长期使用不当,将对人体造成极大的危害[1-3]。2012年12月14日,国家食品药品监督管理局发布了《保健食品中可能非法添加的物质名单(第一批)》[4],列出声称可缓解体力疲劳(抗疲劳)、增强免疫力(调节免疫)的功能产品中可能添加的那红地那非、红地那非、伐地那非等11种磷酸二酯酶5型抑制剂(phosphodiesterase type 5 inhibitor,PDE5),同时公布了检测依据[5-6]。这2种方法均采用高效液相色谱法,分别检测红地那非、他达拉非等7种和11种非法添加成分,每次样品的仪器检测时间在40~60 min,对试剂、耗材的损耗均较大,并且标准中有个别成分分离效果欠佳,受色谱柱和仪器等诸多因素的影响,很难重现标准中个别成分的分离效果。如果能够快速、有效地检测该类违法添加成分,将对加强市场监管和保障人民群众健康起到积极的作用。
与传统的高效液相色谱相比,超高效液相色谱具有更快的分离速率、更高的分辨率和灵敏度,可适用于复杂基质中药物的分离、分析[7-9]。本实验利用超高效液相色谱的高分辨率和高灵敏度等特性,建立了一种同时、快速检测那红地那非、红地那非、伐地那非、羟基豪莫西地那非、枸橼酸西地那非、豪莫西地那非、氨基他达拉非、他达拉非、硫代艾地那非、伪伐地那非、那莫西地那非、康力龙、丙酸睾酮、苯丙酸诺龙共14种性功能类化学药物的方法。该方法结合二极管阵列检测器的光谱特征分析,可在一次运行中同时完成样品快速筛查、光谱确证和定量分析,线性关系、回收率、分离度均良好,检测简便、快速、灵敏度高且重复性好。14种性功能类药物不仅覆盖了国家食品药品监督管理局最新公布的品种,还根据相关文献[10-14]增加了3种可能用于违禁添加的激素药物,该方法可作为抗疲劳及增强免疫力的保健食品中违法添加性功能类化学药物的快速筛查方法。
1 材料与方法
1.1 材料与试剂
检测样品为2012年全国保健食品风险监测工作中,从陕西省11个市(区)抽查到的声称具有抗疲劳和增强免疫力功能的保健食品,共计171批(每一批次为同一品种3~5盒)。
对照品:枸橼酸西地那非、他达拉非、丙酸睾酮、苯丙酸诺龙(99.3%) 中国食品药品检定研究院;伐地那非(99.5%)、康力龙(99.5%) 德国Dr. Ehrenstorfer公司;那红地那非(99.9%)、红地那非(99.1%)、羟基豪莫西地那非(98.8%)、豪莫西地那非(98.7%)、氨基他达拉非(99.9%)、硫代艾地那非(99.7%)、伪伐地那非(99.5%)、那莫西地那非(99.7%) 加拿大TLC Pharma Chem公司。
甲醇、乙腈、三乙胺(HPLC级) 美国Tedia公司;磷酸(分析纯) 国药集团化学试剂有限公司。
1.2 仪器与设备
1290 infinity超高效液相色谱仪(配有1290二极管阵列检测器) 美国Agilent公司;2695-Quattro Micro API三重四极杆液相色谱-质谱联用仪 美国Waters公司;AE-240双量程电子天平 瑞士Mettlor Toledo公司;Rotavapor R-210旋转蒸发仪 瑞士Büchi公司;AS20500B超声波清洗器 天津奥特赛恩斯仪器有限公司。
1.3 方法
1.3.1 色谱及光谱条件
色谱柱:ZORBAX SB-C18(150 mm×2.1 mm,1.8 μm);柱温30℃;流速0.35 mL/min;进样量1 μL。分别以乙睛-0.7%三乙胺溶液(用磷酸调至pH 2.8)、甲醇-0.7%三乙胺溶液(pH 2.8)、乙腈+甲醇混合液-0.7%三乙胺溶液(pH 2.8)梯度洗脱,用含14种药物的低浓度混合标准溶液优化最佳分离条件。梯度洗脱(洗脱条件见表1);检测波长230 nm。
光谱范围190~400 nm;光谱步进值1.0 nm;光谱采集模式:全部。
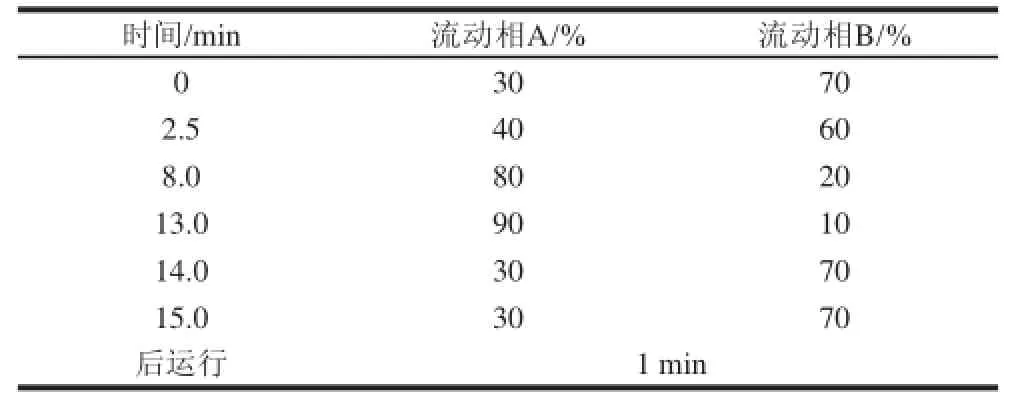
表1 梯度洗脱条件Table 1 Conditions of gradient elution
1.3.2 对照品溶液的配制
准确称取1.1节所述14种对照品各20.0 mg,分别置于10 mL容量瓶中,用甲醇定容至刻度,得单标储备液,质量浓度约为2 mg/mL。再从各单标储备液中准确移取1.0 mL,置于同一25 mL容量瓶中,为消除样品基质的影响,采用阴性样品甲醇提取液(参照1.3.3节处理方法)定容至刻度,得混合标准储备液,质量浓度约80 øg/mL。再用阴性样品甲醇提取液将混合标准储备液梯度稀释成标准曲线各系列质量浓度,得14种性功能药物的系列混合标准曲线溶液,质量浓度为8~80 øg/mL。由于抗疲劳类及增强免疫力类保健食品制剂配方的多样性,本步骤所用的阴性样品为历次抽检中有代表性的固体样品,辅料成分为硬脂酸镁、乳糖、预胶化淀粉等,经检测不含14种性功能药物。
1.3.3 样品前处理
取1.1节所述来源样品,参考文献[6,15-20]进行样品前处理。
固体样品:取样品5次口服剂量(片剂除去包衣,胶囊剂取内容物),研细,精密称取1次服用量,置50 mL容量瓶中,加甲醇适量,超声处理20 min,冷却,加甲醇定容至刻度,摇匀,过滤,取滤液作为供试品溶液。
液体样品:准确移取相当于1次口服剂量的溶液,60℃旋蒸至近干,转移至50 mL容量瓶中,用甲醇定容至刻度,摇匀,经0.22 μm滤膜过滤,取滤液作为供试品溶液。同批样品均做2份平行样,供试品溶液若检出药物含量过高,可根据具体情况再进行稀释。
1.3.4 方法的稳定性及重复性
取混合标准对照品溶液分别在0、12、24、48、72 h进样,计算14种性功能药物峰面积的相对标准偏差(relative standard deviation,RSD)。同时,选取检出的阳性样品,按1.3.3节方法处理,分别在0、12、24、48、72 h相同条件进样,计算检出样品对应药物含量的RSD,考察方法的稳定性。
取同批次阳性样品6份,按1.3.3节方法平行处理,得到供试品溶液并测定。以检出药物峰面积的RSD考察方法的重复性。
1.3.5 回收率和精密度
分别选取固体(片剂)和液体(口服液)基质的空白样品。加入适量的混合标准工作液,使加标质量浓度达到线性最低点质量浓度、2倍线性最低点质量浓度、4倍线性最低点质量浓度3个添加水平。按1.3.3节中的方法进行处理,每种基质的每个添加水平平行做3份样,每个样品重复测定2次,计算样品的回收率及精密度。
1.3.6 光谱确证分析
同时采集对照品和样品在190~400 nm波长处的光谱,根据14种性功能药物的特征吸收光谱建立光谱库,当检测到样品有与对照品保留时间一致的色谱峰时,即与该标准对照药物进行光谱匹配度检索,匹配度达90%以上且峰纯度较高(>90%)时,可判断该类保健食品中添加了某种性功能药物(必要时可用质谱进行确证),同时可计算出该类药物的添加量。
1.3.7 方法的验证
为了验证本方法的可靠性,以含有氨基他达拉非阳性样品为例,进行质谱确证[6,21-25]。
质谱条件:电喷射离子源;正离子模式;多反应监测模式;电离电压3.0kV;锥孔电压25V;源温度120°C;脱溶剂气温度380°C;碰撞气:氩气3.0×10-3mbar;脱溶剂气流速800L/h;锥孔气流速50L/h。氨基他达拉非母离子(m/z)391;子离子(m/z)262,碰撞能量35eV;子离子(m/z)169,碰撞能量30eV;子离子(m/z)134.9,碰撞能量20eV。
2 结果与分析
2.1 色谱条件的优化
以ZORBAX SB-C18作为分析柱,以流动相A乙腈-甲醇(90∶10,V/V)、流动相B 0.7%三乙胺溶液(pH 2.8)进行梯度洗脱,可使14种性功能药物保持足够的分离度和良好的峰形。经相同色谱条件下的对照品单标溶液定位,可确定14种药物的出峰顺序和保留时间;同时在230 nm波长处,检测信号灵敏度较高,分离效果满足检测需要。此条件下梯度分析仅需15 min。14种性功能药物混合标准溶液的色谱图见图1。乙腈-0.7%三乙胺溶液及甲醇-0.7%三乙胺溶液梯度洗脱,均不能有效分离这14种性功能药物,色谱图见图2、3。
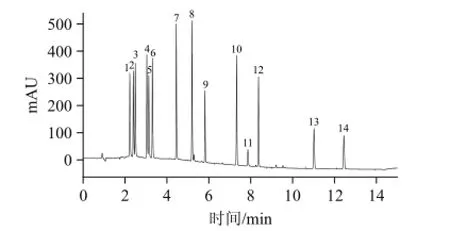
图1 梯度洗脱混合标准溶液色谱图 (流动相A:乙腈-甲醇,流动相B:0.7%三乙胺溶液(pH 2.8)) .8Fig.1 Chromatogram of mixed standard solution with mobile phase A: acetonitrile-methanol, and mobile phase B:0.7% triethylamine (pH 2.8) by gradient elution
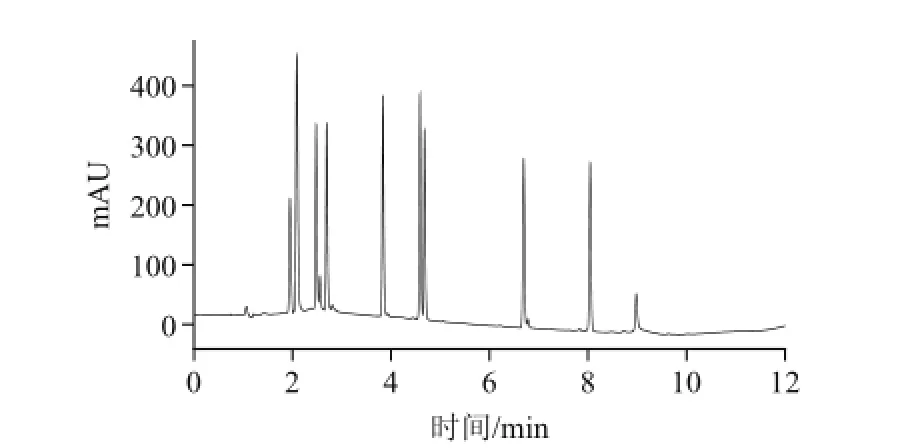
图2 梯度洗脱混合标准溶液色谱图(流动相为乙睛-0.7%三乙胺溶液(pH 2.8)) .8)Fig.2 Chromatogram of mixed standard solution with acetonitrile-0.7% triethylamine (pH 2.8) by gradient elution
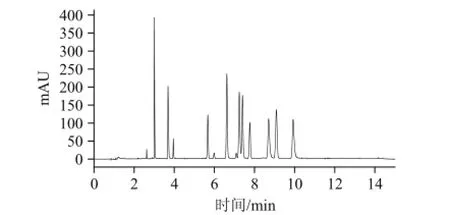
图3 梯度洗脱混合标准溶液色谱图(流动相为甲醇-0.7%三乙胺溶液(pH 2.8)) .8Fig.3 Chromatogram of mixed standard solution with methanol-0.7% triethylamine (pH 2.8) by gradient elution
2.2 线性关系、定量限和检测限
将1.3.2节中得到的14种性功能药物的系列混合标曲溶液,按优化后的色谱条件进行检测,以对应的色谱图峰面积为纵坐标(y)、质量浓度为横坐标(x)进行回归分析。结果表明,14种性功能药物的质量浓度与其峰面积在8~80 øg/mL内呈良好的线性关系,线性相关系数(r)均大于0.999 5,说明本方法适用于保健食品中违法添加的14种性功能药物的定量分析。
在本实验条件下,将混合标曲最低点质量浓度乘以进样体积(1 μL)作为本方法的定量限,为8 ng。
在本实验条件下,将混合标曲溶液连续稀释,以对应质量浓度的色谱峰响应值大于3倍信噪比的质量浓度(噪声水平:6×SD=0.436 0 mAU)乘以进样体积(1 μL)得到本方法的检测限,为2~3 ng(表2)。14种性功能药物的线性方程、相关系数、线性范围、定量限、检测限见表2。
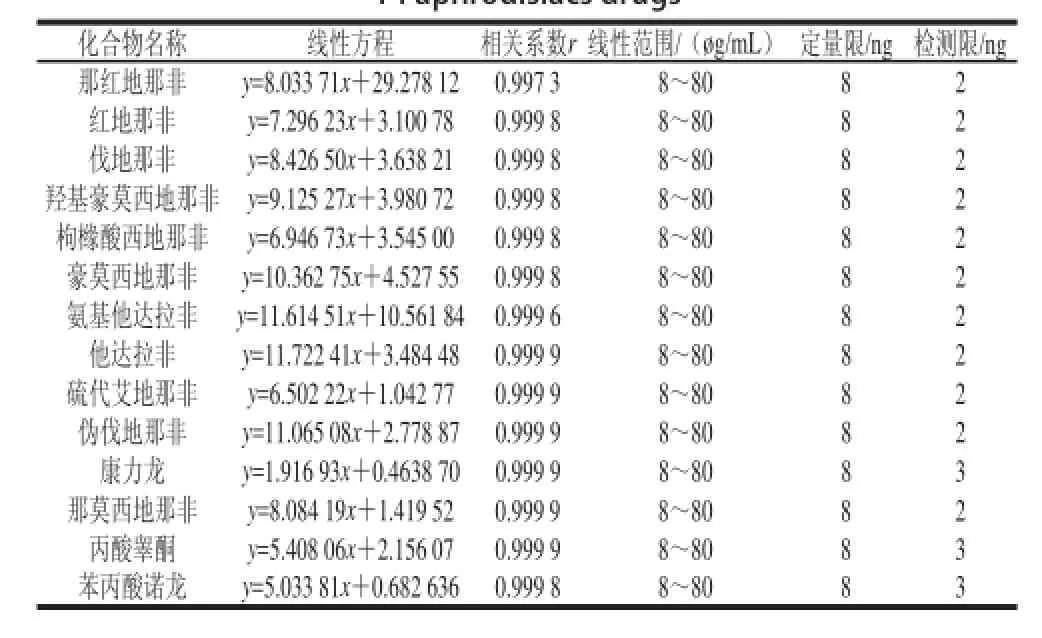
表2 14种性功能药物的线性方程、相关系数、线性范围、定量限、检测限Table 2 Calibration curves, correlation coefficients ( ), linear ranges, limits of quantification (LOQs), limits of detection (LODs) of 14 aphrodisiacs drugs
2.3 稳定性
按1.3.4节中的方法,计算14种性功能药物峰面积的RSD,RSD在0.77%~2.96%。同时选取的阳性样品,对应药物含量的RSD在1.58%~3.64%,说明对照品和样品在72 h内的稳定性良好。
2.4 重复性
按1.3.4节中的方法,检出药物峰面积的RSD最大为3.1%,说明本方法重复性良好。
2.5 回收率和精密度
按1.3.5节中的方法,14种性功能药物在3个添加水平的固体基质中回收率为91.6%~105.6%;液体基质中的回收率为90.1%~106.5%,RSD均小于5%(表3)。
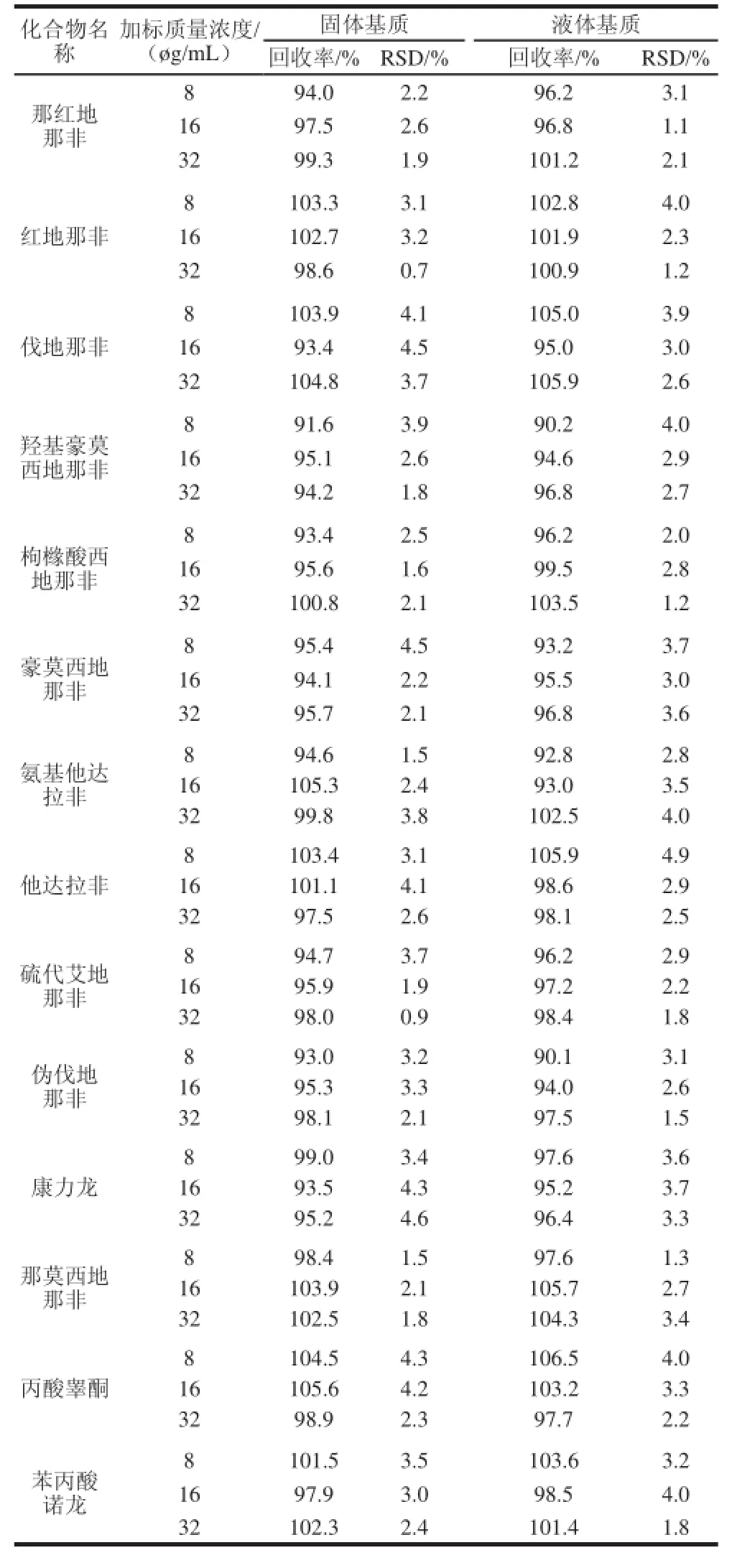
表3 14种性功能药物在不同基质的保健食品中的加标回收率和精密度(n==66)Table 3 Recoveries and precision (RSD) of 14 aphrodisiac drugs spiked in different health food matrices (n == 66))
2.6 光谱确证分析
按1.3.6节中的方法进行光谱确证分析,图4为14种性功能药物的光谱库。
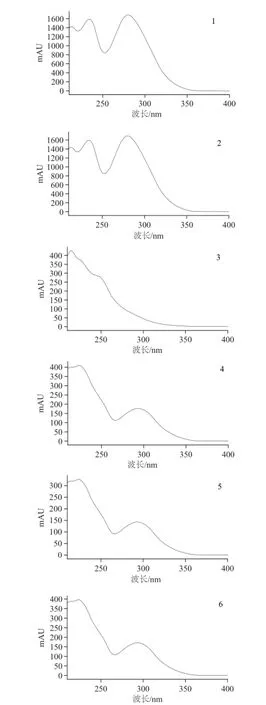

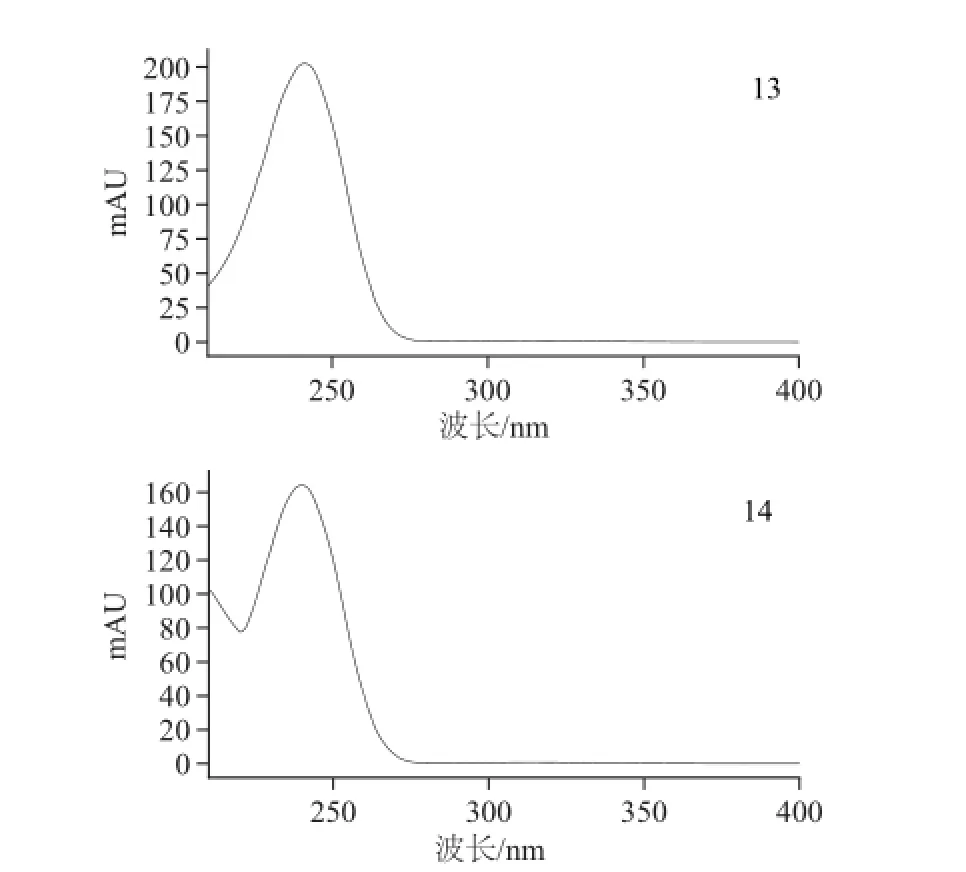
图4 14种性功能药物的特征吸收光谱库Fig.4 Characteristic absorption spectral library of 14 aphrodisiac drugs
2.7 样品的测定
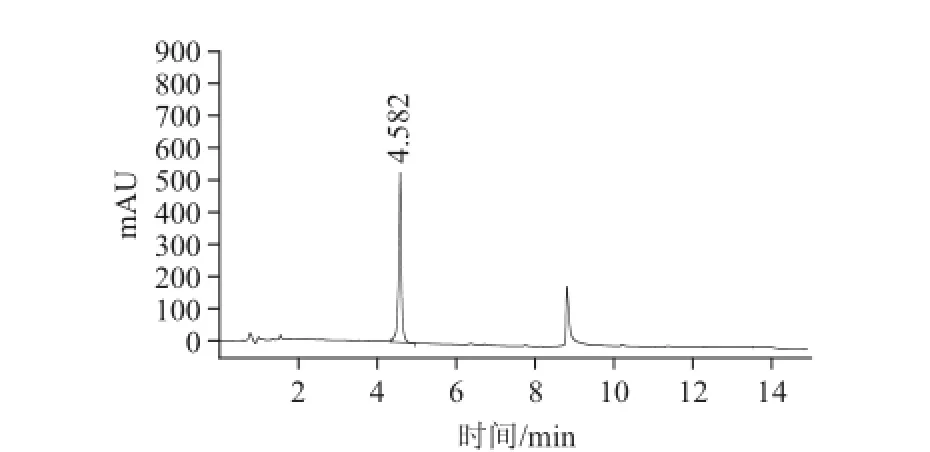
图5 氨基他达拉非阳性样品色谱图(t=4.582 min)Fig.5 Chromatogram of amino tadalafil-positive sample
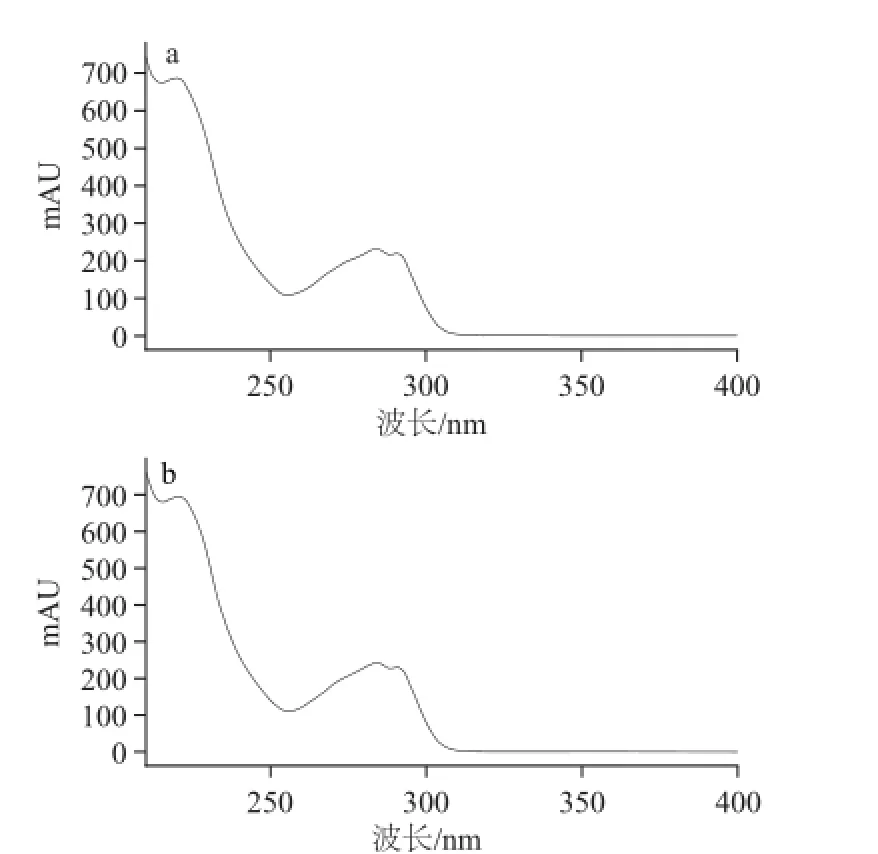
图6 氨基他达拉菲对照品(a)与检出阳性样品(b)光谱对比图Fig.6 Comparison spectrua of amino tadalafil standard and positive sample
取1.1节中所述样品,按照1.3.3节中所述方法进行提取,并按优化后的色谱条件进行检测。共检出非法添加样品11批,某阳性样品色谱图如图5所示,检出的添加物与氨基他达拉非保留时间一致,且与氨基他达拉菲对照品光谱匹配度达99%,确定为样品添加有氨基他达拉非。光谱对比见图6。
按1.3.7节方法,验证本方法的可靠性,样品中母离子和3对子离子均有检出,离子丰度比符合要求,再次确认检出物为氨基他达拉非。多反应监测模式样品图谱见图7。
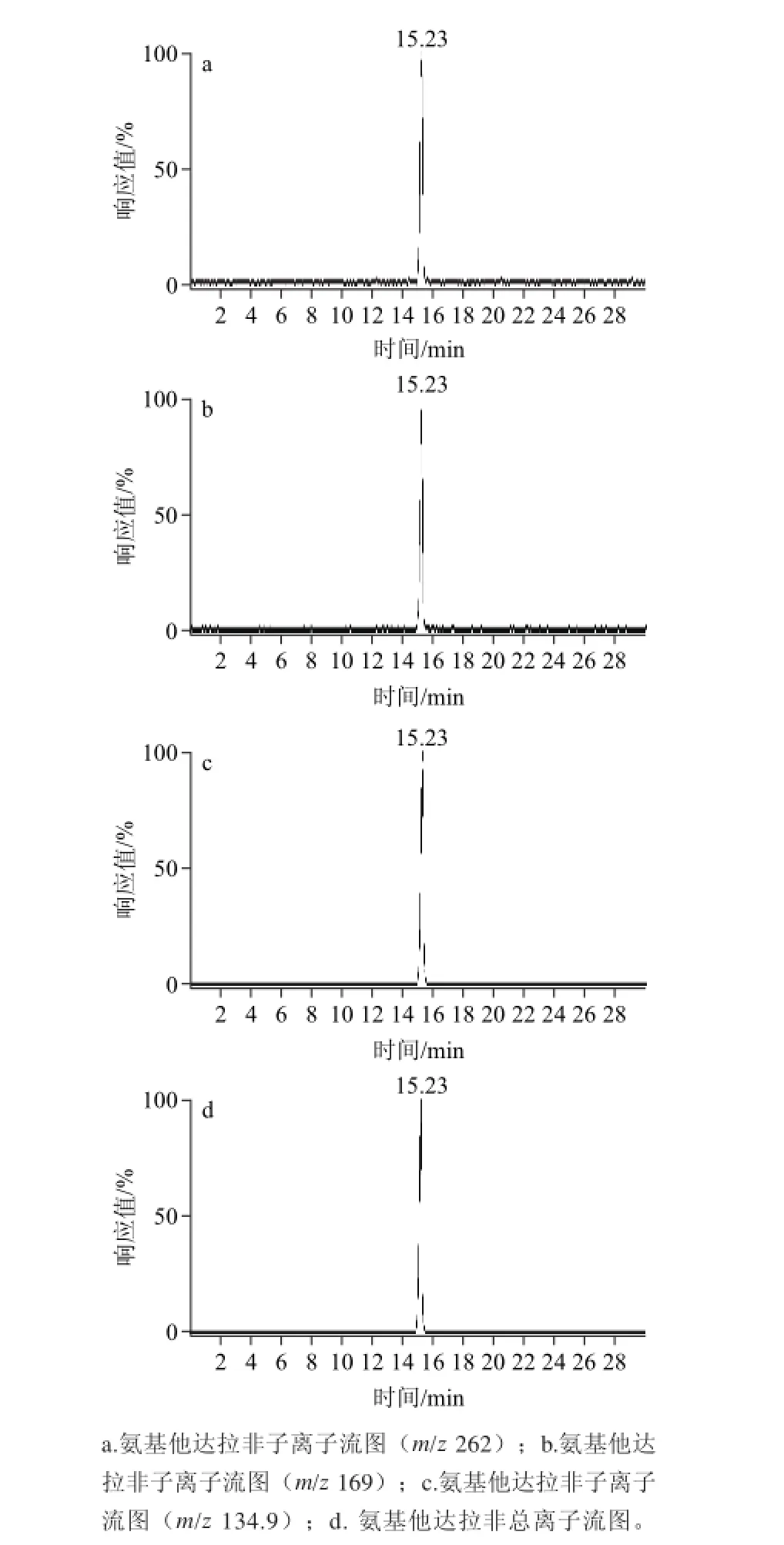
图7 阳性样品多反应监测模式图谱Fig.7 MRM chromatogram of amino tadalafil-positive sample
3 结 论
本研究建立了UPLC-DAD检测法,可同时、快速测定抗疲劳及增强免疫力类保健食品中非法添加的14种性功能药物。该方法实现了对14种性功能药物的同时、有效分离,分离效果优于目前国家食品药品监督管理局推荐标准[5-6]。该方法简便、快速、灵敏度高、重复性好,并可同时采集光谱数据,使样品初筛、光谱确证、含量测定同时完成,可用于市场监管中抗疲劳和增强免疫力2类保健食品中违法添加物的快速检测。
[1] 陈新谦, 金有豫. 新编药物学[M]. 17版. 北京: 人民卫生出版社, 2011: 622.
[2] 董永成, 杜士明, 陈永顺, 等. 中成药及保健品非法添加化学成危害及对策[J]. 时珍国医国药, 2006, 17(8): 1601-1602.
[3] 颜杰, 刘志强, 程振田. 中成药及中药保健食品中非法添加化学药品现状与对策[J]. 中国药学杂志, 2007, 42(9): 716-718.
[4] 国家食品药品监督管理局. 保健食品中可能非法添加的物质名单:第一批[EB/OL]. (2012-12-14) [2013-4-25]. http://www.sda.gov.cn/ WS01/CL1162/76614.html.
[5] 广东省食品药品监督管理局. 药品检验补充检验方法和检验项目批准件2008016—2008 补肾壮阳类中成药中西地那非及类似物的检测方法[S]. 北京: 国家食品药品监督管理局, 2008.
[6] 中国药品生物制品检定所. 药品检验补充检验方法和检验项目批准件2009030—2009 补肾壮阳类中成药中PDE5型抑制剂的快速检测方法[S]. 北京: 国家食品药品监督管理局, 2009.
[7] 刘颖, 周建良, 李萍. 快速高效液相色谱分离技术在中药分析中的应用[J]. 色谱, 2009, 27(5): 682-689.
[8] 郝桂明, 唐素芳. 超高效液相色谱在药物分析中的应用[J]. 天津药学, 2009, 21(6): 64-69.
[9] 赵明霞, 胡基埂, 吴方千, 等. 超高压液相色谱系统的研究进展[J].分析试验室, 2009, 28(增刊): 137-140.
[10] 顾炳仁, 许奇, 缪刚. UPLC同时测定中成药及保健品中非法添加12种激素成分[J]. 药物分析杂志, 2010, 30(11): 2185-2187.
[11] 彭涛, 李晓娟, 代汉慧, 等. 色质联用技术在保健食品违禁化学物质分析中的应用[J]. 质谱学报, 2012, 33(6): 370-379.
[12] 孙鑫贵, 李春雨, 赵榕. 保健食品违法添加药物状况及管理对策[J].首都公共卫生, 2010, 4(4): 153-155.
[13] 汪国权, 杨玉林, 金玉娥. 中成药中违禁添加药物的液质联用仪测定研究[J]. 上海预防医学杂志, 2005, 17(4): 153-155.
[14] 潘涛, 王大章, 郭睿莉, 等. 固相萃取-高效液相色谱法检测保健食品中违禁添加物诺龙[J]. 食品研究与开发, 2009, 30(10): 114-116.
[15] 陈安珍, 王尊文, 杨钊, 等. UPLC-MS/MS检测补肾壮阳类中成药及保健品中添加的化学药[J]. 中成药, 2009, 31(11): 1712-1714.
[16] 刘畅, 夏晶, 胡青, 等. LC/MS(n)法检测补肾壮阳类中成药和保健食品中非法添加5种性功能类化学药品[J]. 中成药, 2009, 31(9): 1371-1374.
[17] 张鲁南, 张梦琪, 陈莉, 等. 性保健品中可能违禁添加7种药物的LCMS/MS法测定[J]. 中国医药工业杂志, 2010, 41(10): 755-758.
[18] 王自. RRLC-Q-TOF-MS法测定保健食品中11种PDE5抑制剂非法添加[J]. 临床合理用药, 2013, 6(6B): 44-46.
[19] 曲晓宇, 董雷, 张四喜, 等. HPLC-MS/MS法同时检测抗疲劳药物及保健品中非法添加的7种壮阳类化学药物[J]. 中国药房, 2013, 24(33): 3129-3130.
[20] 于泓, 胡青, 张甦, 等. 补肾壮阳类中药及保健食品中31种5型磷酸二酯酶抑制剂的高分辨四极杆飞行时间质谱定性定量检测方法[J].中国药学杂志, 2013, 48(15): 1312-1318.
[21] HADWIGER M E, TREHY M L, YE W, et al. Identification of amino-tadalafil and rimonabant in electronic cigarette products using high pressure liquid chromatography with diode array and tandem mass spectrometric detection[J]. Journal of Chromatography A, 2010, 1217(48): 7547-7555.
[22] VENHUIS B J, KASTE D D. Towards a decade of detecting new analogues of sildenafil, tadalafil and vardenafil in food supplements: a history, analytical aspects and health risks[J]. Journal of Pharmaceutical and Biomedical Analysis, 2012, 69: 196-208.
[23] ZOU P, HOU P, LOW M, et al. Structural elucidation of a tadalafil analogue found as an adulterant of a herbal product[J]. Food Additives and Contaminants, 2006, 23(5): 446-451.
[24] KIM S H, KIM H J, SON J, et al. Simultaneous determination of synthetic phosphodiesterase-5 inhibitors in dietary supplements by liquid chromatography-high resolution/mass spectrometry[J]. Mass Spectrometry Letters, 2012, 3(2): 50-53.
[25] MAO D Z, WENG X X, YANG Y J. Rapid screening of sildenafil and tadalafil adulterated in healthcare products by Micro-Raman spectroscopy[J]. Journal of Raman Spectroscopy, 2012, 43(12): 1985-1990.
Rapid Determination of 14 Illegally Added Aphrodisiac Drugs in Functional Foods by Ultra-High Performance Liquid Chromatography-Photodiode Array Detector
LIN Fang, LI Tao*, GENG Qing-guang, LIU Hai-jing, ZHU Xiao-hong, WANG Song (Shaanxi Institute for Food and Drug Control, Xi’an 710061, China)
An ultra performance liquid chromatography-photodiode array detection method (UPLC-DAD) has been established for rapid and simultaneous determination of 14 illegally added aphrodisiacs (nor-acetylsildenafil, acetildenafil, vardenafil, hydroxyhomosildenafil, sildenafil citrate, homosildenafil, amino tadalafil, tadalafil, thioaildenafil, pseudovardenafil, norneosildenafil, stanozolol, testosterone propionate, and nandrolone phenylpropionate) in anti-fatigue and immunity promoting functional foods. ZORBAX SB-C18column was applied with mobile phase A consisting of acetonitrilemethanol (90:10, V/V) and phase B consisting of 0.7% triethylamine (pH 2.8). Linear gradient elution was used with a flow rate of 0.35 mL/min and detection wavelength of 230 nm for rapid screening and quantification of these drugs. Characteristic absorption spectral library of 14 aphrodisiac dru gs have been established for identifying them. The results showed that the 14 aphrodisiac drugs could be effectively separated within 15.0 min, and the standard curves had good linearity over the concentration range of 8–80 μg/mL. The correlation coefficients were all above 0.999 5. The average recoveries ranged from 90.1% to 106.5% with relative stand deviations (RSDs) of 0.7%–4.9%. The detection limits for the 14 aphrodisiacs drugs ranged from 2 to 3 ng. These results indicate that the method is simple and rapid with high sensitivity and good reproducibility, and suitable for the rapid and simultaneous determination of the 14 illegally added aphrodisiac drugs in antifatigue and immunity-improving health foods.
health food; aphrodisiacs drugs; illegally added; rapid determination; ultra performance liquid chromatographyphotodiode array detector (UPLC-DAD)
TS207.7;O657.72
A
1002-6630(2014)04-0163-07
10.7506/spkx1002-6630-201404034
2013-06-03
2014年陕西省科技统筹创新工程计划项目“陕西省食品药品快速检测公共服务平台建设”项目;陕西省社会科学基金项目(13G020)
林芳(1982—),女,主管药师,硕士,研究方向为食品、保健食品理化检验及安全性检测。E-mail:fanqiehuayuan@126.com
*通信作者:李涛(1978—),男,副主任药师,学士,研究方向为食品及保健食品检验。E-mail:westyx@126.com
