盐酸介质中氯化苄基喹啉铵的缓蚀性能及电化学行为研究
2014-01-14胡琳莉艾俊哲
胡琳莉,梅 平,艾俊哲
(长江大学化学与环境工程学院,湖北 荆州434023)
缓蚀技术是一种经济、有效、通用性强的金属防腐蚀方法。喹啉类化合物由于具有多个大π电子共轭体系和杂原子N作为吸附活性中心,其优异的缓蚀性能得到广泛的研究与应用。陈琼等[1]、El-Meligi等[2]通过分子模型、化学计算和电化学方法研究了喹啉衍生物的缓蚀作用机理;潘碌婷等[3]、毕刚等[4]制备了异喹啉类缓蚀剂,并对其缓蚀性能进行了研究。作者所在课题组[5-6]前期曾以喹啉与不同结构的季铵化试剂合成了多种喹啉衍生物,研究了长链取代、芳香基取代等喹啉衍生物的缓蚀性能。在此进一步深入研究氯化苄基喹啉铵(QA)在盐酸介质中的缓蚀性能及电化学行为。
1 实验
1.1 试剂与仪器
喹啉(分析纯)、氯化苄(分析纯)、盐酸、丙炔醇(BCC)、JHC-2、OP-10。
红外光谱仪;鼓风干燥箱;真空泵;恒温水浴(多口);分析天平(0.1mg);游标卡尺;CHI660型电化学工作站,上海辰华仪器公司;CS300型电化学测试系统,华中科技大学。
1.2 合成方法
在干燥的三口烧瓶中加入适量无水乙醇作溶剂,再按物质的量比1∶1.1加入喹啉和氯化苄,搭建搅拌回流装置,加热反应一定时间。粗产品用无水乙醇-乙酸乙酯混合溶剂重结晶,烘箱干燥后得橙红色粉末即氯化苄基喹啉铵(QA)。
1.3 性能测试
依据中国石油天然气行业标准SY/T 5405-1996《酸化用缓蚀剂性能试验方法及评价指标》,采用静态挂片失重法测定缓蚀剂在盐酸介质中对N80钢的缓蚀性能;采用CS300型电化学测试系统测定腐蚀体系稳态极化下的动电位极化曲线;采用CHI660型电化学工作站测试体系的电化学阻抗谱,并用Zview软件分析测试数据,探讨QA的缓蚀机理。采用不同质量分数的盐酸溶液作为腐蚀介质。
2 结果与讨论
2.1 氯化苄基喹啉铵的缓蚀性能评价
60℃下,配制不同质量分数的盐酸溶液,并加入不同用量的QA,对其进行缓蚀性能挂片测试,结果如图1所示。
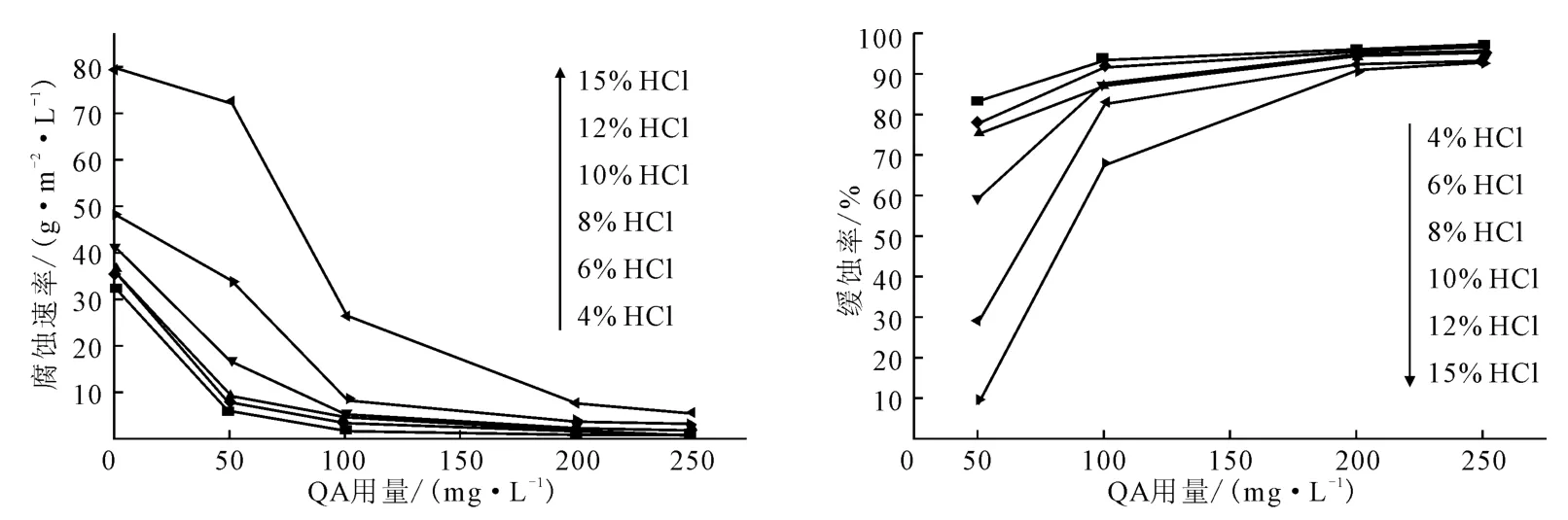
图1 盐酸溶液中QA对N80钢的缓蚀性能Fig.1 The corrosion inhibition performance of QA on steel N80in hydrochloric acid solutions
由图1可知:(1)当不加QA时,N80钢片在盐酸溶液中腐蚀较严重,4%盐酸中钢片表面比较光滑,腐蚀速率为32.61g·m-2·L-1;随着盐酸质量分数的增大,钢片表面腐蚀程度加深,在15%盐酸中钢片表面呈多孔状,腐蚀速率为80.37g·m-2·L-1。(2)加入一定量QA后,钢片表面光滑,腐蚀情况明显好转,在相同盐酸介质中,QA用量越大,N80钢的腐蚀速率越小,QA用量达到200mg·L-1时,缓蚀效果良好,腐蚀速率控制在1~3g·m-2·L-1,缓蚀率达93%以上;再继续增大QA用量,N80钢腐蚀速率基本稳定。
2.2 辅缓蚀剂与氯化苄基喹啉铵的协同效应
BCC与JHC-2均有较强的缓蚀性能,以BCC与JHC-2作为辅缓蚀剂,分别与QA复配,控制总量为200mg·L-1,挂片测试二元复配体系在60℃下、12%盐酸中的缓蚀性能,结果见图2。
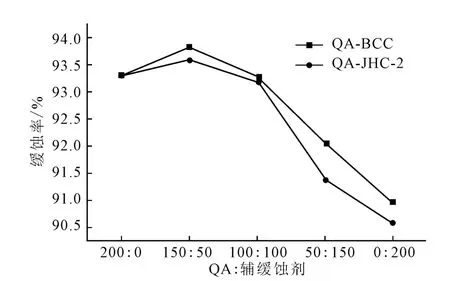
图2 辅缓蚀剂与QA的协同效应Fig.2 Synergistic effect of auxiliary inhibitors and QA
由图2可知:(1)辅缓蚀剂BCC与JHC-2在相同条件下的独立缓蚀性能均弱于QA,但复配后二元复配体系缓蚀率均高于单一的辅缓蚀剂;当复配体系以QA为主时,缓蚀性能也高于独立的QA,说明辅缓蚀剂与QA有协同效应。(2)QA-BCC二元复配体系的缓蚀性能在相同配比条件下略高于QA-JHC-2二元复配体系,但均在配比[质量浓度(mg·L-1)比,下同]QA∶BCC或QA∶JHC-2为150∶50时,缓蚀效果达到最佳。
2.3 非离子表面活性剂OP-10的增效作用
非离子表面活性剂OP-10能在金属表面与缓蚀剂共同吸附成三维网状膜,改变金属表面的界面性质及电荷状态。由此,选择协同效果较好的二元复配体系(QA∶BCC或QA∶JHC-2均为150∶50),添加OP-10,在60℃下、12%盐酸中进行缓蚀性能挂片测试,结果见图3。
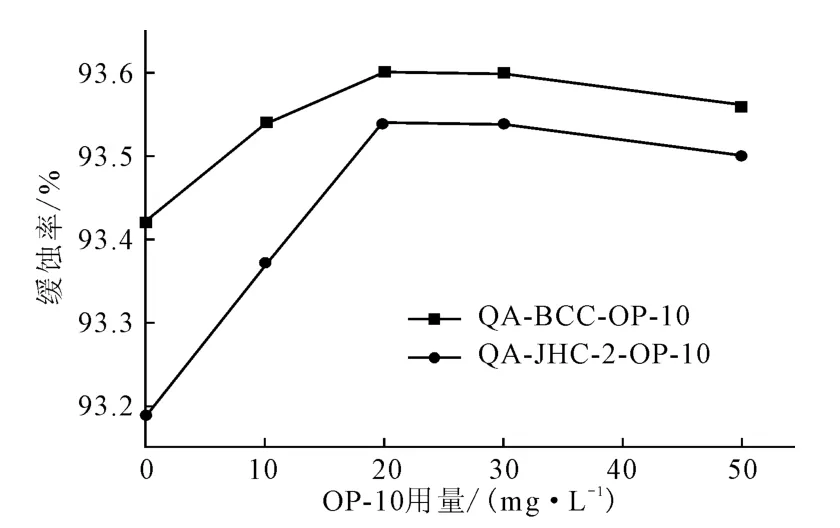
图3 表面活性剂OP-10对二元复配体系的增效作用Fig.3 Synergistic effect of surfactant OP-10 on the binary complex system
由图3可知,随着OP-10用量的增大,缓蚀率增大,说明非离子表面活性剂OP-10对2种复配体系的缓蚀性能有明显的增效作用,均在OP-10用量为20 mg·L-1时,缓蚀效果达到最好;其后随OP-10用量继续增大,缓蚀率有所回落。因此,确定适宜的三元复配体系配比QA∶BCC∶OP-10或QA∶JHC-2∶OP-10均为150∶50∶20。
2.4 电化学行为研究
2.4.1 极化曲线分析
60℃下,分别测定QA(200mg·L-1)及三元复配体系QA-BCC-OP-10(150∶50∶20)、QA-JHC-2-OP-10(150∶50∶20)在12%盐酸溶液中的动电位极化曲线,结果见图4。
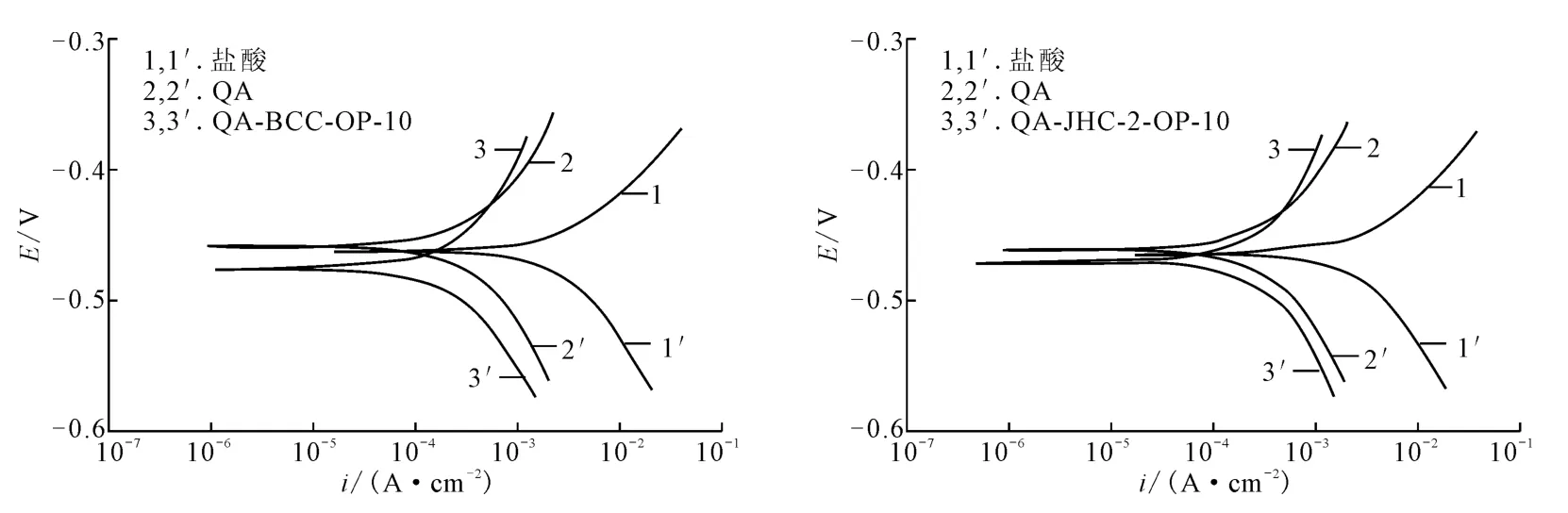
图4 12%盐酸溶液中QA及三元复配体系的极化曲线Fig.4 Polarization curves of QA and the ternary complex systems in 12%HCl solution
由图4可知,加入缓蚀剂后,阴极极化曲线和阳极极化曲线均向低电流方向移动,腐蚀电位明显降低,说明所加入的缓蚀剂对金属的溶解有明显的阻化作用。由图4还可知,加入QA后,自腐蚀电位明显正移,说明QA属于阳极型缓蚀剂;而在分别加入三元复配体系QA-BCC-OP-10或QA-JHC-2-OP-10后,自腐蚀电位均明显负移,说明2种三元复配体系均为阴极型缓蚀剂。
2.4.2 电化学阻抗分析
电化学阻抗谱(EIS)中高频弧反映了电极表面活化过程特征,表明了缓蚀剂在电极表面形成的膜的性质;弧直径与电极反应中电荷的转移电阻Rt相对应,直接反映缓蚀效果。
60℃下,在12%盐酸溶液中,加入不同量的QA后,N80钢在开路电位平稳后测得的EIS如图5所示,EIS所得参数解析结果见表1。
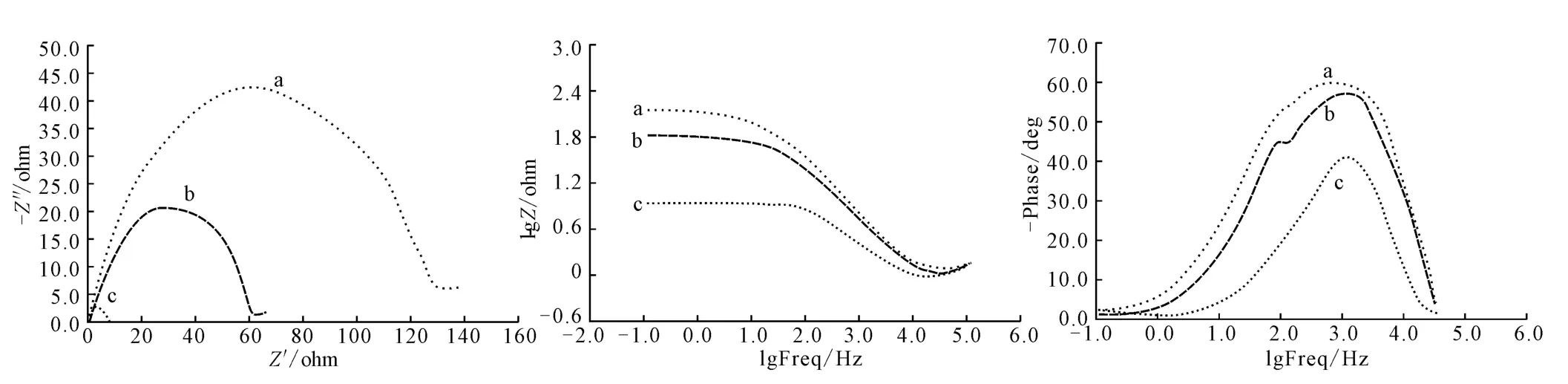
图5 12%盐酸溶液中QA的电化学阻抗谱Fig.5 Electrochemical impedance spectroscopy of QA in 12%HCl solution
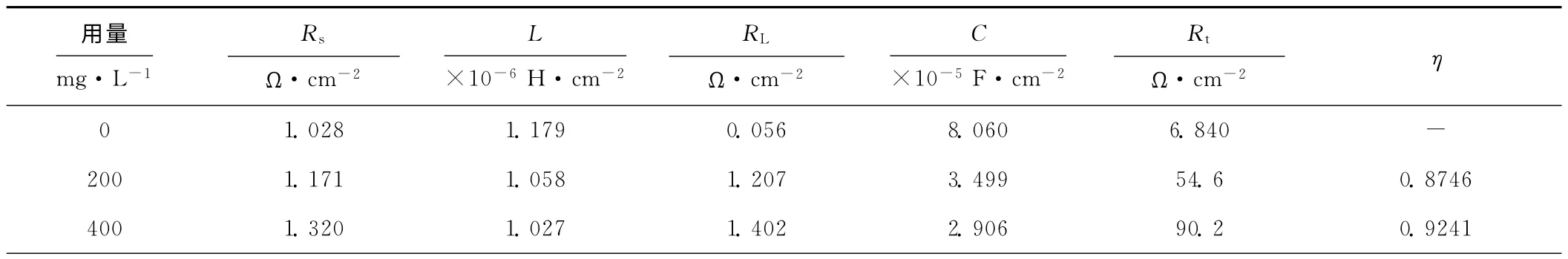
表1 QA在12%盐酸溶液中的电化学阻抗谱解析结果Tab.1 The analytic results of electrochemical impedance spectroscopy of QA in 12%HCl solution
由图5可知,加入QA后得到的是单容抗弧,说明QA主要通过界面吸附起缓蚀作用,包含化学吸附与物理吸附。其中化学吸附主要来自于带很强正电性的季氮阳离子吸附金属表面多余的电子形成反配位键以及电子云密度极大的共轭体系大π电子与Fe原子的空d轨道形成π-d配位键;物理吸附主要是Cl-在金属表面产生特性吸附,使季氮阳离子通过静电引力吸附在金属表面。
由表1可知,随缓蚀剂QA用量的增大,容抗弧增大,其对应的转移电阻Rt增大,N80钢腐蚀速度减慢,腐蚀反应受到抑制,即缓蚀效果增强,与静态挂片实验结论一致。
3 结论
(1)在盐酸介质中QA对N80钢的缓蚀作用明显,用量为200mg·L-1时其对N80钢的缓蚀率达到93%以上。
(2)辅缓蚀剂BCC及JHC-2对QA的缓蚀作用具有明显协同效应,其最佳配比(mg·L-1)QA∶BCC(JHC-2)为150∶50。
(3)OP-10对QA-BCC(JHC-2)二元复配缓蚀剂体系有明显增效作用,最佳配比(mg·L-1)QA∶BCC(JHC-2)∶OP-10为150∶50∶20。
(4)电化学行为分析表明,QA是以抑制阳极反应为主的界面吸附型缓蚀剂,而复配后的三元复配缓蚀剂体系则是性能优异的阴极型缓蚀剂。
[1]陈琼,涂进新.吡啶和喹啉衍生物的电子结构与其缓蚀率的关系[J].武汉大学学报(自然科学版),1993,(1):122-124.
[2]EL-MELIGI A A,TURGOOSE S,ISMAIL A A.Effect of corrosion inhibitors on scale removal during pickling of mild steel[J].British Corrosion Journal,2000,35(1):75-77.
[3]潘碌婷,肖锦.异喹啉季铵盐在盐酸中对A3钢的吸附及其缓蚀作用[J].环境污染治理技术与设备,2001,2(3):56-58.
[4]毕刚,谷荧红.N-取代烷基异喹啉季铵盐的缓蚀性能[J].材料保护,1997,30(2):4-7.
[5]梅平,张引,胡琳莉,等.双喹啉季铵盐QAD的合成及其缓蚀性能研究[J].长江大学学报[自然科学版:理工(上旬)],2010,7(3):26-29.
[6]李天斌,胡琳莉,梅平.喹啉衍生物在土酸体系中对N80钢的缓蚀性能研究[J].石油天然气学报,2011,33(8):155-157.
