季铵盐型gemini表面活性剂的合成及性能研究
2014-01-14汪小宇
赖 璐,汪小宇,梅 平
(1.长江大学化学与环境工程学院,湖北 荆州434023;2.中国石油川庆钻探工程有限公司,陕西 西安710000)
gemini表面活性剂通过连接基团将两个单链表面活性剂连接起来,减弱了离子头基间的静电斥力,增强了碳氢链间的疏水结合力,使表面活性剂分子在溶液表面排列得更紧密,具有比传统单链表面活性剂更高的表面活性。因此,gemini表面活性剂在三次强化采油等众多领域有着广阔的应用前景[1-3]。季铵盐型gemini表面活性剂分子中含有两个亲水头基(季氮离子)和两条疏水碳链[4-7],不仅表面活性高,还具有一系列独特的物理化学性质[8-10]。
作者以N,N-二甲基十二烷基叔胺与2,2′-二氯乙醚为原料,合成了季铵盐型gemini表面活性剂QAGS(图1),研究了反应时间、溶剂类型及用量以及反应物物质的量比对产率的影响,并考察了QAGS的表面活性。

图1 季铵盐型gemini表面活性剂QAGS的合成路线Fig.1 The synthetic route of quaternary ammonium gemini surfactant QAGS
1 实验
1.1 试剂与仪器
N,N-二甲基十二烷基叔胺(95%),Acros公司;2,2′-二氯乙醚(工业品,99%),上海富蔗化工公司;乙腈(分析纯),天津光复精细化工研究所;十二烷基二甲基苄基氯化铵(1227,工业品),公安县精细化工厂。实验用水为去离子水,其它试剂均为分析纯。
NEXUS470型傅立叶红外光谱仪,美国Thermo Nicolet公司;PE 2400Ⅱ型元素分析仪,美国Perkin Elmer公司;JK99B型自动张力仪,上海中晨数字技术设备有限公司;R-1002型旋转蒸发仪,郑州长城科工贸有限公司;WRS-1B型数字熔点仪,上海精密科学仪器有限公司;DZ-2BC型真空干燥箱,天津泰斯特仪器有限公司;JJ-1型电动搅拌器,上海浦东物理光学仪器厂;HH-4型恒温水浴锅,苏州威尔实验用品有限公司;BS-210S型电子天平,德国赛多利斯公司。
1.2 QAGS的合成及表征
称取26.9g N,N-二甲基十二烷基叔胺、7.22g 2,2′-二氯乙醚和45mL乙腈,置于干燥的四口烧瓶中,加热升温至回流,反应72h;将反应液置于旋转蒸发仪中,减压蒸除溶剂;以丙酮与乙醚的混合溶剂(体积比为1∶5)重结晶3次,将所得固体置于真空干燥箱内,50~60℃下干燥12h,所得产物即为目标产物季铵盐型gemini表面活性剂QAGS。
采用IR和元素分析方法对合成产物进行结构表征。
1.3 QAGS的表面活性测定
称取一定量的QAGS,配制成0.01mol·L-1水溶液,采用连续稀释法配制成不同浓度的溶液。采用铂金板法测定其在(298±0.1)K时的表面张力σ,绘制σ~c图。仪器测定前用蒸馏水校正。
2 结果与讨论
2.1 QAGS的结构表征
2.1.1 红外光谱(图2)
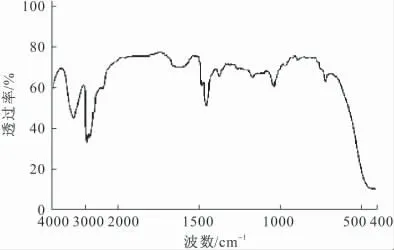
图2 QAGS的红外光谱Fig.2 IR Spectrum of QAGS
由图2可以看出,甲基、亚甲基的伸缩振动吸收带在2800~3100cm-1范围内,其弯曲变形振动吸收带在1360~1500cm-1和710~730cm-1范围内;-C-O-C-伸缩振动吸收带在1000~1120cm-1范围内;C-N伸缩振动吸收带在870~1250cm-1范围内;1600~1660cm-1和3300~3500cm-1范围内的吸收带表明样品中含有少量缔合H2O。
2.1.2 元素分析(表1)

表1 QAGS元素分析结果/%Tab.1 The results of elemental analysis of QAGS
由表1可以看出,实测元素含量与理论值偏差不超过±0.4%。因此,可以确定所得产物即为目标产物QAGS。
2.2 合成条件优化
2.2.1 反应时间对产率的影响
固定反应物加量为N,N-二甲基十二烷基叔胺26.9g、2,2′-二氯乙醚7.22g,溶剂乙腈40mL,反应温度为80℃,考察反应时间对产率的影响,结果如图3所示。

图3 反应时间对产率的影响Fig.3 The effect of reaction time on the yield
由图3可以看出,在其它条件不变的情况下,QAGS的产率随着反应时间的延长而上升;反应72h后,产率变化不大。因此,选择适宜的反应时间为72h。
2.2.2 溶剂类型对产率的影响
固定反应物加量为N,N-二甲基十二烷基叔胺26.9g、2,2′-二氯乙醚7.22g,反应时间为72h,反应温度为回流温度,分别以不同溶剂作为反应介质,溶剂加量为45mL,考察溶剂类型对产率的影响,结果如表2所示。

表2 溶剂类型对产率的影响Tab.2 The effect of solvent type on the yield
由表2可以看出,乙腈作为溶剂时,产率最高,可达22.76%。乙腈为非质子传递溶剂,其非质子传递性和强极性均有利于双分子亲核取代(SN2)反应。丙酮作为溶剂时,产率最低,仅有9.52%,可能是由于丙酮沸点较低导致反应温度也较低,反应物分子未能获得较高活性,加上丙酮的极性相对较弱,不利于SN2反应,使得产率较低。因此,选择适宜的溶剂为乙腈。
2.2.3 溶剂乙腈加量对产率的影响
固定反应物加量为N,N-二甲基十二烷基叔胺26.9g、2,2′-二氯乙醚7.22g,反应时间为72h,反应温度为回流温度,考察溶剂乙腈加量对产率的影响,结果如图4所示。
由图4可以看出,在乙腈加量为45mL时,产率最高为22.76%,乙腈的加量过多或过少,产率均有所降低。这可能是由于,溶剂乙腈加量过少时,反应物分子不能充分接触、碰撞,导致产率下降;乙腈加量过多时,叔胺浓度(相对含量)降低,分子扩散程度扩大,而对于SN2反应,亲核试剂浓度降低时,反应速率会下降,故产率也相应降低[11]。因此,选择适宜的乙腈加量为45mL。
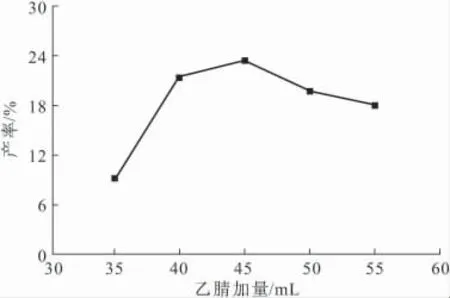
图4 溶剂乙腈加量对产率的影响Fig.4 The effect of acetonitrile dosage on the yield
2.2.4 反应物物质的量比对产率的影响
固定反应物2,2′-二氯乙醚加量为7.22g,反应时间为72h,溶剂乙腈加量为45mL,反应温度为回流温度,改变N,N-二甲基十二烷基叔胺的加量,考察反应物物质的量比(N,N-二甲基十二烷基叔胺与2,2′-二氯乙醚的物质的量比,下同)对产率的影响,结果如图5所示。

图5 反应物物质的量比对产率的影响Fig.5 The effect of the reactant molar ratio on the yield
由图5可以看出,产率随着N,N-二甲基十二烷基叔胺加量的增加而上升。当反应物物质的量比超过3.0∶1,即N,N-二甲基十二烷基叔胺的加量超过理论值的50%时,继续增大其加量,对产率影响不大。为降低反应后提纯的难度,选择适宜的反应物物质的量比为3.0∶1。
2.3 QAGS溶液的表面活性研究
溶液表面张力的降低可作为表面活性剂表面活性大小的量度。测定了一系列不同浓度QAGS水溶液的表面张力,以表面张力σ对c作图,得到σ~c曲线,如图6所示。

图6 QAGS的表面张力曲线Fig.6 The curve of surface tension of QAGS
由图6可以看出,QAGS水溶液的表面张力随着浓度的增大而急剧下降,当浓度达到1.054mmol·L-1后,表面张力基本不变。表面活性剂在溶液表面的吸附会影响表面的性质。在实际应用中,如润湿、乳化、起泡、洗涤等都与表面活性剂的吸附密切相关。吸附量Г可由Gibbs方程求得。对二组分的稀溶液而言,Gibbs方程可表示为[12]:

式中:Г为溶质在表面层的吸附量,mol·m-2;c为溶质在溶液本体中的浓度,mol·L-1;σ为溶液的表面张力,N·m-1;R为摩尔气体常数,J·mol-1·K-1;T为热力学温度,K。
在表面张力与浓度关系曲线(图6)上选取任一点,求出该点处曲线切线的斜率,即相应浓度点的将其代入式(1),求得该浓度下,溶质在溶液表面的吸附量Г。
以Г对c作图,得到Г~c曲线,即为QAGS水溶液表面的吸附等温线,如图7所示。
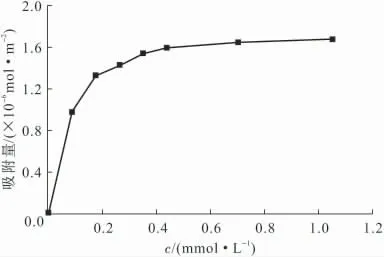
图7 吸附等温线Fig.7 The adsorption isotherm curve
由图7可以看出,Г随着浓度c的增加而增大,当浓度达到0.439mmol·L-1时,吸附达到饱和,饱和吸附量Гm为1.597×10-6mol·m-2。表面活性剂分子在溶液表面成单分子吸附,根据式(2),由饱和吸附量可求得表面活性剂的分子截面积[12]。
am=1/(NAГm) (2)
式中:am为分子截面积,nm2;NA为阿佛伽德罗常数。
计算得到QAGS的分子截面积为1.04nm2。
3 结论
(1)以N,N-二甲基十二烷基叔胺和2,2′-二氯乙醚为原料、乙腈为溶剂,合成了季铵盐型gemini表面活性剂QAGS。采用红外光谱和元素分析方法,对合成产物进行了结构表征,合成产物即为目标产物QAGS。
(2)考察了反应时间、溶剂类型及用量以及反应物物质的量比对产率的影响,确定适宜的反应条件为:N,N-二甲基十二烷基叔胺和2,2′-二氯乙醚物质的量比3.0∶1,反应介质为乙腈,乙腈加量45mL,反应时间72h。在此条件下,QAGS的产率达22.76%。
(3)测定了QAGS的表面活性。结果表明,QAGS水溶液的表面张力随着浓度的增大而急剧下降,浓度达到1.054mmol·L-1后,表面张力基本不变。QAGS在水溶液表面层的饱和吸附量为1.597×10-6mol·m-2,QAGS的分子截面积为1.04nm2。
[1]ZANA R.Dimeric(gemini)surfactants:Effect of the spacer group on the association behavior in aqueous solution[J].Journal of Colloid and Interface Science,2002,248(2):203-220.
[2]ZANA R.Dimeric and oligomeric surfactants.Behavior at interfaces and in aqueous solution:A review[J].Advances in Colloid and Interface Science,2002,97(1-3):205-253.
[3]ATKIN R,CRAIG V S J,WANLESS E J.Mechanism of cationic surfactant adsorption at the solid-aqueous interface[J].Advances in Colloid and Interface Science,2003,103(3):219-304.
[4]WANG M N,FAN Y X,HAN Y C,et al.Coacervation of cationic gemini surfactant with N-benzoylglutamic acid in aqueous solution[J].Langmuir,2013,29(48):14839-14847.
[5]ZHUANG L H,WANG G W,YU K H.Enhanced adsorption of anionic dyes from aqueous solution by gemini cationic surfactantmodified diatomite[J].Desalination and Water Treatment,2013,51(34-36):6526-6535.
[6]梅平,段明峰,熊洪禄,等.双季铵盐的合成试验研究[J].长江大学学报(自然科学版),2005,2(7):204-207.
[7]赖璐,梅平,李逹,等.双季铵盐型表面活性剂的吸附特性研究[J].长江大学学报(自然科学版),2006,3(3):38-40.
[8]MANET S,KARPICHEY Y,Bassani D,et al.Counteranion effect on micellization of cationic gemini surfactants 14-2-14:Hofmeister and other counterions[J].Langmuir,2010,26(13):10645-10656.
[9]LUCHETTI L.Kinetic and spectroscopic investigations of aqueous micelles of cationic surfactants[J].Central European Journal of Chemistry,2010,8(6):1318-1322.
[10]LI R,CHEN Q B,ZHANG D Z,et al.Mixed monolayers of gemini surfactants and stearic acid at the air/water interface[J].Journal of Colloid Interface Science,2008,327(1):162-168.
[11]高鸿宾.有机化学[M].北京:高等教育出版社,1999:188-197.
[12]天津大学物理化学教研室.物理化学(下册)[M].第四版.北京:高等教育出版社,2001:180-185.
