龙葵生物碱自微乳化制剂配方研究
2014-01-10贾晓斌刘美辉朱劲华
张 威,贾晓斌,刘美辉,朱劲华*
1江苏建康职业学院,南京 210029;2 江苏省中医药研究院,南京 210028
龙葵(Solanum nigrum)别名苦葵、天茄子、老鸦眼睛草、水茄、天泡果、天泡草、老鸦酸浆草、山海椒等[1],主要用于抗癌。李时珍著《本草纲目》记载:其味苦,微甘,寒,滑,无毒。主治痈疽肿毒,跌打损伤,功能消肿散血,通利小便。临床上广泛运用龙葵水煎剂或注射剂治疗宫颈癌、食道癌、乳腺癌、肺癌、肝癌、绒毛膜上皮癌、卵巢癌、肉瘤等多种恶性肿瘤[2],因而龙葵也被中医学列为十大抗肿瘤中草药之一。近年来,龙葵的抗癌作用受到广泛关注,对其抗癌有效成分进行大量的研究证明,其抗肿瘤的主要成分为生物碱[3-6];如贾艳菊等[5]用MTT 法观察龙葵生物碱的体外抗肿瘤作用,结果发现100~800 μg/mL 的龙葵生物碱对HeLa 细胞的生长均表现出一定的抑制作用。李明慧等[7]观察龙葵甾体类生物碱对荷瘤(S180)小鼠及对Lewis 肺癌移植瘤小鼠的影响,结果发现龙葵甾体类生物碱不仅具有抑制肿瘤增长的作用,还可显著提高荷瘤小鼠血清TNFa、IL-2、IL-6、IL8 的水平。李志雄等[8]研究龙葵碱对前列腺癌LNCaP 及Du145 细胞系的抑制作用及机制,发现龙葵碱可以通过线粒体途径诱导两种细胞凋亡的发生,能将肿瘤细胞周期阻滞在S 期,由此产生抑制增殖作用。龙葵生物碱因具有环状结构而难溶于水,可选择自微乳给药系统[9](Self-microe mulsifying Drug Delivery System,SMEDDS)作为龙葵生物碱的给药载体,以提高其生物利用度,促进药物的吸收。自乳化药物传递系统是由油相、非离子表面活性剂和助表面活性剂组成的固体或液体制剂,其基本特征是可在胃肠道内或环境温度适宜(通常指体温37 ℃)及温和搅拌的条件下,自发乳化形成粒径在100~500 nm 左右的乳剂。而当亲水性表面活性剂(HLB >12)含量较高(≥40%,W/W)或同时使用助乳化剂时,在轻微搅动下可制得更精细的乳剂(粒径50 nm 左右),则被称为自微乳化药物传递系统[10]。目前最常用自乳化药物传递系统的乳化剂有乙氧基聚氧乙烯甘油酯、聚氧乙烯油酸酯、聚氧乙烯辛基苯基醚及吐温等;常用的助乳化剂多为中、短链的一元或二元醇,如乙醇、丙二醇等;常用的油相有蓖麻油、豆油、花生油、橄榄油、肉豆蔻酸异丙酯、脂肪酸三酰甘油等[11]。本文选用常见的乳化剂、助乳剂及油相作为龙葵生物碱的自微乳制剂配方,对各因素进行研究,以找到龙葵生物碱自微乳制剂的最佳配方[12],为进一步通过自乳化药物传递系统给药的药效研究提供基础。
1 仪器和试药
85-2 型恒温磁力搅拌器(上海司乐仪器有限公司);AL204 型梅特勒-托利多十万分之一分析天平和百万分之一天平(上海亚津电子科技有限公司);JJ-800 型精密电子天平(美国双杰仪器公司);H.H.S 数显电热恒温水浴锅(上海锦凯科学仪器有限公司);3000HSA 型激光粒度分析仪(英国马尔文仪器有限公司);岛津UV-2450/2550 紫外-可见分光光度计(岛津公司)。
吐温-20(天津科密欧化学试剂有限公司),聚氧乙烯辛基苯基醚(OP 乳化剂,上海玖意化学试剂有限公司),油酸(上海实意化学试剂有限公司),1,2-丙二醇(PPD,上海谱振生物科技有限公司),龙葵总生物碱提取物(自提,批号:20120302),注射用水(南京易普易达科技发展有限公司)。
2 方法与结果
微乳的粒径是SMEDDS 质量控制和处方筛选的重要指标,也是区分乳剂、亚微乳、微乳的重要指标。本试验微乳的制备是按照下列各表固定处方中表面活性剂、助表面活性剂、油相中的用量,将表面活性剂、助表面活性剂、油相混合均匀,然后加入龙葵甾体生物总碱,充分搅拌使提取物溶解完全,得到棕红色SMEDDS 浓缩液,经稀释后通过马尔文粒度仪测定其粒径。又因为透光率和自微乳的粒径有的紧密相关性,即对于粒径足够小且分散稳定的微乳而言,透光率越高,乳滴的粒径越小,自乳化效果也就越好。将所得SMEDDS 浓缩液,加水稀释,在600 nm 下测定透光率[13]。以各因素变化对粒径和透光率的影响,观察各因素对乳化效果的影响。
2.1 表面活性剂吐温-20 的用量对透光率的影响[14]
按照表1 列出的量,将吐温-20、OP 乳化剂、油酸、1,2-丙二醇混合,再将龙葵甾体总生物碱提取物10 mg 加入,充分搅拌使生物碱提取物溶解完全,得该处方自微乳浓缩液。精密取出1 mL 微乳浓缩液加入到10 mL 注射用水中,轻微震荡后测量其粒径,并以透光率为指标,在600 nm 处测定透光率的值,结果见表1。

表1 吐温-20 对粒径和透光率的影响Table 1 Effect of Tween-20 on particle size and transmittance of SMEDDS
从试验结果可见,吐温-20 的最佳用量在200~300 mg 之间。从上述实验结果可以看出,虽然吐温-20 用量为300 mg 时粒径最小(25.3 nm)、透光率最高(81.3%),较吐温-20 用量为200 mg 时用量增加了50%,粒径只减小3 nm,透光率只增加2%。为了便于筛选,综合考虑吐温-20 的用量及其对粒径的影响,下面试验中吐温-20 的用量均以200 mg 加入。
2.2 表面活性剂OP 乳化剂的用量对透光率的影响[15]
按照表2 列出的量,将吐温-20、OP 乳化剂、油酸、1,2-丙二醇混合,再将龙葵甾体总生物碱提取物10 mg 加入,充分搅拌使生物碱提取物溶解完全,得该处方自微乳浓缩液。精密取出1 mL 微乳浓缩液加入到10 mL 注射用水中,轻微震荡后测量其粒径,并以透光率为指标,在600 nm 处测定透光率的值,结果见表2。

表2 OP 乳化剂对粒径和透光率的影响Table 2 Effect of polyoxyethylene octyl phenyl ether on particle size and transmittance of SMEDDS
从试验的结果可见,OP 乳化剂的用量以200 mg 为最佳。从上述实验结果可以看出,随着OP 乳化剂使用量的增加,微乳的粒径先减小后增大,整个体系透光率的变化是先增大后减小。当OP 乳化剂的用量为200 mg 时,粒径最小,透光率最大。为了便于筛选,下面试验中均以OP 乳化剂200 mg 的用量加入。
2.3 油酸的用量对微乳透光率的影响
按照表3 列出的量,将吐温-20、OP 乳化剂、油酸、1,2-丙二醇混合,再将龙葵甾体总生物碱提取物10 mg 加入,充分搅拌使生物碱提取物溶解完全,得该处方自微乳浓缩液。精密取出1 mL 微乳浓缩液加入到10 mL 注射用水中,轻微震荡后测量其粒径,并以透光率为指标,在600 nm 处测定透光率的值,结果见表3。

表3 油酸对粒径和透光率的影响Table 3 Effect of oleic acid on particle size and transmittance of SMEDDS
从试验的结果可见,油酸用量以50 mg 较佳。根据“膨胀胶束理论”,油相的加入会将原来混合乳化剂的胶束溶液中的胶束基团进一步溶胀,导致乳滴粒径的逐渐增大,从而使整个体系的透光率逐渐减小。实验结果表明随着油相量的增加,微乳相应的粒径应随油相含量的增大而增加,其透光率大幅度减少。这与“膨胀胶束理论”所阐明的结果相一致。但同时发现,加入的油相在一定范围(40~60 mg)之内并没有使整个体系的粒径和透光率发生很大的变化,这可能和体系中使用了混合表面活性剂有关。因为混合表面活性剂的存在使得O/W 型微乳的粒子表面的柔韧性以及抗水稀释能力大大加强,所以在一定范围内,混合表面活性剂、助表面活性剂可以很好的控制油/水界面张力在一定范围内。
2.4 助表面活性剂1,2-丙二醇的用量对透光率的影响
按照表4 列出的量,将吐温-20、OP 乳化剂、油酸、1,2-丙二醇混合,再将龙葵甾体总生物碱提取物10 mg 加入,充分搅拌使生物碱提取物溶解完全,得该处方自微乳浓缩液。精密取出1 mL 微乳浓缩液加入到10 mL 注射用水中,轻微震荡后测量其粒径,并以透光率为指标,在600 nm 处测定透光率的值,结果见表4。

表4 1,2-丙二醇对粒径和透光率的影响Table 4 Effect of 1,2-propanediol on particle size and transmittance of SMEDDS
本试验使用了1,2-丙二醇作为助表面活性剂,主要为了调节微乳体系的HLB 值。从试验结果看,随着助表面活性剂用量的增加,整个体系粒径开始慢慢变小,透光率随之增大,但达到一定阶段之后,即使再增大助表面活性剂的用量也不能使其粒径和透光率发生大的改变。从尽量减少微乳体系中表面活性剂、助表面活性剂的角度出发,1,2-丙二醇的加入量以500 mg 为佳。
2.5 龙葵总生物碱提取物的用量对微乳透光率的影响
按照表5 列出的量,将吐温-20、OP 乳化剂、油酸、1,2-丙二醇混合,再将龙葵甾体总生物碱提取物以不同的量加入,充分搅拌使生物碱提取物溶解完全,得该处方自微乳浓缩液。精密取出1 mL 微乳浓缩液加入到10 mL 注射用水中,轻微震荡后测量其粒径,并以透光率为指标,在600 nm 处测定透光率的值,结果见表5。
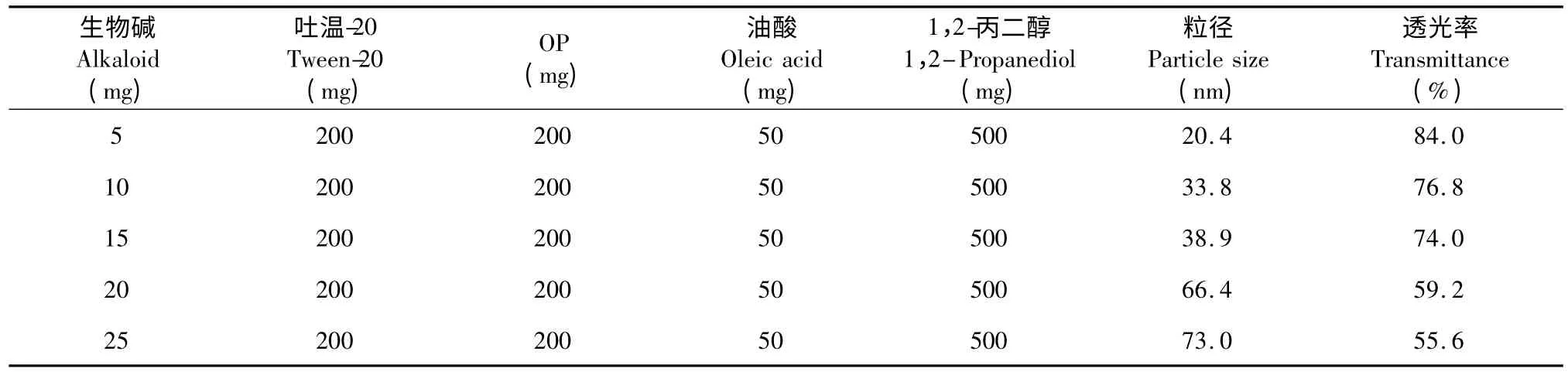
表5 龙葵总生物碱提取物的用量对粒径和透光率的影响Table 5 Effect of amount of S.nigrum alkaloid on particle size and transmittance of SMEDDS
从试验结果看,当体系载药后,增个体系的粒径不断增大。当龙葵甾体总生物碱提取物在5~15 mg 时,粒径增大、透光率减小较缓,但当龙葵甾体总生物碱提取物由15 mg 变成20 mg 时,粒径几乎增大了一倍,透光率减小了15%。综合考虑载药量和粒径增大两个方面的因素,选择体系中的龙葵总生物碱提取物的加入量以10 mg 为佳。
3 结论
处方中乳化剂的用量越大,其微乳的毒性相应也会增加,所以实验中在保证微乳自乳化效率的前提下,尽可能的降低乳化剂的含量。最终确定最佳处方为:吐温-20 200 mg,OP 乳化剂200 mg,油酸40 mg,1,2-丙二醇500 mg,龙葵总生物碱提取物10 mg。此SMEDDS 配方为进一步通过正交试验、星点设计等方式进一步探索龙葵生物碱自微乳化制剂最佳配方奠定必要的基础。
1 Chinese Materia Medica Editorial Committee of State Administration of Traditional Chinese Medicine(国家中医药管理局《中华本草》编委会).Chinese Materia Medica(中华本草).Shanghai:Shanghai Scientific and Technical Publishers,1999.7.
2 Gui XL(归小龙).Effects of antitumor of alkaloids from Solanum nigrum.Chin J Inf Tradit Chin Med (中国中医药信息杂志),2009,S1(16):80-82.
3 Guo JH(顾锦华),Zhang W(张伟),Li F(李峰),et al.The antineoplastic effect of Solanum nigrum compound capsule and its influence on tumor cell cycle.Lishizhen Med Mater Med Res(时珍国医国药),2006,11:2463-2464.
4 Li J,Li QW,Feng T.Aqueous extract of Solanum nigrum inhibit growth of cervical carcinoma (U14)via modulating immune response of tumor bearing mice and inducing apoptosis of tumor cells.Fitoterapia,2008,2:548-556.
5 Jia YJ(贾艳菊),Dai L(代玲),Zhang C(张灿).Study on apoptosis of HeLa cells induced by solanine.Prog Veterin Med(动物医学进展),2010,31(8):51-54.
6 Ding X(丁霞),Gao SG(高思国),Li GY(李冠业).Research of antitumor effects in vitro from Solanum nigrum different extract part.Lishizhen Med Mater Med Res(时珍国医国药),2011,22:1244-1246.
7 Li MH(李明慧),Sun SQ(孙世清),Cao L(曹亮),et al.Effects of steroid alkaloids from Solanum nigrum on S180and Lewis lung carcinoma bearing mice.Chin J Nat Med(中国天然药物),2008,6:223-226.
8 Li ZX(李志雄),Liang WB(梁蔚波),Tang H(唐晖),et al.Effects of alkaloids from Solanum nigrum on prostatic carcinoma LNCaP and Du145.Guangdong Med J(广东医学),2013,34:1153-1156.
9 Li JH(李剑惠),Hu Y(胡英),Qin FH(钦富华).Preparation and quality evaluation of loratadine self-emulsilying drug delivery system.Central South Pharm (中南药学),2008,6:414-416.
10 Li ZM(李兆明),Chen Z(陈智),Yu F(于峰),et al.Development of self-microemulsifying drug delivery system.Qilu Pharm Aff(齐鲁药事),2009,2:98-100.
11 Yuan HJ(袁海建),Chen Y(陈彦),Jia XB(贾晓斌).Research and application of traditional Chinese medicine SMEDDS.China J Tradit Chin Med Pharm(中华中医药杂志),2008,6:524-527.
12 Han J(韩静),Cui SM(崔升淼).Design and in vitro evaluation of self-microemulsifying drug delivery system for puerarin.Central South Pharm (中南药学),2009,10:731-734.
13 Zhang XN(张学农).Antitumor Medicines-Research of Paclitaxel Microemulsion (抗肿瘤药物——紫杉醇微乳的研究).Beijing:Peking University,2002.
14 Song J(宋洁),Li YL(李永玲).Research of perilla-oil SMEDDS prescription.Chin J Conval Med (中国疗养医学),2010,1(19):75-76.
15 Shen X (沈熊),Wu W (吴伟).Self-emulsifying and self-emulsifying drug delivery system.Fudan Univ J Med Sci (复旦学报,医学版),2003,30:180-183.
