虎耳草的化学成分及生物活性研究
2014-01-09黄志金龚小见杨占南
先 春,黄志金,周 欣*,龚小见,赵 超,杨占南
1贵州师范大学贵州省山地环境信息系统与生态环境保护重点实验室;2 贵州师范大学天然药物质量控制研究中心,贵阳 550001
虎耳草(Saxifraga stolonifera (L.)Meerb.)为虎耳草科(Saxifragaceae)虎耳草属多年生常绿草本植物,又名金丝荷叶、耳朵红、老虎草、烂耳草、天荷叶等。收载于《贵州省中药材、民族药材质量标准》2003 年版,是贵州特色苗药材,资源丰富。全草入药;微苦、辛,寒,有小毒;祛风清热,凉血解毒[1-2]。近年来,已有报道虎耳草的乙醇提取物中含有多元酚、黄酮、有机酸等成分[3-5];虎耳草提取物对前列腺癌细胞有诱导凋亡的作用[6],乙醇提取物有抑菌作用[7],以及其活性成分槲皮素等对人胃腺癌细胞的增殖具有抑制作用[8]等功效。从目前的研究现状看,为进一步探索虎耳草活性部位的活性成分,对综合利用和评价虎耳草的药用植物资源具有重要的科学意义。
1 仪器与材料
北京泰克仪器有限公司生产的X-4 型双目镜显微熔点测定仪(温度计未校正);美国Varian 公司生产的INOVO 400 MHz 型核磁共振谱仪,以TMS 为内标;美国惠普公司生产的HPMS 5973 质谱仪;德国布鲁克光谱仪器公司生产的TENSOR 27 红外仪。柱色谱硅胶(200~300 目,300~400 目),薄层用硅胶GF254和薄层用硅胶H 均由青岛海洋化工厂生产;Sephadex LH-20 凝胶由Pharmacia 公司提供;溶剂均为工业纯(重蒸)。虎耳草采集于贵州省都匀市,原植物经贵阳中医学院陈德媛教授鉴定为虎耳草(Saxifraga stolonifera (L.)Meerb.),标本保存于贵州师范大学天然药物质量控制研究中心。
2 提取与分离
选取虎耳草全草25 kg(干燥),粉碎后用80%乙醇热回流提取3 次(每次2 h),合并提取液后浓缩至无醇味并回收乙醇,浸膏依次用石油醚,乙酸乙酯,正丁醇萃取,分别得到石油醚、乙酸乙酯、正丁醇部分,各部分的浸膏分别为:400,300,400 g。本研究主要对虎耳草乙酸乙酯部分进行分离纯化,首先用200~300 目硅胶以石油醚∶乙酸乙酯(30∶1~1∶1),氯仿∶甲醇(30∶1~0∶1)梯度洗脱分段。合并后分得四个部分,即石油醚∶乙酸乙酯(30∶1~15∶1)部分;石油醚∶乙酸乙酯(15∶1~0∶1)部分;氯仿∶甲醇(30∶1~20∶1)部分和氯仿∶甲醇(20∶1~0∶1)部分。弃去第一部分(油脂)和第四部分(大极性),合并二、三部分以石油醚∶乙酸乙酯(20∶1~1∶1),氯仿∶甲醇(30∶1~2∶1)经硅胶柱色谱梯度洗脱,分离纯化得到化合物原儿茶酸(1)(50 mg),琥珀酸(2)(40 mg),桦木酸(3)(50 mg),原儿茶酸甲酯(4)(60 mg)。再次合并二、三部分后经凝胶柱色谱以氯仿∶甲醇(5∶1~0∶1)梯度洗脱,得到化合物5,7-二羟基色原酮(5)(10 mg),槲皮素3-O-β-L-鼠李糖苷(6)(40 mg),槲皮素5-O-β-D-葡萄糖苷(7)(1.5 g)。虎耳草正丁醇部分以甲醇∶水(1∶0~0∶1)经聚酰胺柱纯化后用薄层显色合并、各段再经MCI、凝胶柱色谱以氯仿∶甲醇(5∶1~1∶1)反复纯化,得到化合物1-O-β-D-glucopyranosyl-(2S,3S,4R,8E/Z)-2-[(2' R)-2'-hydroxytetracosanoylamino)]-8-octadecene-1,3,4-triol(8)(20 mg)。
3 结构鉴定
化合物1 白色针晶(甲醇),C7H6O4;mp:195~197 ℃。EI-MS m/z:154[M]+,137,109,81.1H NMR(CD3OD,400 MHz)δ:7.41(1 H,s,H-2),7.40(1 H,d,J=8.0 Hz,H-6),6.78(1 H,d,J=8.0 Hz,H-5).13C NMR(CD3OD,100 MHz)δ:122.5(C-1),116.3(C-2),144.7(C-3),150.2(C-4),114.4(C-5),121.7(C-6),168.9(C-7)。上述数据与文献[9]报道基本一致,故鉴定该化合物为3,4-二羟基苯甲酸(3,4-dihydroxy benzoic acid),别名原儿茶酸。
化合物2 白色晶体(甲醇),C4H6O4;mp:185~187 ℃。EI-MS m/z:118[M]+,100,74,55,45.1H NMR(CD3OD,400 MHz)δ:2.69(4 H,s,CH2×2)。13C NMR(CD3OD,100 MHz)δ:175.4(COOH),29.1(-CH2)。上述数据与文献[3]报道基本一致,故鉴定化合物为琥珀酸(amber acid)。
化合物3 白色无定形粉末,C30H48O3;mp:278~279 ℃。EI-MS m/z:456[M]+,248,207,175,107,65,43.1H NMR(CD3OD,400 MHz)δ:4.69(1 H,s,H-29a),4.58(1 H,s,H-29b),1.68(3 H,s,H-30),0.99(3 H,s,H-23),0.95(3 H,s,H-24),0.93(3 H,s,H-25),0.84(3 H,s,H-26),0.73(3 H,s,H-27).13C NMR(CD3OD,100 MHz)δ:38.6(C-1),27.3(C-2),78.3(C-3),38.7(C-4),55.5(C-5),18.1(C-6),34.2(C-7),40.6(C-8),50.40(C-9),36.8(C-10),20.7(C-11),25.5(C-12),38.3(C-13),42.2(C-14),29.5(C-15),32.0(C-16),56.2(C-17),26.6(C-18),48.2(C-19),150.6(C-20),30.3(C-21),37.0(C-22),26.7(C-23),15.4(C-24,-26),15.4(C-25),14.8(C-27),179.4(C-28),18.2(C-29),108.9(C-30)。上述数据与文献[10]报道基本一致,故鉴定该化合物为桦木酸(betulinic acid)。
化合物4 白色无定形粉末,C8H8O4;mp:132~134 ℃。EI-MS m/z:168[M]+,153,125,97.1H NMR(CD3OD,400 MHz)δ:7.68(1 H,dd,J=7.8,1.8 Hz,H-6),7.53(1 H,d,J=1.8 Hz,H-2),6.82(1 H,d,J=7.8 Hz,H-5),3.90(3 H,s,-OCH3)。13C NMR(CD3OD,100 MHz)δ:121.7(C-1),112.4(C-2),147.3(C-3),151.3(C-4),114.5(C-5),123.9(C-6),168.7(C-7),55.0(OCH3)。上述数据与文献[11]报道基本一致,故鉴定该化合物为3,4-二羟基苯甲酸甲酯(3,4-Dihydroxybenzoic acid methyl ester),别名原儿茶酸甲酯。
化合物5 黄色针晶(甲醇),C9H6O4;mp:256~267 ℃。EI-MS m/z:178[M]+,150,109,69.1H NMR(CD3OD,400 MHz)δ:7.97 (1 H,d,J=6.0 Hz,H-2),6.32(1 Hd,J=2.0 Hz,H-8),6.19(1 H,d,J=6.0 Hz,H-3),6.05 (1 H,d,J=2.0 Hz,H-6),.13C NMR(CD3OD,100 MHz)δ:156.8(C-2),110.3(C-3),182.0(C-4),162.1(C-5),98.9(C-6),164.8(C-7),93.8(C-8),158.5(C-9),105.2(C-10)。上述数据与文献[12]报道基本一致,故鉴定该化合物为5,7-二羟基色原酮(5,7-Dthydroxychromone)。
化合物6 黄色粉末,C21H20O11;mp:166~168℃。IR (KBr):υmaxcm-1:3410,1652,1455,1360,1271,1201,1168,964,917.ESI-MS m/z:447[MH]-,471[M+Na]+,302,273,153,137.1H NMR(DMSO-d6,400 MHz)δ:12.64 (1 H,s,5-OH),7.29(1 H,s,H-2'),7.24(1 H,d,J=8.4 Hz,H-6'),6.84(1 H,d,J=8.4 Hz,H-5'),6.38(1 H,s,H-6),6.19(1 H,s,H-8).13C NMR(DMSO-d6,100 MHz)δ:156.5(C-2),134.2(C-3),177.8(C-4),161.3(C-5),98.7(C-6),164.2(C-7),93.7(C-8),157.4(C-9),104.1(C-10),120.8(C-1'),115.8(C-2'),145.2(C-3'),148.5(C-4'),115.5(C-5'),121.2(C-6'),101.8(C-1''),70.4(C-2''),70.6(C-3''),71.2(C-4''),70.1(C-5''),17.5(C-6'')。上述数据与文献[13]报道基本一致,故鉴定该化合物为槲皮素3-Oβ-L-鼠 李 糖 苷(Quercetin 3-O-β-L-rhamnopyranoside)。
化合物7 黄色粉末,C21H20O12;mp:256~267℃。IR (KBr):υmaxcm-1:3397,1623,1559,1457,1334,1276,1075,992,924.ESI-MS m/z:463[MH]-,487[M+Na]+,302,273,153,137.1H NMR(C5D5N,400 MHz)δ:10.95 (1 H,s,7-OH),9.56(1 H,s,3-OH),7.64(1 H,s,H-2'),7.50(1 H,d,J=7.6 Hz,H-6'),6.87(1 H,d,J=7.6 Hz,H-5'),6.73(1 H,s,H-8),6.63(1 H,s,H-6),4.77(1 H,s,H-1'').13C NMR(C5D5N,100 MHz)δ:143.6(C-2),137.4(C-3),171.8(C-4),158.5(C-5),103.1(C-6),162.5(C-7),97.3(C-8),157.2(C-9),106.4(C-10),122.1 (C-1'),114.8 (C-2'),145.1 (C-3'),147.4(C-4'),115.7(C-5'),119.6(C-6'),103.9(C-1''),73.8(C-2''),75.7(C-3''),69.7(C-4''),77.6(C-5''),60.8(C-6'')。上述数据与文献[14]报道基本一致,故鉴定该化合物为槲皮素5-O-β-D-葡萄糖苷(Quercetin 5-O-β-D-glucopyranoside)。
化合物8 白色无定型粉末,C48H93NO10;IR(KBr):υmaxcm-1:3417,2923,1633,1405,1199,1100。ESI-MS m/z:842[M-H]-,882[M+K]+.1H NMR(C5D5N,400 MHz)δ:8.58(1 H,d,J=9.2 Hz,-NH),5.50(2 H,m,H-8),5.29(1 H,m,H-2),4.95(1 H,d,J=8.0 Hz,H-1''),4.71(1 H,m,H-1b),4.57(1 H,m,H-2'),4.52(各1 H,m,H-1a),4.34(1 H,m,H-6''b),4.29(1 H,m,H-6''a),4.18~4.20(3 H,m,H-4,3'',4''),3.99(1 H,t,J=8.0 Hz,H-2''),3.86(1 H,m,H-5''),1.23~1.30((CH2)n,brs),0.85(6 H,t,J=6.8 Hz,CH3×2);13C NMR(C5D5N,100 MHz)δ:70.5(C-1),51.7(C-2),75.9(C-3),72.4(C-4,2'),33.9(C-5),26.7(C-6),27.6(C-7Z),32.2(C-7E),130.4(C-8Z),130.9(C-8E),130.2(C-9Z),130.7(C-9E),28.0(C-10Z),33.1(C-10E),34.0(C-11),33.4(C-12),175.8(C-1'),35.6(C-3'),25.9(C-4'),26.8~30.2(C-5'~22'和C-13~16),23.0(C-17,23'),14.4 (C-18,24'),105.6(C-1''),75.2(C-2''),78.5(C-3''),71.4(C-4''),78.6(C-5''),62.6(C-6'')。上述数据与文献[15]报道基本一致,鉴定该化合物为1-O-β-D-glucopyranosyl-(2S,3S,4R,8E/Z)-2-[(2'R)-2'-Hydroxytetracosanoylamino)]-8-octadecene-1,3,4-triol。
4 抗前列腺癌细胞的活性测定(MTT法)
细胞增殖检测[16](MTT 法测定PC-3 前列腺癌细胞增殖)调整细胞密度为5 ×104·mL-1,接种在96 孔培养板上,每孔200 μL,每组三个复孔,各组加入不同浓度药物培养48 h,72 h 于培养结束前4 h加入MTT(1 mg/mL)20 μL。弃去上清液,每孔加入DMSO 150 μL,振荡后在酶标仪490 nm 波长测定OD 值,并做t 检验,计算细胞生长抑制率[17],结果见表1。
表1 虎耳草不同化合物对PC-3 前列腺癌细胞凋亡的影响()Table 1 Different compounds of Saxifraga stolonifera (L.)Meerb.on PC-3 prostate cancer cell apoptosis()
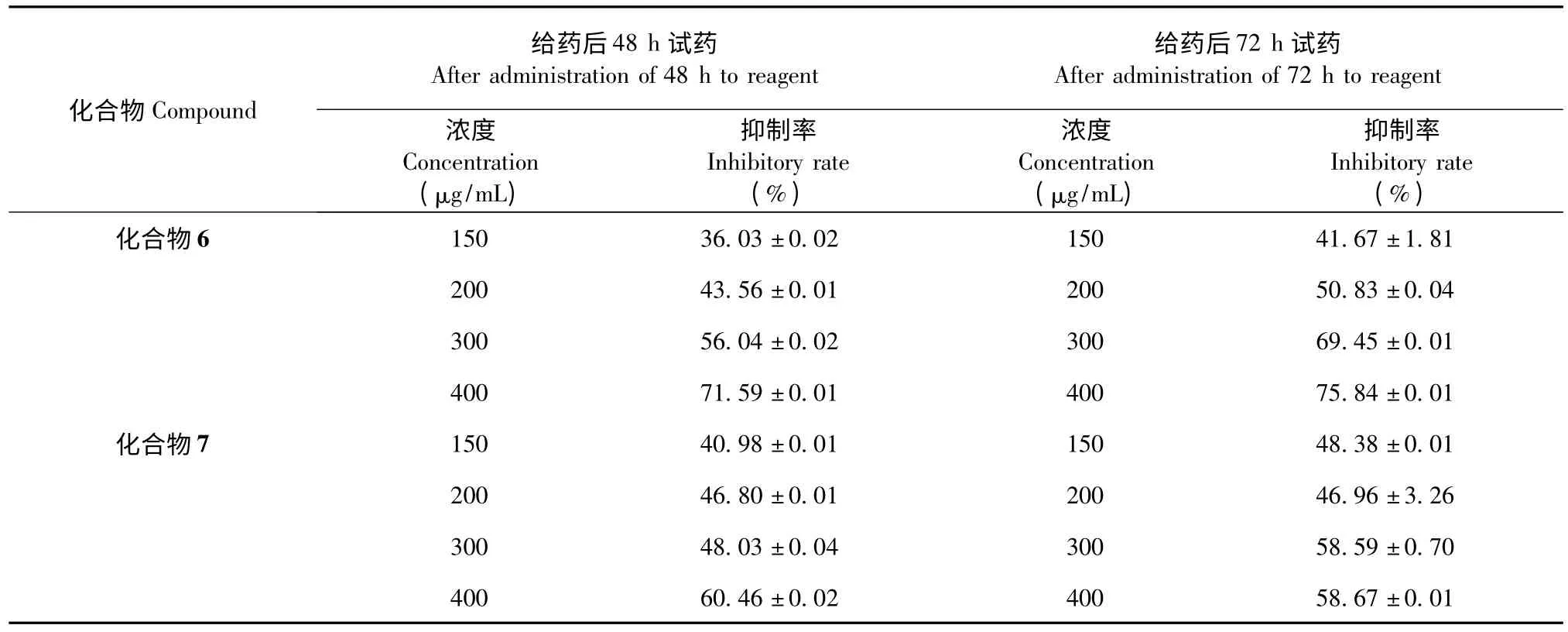
表1 虎耳草不同化合物对PC-3 前列腺癌细胞凋亡的影响()Table 1 Different compounds of Saxifraga stolonifera (L.)Meerb.on PC-3 prostate cancer cell apoptosis()
结果显示,槲皮素3-O-β-L-鼠李糖苷(化合物6)和槲皮素5-O-β-D-吡喃葡萄糖苷(化合物7)对PC-3 前列腺癌细胞的生长有一定的抑制作用。
5 抑菌活性研究
5.1 试剂、材料与菌种
试剂:DMSO 等均为分析纯。
材料:M-H 培养基、营养琼脂购于杭州微生物试剂厂,庆大霉素等。
菌种:大肠杆菌(CMCC 44113)、枯草芽孢杆菌(CMCC 63501)、伤寒沙门氏菌(CMCC 50071)、金黄色葡糖球菌(CMCC 26112)、铜绿假单胞菌(CMCC 10211)、藤黄八叠球菌(CMCC 28001),[菌种均购自中国菌种保藏中心]。
5.2 试验方法
采用平板打孔法,选用内径6 mm,外径7 mm的牛津杯,选用处于对数生长期的试验菌种,细胞密度为1.0 ×106~1.0 ×108个/mL,试验样品用二甲基亚砜(DMSO)试剂溶解。样品准确称取5 mg,用0.5 mL DMSO 溶解,浓度配制为:10 mg/mL,每孔加入样品溶液40 μL。选用DMSO 为空白对照,庆大霉素为阳性对照,每孔加入庆大霉素也为40 μL。在枯草芽孢杆菌实验中的浓度0.025 mg/mL,在其余五种菌的实验中浓度为0.25 mg/mL,通过观察各种抑菌圈的半径,得出抑菌效果,结果见表2。
5.3 抑菌作用实验结果及结论
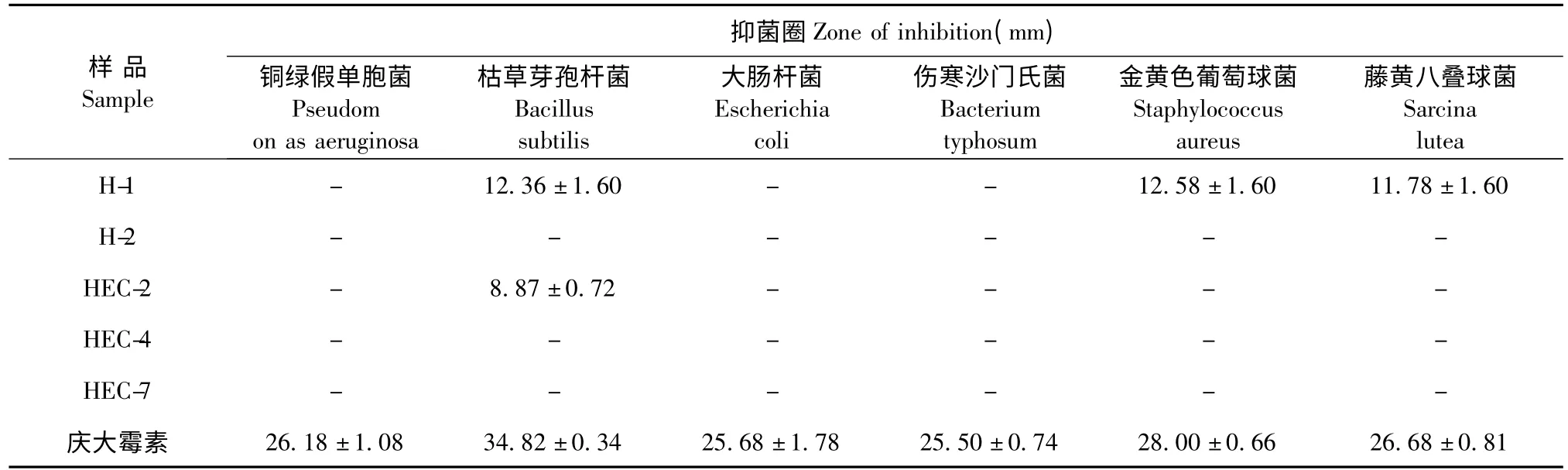
表2 虎耳草不同浸膏及化合物的抑菌活性筛选Table 2 Different extracts and compounds of Saxifraga stolonifera (L.)Meerb.on antibacterial activity screening
抑菌实验研究发现:虎耳草80%醇提物的乙酸乙酯萃取部分对枯草芽孢杆菌抑菌圈大小为12.36±1.60、对金黄色葡糖球菌抑菌圈大小为12.58 ±1.60、对藤黄八叠球菌抑菌圈大小为11.78 ±1.60,由此说明虎耳草乙酸乙酯萃取部位具有潜在的抑菌作用。其中,化合物2(琥珀酸)对枯草芽孢杆菌抑菌圈大小为8.87 ± 0.72,表明此化合物对枯草芽孢杆菌有潜在的抑制作用。
1 Drug Administratin of Gui Province(贵州省药品监督管理局).Chinese Medicinal Materials in Guizhou Province,National Quality Standards for Medicines(贵州省中药材、民族药材质量标准).Guizhou Science and Technology Publisher,2003.235.
2 Jiangsu Medical College(江苏新医学院).Dictionary of traditional Chinese medicine,the first volume(中药大辞典,上册).Shanghai science and technology Publisher,2005.1335.
3 Luo HW(罗厚蔚),Wu BJ(吴葆金),Chen JA(陈节庵),et al.The effective components of Saxifraga stolonifera (L.)Meerb.J China Pha Univ(中国药科大学学报),1988,19:1-3.
4 Aoyagi Y,Kasuga A,Vujirma S,et al.Isolation of antioxidative compounds from Saxifraga Stolonifera.Nip Shok Kag Kog Kai,1995,42:1027-1030.
5 Feng WS(冯卫生),Li Z(李 振),Zheng XK(郑晓珂),et al.Chemical constituents of Saxifraga stolonifera(L.)Meeb.Acta Phar Sin(药学学报),2010,45:742-746.
6 Ding JX(丁家欣),Zhang L S(张立石),Zhang L(张 玲),et al.The influence of Saxifraga stolonifera (L.)Meeb to prostate anceer.Chin J Bas Med Trad Chin Med(中国中医基础医学杂志),2005,11:905-907.
7 Liu SW(刘世旺),Xu YX(徐艳霞),Shi HW(石宏武).The influence of Ethanol extract of Saxifraga stolonifera(L.)Meeb to bacteria growth curve.J Anhui Agri Sci(安徽农业科学),2007,35:943-946.
8 Chen Z,Liu YM,Yang S,et al.Studies on the chemical constituents and anticancer activity of Saxifraga stolonifera (L.)Meeb.Bio & Med Chem,2008,16:1337-1344.
9 Lv J(吕 洁),Kong LY(孔令义).Studies on the Constituents of Hypericum japonicum Thunb·ex Murray.Mod Chin Med(中国现代中药),2009,(11):12-14.
10 Xue HQ(薛慧清),Yang HP(杨红澎),Wang HQ(汪汉卿),et al.Study on triterpenes from of Ligularia xanthotricha.China J Chin Mater Med(中国中药杂志),2008,33:272-275.
11 Feng C(冯 超),Li XM(李晓明),Tian MQ(田敏卿),et a1.Chemical constituents of medicinal mangrove plant Hibiscus tilisceus.Mar Sci(海洋科学),2008,32(9):57-60
12 Pendse R,Rama R AV,Venkataraman K.5,7-Dthydroxychromone from Arachis hypogoea Shells.Phytochemistry,1973,12:2033-2034.
13 Zhou ZH(周志宏),Zhang YJ(张颖君),Yang CR(杨崇仁).Saluenin,a New Flavonol Glycoside from Camellia saluenensis.Act Bot Yunnan(云南植物研究),2000,22:90-96.
14 Tamura Y,Nakajima K,Nakayasu K,et al.Flavonoid 5-glucosides from the cocoon shell of silkworm,Bombyx Mori Phytochemistry,2002,59:275-278.
15 Yoon JK,Min HY,Eun JL,et al.Phytochemical Studies on Paeoniae Radix (4)-Cerebrosides and Other Constituents.Nat Prod Sci,2008,14:161-166.
16 Li HY(李红艳),Xia QS(夏启胜),Xu M(徐梅),et al.Study of the optimal experiment conditions of MTT,MTS and WST-1 in cell proliferation assay.Chin J Rehabilitation Med(中国康复医学杂志),2005,20:824-826.
17 Zhang LS(张立石),Ding JX(丁家欣),Zhang QH(张秋海),et al.The inhibition of the extract of Saxifraga stolonifera (L)Meeb to rat fibers cell.Chin J Bas Med Trad ChinMed(中国中医基础医学杂志),2005,11:920,922.
