食品中柠檬酸的阻抑动力学光度法检测
2013-12-29王晓菊
蔡 艳,高 烨,王晓菊
柠檬酸广泛存在于动植物组织和各种水果、蔬菜中,是对人体有益的一种物质。柠檬酸与人类的健康密切相关,可增强体内正常代谢,而且在食品工业上经常作为食品添加剂。虽然柠檬酸对人体无直接危害,但它可以促进体内钙的排泄和沉积,如长期食用含柠檬酸的食品,有可能导致低钙血症。因此,柠檬酸的测定在食品工业中都具有重要的意义。目前,已报道的测定柠檬酸的方法有离子交换色谱法[1]、高效液相色谱法[2]、毛细管电泳法[3]、流动注射化学发光法[4]、红外光谱技术法[5]、电分析法[6]、荧光猝灭法[7]、分光光度法[8]、核磁共振法[9]、质谱法[10]等。
催化动力学光度法具有选择性好,所需仪器设备简单等特点,近年来渐受重视,广泛用于各种元素的测定,在痕量柠檬酸的测定中已有应用[11-12],但以中性红为指示剂,分析测定痕量柠檬酸的研究尚未见报道。
研究表明,在硫酸和十六烷基三甲基溴化铵介质中,痕量柠檬酸对H2O2氧化中性红的褪色反应有较强的阻抑作用,且在一定浓度范围内,体系的吸光度变化值与柠檬酸浓度之间有较好的线性关系。由此,本文建立了一种表面活性剂增敏阻抑催化动力学光度法测定痕量柠檬酸的新方法。
1 材料与方法
1.1 主要仪器与试剂
723 型可见分光光度计(上海光谱仪器有限公司);SDC-6型数控低温超级恒温槽(重庆试验设备厂)。
柠檬酸标准溶液:按常规方法配制1.0 g·L-1的柠檬酸标准溶液,临用前稀释成1.0μg·mL-1工作液。硫酸溶液:1.0 mol·L-1;中性红溶液(Neutral red,NR):1.0×10-3mol·L-1;过氧化氢溶液:3%(体积分数);十六烷基三甲基溴化铵(CTMAB)溶液:1.0×10-3mol·L-1;Fe3+溶液:0.01 g·L-1。所用试剂均为分析纯或优级纯,实验用水为二次石英亚沸蒸馏水。
1.2 实验方法
于2支25mL具塞比色管中分别依次加入2.0 mL硫酸溶液,1.0 mL中性红溶液,1.0 mLCTMAB溶液,1.0 mLFe(Ⅲ)溶液,2.0 mL过氧化氢溶液,其中一支具塞比色管加入一定量的柠檬酸工作溶液(为阻抑反应体系),另一支不加柠檬酸工作溶液(非阻抑反应体系),加水稀释至刻度,摇匀后置于80℃水浴中加热15 min,同时取出冰水冷却20 min。用1.0cm比色皿在520 nm处分别测量阻抑反应体系的吸光度A和非阻抑反应体系的吸光度A0,计算ΔA=A-A0。
2 结果与讨论
2.1 吸收曲线
配制不同体系的溶液,按照试验方法在分光光度计上扫描吸收光谱,得吸收曲线(图1)。图1中曲线2和曲线3表明,柠檬酸在硫酸介质中对Fe(Ⅲ)催化过氧化氢氧化中性红的褪色反应中具有显著的抑制作用,使吸光度值增大。在上述反应体系中加入表面活性剂CTMAB后,使体系的吸光度差值增大,由此可知CTMAB具有增敏作用。从图1还可以看出,各条曲线均在520 nm处有最大吸收峰,故试验选择520 nm为工作波长。
2.2 反应条件
2.2.1 反应介质的选择
试验了硫酸、乙酸、乙酸-乙酸钠、氯化铵-一水合氨、一水合氨溶液等多种介质,用量1.0 mL测其ΔA。实验结果表明硫酸对该指示反应增敏效果最好,ΔA值最大;考察硫酸用量,其用量在1.8~2.2mL时ΔA达最大,所以本法选择1.0 mol·L-1硫酸溶液为反应介质,最佳用量2.0mL。
2.2.2 表面活性剂的选择
分别实验了阴离子表面活性剂十二烷基苯磺酸钠、琥珀酸二异辛酯磺酸钠,阳离子表面活性剂溴化十六烷基吡啶、氯化十六烷基吡啶、十六烷基三甲基溴化铵(CTMAB),非离子表面活性剂乳化剂OP等对反应的影响。实验表明,只有CTMAB有增敏作用,效果最好,吸光度明显降低,选用1.0mL CTMAB,体系ΔA数值最大,且重现性较好。所以选择CTMAB为增敏剂,其用量为1.0mL。
2.2.3 试剂用量的选择
按实验方法试验不同体积的中性红溶液,实验结果表明,中性红用量在1.0 mL时,ΔA数值最大,所以中性红指示剂实际用量为1.0mL。仅改变过氧化氢,随着过氧化氢用量的增大,阻抑和非阻抑反应速率均增大,但程度不同。当过氧化氢用量为2.0 mL时,ΔA最大且稳定重现性好。故实验选用过氧化氢的用量为2.0 mL。仅改变Fe(Ⅲ)的用量,其用量在为0.8~1.2 mL范围时,ΔA达最大。故实验选用Fe(Ⅲ)用量为1.0 mL。
2.2.4 反应时间的选择和速率常数
考察加热时间对阻抑反应的影响,实验表明,加热反应时间在2~15 min内ΔA与时间t有良好直线关系,因此该阻抑反应可被看作是假零级反应。其线性回归方程为:△A=-2.38×10-3t+0.013,表观速率常数k为2.38×10-3mol·L-1·min-1。若加热时间延长15 min,△A逐渐下降,故本法选反应时间为15 min。
2.2.5 反应的终止及体系稳定性
由于冰水下本阻抑反应体系几乎不反应,因此可以通过冰水中冷却20 min终止反应。实验表明,冰水中冷却20 min,2 h内吸光度几乎不变,表明本阻抑反应具有很好的稳定性。
2.2.6 反应温度的选择和反应活化能
按实验方法进行测定,随温度升高,反应速度加快,反应温度在60℃~800℃之间反应速率迅速加快,800℃时ΔA达到最大,实验中选择反应温度为800℃。
反应温度在70℃~80℃间时,测定不同温度下的表观速率常数k,用-lnk对1/T(开尔文温度K)作图得直线方程,求得阻抑反应表观活化能Ea=126.2kJ·mol-1。
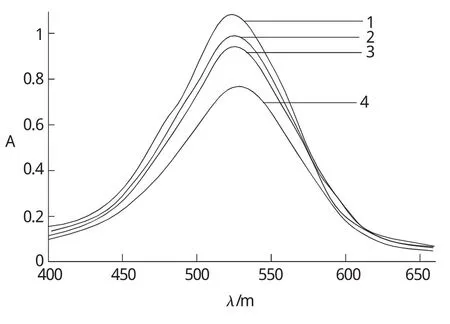
图1 吸收光谱
2.3 校准曲线
在上述选定的实验条件下,阻抑体系的吸光度和非阻抑反应的吸光度之差ΔA与柠檬酸的质量浓度C在0.8~200μg·L-1范围内成直线关系,线性回归方程为△A=2.87×10-3C(μg·L-1)+0.0179,相关系数R=0.9991。对空白进行11次重复测定,所得结果的相对标准偏差Sbc=2.4×10-3,用空白试液的标准偏差除以校准曲线的斜率(3Sbc/K)求得柠檬酸的检出限为2.51×10-6g·L-1。
另外,按实验方绘制不加入CTMAB时柠檬酸质量标准工作曲线,其回归方程为:△A=4.28×10-4C(μg·L-1)+0.0191,相关系数r=0.9926。对比加入及不加CTMAB时的工作曲线可看出,其斜率相差6倍。可见,由于加入增敏剂,灵敏度提高了近6倍。
2.4 干扰试实验
考察了20多种常见共存离子及有机物质对25mL溶液中含1.0μg柠檬酸的影响,结果表明,当相对误差不大±5%时,共存物的允许倍数为:1000倍的K+、Na+、Ac-、NO-3、SO2-4Mo(VI)、Zn2+、F-; 500倍的Cd2+、Co2+、Ni2+、Cr(VI)、Pb2+、Mg2+、Ba2+、VO-3、PO3-4;300倍的氨基乙酸、尿酸、酒石酸、苦味酸;100倍的苯胺、盐酸羟胺、间苯三酚;50倍的甲醛、间苯二酚、EDTA;30倍的草酸等不干扰柠檬酸的测定。
2.5 样品分析
将不同厂家生产的汽水适当稀释,取一定量按实验方法进行分析测定,并做加标回收实验,结果见表1。
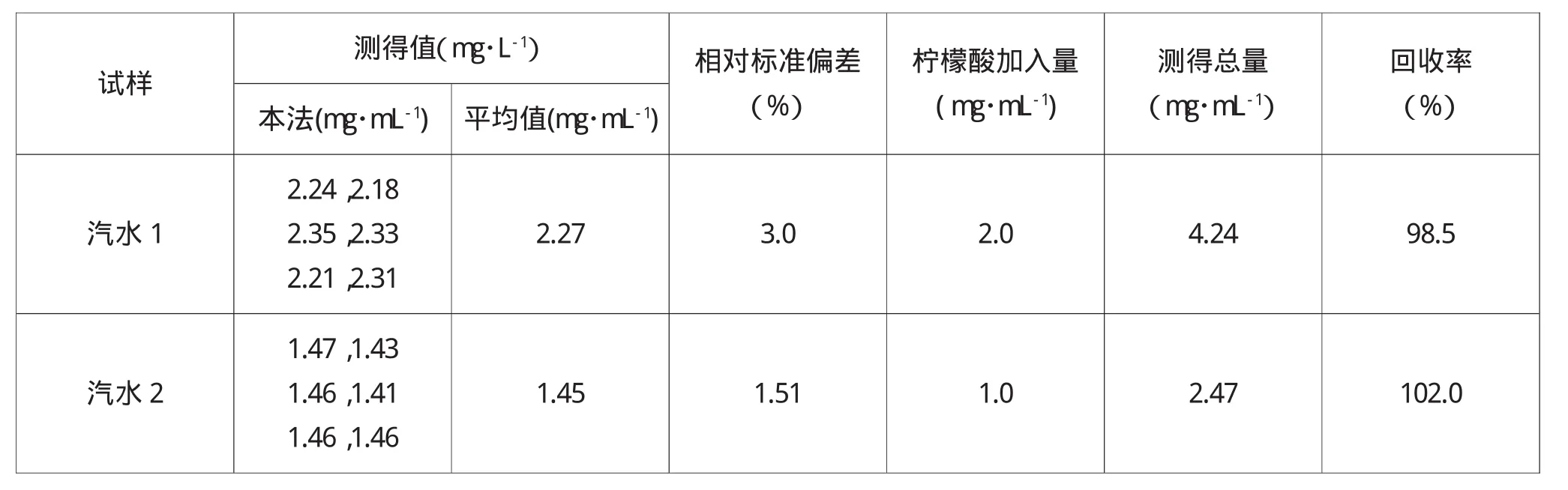
表1 样品测定结果
3 结论
基于在H2SO4和阳离子表面活性剂十六烷基三甲基溴化铵溶液中柠檬酸对Fe(Ⅲ)催化H2O2氧化中性红的褪色反应具有抑制作用,从而提出了一种阻抑褪色动力学光度法测定汽水中痕量柠檬酸的新方法。柠檬酸浓度在0.8~200μg·L-1范围内,具有良好的线性关系,其相关系数为γ=0.9991。方法准确可靠,精密度好,回收率在98.5%~102%之间。
[1]谢国海,陈志强,叶章群,等.离子交换色谱同时测定尿液草酸及柠檬酸的研究[J].色谱,2006,21(5):365-366.
[2]张燕,闫磊,戴洋洋,等.葡萄酒中柠檬酸的液相色谱检测[J].食品研究与开发,2012,33(6):125-127.
[3]王迪,张强,韩东.用毛细管电泳测定发酵液中柠檬酸的含量[J].分析与测试,2000,29(6):34-36.
[4]Moreno-Cid.A, Yebra .M.C, Santos .X.Flow injection determinations of citric acid: a review[J].Talanta, 2004, 63(3):509-514.
[5]岑海燕,何勇,张辉等.可见光/近红外光谱技术快速测定橙汁柠檬酸含量[J].光谱学与光谱分析,2007,27(9):1748-1749.
[6]李茂国,张龙,赵英阳,等.微分电位溶出法测柠檬酸[J].安徽师范大学学报:自然科学版,2000,23(3):256-257.
[7]陈兰化,管明霞.动力学荧光猝灭法测定柠檬酸的研究[J].分析实验室,2005,24(2):19-21.
[8]张廷超,杨惠.微量分光光度法测定人精浆中柠檬酸含量[J].现代检验医学杂志,2004,19(5):32-33.
[9]阎政礼,杨明生.核磁共振法同时测定桔子原汁中主要糖类和柠檬酸[J].食品工业科技,2010,31(8):353-357.
[10]Alireza Ghassempour, Nahid Mashkouri Najafi, Ali Asghar Amiri.Determination of citric acid in fermentation media by pyrolysismass spectrometry[J].Journal of Analytical and Applied Pyrolysis, 2003, 70(2):251-261.
[11]叶青.阻抑催化动力学光度法测定柠檬酸[J].食品工业科技,2006,27(3):180.
[12]丁素芳,晋红梅,朱守圃.活化催化动力学光度法测定柠檬酸[J].中国卫生检验杂志,2009,19(7):1520-1521.
