胆固醇、pH值对金属离子与磷脂酰甘油相互作用成膜的影响
2013-12-14刘志存张灵芝牛蓉芬刘春艳
张 桥,刘志存,张灵芝,赵 锐,牛蓉芬,刘春艳
(陕西师范大学物理学与信息技术学院,西安 710062)
目前,制备优质的LB膜正日益受到关注。利用各种方法对LB膜进行相行为与分子组装的研究对生命过程分析具有重大意义[1]。迄今为止人们对单因素对LB膜的影响的研究已经比较成熟,而研究多因素同时对LB膜的影响还比较少。本文主要研究多因素同时对LB膜的影响。该研究具有广泛的应用价值,有助于制备更高性能的单分子膜,进而有益于阐明生命过程中能量、物质、信息的传递机理[2]。
在LB膜实验中需要考虑3个或者3个以上的因素对其的影响,因此本研究采用正交实验。正交实验不但可以同时安排很多因素进行实验,而且可以同时寻求最优水平的组合。
1 材料与方法
1.1 仪器分析
LB膜分析仪器是由芬兰KSV公司生产,型号为Minitrough,分辨率为4 μN/m,膜天平测量范围为0~150 mN/m,水槽尺寸为364 mm×75 mm×5 mm,滑块压缩速度范围为0.01~400 mm/min,亚相体积为0.16 L,中心深度为70 mm。
1.2 材料
试剂:两亲分子材料——磷脂酰甘油(phosphatidylglycerols,PG),它有2个非极性的尾部。本实验材料的两亲分子的极性头基带有一个单位的负电荷。胆固醇(cholesterol,Chol),又称胆甾醇,是一种环戊烷多氢菲的衍生物。本次实验所使用PG购于美国Sigma-Aldrich公司,胆固醇购买于上海试剂公司。化学试剂包括无水乙醇、甲醇、氯仿、甘氨酸-氢氧化钠缓冲液、磷酸氢二钠-柠檬酸缓冲液、氯化钾(KCl)、氯化镁(MgCl2),全是国产分析纯。水为离子交换二次蒸馏水,pH值为6.8。
1.3 实验方法
将磷脂酰甘油材料溶于氯仿与甲醇体积比为49∶1的有机溶剂中,胆固醇材料溶于氯仿与甲醇体积比为3∶1混合的有机溶剂中,均制成0.5 mmol/L的溶液。在制备LB膜时,将浴槽温度控制在24±0.1℃范围之内。首先将配制好的PG溶液用50 μL微量注射器均匀地滴加在亚相液面之上,其次让其静置15 min,目的是为了让分子自动铺展,氯仿与甲醇彻底挥发。最后让LB膜仪器上的2个挡板以10 mm/min速度运动,这时计算机将开始自动记录π-A曲线数据[3-4]。π-A曲线是指:连续改变不同的条件得到PG单分子所占的单分子面积,此时膜压π(mN/M)与PG单分子所占面积A的之间的变化关系。表1为pH值、成膜物质的量、亚相及加入胆固醇量的实验设计数据。
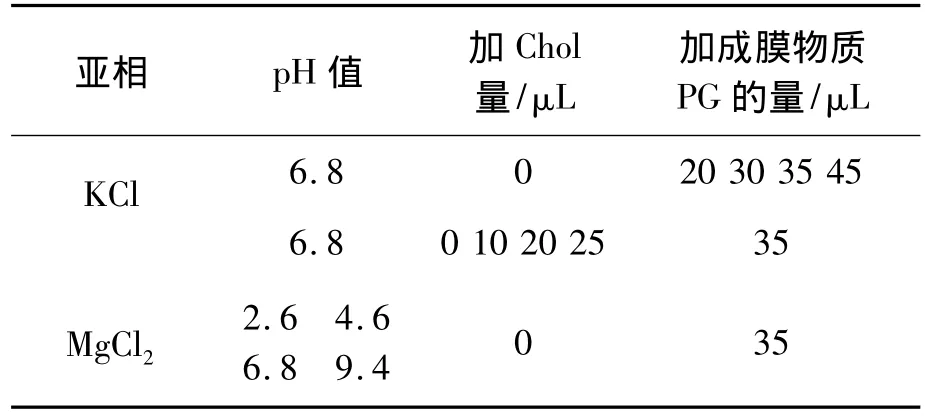
表1 实验设计数据
2 实验结果
2.1 Chol对金属离子磷脂酰甘油单分子的影响
图1与图2是亚相分别为金属离子(KCl、MgCl2),加入 PG 与 Chol(mol/mol)之比为:1∶0、1∶0.3、1∶0.6、1∶0.7 所扫描的 π -A 曲线。从胆固醇对金属离子磷脂酰甘油单分子膜的π-A曲线中明显可以看出:随着加入胆固醇量的增加,气相部分明显减短,崩塌压压明显降低,相变点变化比较凸出,曲线也相对依次外扩,说明胆固醇有加速相变,促进金属离子磷脂酰甘油单分子膜稳定结构的形成[5]。
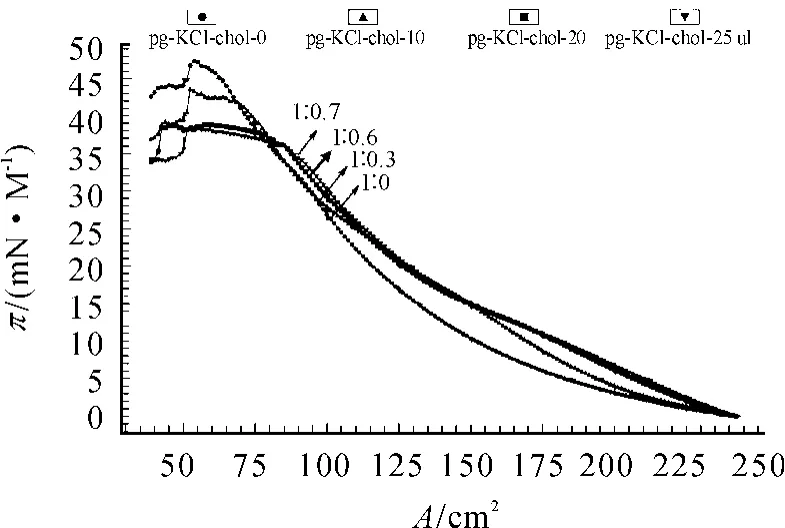
图1 亚相为Kcl溶液,PG与Chol摩尔之比为1∶0、1∶0.3、1∶0.6、1∶0.7 的 π -A 曲线
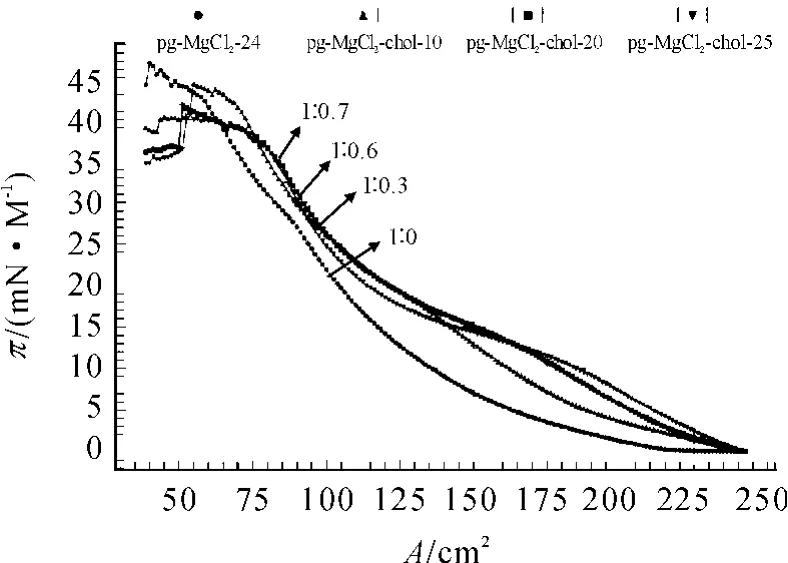
图2 亚相为MgCl2溶液,PG与Chol摩尔之比为1∶0、1∶0.3、1∶0.6、1∶0.7 的 π -A 曲线
2.2 pH值对金属离子单分子膜成膜的影响
图3和图4分别是不同pH值所得到的π-A曲线。当亚相是金属离子,pH值为酸性时,随pH值不断升高,相变点依次逐渐变凸。到pH值为6.8时,曲线相变点最为明显,崩塌压达到最大值。但是当pH值偏碱性,如在pH值为9.4时,磷脂分子更加紧密,形成较低能量的晶格结构,减小了重组的驱动力,磷脂分子相变有所延迟[6-7]。可见在酸性或者碱性条件下都会对金属离子PG单分子膜有影响。
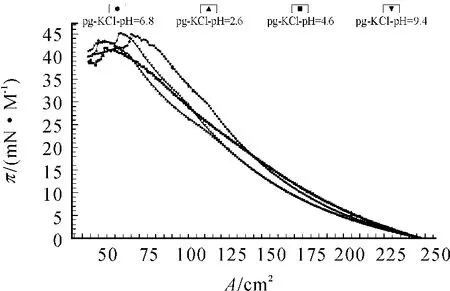
图3 亚相为KCl溶液,pH值为2.6;4.6;6.8;9.4时的π-A曲线

图4 亚相为MgCl2溶液,pH值为2.6;4.6;6.8;9.4时的π-A曲线
2.3 加入成膜物质的量对金属离子单分子膜的影响
图5、6是加不等PG得到的π-A曲线。明显可以看出:当亚相分别是KCl或MgCl2溶液时,金属离子与极性头基之间有静电相互作用,增强了膜之间的结合能力,使膜分子更加紧密的排列[8-9]。加入 PG 的量在 20、30 μL 时,曲线相对依次外扩,气相部分随着PG量的增多而逐渐减少;当加入PG的量为35 μL时,相变点非常凸出,崩塌压可达到48 mN/m;当向加入 PG的量为45 μL时,曲线的外扩依次增大,但崩塌压却降低。以上结果说明成膜物质的量对单分子的形成也是有影响的。
2.4 不同条件下得到分子π-A曲线
以 A(亚相为Water、KCl、MgCl2),B(加入成膜物质的多少,C(亚相pH值的改变)和D(加入胆固醇的多少)为因素,设计出一个四因素三水平的正交实验[10]。图7~9是在不同条件下得到π-A曲线。由于篇幅有限,本文只给出了3幅图。下面利用正交方法来分析PG单分子膜的最佳成膜条件。
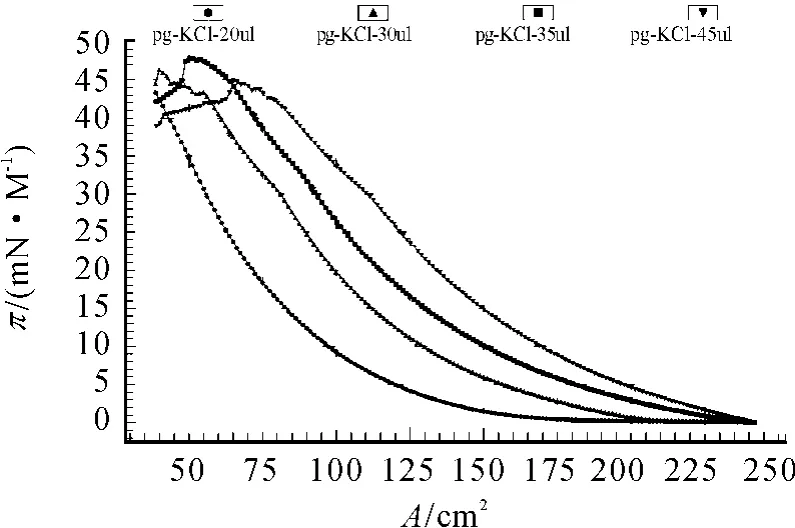
图5 亚相为KCl溶液,加PG为20、30、35、45 μL 时的 π -A 曲线
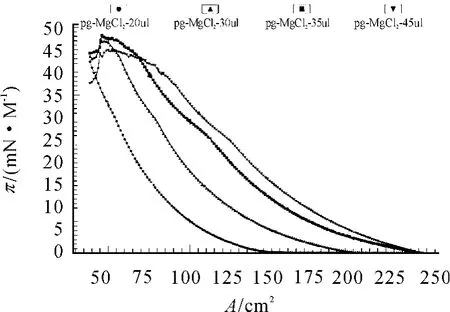
图6 亚相为MgCl2溶液,加PG为20、30、35、45 μL 时的 π -A 曲线
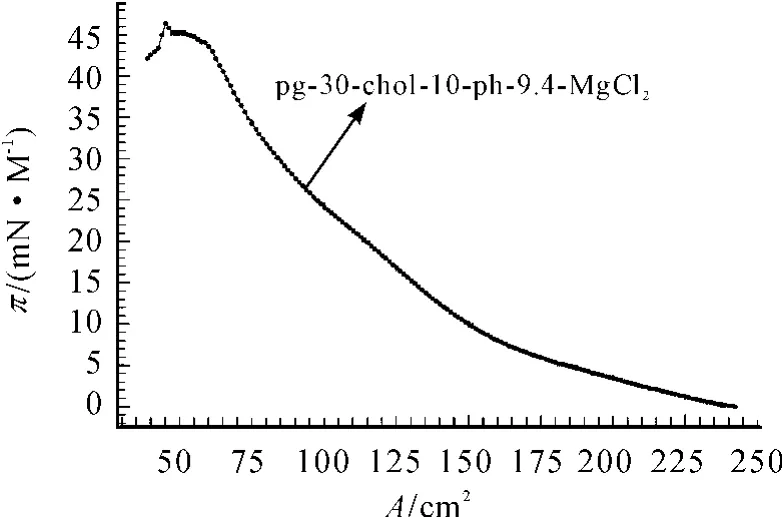
图7 亚相为MgCl2溶液,加PG为30 μL,Chol为10 μL,pH=9.4时的 π-A 曲线
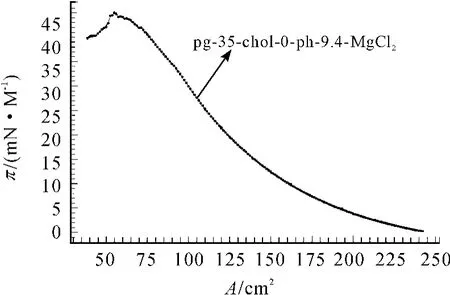
图8 亚相为KCl溶液,加PG为35 μL,Chol为0 μL,pH=9.4时的 π -A曲线
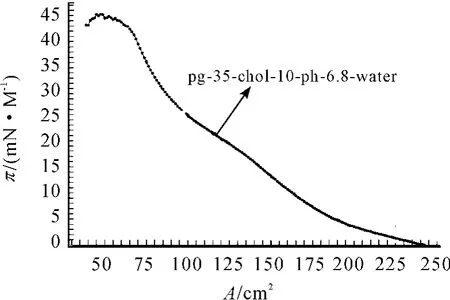
图9 亚相为Water,加 PG 为35 μL,Chol为10 μL,pH=6.8时的 π-A 曲线
2.5 PG单分子面积的正交实验
表2为正交实验设计表。
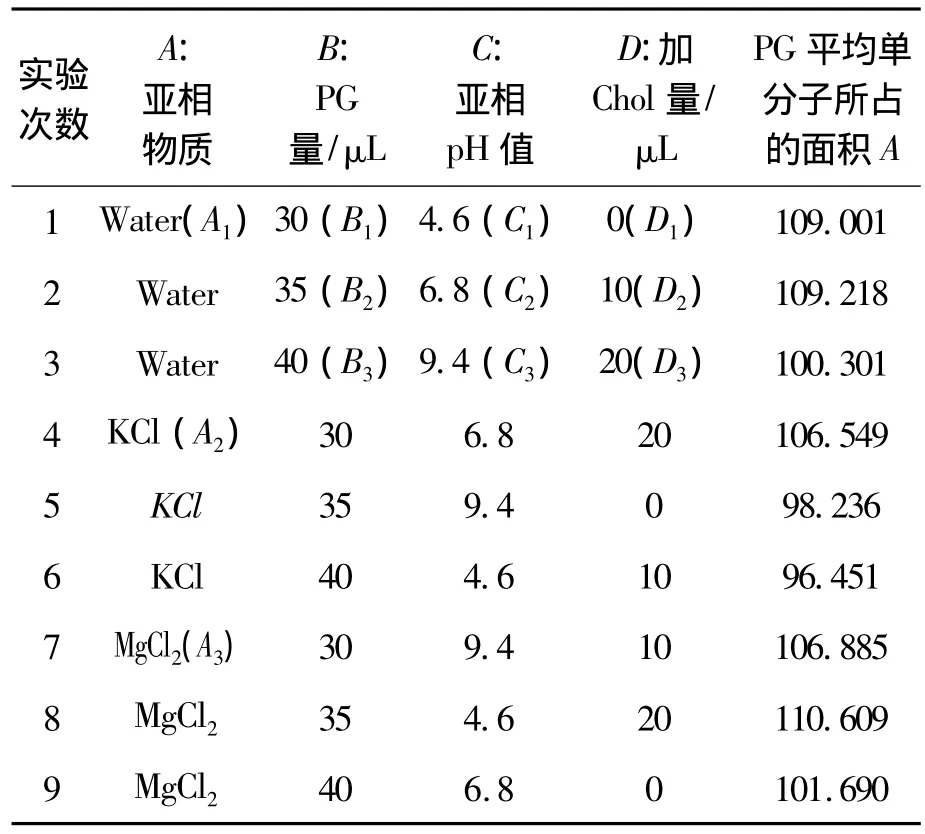
表2 正交实验设计表
图10~11是根据其差分析方法绘制的结果。明显可以看出kA3>kA1>kA2,这样就可断定A3为A因素的最优水平。同理,可以根据计算并确定B1、C2、D3分别为B、C、D因素的最优水平。由此可以得到4个因素的最优水平组合为:A3B1C2D3。R越大,表示该因素的水平变化对试验指标的影响越大,因素越重要。由图12分析可见,RB>RA>RC>RD,因素影响主次顺序为B-A-C-D。
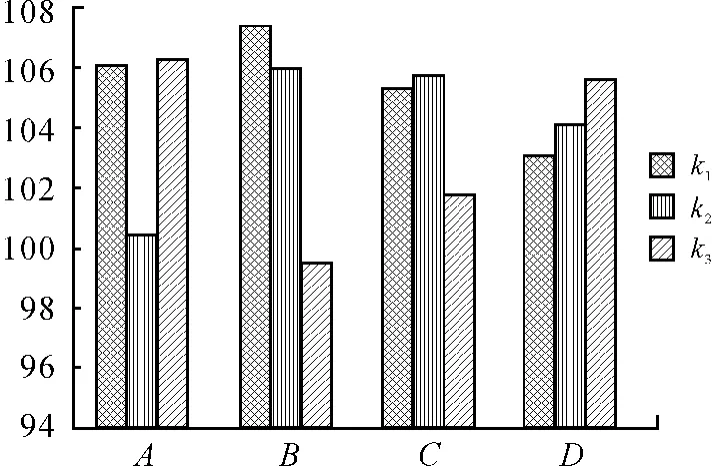
图10 根据极差分析方法绘制的k1、k2、k3值
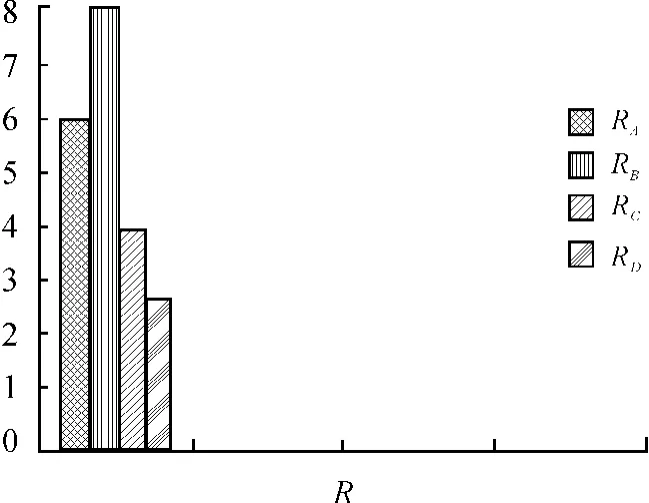
图11 根据极差分析方法绘制的R值
3 结束语
综上所述,胆固醇的量、pH值及成膜物质的多少对形成致密的单分子膜有密切的关系。本文不但分析了单因素对单分子膜的影响,同时也分析了多因素对单分子膜的影响,最后运用正交实验,得到最佳的PG单分子膜的条件是:亚相为MgCl2,加入成膜物质的量为30 μL,亚相的pH值为6.8,加入胆固醇的量为20 μL。此外,得到了PG单分子成膜质量因素的影响主次顺序为:PG量因素高度显著,亚相物质因素显著,亚相pH值因素不太显著,加Chol量因素最不显著,即B-A-C-D。这对于以后研究生物膜结构和功能有很大的意义及价值。
[1]李新民,袁春波,李斌,等.铕对磷脂酰胆碱LB单分子膜结构影响的原子力显微镜观察[J].化学学报,1998,56(3):688-691.
[2]薛萍,欧阳健明,郑文杰.膜/水界面的配位化学[J].广东工业大学学报,2002(2):64-67.
[3]VENETA A,MARGARITA I,ROBERT V,et al.Akinetic study of the formation of β-cyclodextrin complexes with monomolecular films of fatty acids and glycerides spread at the air/water interface[J].Colloids and Surfaces B:Biointerfaces,2005,42(4):9-20.
[4]何平笙.二维状态下的聚合单分子膜和Langmuir-Blodgett膜的聚合[M].合肥:中国科学技术大学出版社,2008:18-20.
[5]王娟,常怡光,孙润广.胆固醇与磷脂酰乙醇胺/磷脂酰胆碱混合膜的热力学特性及其单层膜形态的AFM观察[J].化学学报,2012,70(5):599-601.
[6]郝长春,孙润广.物理因素对磷脂酰胆碱单分子层影响[J].原子与分子物理学报,2007,24(5):928-936.
[7]常曼,刘志存.温度、pH值对金属离子与磷脂酰乙醇胺相互作用成膜的影响[J].重庆理工大学学报:自然科学版,2011,25(12):46-49.
[8]李旸,刘志存.金属离子与单分子膜间的静电相互作用研究[D].西安:陕西师范大学,2011.
[9]蓝永康,刘志存,孙润广.离子与单分子膜间静电相互作用对膜结构及稳定性的影响[D].西安:陕西师范大学,2009.
[10]马艳.PC/PE/Chol复合LB膜的分子结构研究[J].宁夏师范学院学报,2009,30(6):42-44.
