预处理方法对植物生物质中钾元素含量测定的影响
2013-11-08张相龙李博仑郝庆兰
刘 垒 ,张相龙 ,李博仑 ,王 昶,郝庆兰
(1.天津科技大学材料科学与化学工程学院,天津 300457;2.天津科技大学海洋科学与工程学院,天津 300457)
通过热化学转化技术可将植物生物质转化成常规的固体、液体和气体燃料等[1–2].植物生物质中的碱金属元素,尤其是钾元素在植物生物质的热化学转化利用过程中起着很重要的作用[3–5].生物质中钾元素的测定方法种类繁多,目前主要有电感耦合等离子体发射光谱法(ICP-AES)[6]和火焰原子吸收光谱法(FAAS)[7–9]等方法.FAAS 法因其分析速度快、成本低、操作简单、方便等优点而被广泛使用.FAAS 法测定生物质中钾元素含量之前,为了将生物质中的钾元素转换为FAAS 法可测的钾离子,须先对生物质进行预处理.目前生物质预处理的方法主要有干灰化法、湿式消解法、微波消解法、悬浮样法、煮沸法、浸提法等[7,10–14].生物质种类不同,预处理方法亦不相同,其主要原因在于生物质组成和结构的不同以及生物质中钾元素转化为钾离子的难易程度存在差异.
稻壳作为谷物加工的主要副产品之一,其可燃成分在70%以上,热值为12.5~14.6,MJ/kg,大约是煤的1/2,是一种廉价易得的可再生资源.但迄今为止,我国利用稻壳的水平仍比较低.如何合理地对稻壳加以利用,变废为宝,是一亟待解决的问题.与其他农业废弃物生物质相比,稻壳中的钾等碱金属矿物元素的含量较高,它们的存在对稻壳热化学转化反应产物收率和分布产生影响的同时,还可能导致床料团聚、加热面玷污腐蚀、结渣以及沉积等多种问题.Jenson 等[15]和Nowkowki 等[16]的研究表明,小麦秸秆和速生柳生物质在钾盐催化作用下,气体和固体焦炭产物的收率增加,液体产物的收率下降.Raveendran 等[17]对13 种不同类型的生物质进行的热解研究却发现,钾等金属元素对生物质的热解特性有明显影响,当生物质椰糠、花生壳和稻壳中的钾或锌元素的含量较高时,随热解温度升高,生物质热解气相、液相和固相产物收率的变化趋势与其他生物质的相反.但是,一般的稻壳等生物质的工业分析只提供挥发分、灰分、固定碳和水分等含量,元素分析只提供C、H、O、N 和S 的含量,而对于在热化学转化中起着重要作用的钾等碱金属元素的含量很少提供,而且文献报道亦较少.稻壳的灰分主要为二氧化硅和少量的无机矿物元素(以金属氧化物或盐的形式存在),其值的大小并不能代表钾等碱金属元素含量的高低,所以测定稻壳等生物质中钾等碱金属元素的含量对其综合利用具有重要的意义.
本文选用天津蓟县稻壳作为生物质原料,使用干灰化、湿式消解和微波消解的方法进行预处理,采用FAAS 法,对稻壳中钾元素含量进行了考察,以探求一种快速、准确的生物质中钾元素的测定方法,为植物生物质的热化学转化利用过程积累基础数据.
1 实 验
1.1 试剂与仪器
实验中使用的浓硝酸(质量分数65%~68%)、浓硫酸(质量分数 98%)、浓盐酸(质量分数 36%~38%)、双氧水(质量分数30%)、氯化钾、氯化钠和氯化铯均为分析纯试剂.K+标准溶液的质量浓度为1,mg/mL.
生物质中K 含量的测定使用XFX–120 型火焰原子吸收分光光度计(北京瑞利公司),AS–1 型K 空心阴极灯.工作条件:分析线766.5,nm、灯电流3,mA、狭缝0.4,nm、火焰高度5,mm、空气流量6.7,L/min、乙炔流量1.5,L/min.微波消解使用北京祥鹄科技发展有限公司XH100B 型微波仪.
1.2 生物质样品
实验用生物质样品为天津市蓟县水稻的稻壳.稻壳的干燥无灰基工业分析见表1.稻壳生物质样品风干后经粉碎、筛分,选取粒径在100~120 目的颗粒,实验前在105,℃烘干4,h.

表1 稻壳的工业分析Tab.1 Proximate analyses of rice husk
1.3 稻壳的预处理
干灰化法:精确称取0.250,0,g 稻壳样品于瓷坩埚中,移入马弗炉中于500,℃灰化5,h,取出,冷却后将其转移至100,mL 烧杯中,加入6,mol/L HNO320,mL(或6,mol/L HCl 20,mL)溶解稻壳灰,烧杯口放置表面皿,煮沸溶液0.5,h 以去除溶液中过量的酸(煮沸过程中,当溶液煮至近干时,稍微冷却,加入适量超纯水,继续煮沸).煮沸液冷却后用少量水冲洗表面皿,然后将其转移入250,mL 容量瓶中并加超纯水至刻度.同时配制HNO3和HCl 空白溶液.
湿式消解法:精确称取0.250,0,g 稻壳样品于100,mL 烧杯中.加入浓H2SO45,mL(或浓HNO310,mL)和30% H2O24,mL,烧杯口放置表面皿,摇匀放置过夜,在电炉上缓缓加热,当溶液分解冒出浓烟时,逐渐升高温度.当溶液全部呈棕黑色时,从电炉上取下烧杯,稍微冷却,逐滴加入 30%的 H2O20.5,mL 并不断摇动烧杯,再加热至微沸15,min,如此重复3 次,直至溶液澄清后,再加热微沸10,min,除去剩余的H2O2.冷却后用少量超纯水冲洗表面皿,将消解液移入250,mL 容量瓶中并加超纯水至刻度.同时配制浓H2SO4(或浓HNO3)和H2O2溶液用于空白实验.
微波消解法:精确称取0.250,0,g 稻壳样品于100,mL 三口烧瓶中.加入浓HNO340,mL,摇匀放置过夜,消解前向烧瓶中加入30% H2O28,mL,在回流条件下进行微波消解,消解条件为400,W、10,min 和120,℃.待溶液消解至澄清后,从微波仪上取下烧瓶,稍微冷却,逐滴加入30% H2O20.5,mL,并不断摇动三口烧瓶,再加热至微沸15,min,如此重复3 次,直至溶液澄清后,再加热10,min,除去剩余的H2O2.待烧瓶冷却后,用少量超纯水冲洗回流管,将消解液移入250,mL 容量瓶中并加超纯水至刻度.同时配制浓HNO3和H2O2溶液用于空白实验.
1.4 K+的标准曲线及K+的测量
使用XFX–120 型原子吸收分光光度计测定溶液中K+质量浓度时,标准溶液中K+质量浓度在0.5~2.5,μg/mL 范围内,其标准曲线的线性关系较好.本实验采用1,mg/mL 的K+标准溶液(天津科密欧化学试剂有限公司)配制K+质量浓度分别为0.4、0.8、1.2、1.6 和2.0,μg/mL 的标准溶液.为避免测量过程中K+发生电离干扰,实验中加入CsCl 溶液(天津科密欧化学试剂有限公司)作为消电离剂.
分别移取1.3 中采用干灰化法、湿式消解法和微波消解法处理所得溶液5,mL 至25,mL 容量瓶中,并向各待测液中加入适量的CsCl 溶液,用原子吸收分光光度计测定待测液中的K+质量浓度.
2 结果与讨论
2.1 电离干扰对K+测量的影响
利用火焰分光光度计测定待测液中K+含量时,被测K+在火焰原子吸收分光光度计的原子化室中形成钾原子后会继续发生电离,从而使钾原子数减少,溶液吸光度降低,导致样品K 含量的测量值偏低,加入适量的碱金属离子能消除该影响[11].锂、钠、钾、铷和铯的电离电势分别为 5.37、5.09、4.32、4.19 和3.86,eV,Cs 的电离电势最小,因此适量的Cs 可以有效地抑制其他碱金属元素的电离.
稻壳中除钾和钠元素外,其他碱金属的含量较小,所以本实验只考察钾、钠含量对溶液吸光度的影响.根据稻壳中钾和钠元素的质量比[18],配制了含有1.5,μg/mL 的K+和0.024,μg/mL 的Na+混合溶液8 份,其中1 份为空白样,其余7 份分别加入50、100、200、300、400、500 和600,μg/mL 的CsCl 溶液.CsCl 的加入量对K+电离干扰的影响如图1 所示.由图1 可知:当K+待测溶液中不含CsCl 时,溶液中的K+由于受到电离干扰的影响,K+质量浓度仅为0.54,μg/mL,远远低于溶液中K+质量浓度的理论值1.5,μg/mL,相对误差高达-64%.随着K+待测溶液中CsCl 加入量的增加,溶液的吸光度呈现先增加后趋于稳定的趋势.当溶液中CsCl 的加入量超过400,μg/mL 时,待测溶液的吸光度稳定,测得溶液中K+质量浓度值接近理论值 1.5,μg/mL,说明电离干扰已基本被消除.溶液中K+质量浓度越高,所需的消电离剂Cs+质量浓度亦越高.在测量生物质中K 含量时,因水稻品种、产地、土壤肥力等因素的影响,生物质经预处理后获得的待测液中 K+质量浓度,有时会略高于1.5,μg/mL,所以本研究添加CsCl 溶液的质量浓度选择为500,μg/mL.
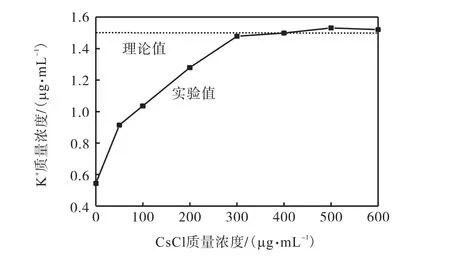
图1 CsCl加入量对K+质量浓度的影响Fig.1 Effect of CsCl amount on K+ concentration in the mixed solution of KCl and NaCl
2.2 K+标准工作曲线及稻壳中K含量测定
在配制的标准K+溶液中加入500,μg/mL 的CsCl消电离剂后,K+溶液的标准工作曲线如图2 所示.由图2 可知,本实验测得的K+溶液标准工作曲线的回归方程为A=0.270,5,ρ+0.006,38,相关系数R2=0.997,0,与未添加CsCl 的K+溶液标准工作曲线(A=0.179,3,ρ+0.019,59,R2=0.983,6)相比,相关性增加[19].

图2 K+溶液的标准工作曲线Fig.2 Standard curve of the potassium ion solution
上述K+溶液标准工作曲线的回归方程可表示为A=aρ+b,则稻壳中K 含量的计算公式为

式中:A 为溶液的吸光度;a 为回归方程的斜率;b 为回归方程的截距;m 为稻壳的质量,g.
2.3 预处理对稻壳中K含量测定的影响
为避免待测溶液酸度过高对碱金属元素测量结果的影响[11],稻壳的不同预处理方法均做了赶酸处理.扣除了试剂和空白背景值,干灰化法、湿式消解法和微波消解法3 种预处理方法测定的稻壳样品中钾元素含量的结果见表2.
干灰化法处理稻壳样品时,须用稀酸溶解稻壳灰,本实验选用的稀酸为6,mol/L HNO3或6,mol/L HCl.由表2 可知,用HNO3和HCl 得到的实验结果相近,但HNO3处理法的钾元素测量值的相对标准偏差(RSD)较小,实验结果精密度较高.在溶解稻壳灰的赶酸处理中,与HCl 处理相比,HNO3能够较稳定地析出,K 含量测量结果的RSD 较小.
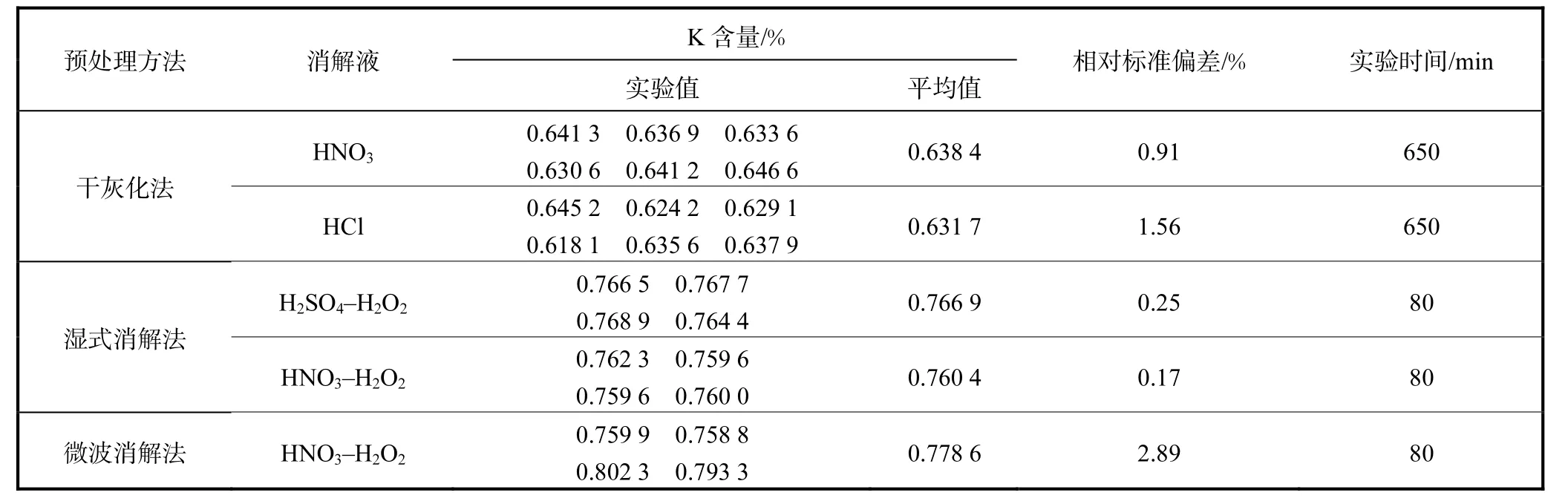
表2 预处理方法对稻壳中钾元素含量测定的影响Tab.2 Effect of pretreatments on the measurement of K content in rice husk
生物质中的钾元素主要存在于无机盐和少量有机官能团中.采用湿式消解法对稻壳进行预处理时,为了将生物质中钾元素完全转化为可以在实验中进行测定的钾离子,选用的消解液应具有较强的氧化性,本实验采用H2SO4–H2O2和HNO3–H2O2消解液.表2 的结果表明,H2SO4–H2O2消解液测得的稻壳中K 含量与HNO3–H2O2相近,这是由于H2SO4–H2O2和HNO3–H2O2的氧化性相近所致.湿式消解法测定的K 含量数据稳定,实验所用装置非常简单,实验耗时较少,在消解过程中基本不会造成钾元素的损失.
采用HNO3–H2O2微波消解法处理稻壳时,K 含量的测量结果较分散,数据的稳定性较差,且实验装置复杂,操作繁琐,能耗较大.
比较稻壳的3 种预处理方法,干灰化法较湿式消解和微波消解测量结果普遍偏低,这是因为生物质样品经马弗炉长时间灰化时,钾元素有一定程度的挥发损失[20];其次,在使用HNO3(或HCl)处理稻壳灰时,溶液中会残留一些黑色难溶物.表2 的结果还表明,干灰化法耗时较长.
稻壳样品通过3 种预处理方法处理后测定的K含量有着明显的差异,究其原因主要是样品消解程度以及处理过程中钾元素的损失程度不同所致.
3 结论
用FAAS 法测定稻壳生物质中钾等碱金属元素的含量时,加入适宜的其他金属元素可以有效消除测量过程的电离干扰.实验中选用电离电势比钾原子小的铯原子,以CsCl 的形式加入到生物质预处理后的K+待测溶液中(加入量为500,μg/mL),有效地消除钾原子电离干扰所导致测量结果偏低的问题.
稻壳等生物质中钾元素的测量结果与其预处理方法有关.湿式消解法相对于干灰化法和微波消解法而言,测量结果的准确性好,稳定性高,且设备要求简单,操作方便、快速.实际应用中,硝酸成本较低,宜采用HNO3–H2O2湿式消解法.
[1]Turn S,Kinoshita C,Zhang Z,et al.An experimental investigation of hydrogen production from biomass gasification[J].International Journal of Hydrogen Energy,1998,23(8):641–648.
[2]Demirbaş A.Fuel properties and calculation of higher heating values of vegetable oils[J].Fuel,1998,77(9/10):1117–1120.
[3]杨昌炎,姚建中,吕雪松,等.生物质中K+、Ca2+对热解的影响及机理研究[J].太阳能学报,2006,27(5):496–502.
[4]Mourant D,Wang Z,He M,et al.Mallee wood fast pyrolysis:Effects of alkali and alkaline earth metallic species on the yield and composition of bio-oil[J].Fuel,2011,90(9):2915–2922.
[5]Shi L,Yu S,Wang F C,et al.Pyrolytic characteristics of rice straw and its constituents catalyzed by internal alkali and alkali earth metals[J].Fuel,2012,96:586–594.
[6]林添明,叶晓云,谢国勋,等.电感耦合等离子体发射光谱粉末进样法测定粮食及茶叶中微量元素的研究[J].分析化学,1991,19(10):1137–1140.
[7]商业部谷物油脂化学研究所.GB/T 14609—1993 谷物中铜、铁、锰、锌、钙、镁的测定法·原子吸收法[S].北京:中国标准出版社,1993.
[8]罗晓薇.火焰原子吸收光谱法测定茶叶中铅铜[J].现代仪器,2004(3):30–32.
[9]Lima A T,Ottosen L M,Ribeiro A B.Electroremediation of straw and co-combustion ash under acidic conditions[J].Journal of Hazardous Materials,2009,161(2/3):1003–1009.
[10]马戈,张景彦,牛刚.火焰原子吸收光谱法测定茶叶中的钾、钠、铷[J].光谱实验室,1999,16(2):147–149.
[11]张翠兰,梁伟.土壤、植物中钾、钠的原子吸收光谱测定[J].分析化学,1982,10(6):382–383.
[12]国家饲料质量监督检验中心(武汉).GB/T 18633—2002 饲料中钾的测定·火焰光度法[S].北京:中国标准出版社,2002.
[13]农业部果品及苗木质量监督检验测试中心(郑州),中国农业科学院郑州果树研究所.NY/T 2017—2011 植物中氮、磷、钾的测定[S].北京:中华人民共和国农业部,2011.
[14]刘立行,张启凯,胡洋.悬浮液进样–火焰原子吸收光谱法测定面粉的钙和镁[J].光谱学与光谱分析,1999,19(3):424–425.
[15]Jensen A,Dam-Johansen K,Wójtowicz M A,et al.TGFTIR study of the influence of potassium chloride on wheat straw pyrolysis[J].Energy Fuels,1998,12(5):929–938.
[16]Nowakowski D J,Jones J M,Brydson R,et al.Potassium catalysis in the pyrolysis behaviour of short rotation willow coppice [J].Fuel,2007,86(15):2389–2402.
[17]Raveendran K,Ganesh A,Khilar K C.Influence of mineral matter on biomass pyrolysis characteristics[J].Fuel,1995,74(12):1812–1822.
[18]谭洪,王树荣.酸预处理对生物质热裂解规律影响的实验研究[J].燃料化学学报,2009,37(6):668–672.
[19]唐伟,孙晓怡.在火焰原子吸收法中使用消电离剂测定降水中钾[J].黑龙江环境通报,2002,26(4):89–90.
[20]邢大荣.干式灰化法植物标准试样桃叶中元素的损失[J].国外医学:卫生学分册,1986(3):182–183.
