阿司匹林对B-Z化学振荡体系的影响及其分析检测
2013-10-26常珊珊张庆富
王 莉,常珊珊, 张庆富,
阿司匹林对B-Z化学振荡体系的影响及其分析检测
王 莉1,常珊珊2,*张庆富1,2
(1. 聊城市环境保护局,山东,聊城 252000;2. 聊城大学化学化工学院,山东,聊城 252059)
在连续搅拌反应器(CSTR)中,研究了阿司匹林对封闭体系中B-Z振荡反应体系的影响。研究结果表明:阿司匹林溶液浓度在5.00 × 10-6~ 5.00 × 10-1mol/L范围内,振荡反应的振幅变化值(Δ)与阿司匹林浓度()的关系符合方程:Δ34.70.154,R0.999,最低检测限达10-6mol/L。
B-Z化学振荡;阿司匹林;组分浓度;振幅变化值
化学振荡反应是指在有些自催化反应中,反应体系的某些状态量(如浓度)随时间或空间发生周期性变化的一类化学反应,它属于非线性动力学的研究范畴[1-2]。20世纪中叶,前苏联化学家Belousov与Zhabotinsky等研究发现在铈离子催化下,溴酸盐在硫酸介质中氧化柠檬酸时出现了有趣的化学振荡现象,后来被称之为B-Z振荡反应。1995年,Dolores Perez-Bendito及其合作者报道了利用微量被测物质对化学振荡体系的扰动作用进行分析测定的研究工作,为微量被测物质的分析鉴定提供了一条重要途径。其原理是微量被测物质的加入,会明显地改变一个稳定的化学振荡曲线中的振幅、周期等信号参数,且这些信号参数的变化值与加入被测物质的量具有良好的相关性,这一研究使化学振荡现象步入分析检测的实用阶段[3]。目前,化学振荡现象已被广泛用于检测一些痕量金属离子和无机阴离子 (如Hg2+[4]、Cl- [5])、有机化合物(如牛磺酸[6]、抗坏血酸[7]、苯丙氨酸[8]、维生素[9])以及气体小分子(如NO、CO[10])等。
阿司匹林(Aspirin),即乙酰水杨酸(Acetylsalicylic acid),是应用最早和最广泛的解热镇痛类药物。大量研究表明它除具有解热、镇痛、消炎、抗风湿、抗血小板聚集等作用外,还具有预防和治疗缺血性心脏病、心绞痛、心肺梗塞、脑血栓等疾病的功效,受到人们的普遍关注。目前,阿司匹林的检测方法有高效液相色谱法[11-13]、可见分光光度法[14]、毛细管电泳法[15]、荧光光谱法[16, 17]等,但以上方法所需设备复杂、成本高,难以普及推广。鉴于此,我们研究了阿司匹林对B-Z振荡反应的影响,以期建立一种简便、快速、低成本的检测阿司匹林的分析方法。

图1 阿司匹林的结构图
1 实验部分
1.1 仪器与试剂
CS501-SP型恒温水浴器(重庆四达实验仪器厂),BZOAS-ⅡS型振荡实验装置(南京大学应用物理研究所),铂电极,液接饱和甘汞电极,微量进样器。
实验所用硫酸、硫酸铈铵、丙二酸、阿司匹林均为分析纯,溴酸钾为优级纯。
1.2 实验方法
打开恒温水浴器和B-Z振荡实验装置,将0.450 mol/L丙二酸,0.250 mol/L溴酸钾,3.00 mol/L硫酸各10.0 mL依次加入到恒温夹套反应器中,待反应液搅拌均匀并恒温到303.2 K后,再将恒温后的10.0 mL 4.00 × 10-3mol/L硫酸铈铵加入,记录电位随时间变化的曲线。为保证进样点的重复性,待振荡曲线稳定后在铂电极指示电位的最低点分别加入1.00 mL不同浓度的阿司匹林溶液,观察不同浓度的阿司匹林对B-Z振荡体系的影响。
2 结果与讨论
2.1 底物组分浓度对B-Z振荡反应的影响
本实验中,B-Z振荡体系的底液由一定浓度的丙二酸、溴酸钾、硫酸和硫酸铈铵组成,各组分的浓度对该振荡反应的影响十分敏感。为了在底液中加入一定量的阿司匹林时能得到稳定而较大的振幅变化值,实验中以振幅的改变值(Δ)为依据,采取单一因素分析法,依次研究了丙二酸、溴酸钾、硫酸和硫酸铈铵的浓度对该振荡反应振幅的影响(如表1)。

表1 303.2K,不同浓度的底物组分对振荡反应振幅的影响(mol/L)

从图2可以看出,丙二酸浓度为 0.450 mol/L, 溴酸钾浓度为 0.250 mol/L, 硫酸浓度为3.00 mol/L, 硫酸铈铵浓度为 4.00 × 10-3mol/L时,所得振荡曲线的振幅变化值最大。实验结果表明:在温度为303.2 K时,阿司匹林参与的丙二酸—溴酸钾—硫酸—硫酸铈铵化学振荡体系适合在此浓度条件下进行研究。
2.2 温度对B-Z振荡反应的影响
温度是影响化学振荡反应的重要因素之一。温度过低时,振荡周期过长,单位时间内的进样次数减小,检测的效率降低;而温度过高时,振荡周期过短,则会影响检测的准确性。因此,在对阿司匹林进行分析测试时,温度的确定是非常重要的。实验结果表明,当温度为303.2 K时,阿司匹林对B-Z振荡体系的影响最大(图3),因此,选择303.2 K为检测温度。

图3 振幅变化值与温度的关系曲线图

图4 – ln(1/t诱导)对1/T的关系曲线图

图5 –ln(1/t振荡)对1/T的关系曲线图
在该振荡反应中,当丙二酸浓度为0.450 mol/L,溴酸钾浓度为0.250 mol/L,硫酸浓度为3.00 mol/L,硫酸铈铵浓度为4.00 × 10-3mol/L时,通过改变反应温度,考察温度(T)对诱导时间(诱导)和振荡周期(振荡)的影响。研究结果表明,随着温度的升高,振荡反应的诱导和振荡均减小,分别将ln(1/诱导)和ln(1/振荡)对1/进行线性拟合,可得到良好的线性关系(图4,5),其线性方程分别写作式(1)、式(2):
ln(1/诱导) =诱导+诱导(1)
ln(1/振荡) =振荡+振荡(2)
式中,诱导、振荡为常数,(KJ·mol-1·K-1)为摩尔气体常数。将上述方程与Arrhenius经验公式lnE/RT + A相比可知,在303.2 K时,该振荡反应的诱导表观活化能和振荡表观活化能分别为: 55.2 kJ/mol 和61.4 kJ/mol。
2.3 不同浓度的阿司匹林对B-Z振荡反应振幅的影响
在上述优化条件下,将不同浓度的阿司匹林加入振荡体系中,结果发现加入的阿司匹林浓度对该振荡反应的振幅有着明显的影响(表2)。
从图6可以看出,在阿司匹林浓度为5.00 × 10-6~ 5.00 × 10-1mol/L范围内,可观察到进样后Δ随浓度的增大而增大,拟合得出其方程式为:Δ= 34.70.154,2= 0.999。当阿司匹林浓度低于10-6mol/L时,由于Δ偏小,误差较大,因此其检测下限为10-6mol/L。将1.00 mL 3.00 × 10-3mol/L的阿司匹林试样加入体系中,测得Δ= 14.1 mv,其回收率为99.6%。由此可见,该测定体系不存在显著的系统误差,结果可靠。
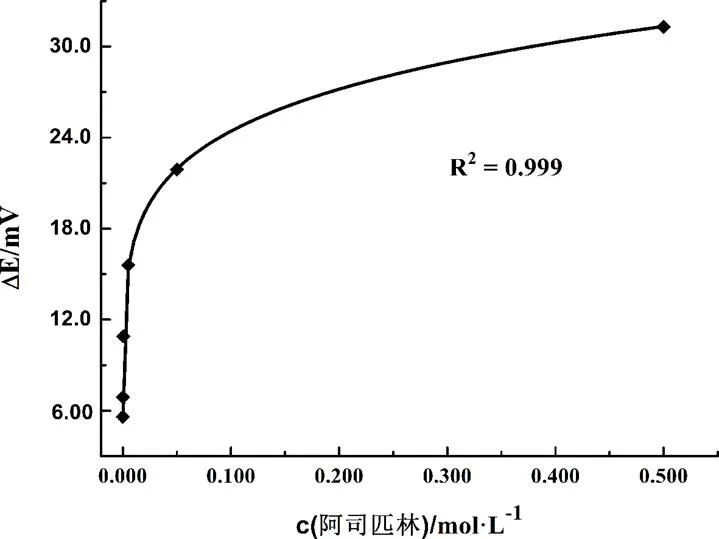
图6 振幅改变量与阿司匹林浓度的关系曲线图

表2 303.2 K,不同浓度的阿司匹林对振荡反应的影响
3 结语
以上研究结果表明:(1)阿司匹林参与B-Z化学振荡体系的最佳底物组分浓度分别为:丙二酸0.450 mol/L,硫酸3.00 mol/L,溴酸钾0.250 mol/L,硫酸铈铵4.00 × 10-3mol/L。(2)阿司匹林参与B-Z化学振荡体系的最佳反应温度为303.2 K,据Arrhenius公式得该温度下的诱导表观活化能和振荡表观活化能分别为:55.2 kJ/mol和61.4 kJ/mol。(3)阿司匹林浓度在5.00 × 10-6~ 5.00 × 10-1mol/L范围内,振幅变化值(Δ)与阿司匹林溶液浓度()的关系符合方程式:Δ= 34.70.154,2= 0.999。
本研究所建立的利用微扰技术来测定阿司匹林的方法,与高效液相色谱法、可见分光光度法、毛细管电泳法、荧光光谱法等相比,不仅同样具有快速、准确的特点,而且该方法灵敏度高,设备简单,操作方便,成本低,便于自动化,这为利用化学振荡反应建立定量检测阿司匹林的方法提供了理论依据和应用可能。同时,由于化学振荡与生物体系中的生物振荡具有相似性,可以通过分析药物对化学振荡反应的干扰,更深入地认识药物对生物系统周期现象的影响,为新药物的开发提供重要信息。
[1] 张洪林,杜敏,魏西莲.物理化学实验[M]. 青岛:中国海洋大学出版社,2009:132-135.
[2] 宗春燕,李融,薛冬. 非线性化学动力学研究进展[J]. 泰州职业技术学院学报,2011,11(4):53-56.
[3] 朱鹏,杨双双,陈昌云. 化学振荡反应及其在化学分析检测中的应用展望[J]. 化学分析计量,2012,21(3):99-103.
[4] 杨武,李铭,任杰,等. 利用硫修饰的化学振荡体系非平衡定态检测土壤中的痕量汞离子[J]. 西北师范大学学报:自然科学版,2011,47(2):55-58.
[5] 杨华,高锦章,杨武,等. 卤素对铈离子B-Z振荡反应的影响[J]. 西北师范大学学报,2003,39(3):5-48.
[6] 王莉,郝文龙,张庆富,等. 牛磺酸对B-Z化学振荡体系的影响及其分析检测[J]. 聊城大学学报:自然科学版,2012,25(1):52-56.
[7] 范文琴,王永辉. 抗坏血酸对CH2(COOH)2-BrO3-- Mn2+-H2SO4体系化学振荡反应的影响[J]. 大连交通大学学报,2009,30(3):66-70.
[8] 任杰,姬良亮,高锦章,等. 利用Cu(II)催化化学振荡体系检测饮料中的苯丙氨酸[J]. 分析测试学报,2011,30(11) :1311-1315.
[9] 王姣亮,龙立平,李旺英,等. B族维生素对B-Z振荡的扰动及其测定[J]. 化学试剂,2011, (2):138-141.
[10] Strizhak P E, Khavrus V O. Determination of gases(NO, CO, Cl2) using mixed mode regimes in the Belousov-Zhabotinsky oscillating chemical reaction [J]. Talanta,2000,51(3):935- 947.
[11] 杨云雷,宋金环. 高效液相色谱法测定复方阿司匹林片中阿司匹林的溶出度[J]. 黑龙江科技信息,2012, 17:45.
[12] 姜洪涛. HPLC法测定菊蓝抗流感片中阿司匹林的含量[J]. 中国医药导报,2010,7(12):75-76.
[13] 赵昌军. RP-HPLC法测定淀粉阿司匹林的含量[J]. 齐鲁药事,2010,29(3):152-154.
[14] 陈兴荣,董光平,赖林. 分光光度法测定阿司匹林肠溶片的含量[J]. 数理医药学杂志,2010,23(4):478-479.
[15] 刘海兴,刘凤芹,于爱民,等. 毛细管电泳法测定阿司匹林中乙酰水杨酸的含量[J].潍坊学院学报,2006, 6(4): 76-77.
[16] 魏永锋,李小花,马冬梅. 同步扫描荧光光谱法同时测定阿司匹林和水杨酸[J]. 光谱学与光谱分析,2005,25(4):588-590.
[17] 李蕾,陈江敏. 荧光分光光度法测定阿司匹林中游离水杨酸—PEG1500-OP-(NH4)2SO4-H2O双水相体系萃取分离[J]. 理化检验:化学分册,2008,44(1):58-60.
EFFECTS OF ASPIRIN ON B-Z CHEMICAL OSCILLATING SYSTEM AND ITS ANALYTICAL DETERMINATION
WANG Li1, CHANG Shan-shan,*ZHANG Qing-fu1, 2
(1. Liaocheng Environmental Protection Agency, Liaocheng, Shandong 252000, China; 2. College of Chemistry and Chemical Engineering, Liaocheng University, Liaocheng, Shandong 252059, China)
Effects of aspirin on B-Z oscillating system in closed system were investigated in a continuous-flow stirred tank reactor (CSTR). The results showed that the relationship between the amplitude changing values (Δ) of oscillating reactions and the aspirin concentration (c) was in accordance with the equation Δ34.70.154(R=0.999) in the aspirin concentration range from 5.00×10-6to 5.00×10-1mol/L, the lowest detection limit was 10-6mol/L.
B-Z chemical oscillation;aspirin; reactant concentration; amplitude changing values
O643
A
10.3969/j.issn.1674-8085.2013.01.007
1674-8085(2013)01-0031-04
2012-11-18;
2012-12-16
聊城大学博士科研启动基金项目(31805)
王莉(1980-),女,山东聊城人,工程师,硕士,主要从事环境监测分析研究工作(E-mail: wangli1980@126.com);
常珊珊(1989-),女,山东德州人,硕士生,主要从事环境和药物研究研究工作(E-mail: changshanshan@126.com);
*张庆富(1981-),男,山东临沂人,副教授,博士,硕士生导师,主要从事环境与药物研究工作(E-mail: qingfuzhang@126.com).
