化学发光法检测血清胰岛素的现状分析
2013-10-25张国军谭延国张然星车冬丽郑芳芳王晓宁
张国军 谭延国 张然星 张 岩 亢 涛 车冬丽 郑芳芳 王晓宁 李 佩
(1.首都医科大学附属北京天坛医院检验科,北京100050;2.首都医科大学附属复兴医院检验科,北京100038;3.中国中医科学院望京医院检验科,北京100102)
由于胰岛素(insulin,INS)在糖尿病等相关疾病的发生、发展、预后和诊治中的独特地位,对其血清水平的测定早已成为临床实验室的常规检测项目,并得到日益的重视。随着生物科技的发展,其检测方法也逐步由放射免疫学的检测方法,逐渐向酶联免疫吸附试验、化学发光免疫分析法发展。现阶段化学发光法已成为检测血清胰岛素水平的主流方法,并且由于自动化检测系统的普及,极大地提升了实验的精密度。但迄今为止,由于仍无胰岛素的国际参考品问世、胰岛素在体内分子形式的不均一性、检测过程中的交叉反应等因素,常导致不同检测系统间的结果的差异较大。本课题组前期研究[1]用3种化学发光系统检测血清的研究结果初步显示,不同检测系统间其水平差异非常显著。同时发现,可能存在独立于不同检测系统的通用参数。本文通过大样本、多种检测系统进行进一步的论证。
1 材料和方法
1.1 仪器和试剂
化学发光检测方法为直接化学发光免疫分析法(chemiluminescent immunoassay,CLIA)、电化学发光免疫分析法(electrochemiluminescence immunoassay,ECLIA)、微粒子化学发光免疫分析法(chemiluminescent microparticle immunoassay,CMIA)和化学发光酶免疫分析法(chemiluminescence enzyme immunoassay,CLEIA)。CLIA、ECLIA和CMI依次采用拜耳公司的ADVIA Centaur全自动分析系统、罗氏公司的Cobas e411全自动分析系统和亚培公司i-2000全自动分析系统,CLEIA采用北京源德生物医学工程公司的半自动分析系统(CLEIA-1)和北京科美公司的CHEMCLIN-6000全自动分析系统(CLEIA-2)。检测所用的定标液、质控品、试剂盒均为各检测系统的配套产品。
1.2 标本来源
临床血清标本来自首都医科大学附属北京天坛医院检验科收集的100名未使用外源性胰岛素治疗的住院患者,其中,男性50名,女性50名,所有患者均按照口服葡萄糖耐量试验(oral glucose tolerance test,OGTT)的要求于空腹、服糖后 0.5、1、2 和 3 h 分别采集3 mL静脉血,共计500份标本。离心后及时分离、分装血清,置于-80℃冰箱冻存,并于同一时间复溶后完成所有测定。
1.3 检测方法
对每个标本,分别采用上述5种检测系统测定每个患者空腹及服糖后各时间点血清INS浓度,每次测定均同时测定室内质控品进行质量监测。所有测定均在实验室可控范围内,并严格按试剂盒的说明进行。血清INS的浓度单位为mIU/L。
1.4 统计学方法
使用SPSS 19.0统计学软件对数据进行处理分析,以OGTT中空腹和服糖后各时间点血清INS绝对值、服糖后各时间点INS浓度分别与其各自空腹浓度的比值为观察指标,不同检测系统INS水平分组并进行两两比较。非正态分布的配对数据,多组间总体比较用Friedman检验,两两比较做Wilcoxon配对秩和检验,相关分析用Spearman相关分析,并进行回归与曲线估计,以P<0.05为差异有统计学意义。
2 结果
2.1 不同系统检测血清INS结果现状分析
2.1.1 不同检测系统间血清胰岛素水平的差异性分析
经正态性检验,所有指标均不符合正态性分布(P均为0.000)。各种检测系统所测定的血清INS水平以四分位数M(P25,P75)描述。
经Friedman秩和检验分时段比较显示,整体上5种不同的检测系统间在不同的时间点,血清胰岛素水平差异均有统计学意义(P均为0.000),详见表1。
2.1.2 不同检测系统间血清胰岛素水平及“比值”的关系
经Spearman秩相关分析,任意两个检测系统间血清INS水平都存在非常显著的相关关系(P均为0.000)。经回归及曲线估计,除CLEIA2外,任意两种检测系统间均符合直线相关关系(P均为0.000)。而由CLEIA2测得的INS水平与其他任意一种检测系统的拟合曲线均更为显著地符合二次方程关系(P均为0.000)。
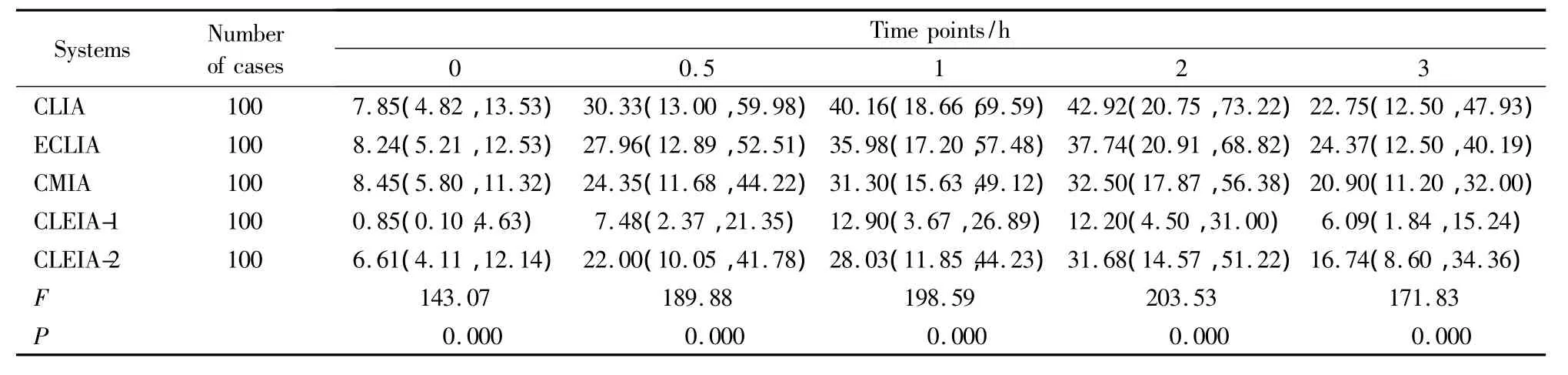
表1 5种不同检测系统血清胰岛素水平统计描述及差异性分析Tab.1 Statistical description of serum insulin level and difference among 5 systems
对每位患者OGTT服糖后各时间点INS水平分别与其自身空腹水平的“比值”,在不同检测系统间行Spearman秩相关分析。结果显示,任意两个检测系统间,都存在显著的相关关系(P均为0.000)。经回归及曲线估计显示,任意两个检测系统“比值”的拟合曲线更符合二次方程关系(二次方程的R2比一次方程的值更高,且P均为0.000)。同使用INS直接回归相比,除检测系统CLEIA1分别与其他各检测系统的散点图更加发散外(R2分别为0.443,0.553,0.591,0.599),其余各检测系统间“比值”的散点图则更为集中(R2有不同程度的增高)。
2.2 不同检测系统间血清胰岛素水平(Ins)及“比值”(Ins-R)的分时段两两比较
2.2.1 不同检测系统间分时间点比较,“比值”间的统计学描述和整体上的差异性分析
如表2所示,各种检测系统所测定的血清INS“比值”以M(P25,P75)方式描述。经Friedman秩和检验显示,分别对不同的时间点而言,整体上5种不同的检测系统间血清胰岛素“比值”差异均有统计学意义(P=0.000),详见表2。
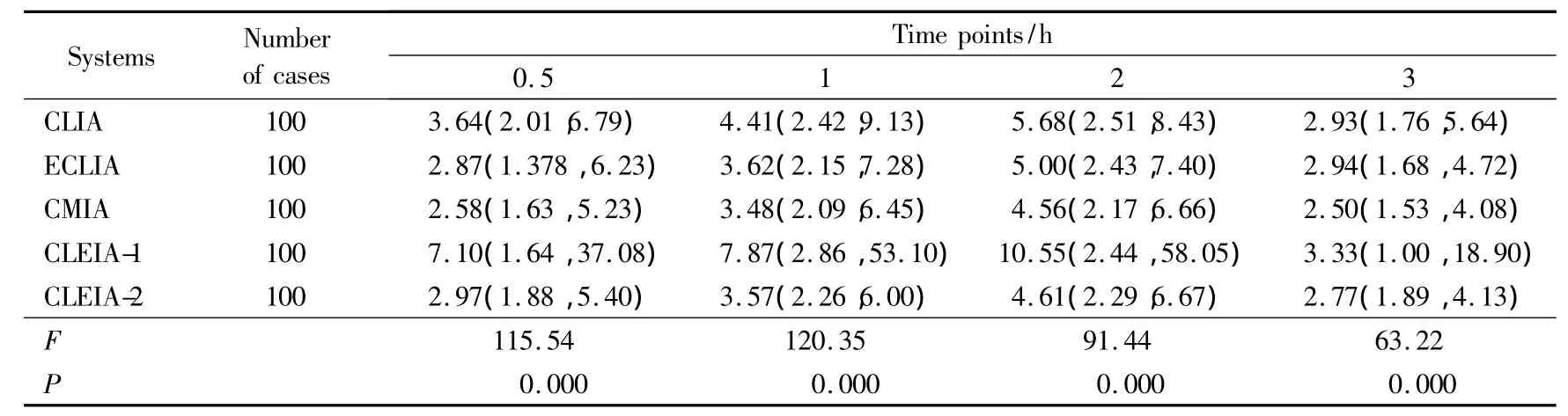
表2 5种不同检测系统血清胰岛素“比值”的统计描述及整体上差异性分析Tab.2 Statistical description of serum insulin ratio and difference among 5 systems
2.2.2 不同检测系统间分时间点两两比较,“比值”间相关性和差异性
对100例患者而言,每位患者服糖前后均抽取5次标本,分别对每个抽血时间点的血清INS水平以及“比值”进行两个检测系统间的相关性分析和差异性比较(Wilcoxon配对秩和检验)。
结果显示,无论对每个时间点的INS水平还是“比值”,任意两个检测系统间均存在非常显著的相关关系(P均为0.000)。
对于INS水平而言,在空腹时,ECLIA同 CLIA、CMIA同CLIA两组检测系统间差异无统计学意义(P=0.562和0.935)。对餐后3 h而言,ECLIA同CLIA两个检测系统间差异无统计学意义(P=0.440)。其他各时间点,任意两个检测系统间差异均有统计学意义(P<0.01)。
对于“比值”而言,CLEIA2同ECLIA间餐后0.5 h比较,差异无统计学意义;CLEIA2同CMIA两个检测系统间餐后1.0、2.0和3.0 h差异均无统计学意义(P>0.05)。而其余各时间点,任意两个检测系统间差异均有统计学意义(P均<0.05),详见表3。
3 讨论
鉴于胰岛素和C-肽在反映有关胰腺β细胞相关疾病方面的独特价值,已成为临床常规检测的实验项目。但迄今在临床普及和使用过的检测方法,从经典的放射免疫分析技术、酶免疫分析技术、到如今广泛应用的各种类型的化学发光免疫分析技术,都基于免疫学原理。由于INS和C-P在体内分子形式的不均一性、交叉反应以及无统一的国际参考品[2],导致不同检测系统间测定结果客观上存在较大差异性的事实,这限制了临床资料的可比性,以及根据测定结果进行的临床实践活动。所以积极去发现不同检测系统间存在的内在规律,是临床工作的迫切需求。
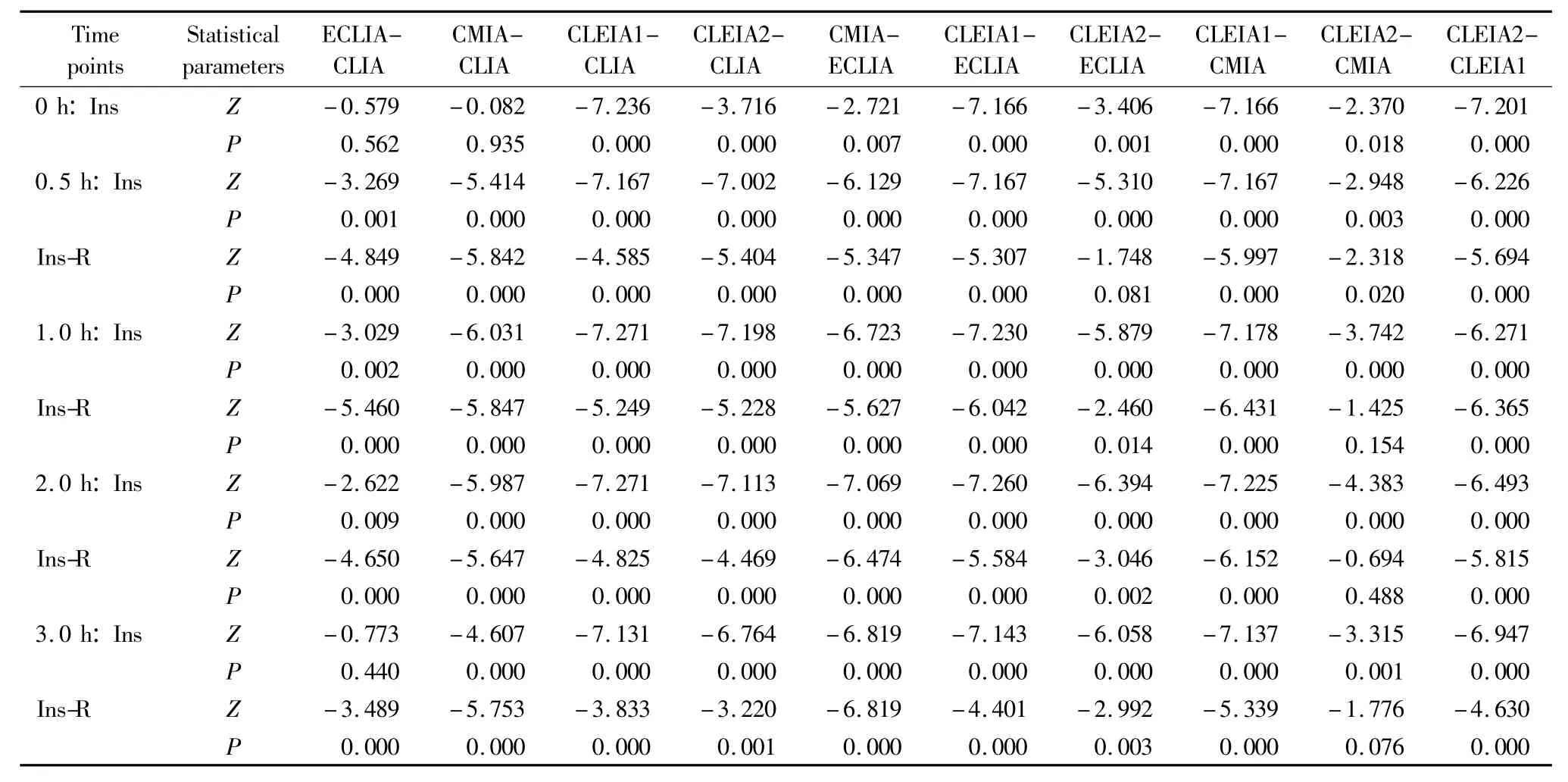
表3 不同检测系统间胰岛素水平(Ins)及“比值”(Ins-R)的分时段比较Tab.3 Comparison of insulin(Ins)and“ratios”(Ins-R)in temporal manner
血清胰岛素水平在各检测系统间存在着较大的差异,由本研究的回归方程显示,其他检测系统测定值基本是CLEIA1的1.5~2.0倍。而其他检测系统间也相差百分之几到百分之三十左右。既然如此,是否各种检测系统得到的胰岛素测定值就完全不同通用了呢?本研究结果显示,在空腹水平时,ECLIA同 CLIA、CMIA同CLIA 2组检测系统间可以认为是通用的。对餐后3 h而言,ECLIA同CLIA 2个检测系统间可以认为是互通的。其他各时间点,任意两个检测系统间则完全不能互通。基于以上事实,我们可以得出结论,即有些检测系统间对于较低浓度的胰岛素测定值还是可以通用的。而随着胰岛素水平的增高,不同检测系统间的差异性得到了放大,以至于2种检测系统间的测定数据完全不能通用和替代。
由于临床上常将某患者服糖后测定的胰岛素水平与空腹水平进行比较,以此判定胰腺的功能。为此,我们将某位患者服糖后的胰岛素水平与其空腹水平相比,得到一个“比值”,看不同检测系统间此校正后的参数是否可以通用。先前的小样本研究[1]显示,该参数可能是较为有前途的。为此,我们进行了此次大样本的研究。本研究显示,对于“比值”而言,检测系统CLEIA2同ECLIA间餐后0.5 h比较,差异无统计学意义;CLEIA2同CMIA 2个检测系统间餐后1.0、2.0和3.0 h比较,差异无统计学意义。而其余各时间点,任意2个检测系统间差异均有统计学意义。由此本研究得出结论,即“比值”也不是放之四海皆准的通用参数,而也是与特定的检测系统、特定的时间点相关联。
虽然各种检测系统的血清胰岛素的测定水平并不是完全等同的,但其无论是绝对值还是“比值”,从整体上还是分时段分析上,任意2种检测系统间均存在高度的相关性(P均为0.000)。整体上,对胰岛素的绝对水平在任意2个检测系统间的回归分析显示,R2由0.690~0.957。这说明5种系统在检测临床标本时,其测定结果能够较为一致地反映血清胰岛素在OGTT中的变化趋势及峰值出现的时间。相关性最好的2个检测系统是ECLIA和CMIA,R2达到0.957。也就是说,其结果的相互转换基本上可以按照回归方程进行换算。
本研究发现了一个较为奇特的现象,即血清胰岛素水平在不同的检测系统间,其符合的数学模型可能是不同的。对于CLEIA2以外的4个检测系统,任意2个之间均较好的符合直线相关关系。而CLEIA2则与其他任意一个检测系统更为符合二次方程曲线数学模型。这在以往的文献中很少见到。这个发现对我们比较两种检测系统的测定结果具有一定的指导意义。
同使用胰岛素绝对值直接回归所得到的曲线相比,对“比值”的研究显示,CLEIA1分别与其他各检测系统的散点图更加发散外,其余各检测系统间“比值”的散点图则更为集中(R2有不同程度的增高)。而且所有检测系统间的比值均呈现二次方程的数学模型关系。从此可以看出,虽然“比值”并非存在于各个检测系统间的完全通用的参数,但至少是比绝对值更好的、可用于不同检测系统间进行更有效比较的参数。
为了解决不同检测系统间或临床实验室的测定结果间存在的客观的、显著的差异,建立和完善检测血清胰岛素、C-肽的标准化参考系统,是解决问题的关键。这在国外的相关研究[3-7]中也引起了高度关注,并且已经取得了一定的成果[8-10]。我们期待着成熟的国际标准品问世,并能够应用于临床实践。
[1]张燃星,刘健彬,谭延国.几种化学发光法检测系统测定血清胰岛素的临床效果评价[J].中华临床医师杂志:电子版,2010,4(11):2218-2221.
[2]Sapin R.Insulin assays:previously known and new analytical features[J].Clin Lab,2003,49(3-4):113-121.
[3]Marcovina S,Bowsher R R,Miller W G,et al.Standardization of insulin immunoassays:report of the American Diabetes Association work group[J].Clin Chem,2007,53(4):711-716.
[4]Manley S E,Stratton I M,Clark P M,et al.Comparison of 11 human insulin assays:implications for clinical investigation and research[J].Clin Chem,2007,53(5):922-932.
[5]Wiedmeyer H M,Polonsky K S,Myers G L,et al.International comparison of c-peptide measurements[J].Clin Chem,2007,53(4):784-787.
[6]Little R R,Rohlfing C L,Tennill A L,et al.Standardization of C-Peptide measurements[J].Clin Chem,2008,54(6):1023-1026.
[7]Miller W G,Thienpont L M,Van Uytfanghe K,et al.Toward standardization of insulin immunoassays[J].Clin Chem,2009,55(5):1011-1018.
[8]Cabaleiro D R,Stöckl D,Kaufman J M,et al.Feasibility of standardization of serum C-peptide immunoassays with isotope-dilution liquid chromatography-tandem mass spectrometry[J].Clin Chem,2006,52(6):1193-1196.
[9]Cabaleiro D R,Uytfanghe K V,Stove V,et al.Pilot Study for the Standardization of insulin immunoassays with isotope dilution-liquid chromatography/tandem massspectrometry[J].Clin Chem,2007,53(8):1462-1469.
[10]崔常清.胰岛素抵抗的机制与临床研究进展[J].中国煤炭工业医学杂志,2012,15(7):1119-1121.
