SPE-HPLC 联用测定减肥食品中盐酸芬氟拉明
2013-10-21申书昌
贾 波,申书昌
(1.齐齐哈尔大学 分析测试中心,黑龙江 齐齐哈尔 161006;2.齐齐哈尔市质量监督检验所,黑龙江 齐齐哈尔 161005)
食品安全分析检测样品的复杂性、分析介质的多样性及超低含量的待测物质量浓度等因素,对于分析化学样品处理技术不断提出更高的要求[1].被分析目标化合物的提纯、分离、净化和浓缩等样品前处理过程,不仅能够去除干扰物,而且能够提高检测灵敏度和分析结果的准确可靠性.针对不同的检测项目,分析工作者发展了行之有效的样品前处理技术.固相萃取(SPE)是20世纪70年代发展起来的一种样品前处理技术[2-3],在食品安全分析检测样品前处理中得到了较多的应用[4-5].SPE 是萃取柱内固定相对目标化合物的吸附、解吸附/洗脱的过程,合理使用萃取材料尤为重要.目前,商品化的固相萃取柱有十几种,其性质和应用范围有所不同.在我国,尽管有些分析方法中规定了使用SPE 样品处理技术,但由于固相萃取柱主要来源于进口商品,价格较贵,一次性使用,不同型号产品不可替换等原因,使得这项工作的开展落后于国外一些分析检测行业.在商品化的固相萃取填料中,硅胶基质填料化学稳定性差,不能在强酸和碱性溶液中使用,聚合物基质填料吸附容量大,pH 适用范围广,但机械强度差.因此自行研制开发无机/高分子聚合物复合固相萃取填料具有十分重要的价值和意义[6].
盐酸芬氟拉明为苯丙胺类药物,是一种抑制食欲型减肥药,可对人体神经系统造成损伤,口服盐酸芬氟拉明可导致急性肾衰.我国卫生部禁止在保健品中添加盐酸芬氟拉明.目前所报道的盐酸芬氟拉明的检测主要是高效液相色谱法、质联法及其联用法[7-9],而固相萃取用于样品中盐酸芬氟拉明的测定尚未见报道.
苯乙烯-甲基丙烯酸共聚物[10]具有优良的耐热性、耐热水性、耐化学性和透明性,由于结构中的苯环和羧基,使其具有良好的亲脂性和阳离子交换特性.本文制备了苯乙烯/甲基丙烯酸-二氧化钛纳米复合材料[11]固相萃取柱,使用该柱对减肥饼干和减肥咖啡中盐酸芬氟拉明进行提取,用洗脱液洗脱后,用液相色谱检测,使用单因素分析法对柱温,流速,流动相配比等色谱条件进行优化.
1 实验部分
1.1 实验材料与仪器
1100 高效液相色谱仪(美国安捷伦公司),MTN-20800D 氮吹仪(天津奥特赛恩斯仪器有限公司),AS20500AT 超声清洗震荡器(天津奥特赛恩斯仪器有限公司),旋涡振荡器、TGL-16M 离心机(湘仪离心机仪器有限公司),MODEL 固相萃取仪(天津奥特赛恩斯仪器有限公司).
盐酸芬氟拉明对照品(质量分数≥98.0%,中国药品生物制品检定所),甲醇(色谱纯,天津市科密欧化学试剂有限公司),无水乙醇(分析纯,天津市兴复发展有限公司)、乙腈(色谱纯,天津市科密欧化学试剂有限公司),乙酸钠(分析纯,哈尔滨化工化学试剂厂)、钛酸四丁酯(分析纯,天津市光复精细化工研究所),甲基丙烯酸(分析纯,天津市大茂化学试剂厂),苯乙烯(分析纯,天津市大茂化学试剂厂).实验用水均为超纯水
1.2 固相萃取柱的制备及样品分析
1.2.1 苯乙烯/甲基丙烯酸-二氧化钛复合材料固相萃取柱的制备
在250 mL 圆底烧瓶中加入100 mL 水、25 mL无水乙醇和0.5 mL 甲基丙烯酸,用75 %的HNO3调节体系的pH值为1~2 之间,加入15 mL,5%钛酸四丁酯乙醇溶液,55 ℃下搅拌反应2 h,然后加入5 mL 苯乙烯,在N2保护下充分搅拌后,加入20 mL 水溶液,于80℃恒温反应8 h,用砂芯漏斗过滤除去不溶物,之后破乳、过滤、洗涤、在室温下真空干燥得粉末样品.
取一支2.5mL 医用塑料注射器管,下端安装一层玻璃棉,称取0.3 g 二氧化硅/聚苯乙烯材料填至塑料注射器管中,适度加压后再加一层玻璃棉,制成固相萃取小柱.
1.2.2 色谱分析条件
色谱柱为XDB-C18(150 mm× 4.6 mm i.d.,5 μm);柱温为室温;检测波长为263 nm;流动相为甲醇/乙腈+乙酸钠水溶液(乙腈和乙酸钠(0.02 mol/L)的配比为1∶1),流速为1.0 mL/min;进样量为20 μL.
1.2.3 标准曲线的制作
取盐酸芬弗拉明用甲醇配置成质量浓度为0.1、0.2、0.3、0.4、0.5、0.6 mg/mL 标准系列,用HPLC 测定系列标准溶液的峰面积,按峰面积对标准系列的质量浓度作图绘制标准曲线.
1.2.4 样品分析
用2 mL 甲醇润湿活化苯乙烯/甲基丙烯酸-二氧化钛固相萃取小柱,再用5 mL 去离子水淋洗固相萃取柱.称取1 g 样品于锥形瓶中,用30 mL去离子水分3 次提取,提取温度为50 ℃,超声时间20 min,合并提取液,离心10 min,上层清液过固相萃取柱,流速为5 mL/min,真空抽干水分.用5 mL甲醇洗脱SPE 柱,收集洗脱液,用氮气吹脱浓缩至1 mL,用0.45 μm 的滤膜过滤后,用高效液相色谱进行检测.
2 结果与讨论
2.1 色谱条件的选择
2.1.1 温度对盐酸芬氟拉明保留时间及峰面积的影响
盐酸芬氟拉明的质量浓度为0.3 mg/mL,流速为1.0 mL/min,流动相为甲醇∶乙腈+乙酸钠溶液(75∶25).随着柱温的升高盐酸芬氟拉明的保留时间有所减小,而峰面积稍有增加,因此选择在室温下工作,见表1.

表1 柱温对保留时间及峰面积的影响
2.1.2 流动相配比对盐酸芬氟拉明保留时间及峰面积的影响
盐酸芬氟拉明的质量浓度为0.3 mg/mL,柱温为室温,流动相流速为1.0 mL/min.随着甲醇比例的增加盐酸芬氟拉明的峰面积显著增加,而保留时间有所减小,配比为85∶15 时其峰面积最大值,保留时间达到最小值,并趋于不变,见表2.
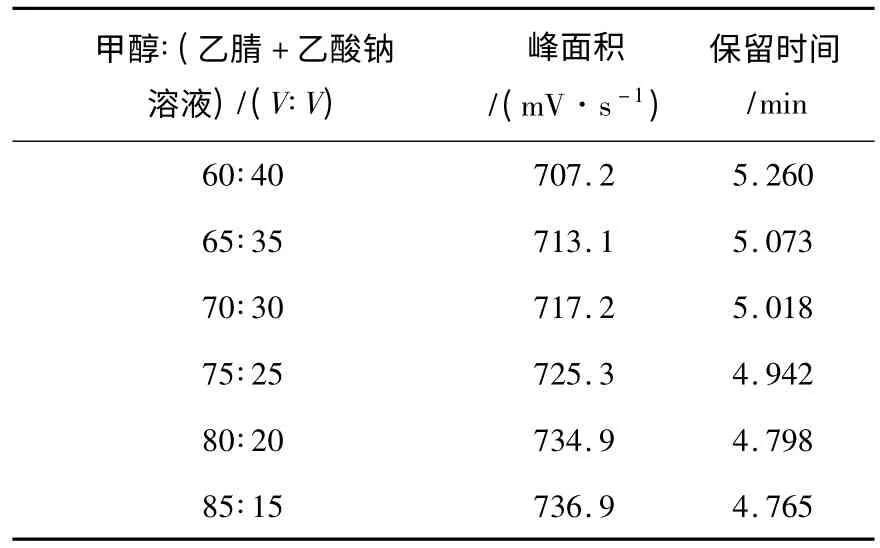
表2 流动相配比对保留时间及峰面积的影响
2.1.3 流动相流速对盐酸芬氟拉明保留时间及峰面积的影响
盐酸芬氟拉明的质量浓度为0.3 mg/mL,柱温为20 ℃,流动相为甲醇∶乙腈+乙酸钠溶液(75∶25).随着流动相流速的减小盐酸芬氟拉明的峰面积显著增加,保留时间也显著增加.这是由于流速的减小使溶质的纵向扩散加大,使谱峰出现区域现象和托尾情况,导致积分面积增大.因此要严格控制流速,本实验确定流速为1.0 mL/min,见表3.
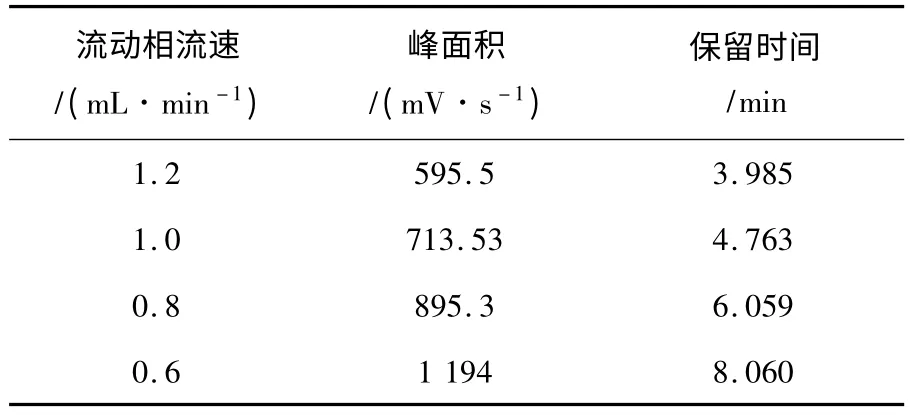
表3 流动相流速对保留时间及峰面积的影响
盐酸芬氟拉明液相色谱图见图1.

图1 盐酸芬氟拉明HPLC 图
2.2 标准曲线及最低检出限
在0.1~0.6 mg/mL 范围内,盐酸芬氟拉明的色谱分面积与质量浓度的线性回归方程为y=2 345x-31.856,相关系数为R2=0.999 6,见图2.根据色谱图基线噪声值的3 倍对应的质量浓度为仪器最低检出限,最低检出限分别为0.034 mg/mL.

图2 盐酸芬氟拉明标准曲线
2.3 样品测定结果
市售减肥胶囊盐酸芬弗拉明质量比为0.073 mg/g,加标回收率为87.6%;减肥咖啡未检出,加标回收率为92.8%.
3 结语
使用自制苯乙烯/甲基丙烯酸-二氧化钛复合材料固相萃取柱对盐酸芬氟拉明吸附能力强,杂质去除效果好.SPE/HPLC 测定减肥食品中盐酸芬氟拉明方法简便,结果准确.
[1]刘 艳,贾 丽,张经华,等.食品安全检测中样品前处理技术研究进展[J].现代仪器,2010(3):6-8.
[2]张海霞,朱彭龄.固相萃取[J].分析化学,2000,28(9):1172-1180.
[3]WIR-FERENC A,BIZIUK M.Solid Phase Extraction Technique-Trends,Opportunities and Applications[J].Polish Journal of Environmental Studies,2006,15 (5):677-690.
[4]胡国栋.固相萃取技术的进展及在食品分析中的应用的现状[J].色谱,2009,27(1):1-8.
[5]邸玉敏,朱 军,常 靖,等.固相萃取技术(SPE)在苯丙胺类毒品分析中的应用[J].中国法医学杂志,2010,25(2):105-108.
[6]宋文清.新型固相萃取填料的制备、评价及应用研究[D].天津:天津大学,2009:11-24.
[7]谭小秋,高燕红.高效液相色谱法测定减肥食品中的盐酸芬氟拉明含量[J].中华预防医学杂志,2001,35(2):124-125.
[8]李美芳,邱颖姮,庞学斌,等.串联四极杆质谱法测定减肥类药品及保健品中非法掺入盐酸芬氟拉明的研究[J].中国药师,2006,9(8):721-722.
[9]郭俊峰,杨冀州,李淑娟.液相色谱-质谱/质谱法快速测定保健品中违禁成分麻黄碱、伪麻黄碱和盐酸芬氟拉明[J].中国国境卫生检疫杂志,2008,31(6):415-417.
[11]王耀先,赵玉庭.苯乙烯甲基丙烯酸共聚物的合成结构与性能研究[J].华东理工大学学报,1995,21(6):702-707.
[12]江贵长,官文超,郑启新.苯乙烯/甲基丙烯酸-二氧化钛纳米微球的性能[J].华中科技大学学报,2003,31(11):99-100.
