镍基Claus尾气加氢还原催化剂水中毒及其机理研究
2013-10-09雷家珩汪海林杜小弟
熊 鑫,雷家珩,陈 凯,汪海林,杜小弟
(武汉理工大学化学系,湖北 武汉 430070)
工业Claus尾气排空前需进一步进行加氢还原处理,由于相关设备的投资和操作成本都较高,近年来研究和开发Claus尾气低温加氢还原催化剂受到学界和产业界的普遍重视[1-2]。
在目前已知的过渡金属硫化物催化剂中,Ni的硫化物催化剂具有最高的活性,其催化转化SO2为H2S的反应温度为190℃[3-4]。但镍基催化剂耐水性差:Etienne Laurent等[5]发现硫化态NiMo/γ-Al2O3在选择性加氢过程中水存在严重水中毒,一方面是水引起γ-Al2O3载体结晶生成一水软铝石相,另一方面水导致活性组分Ni生成无活性的硫酸镍。方伟[6]发现 NiX/γ-Al2O3在选择性加氢还原过程中也存在水中毒现象,并推测其原因是水分子覆盖催化剂表面加氢活性中心。在工业生产中,由于Claus尾气含有近30%的水蒸气而限制了其应用。笔者研究了Ni/Al2O3催化剂在Claus尾气加氢还原过程中的水中毒现象及其机理,为解决镍基Claus尾气催化剂的实用化问题提供了重要的理论依据。
1 实验部分
1.1 原料和仪器
γ-Al2O3球,工业级,淄博骏合环保材料有限公司;Ni(NO3)2·6H2O,分析纯,国药集团化学试剂有限公司。
GC102M型气相色谱仪(TCD检测器,TDX-301色谱柱(2m×3mm)),上海精密科学仪器厂;D/MAX-RB型X射线衍射仪(XRD),日本理学公司;VG.ESCALAB MK-II能谱仪(XPS),英国Vaccum Generator;TriStar 3000全自动比表面及孔隙度分析仪(BET),美国麦克仪器公司;HITACHI S-4700型扫描电镜(SEM),日本日立公司。
1.2 催化剂试样的制备
载体为40~60目的工业γ-Al2O3,堆密度0.74g/mL,孔容0.43mL/g。以质量分数为21%的Ni(NO3)2溶液等体积浸渍载体,60℃恒温浸渍4h,120℃干燥10h后,在450℃焙烧6 h。将上述制备的镍基催化剂置于自制固定床反应器[7](长60cm,内径8mm)中,催化剂装填量为1.0mL。以50mL/min的流速通入混合气(V(H2S)∶V(H2)∶V(N2)=6.5∶60.0∶33.5)400℃预硫化4h即得具有催化活性的硫化物催化剂。
1.3 催化剂活性及结构测试
Ni/Al2O3催化剂试样对SO2加氢还原为H2S的活性评价采用与预硫化相同的反应器,评价用模拟气组成为V(SO2)∶V(H2)∶V(N2)=0.40∶2.4∶97.2,空速2000h-1。模拟气体中水蒸气的引入采用恒流泵直接向加氢还原反应装置中注射蒸馏水汽化的方法。
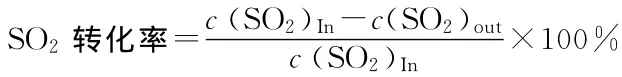
其中c(SO2)In和c(SO2)out分别为反应器入口和出口处SO2浓度,均通过气相测谱法测定。
采用XRD进行催化剂物相分析,测试条件为Cu Kα辐射,功率3kW,步宽0.020°。催化剂表面元素形态分析采用XPS,测试条件为Mg Kα射线源,阳极电压1253eV,真空度为2.7×10-6Pa,以污染碳的C1s电子结合能(284.6eV)校准荷电效应。采用BET进行催化剂孔结构分析。采用SEM进行催化剂表面形貌分析。
2 结果与讨论
2.1 水蒸气对Ni/Al2O3催化活性的影响
实验测得工业Claus尾气含水量对Ni/Al2O3催化剂加氢还原性能的影响见图1。由图1可见:在190℃无水条件下,Ni/Al2O3对Claus尾气模拟气体中SO2还原为H2S的转化率接近100%。当反应体系分别通入10%~30%的水蒸气后,SO2的转化率出现不同程度的下降。其中反应体系含30%水蒸气时SO2的转化率下降最低至73%。进一步的实验表明,当体系停止加入水蒸气后,SO2的转化率又逐渐恢复至97%左右。由此说明Ni/Al2O3遇水后会发生中毒现象,但这种中毒是可逆的。
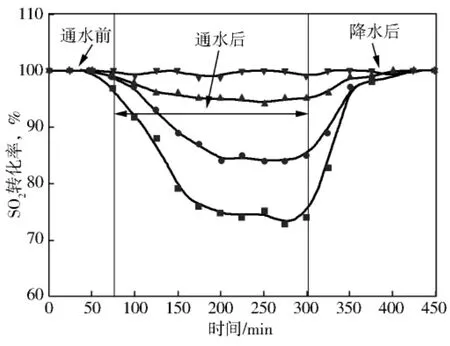
图1 Claus尾气中水蒸气对Ni/Al2O3催化活性影响
2.2 水与SO2和Ni/Al2O3的相互作用
图2为体系通水前后Ni/Al2O3催化剂的XRD谱。由图2(a)中可以看出:通水前 Ni/Al2O3催化剂的物相组成为NiS2和Al2O3;但体系通入30%水蒸气后(图2(b)),Ni/Al2O3催化剂的XRD谱图在2θ角为20.3°和22.6°处各出现一个小尖峰,表明有NiSO3(H2O)6的存在;当体系撤除水蒸气后,NiSO3(H2O)6物相消失(图2(c)),Ni/Al2O3催化剂的物相又恢复为无水情况下的NiS2和Al2O3。即水蒸气存在时H2O与SO2及NiS2生成亚硫酸盐物种,从而降低了Ni/Al2O3的催化活性。
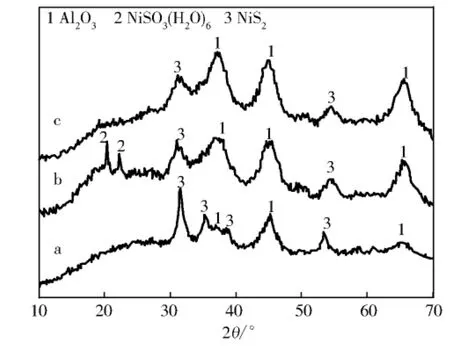
图2 Ni/Al2O3催化剂通水前后的X射线衍射图:
图3为Ni/Al2O3催化剂加30%水蒸气反应后S(2p)XPS谱。
XPS分析表明:体系加水前Ni/Al2O3中元素S的S(2p)只有一种环境——结合能为163eV的,加30%水蒸气反应后其存在环境变为两种——结合能为163eV的和结合能为169.3 eV的,且的信号很强,表明在含水条件下NiS2催化还原SO2仍按硫空位的氧化还原机理进行,只不过水的存在使SO2与催化剂活性组分部分生成镍的亚硫酸盐。
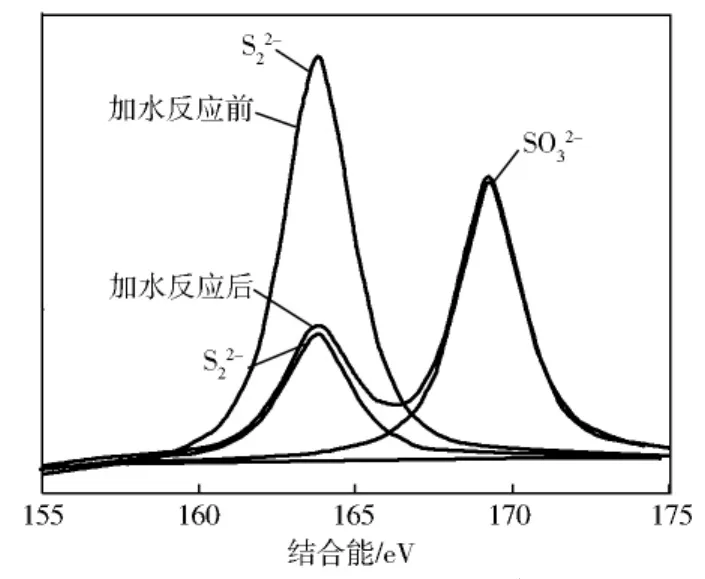
图3 Ni/Al2O3催化剂加30%水蒸气反应前后S(2p)XPS谱图
2.3 水对Ni/Al2O3表面微孔结构的影响
Ni/Al2O3催化剂试样加水前后的BET分析结果见图4。
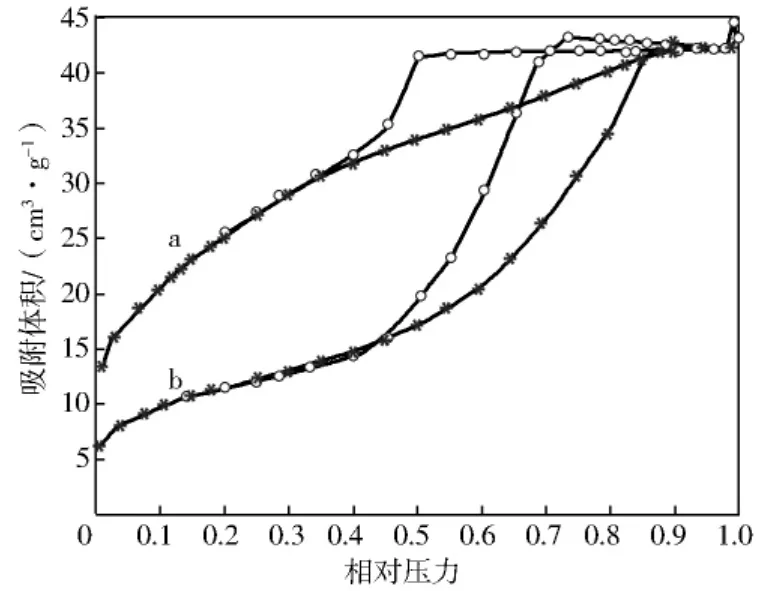
图4 加水反应前后Ni/Al2O3催化剂氮气等温吸附-脱附曲线:
从图4可以看出:加水前后该催化剂都属于IUPAC分类中的IV型等温线[8,9],属中孔分布。所不同的是两者的滞后环相差较大:图4(a)属H2型滞后环,该滞留回环(abcd)比较宽大,而且脱附曲线远比吸附曲线坡度大,说明吸附质脱附时蒸发压力与其饱和蒸汽压差异大,由Kelvin公式可知此时该催化剂试样具有较宽的孔径[8];图4(b)属H1型滞后环,滞留回环相对较狭窄,吸附曲线与脱附曲线相似程度变大,说明吸附质脱附时蒸发压力与其饱和蒸汽压差异小,孔径相对也较为狭窄[8]。且催化剂加水反应前比表面积为92.0274m2/g,单点孔体积为0.0665m3/g,平均孔径为2.8912nm;加水反应后比表面积下降为40.7664m2/g,单点孔体积有所增大,为0.0728m3/g,平均孔径增大到7.1385nm。上述情况表明,体系通入水蒸气后,水蒸气与SO2在催化剂表面生成亚硫酸盐,导致微孔部分堵塞(比较面积下降、平均孔径增大),减弱了其对反应气体的吸附,催化剂出现部分失活。
图5为Ni/Al2O3催化剂在反应体系加水前后不同时间的SEM。从图5(a)可以看出:加水前,催化剂呈现比较好的分散状态,活性组分以小颗粒形态均匀分布,且晶粒较为完整、晶界清晰,因此在较低温度下即对SO2表现出较高的催化加氢反应活性。当加水反应1h后,催化剂表面产生明显沉积物,表面形貌显著改变(图5(b)),说明催化剂表面出现异相,与亚硫酸盐的形成相对应。催化剂加水反应时间增加后(图5(c)、(d)、(e)),表面变化更加明显,沉积层呈现毛绒状,晶粒界面变模糊,说明亚硫酸盐结晶度提高,与XRD测试结果相一致(图2)。反应体系除去水后6h,催化剂的表面形貌基本恢复到加水前的颗粒状(图5(f)),但活性组分发生了一定程度的聚集,晶粒略有增大,晶型也不如加水前规整,从而导致其活性不能完全恢复。

图5 Ni/Al2O3催化剂加水反应前后的SEM
3 结 论
在工业Claus尾气加氢还原过程中,Ni/Al2O3遇水会出现中毒现象。其原因是Ni/Al2O3催化剂表面的活性物质在反应温度150~210℃会与H2O和SO2反应生成亚硫酸镍,覆盖在催化剂表面,从而显著降低了Ni/Al2O3的催化活性。Ni/Al2O3水中毒现象是可逆的。若停止向催化加氢还原反应体系中加水,亚硫酸镍将分解还原为NiS2,Ni/Al2O3的催化活性将得到恢复。
[1]Setphen N,Massie C E W.Catalysts for lower temperature tail gas unit operation[J].Brimstone Sulfur Recovery Symposium,2005:13-16.
[2]Elsner M P,Mliller C.The Claus process:teaching an old dog new tricks[J].Catalysis Today,2003:79-80.
[3]Chen C L,Wang C H,Weng H S.Supported transitionmetal oxide catalysts for reduction of sulfur dioxide with hydrogen to elemental sulfur[J].Chemosphere,2004(56):425-431.
[4]雷家珩,方伟,郭丽萍,等.过渡金属硫化物对Claus尾气催化加氢制备硫化氢的影响[J].现代化工,2007,6(6):39-41.
[5]Etienne Laurent,Bernard Delmon.Influence of water in the deactivation of a sulfided NiMo/γ-Al2O3catalyst during hydrodeoxygenation[J].Journal of Catalysis,1994,146(1):281-285,288-291.
[6]方伟.新型低温Claus尾气加氢还原催化剂的研究[D].武汉:武汉理工大学,2007.
[7]雷家珩,钱菁,郭丽萍,等.一种克劳斯尾气加氢脱硫催化剂快速评价的反应系统:中国,101327417[P].2008-12-24.
[8]Sing K S W,Everett D H,Haul R A W,et al.Reporting physisorption data for gas/solid systems with special reference to the determination of surface area and porosity[J].Pure & Appl Chem,1982,54(11):2201-2218.
[9]Khalili N R,Minzi Pan,Giselle Sandi.Determination of fractal dimensions of solid carbons from gas and liquid phase adsorption isotherms[J].Carbon,2000,38(4):573-588.
