基于硫酸介质的乙二醛常压氧气氧化制备尿囊素
2013-10-09王晓冰郭瓦力邓信忠
王晓冰,郭瓦力,李 萍,邓信忠,戴 玺,朱 虹,李 磊,单 译
(沈阳化工大学化学工程学院,辽宁 沈阳 110142)
尿囊素是一种重要的精细化工产物和尿素深加工产物,广泛应用于医药、农业和轻化工等领域。尿囊素虽然广泛存在于自然界中,但因其含量少,提取工艺复杂,所以一般由化学方法合成。尿囊素的工业生产方法主要有乙二醛硝酸氧化法和草酸电解还原法,前者污染环境、设备腐蚀严重、产物纯度低;后者能耗和设备投资大、电解时间长、生产成本较高[1-3]。乙二醛氧气氧化法以氧气为氧化剂,应用前景良好[4-5],由于氧气价廉、资源丰富,同时对环境友好、反应条件温和、后处理容易、操作简单反应平稳,近年来引人关注。
乙二醛氧化法制备尿囊素共分为两个阶段:乙二醛氧化生成乙醛酸,乙醛酸与尿素缩合环化生成尿囊素[6],其中乙醛酸的合成条件是该工艺的关键。笔者以氧气为氧化剂,硫酸和氯化铝为酸性介质,亚硝酸钠为催化剂,常压下制得乙醛酸,并在无需另加酸性催化剂的条件下完成缩合,开发了氧化产物与尿素反应直接制得尿囊素的工艺路线,产物纯度高、成本低、节能、对设备要求不高,工业化难度小。
1 实验部分
1.1 主要药品及仪器
40%乙二醛溶液、六水氯化铝,分析纯,国药集团化学试剂有限公司;亚硝酸钠、尿素,分析纯,天津市大茂化学试剂厂。
氧化反应装置,自制;WM-2H型无油气体压缩机,天津市医疗器械二厂;UV2600紫外可见分光光度计,TECHCOMP;X-4数字显示显微熔点测试仪,北京泰克仪器有限公司;NEXUS 470傅里叶变换红外光谱仪,美国THERMO NICOLET公司。
1.2 制备方法
取一定量的乙二醛溶液、硫酸、氯化铝、亚硝酸钠、去离子水于反应器中。封闭反应系统,用氧气置换反应器内空气,升温,反应(反应期间保持反应器内始终存在氧气)。待反应结束后,再次升温,通入空气,吹扫剩余的氮化物气体,用碱液对其吸收。一定温度下冷却,过滤析出晶体,减压蒸馏浓缩得到约为30%的乙醛酸溶液。
称取一定量的乙醛酸溶液于反应瓶中,升到一定温度后,加入一定量尿素,开始反应并计时。待反应结束后,冷却静置,过滤,干燥,即制得尿囊素。
1.3 分析方法
1.3.1 中间产物乙醛酸分析
先采用紫外可见分光光度计对不同浓度的乙二醛溶液进行波长扫描,根据朗伯-比尔定律,绘制出乙二醛标准曲线。再测定对待测液中乙二醛含量,根据已绘制的标准曲线,初步计算出氧化反应产物中乙二醛的含量。然后通过化学滴定法对产物中乙二醛和乙醛酸的含量进行分析,计算出乙二醛转化率以及乙醛酸收率。
1.3.2 尿囊素分析
熔点测定:显微熔点测定仪测定产物熔点[7]。
红外分析:采用红外光谱仪分析产物的结构,根据红外光谱显示的特征吸收峰,确定产物是否为尿囊素[8]。
2 结果与讨论
2.1 氧化反应影响因素
2.1.1 酸性介质的影响
1)氯化铝用量
在乙二醛质量分数25%,亚硝酸钠与乙二醛摩尔比0.2(钠醛比),硫酸与乙二醛摩尔比0.4(酸醛比),反应温度30℃,反应时间4h的条件下,考察氯化铝加入量对乙醛酸收率的影响,结果如图1所示。
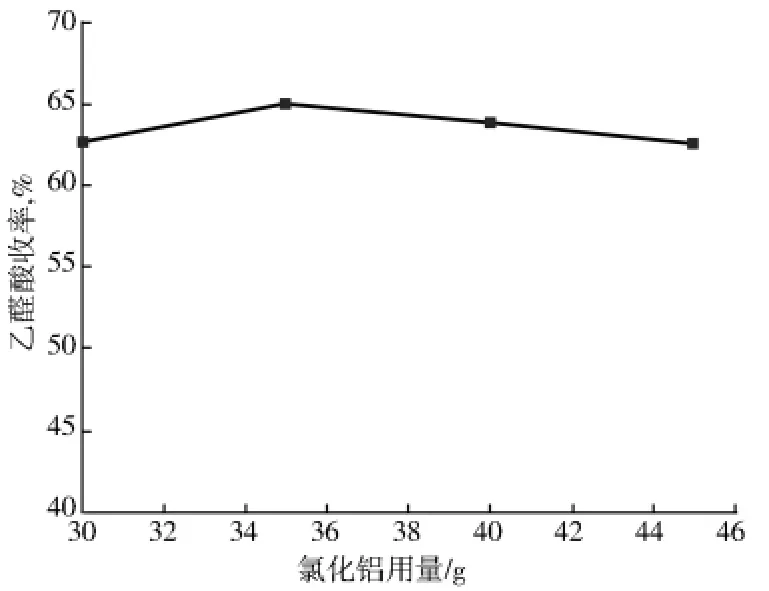
图1 氯化铝加入量与乙醛酸收率的关系
由图1可以看出:氯化铝加入量对乙醛酸收率没有太大影响。由反应机理可知,亚硝酸钠是获取氧化氮的初始原料,而氯化铝是Lewis酸,其存在为反应体系提供了更为温和的酸性环境,使亚硝酸钠逐渐分解产生一氧化氮,而一氧化氮很容易被继续氧化成NOx。酸性介质中加入氯化铝,除了提供酸性介质和与亚硝酸钠反应产生NOx外,还产生了强氧化性的氯化亚硝基(NOCl)。因此用硫酸与氯化铝作为酸性介质氧化乙二醛的反应,选用固定的氯化铝加入量即可,实验选用35g/mol乙二醛。
2)酸醛比
保持其他条件不变,考察酸醛比对乙醛酸收率的影响,结果如图2所示。由图2可以看出:随着酸醛比的增加,乙醛酸收率呈现先增大再减小的趋势。这是因为,亚硝酸钠在酸性条件下释放出强氧化性的NO2,NO2又在一定的酸性条件下氧化乙二醛。但当反应液中氢离子的浓度过高时,NO2氧化能力也随之增强,致使氧化剂进一步将生成的乙醛酸继续氧化成副产物草酸,即氧化反应深度进行,生成乙醛酸的选择性下降,从而导致乙醛酸收率下降。
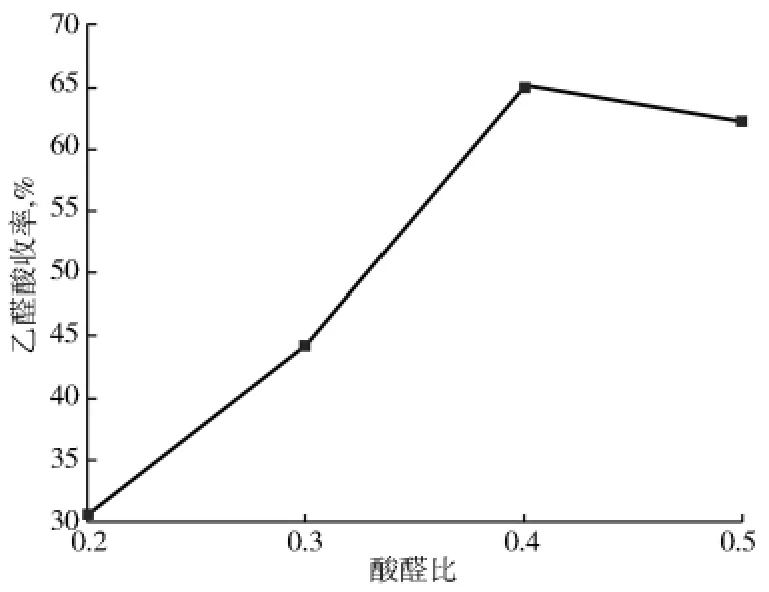
图2 酸醛比与乙醛酸收率的关系
2.1.2 钠醛比
保持其他条件不变,考察钠醛比对乙醛酸收率的影响,结果如图3所示。
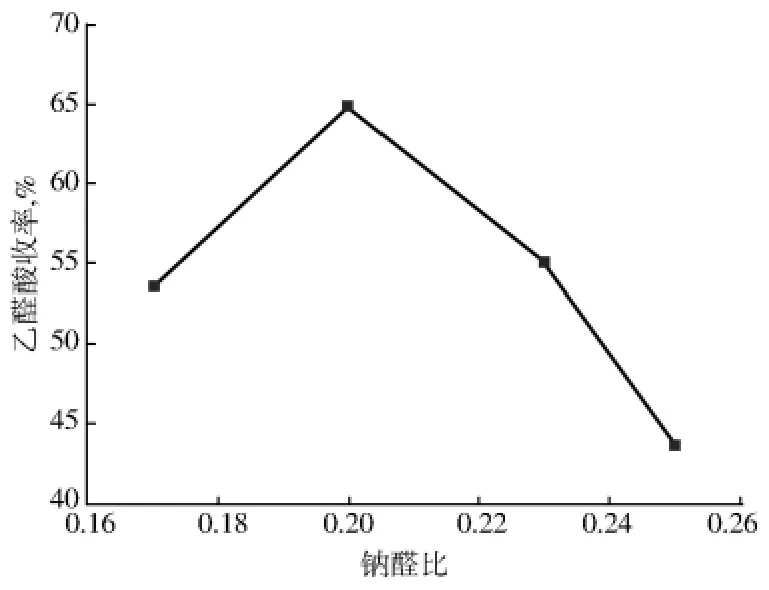
图3 钠醛比与乙醛酸收率的关系
由图3可以看出:随着钠醛比的增加,乙醛酸收率先增大再减小。亚硝酸钠在反应中提供初始氮源,而氮的氧化物又是反应的氧化剂,因此,在一定范围内亚硝酸钠加入量增加,氧化性增强,使得乙醛酸收率变大。然而,亚硝酸钠是一种弱碱盐,在反应液酸度一定的条件下,过多加入亚硝酸钠又会使反应体系酸度降低,致使收率逐渐下降。
2.1.3 乙二醛浓度
保持其他条件不变,考察乙二醛质量分数对乙醛酸收率的影响,结果如图4所示。由图4可以看出:随着乙二醛质量分数的增加乙醛酸收率先增后减。之所以出现这种现象主要是因为乙二醛质量分数较低时,反应液中存在大量的水,这在一定程度上降低了反应体系中酸性介质的浓度,即氢离子浓度,这也就减少了强氧化性NO2的生成,不利于乙二醛的氧化。随着乙二醛质量分数的增加,氢离子浓度增大,NO2增多,有利于氧化反应的进行。但乙二醛是一种具有黏性的有机物,浓度过高时,自聚集程度大,分子间将产生氢键阻止乙二醛继续发生反应,所以氧化效果变差,收率随之减少。
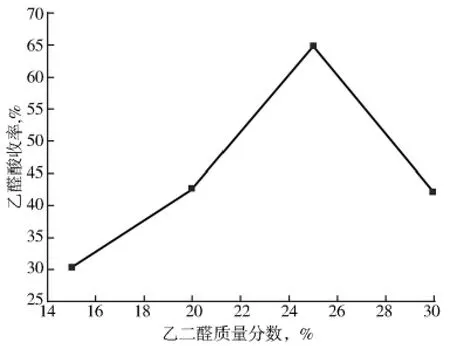
图4 乙二醛质量分数与乙醛酸收率的关系
2.1.4 反应温度
保持其他条件不变,考察反应温度对乙醛酸收率的影响,结果如图5所示。
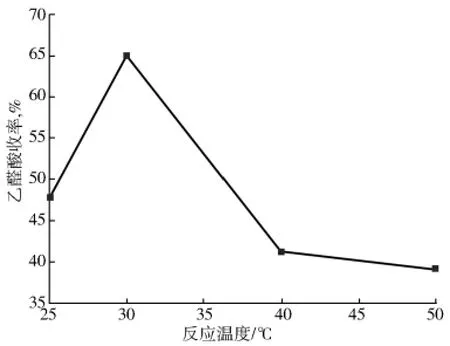
图5 反应温度与乙醛酸收率的关系
由图5可以看出:乙醛酸收率随着反应温度的增加先增大再减小。这是因为温度过低,达不到乙二醛被氧化所需条件,反应速度慢,反应不完全。而该氧化反应为放热反应,温度过高会降低气体在溶液中的溶解度,减少溶液中NO2的量,致使乙二醛转化率降低,乙醛酸的收率下降,同样也不利于氧化反应的进行。
2.1.5 反应时间
保持其他条件不变,考察反应时间对乙醛酸收率的影响,结果如图6所示。由图6可以看出:乙醛酸收率随着反应时间的增加呈现先增大后减小的趋势。这是因为随着反应的进行,NO2会继续与乙醛酸中的醛基发生氧化还原反应生成副产物草酸,所以反应时间过长乙醛酸收率下降,副产物草酸收率升高,反应选择性降低。
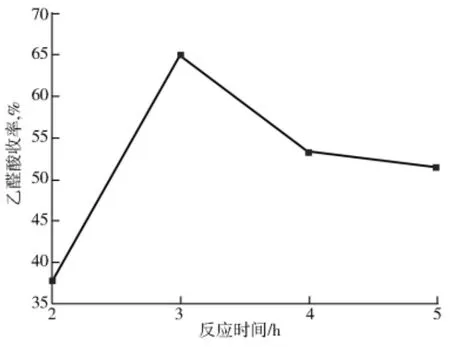
图6 反应时间与乙醛酸收率的关系
2.2 氧化反应条件
为寻找最适宜的反应条件,实验以乙醛酸收率为实验指标,采用L16(45)正交表进行了正交实验。因素水平表见表1,极差分析结果见表2,其中,A(钠醛比),B(酸醛比),C(反应温度/℃),D(反应时间/h),E(w(乙二醛),%)。
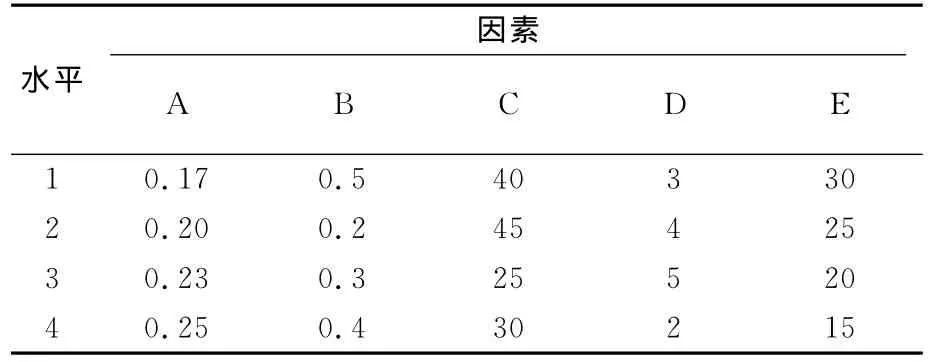
表1 氧化反应正交实验因素水平
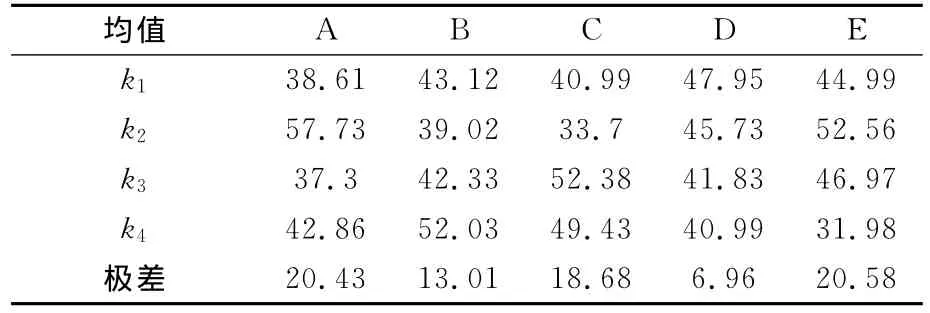
表2 氧化反应正交实验极差分析结果
通过表2的氧化反应正交实验极差分析结果可知:1)乙二醛质量分数对乙醛酸收率的影响最大,其次是钠醛比、反应温度、酸醛比和反应时间。2)适宜工艺的条件为:钠醛比0.2、酸醛比0.4、反应温度25℃、反应时间3h,乙二醛质量分数25%。在此条件下做验证性实验,乙醛酸收率为76.12%。
2.3 缩合反应条件的确定
在最适宜氧化反应的条件下,不另加酸性催化剂,直接进行乙醛酸溶液与尿素的缩合反应。在考察了乙醛酸尿素投料比(以下简称投料比)、反应温度、反应时间对缩合反应的影响基础上,实验以尿囊素收率为实验指标,设计3因素3水平的正交实验,确定适宜的缩合反应条件,其因素水平表见表3,极差分析结果见表4。
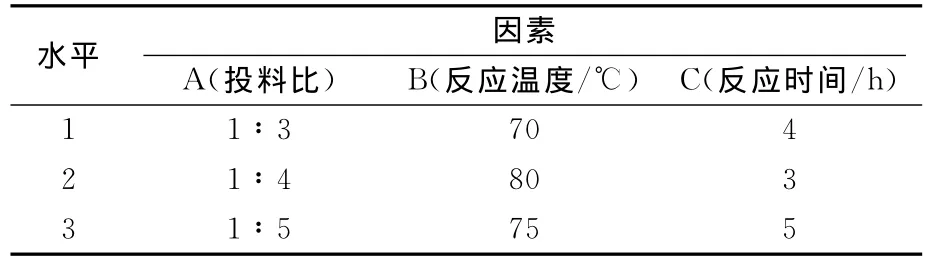
表3 缩合反应正交实验因素水平
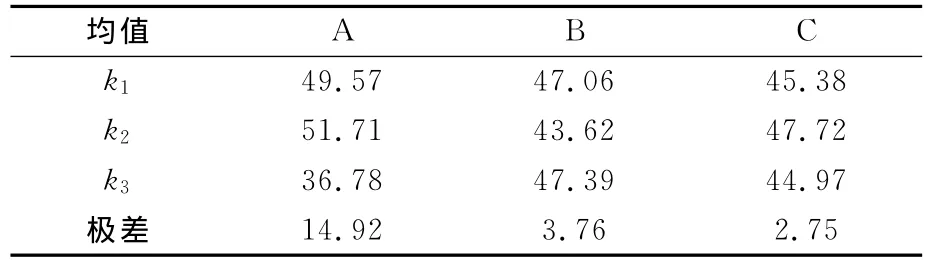
表4 缩合反应正交实验极差分析结果
由表4可知:1)投料比对尿囊素收率的影响最大,其次是反应温度和反应时间。2)适宜工艺条件为:投料比1∶4、反应温度75℃、反应时间3 h。在此条件下做验证性实验,尿囊素收率为60.75%。
2.4 产物尿囊素的确定
显微熔点测定仪测定产物的熔程为238~244℃。
产物经红外光谱分析,再与标准尿囊素谱对比,证明所制备的产物确为尿囊素。
3 结 论
a.以硫酸和氯化铝为酸性介质、亚硝酸钠为催化剂的常压氧气氧化乙二醛制备乙醛酸、进而在不添加酸性催化剂的条件下直接合成尿囊素的技术路线可行。氧化阶段所得反应液经浓缩后可直接应用于后续反应,无需在缩合阶段另加酸性催化剂,简化了流程,降低了成品分离提纯的难度,降低了生产成本,且避免了原料浪费。
b.氧化反应最适宜条件为:乙二醛质量分数25%,钠醛比0.2,酸醛比0.4,反应温度25℃,反应时间3h,在此条件下乙醛酸收率为76.12%。
c.缩合反应最适宜条件为:乙醛酸尿素投料比1∶4,反应温度75℃,反应时间3h,在此条件下尿囊素收率为60.75%。熔点及红外分析表明,产物为尿囊素。
[1]雷彦斌,贾瑛.乙二醛硝酸氧化制备尿囊素正交实验研究[J].化工时刊,2007,21(7):19-21.
[2]李涛.乙醛酸的生产及市场应用[J].精细化工原料及中间体,2008(8):9-10.
[3]王奇华,王存文,陈苏芳,等.空气催化氧化乙二醛合成乙醛酸的研究[J].武汉工程大学学报,2008,30(4):25-27.
[4]张友恭,张昭,樊国栋,等.低压氧法合成乙醛酸的改进[J].精细化工中间体,2003,33(3):56-57.
[5]周智明,徐巧,楼军军,等.一种催化氧气氧化乙二醛制备乙醛酸的新方法[J].北京理工大学学报,2005,25(5):451-453.
[6]李海静,薛铮然.尿囊素的合成研究[J].山东化工,2004,33:10-11.
[7]程芹,崔祐徽,张蕾,等.尿囊素的合成及其表征[J].精细石油化工进展,2005,6(9):17.
[8]王磊.尿囊素的红外光谱定量分析研究[J].分析化学,1991,19(2):211-213.
