谷红注射液的过敏性研究
2013-09-27张博琛张志郑湘临
张博琛,张志,郑湘临*
(1.山东大学 化学与化工学院,山东 济南 250100;2.通化谷红制药有限公司,吉林 梅河口 135000)
谷红注射液的过敏性研究
张博琛1,张志2,郑湘临2*
(1.山东大学 化学与化工学院,山东 济南 250100;2.通化谷红制药有限公司,吉林 梅河口 135000)
目的:评价谷红注射液诱发过敏反应的可能性。方法:通过腹腔注射0.5 mL/只受试制剂致敏豚鼠,14 d后静脉注射2 mL/只受试制剂激发豚鼠,评价豚鼠全身主动过敏反应的风险;另外通过腹腔注射受试制剂致敏大鼠,14 d后收集大鼠血清,皮下注射该血清用以致敏正常大鼠,24 h后静脉注射受试制剂激发大鼠,评价大鼠皮肤被动过敏反应的风险。结果:均未见过敏反应发生。结论:受试制剂谷红注射液诱发动物产生过敏反应的风险较小。
谷红注射液;全身主动过敏;皮肤被动过敏
谷红注射液为乙酰谷酰胺和红花提取物制成的灭菌水溶液,具有抗氧自由基、抗血小板聚集、舒张血管的作用,改善微循环,改善神经细胞代谢,维持神经应激能力,改善脑功能,还可改善血流变及降低血脂。临床广泛用于脑血管疾病、脑外伤、神经外科手术后、冠心病等[1]。但中药注射剂成分较复杂,原料及提取工艺不稳定,很多小分子物质没有相应的质控标准,临床对中药注射剂变态反应需引起足够重视[2]。谷红注射液在临床使用过程中亦发现过敏性休克等不良反应[3-7]。本研究根据I型变态反应原理,分析谷红注射液诱导试验动物引起过敏反应的可能性及原因。
1 材料
1.1 试药
谷红注射液(规格:5 mL,批号:20120814,通化谷红制药有限公司)、卵白蛋白(Sigma,批号:A5253)、吸附百白破联合疫苗(武汉生物制品研究所,批号:201100603-1)、硫化钠(上海统亚化工科技发展有限公司,批号:080108)、伊文斯蓝(北京化学试剂公司,批号:000525)。
1.2 动物
10周龄雄性Hartley豚鼠,体重300~400 g,由辽宁长生生物技术有限公司提供,生产许可证号:SCXK(辽)2010-0001;10周龄Wistar大鼠,雌雄兼用,体重250~300 g,由中国医科大学实验动物中心提供,生产许可证号:SCXK(辽)2008-0005。
2 方法
2.1 豚鼠全身主动过敏试验[8-11]
2.1.1 豚鼠致敏 受试动物随机分为阳性对照组、阴性对照组、谷红注射液低剂量组、谷红注射液高剂量组,每组6只。阳性对照组腹腔注射1%卵白蛋白0.5 mL/只;阴性对照组腹腔注射0.9%氯化钠溶液0.5 mL/只;谷红注射液低剂量组腹腔注射谷红注射液0.9%氯化钠溶液2倍稀释液0.5 mL/只;谷红注射液高剂量组腹腔注射谷红注射液0.5 mL/只(即低剂量组的2倍剂量)。上述给药,隔日1次,共3次。
2.1.2 豚鼠激发 致敏末次给药后第14天一次性静脉注射2 mL/只相应药物进行激发。
2.1.3 结果评价 激发后观察症状3 h,参照表1,反映级数达2级(含2级)以上,认为该受试物出现过敏反应。

表1 过敏症状评价表
2.2 大鼠皮肤被动过敏试验[8,11-12]
2.2.1 抗血清的制备 受试动物随机分为阳性对照组、阴性对照组、谷红注射液低剂量组、谷红注射液高剂量组,每组6只,雌雄各半。阳性对照组腹腔注射5 mg·mL-1卵白蛋白溶液3.57 mL·kg-1,及白百破疫苗0.5 mL/只(含百日咳疫苗效价≥4.0 IU,仅第一次使用);阴性对照组腹腔注射0.9%氯化钠溶液3.57 mL·kg-1;谷红注射液低剂量组腹腔注射谷红注射液0.9%氯化钠溶液2倍稀释液3.57 mL·kg-1(由成人临床最大用量换算得);谷红注射液高剂量组腹腔注射谷红注射液3.57 mL·kg-1(即低剂量组的2倍剂量)。上述给药,隔日1次,共3次。14 d后采血,2 000 r·min-1离心10 min,分离血清。
2.2.2 大鼠被动致敏 上述各组抗血清以0.9%氯化钠溶液稀释成1∶2,1∶8,1∶32 3种不同浓度。取正常大鼠24只,随机分为阳性对照组、阴性对照组、谷红注射液低剂量组、谷红注射液高剂量组,每组6只,雌雄各半,在其背中线两侧预先脱毛(3×4)cm2共3处,皮内注射相应组别的3种不同浓度抗血清各0.1 mL。
2.2.3 大鼠激发 大鼠被动致敏24 h后,各组静脉注射与致敏剂量相同的激发抗原加等量的伊文思兰染料(1%)共1 mL。
2.2.4 结果评价 30 min后断头处死各组动物,剪取背部皮肤,测量皮肤内层的斑点大小。皮肤内层斑点直径大于5 mm者判定为被动过敏阳性。
2.3 数据统计
数据统计分析采用SPSS 16.0软件包,大鼠被动过敏阳性率差异采用x2检验,定义P<0.05为差异具有统计学意义。
3 结果
3.1 受试药物对受试动物体重变化的影响
全身主动过敏试验过程中,各组豚鼠体重变化趋势无统计学意义,见图1;制备抗血清的各组大鼠在试验过程中体重变化趋势无统计学意义,见图2。
3.2 豚鼠全身主动过敏反应
给药激发后,阳性对照组6只豚鼠均出现痉挛、抽搐、休克死亡;阴性对照组、谷红注射液低剂量组、谷红注射液高剂量组均未见明显反应。评分结果见表2。
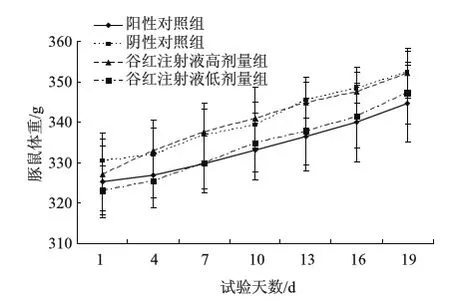
图1 谷红注射液对豚鼠体重变化的影响
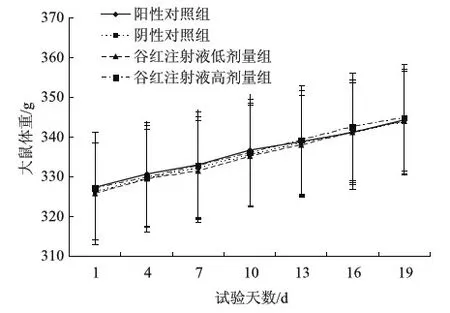
图2 谷红注射液对大鼠体重变化的影响
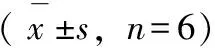
表2 谷红注射液主动过敏试验
3.3 大鼠皮肤被动过敏反应
试验中阴性对照组和谷红注射液低、高剂量组受试动物各滴度皮肤内层斑点直径均小于5 mm,阳性率均为0;阳性对照组受试动物各滴度皮肤内层斑点直径均大于5 mm,阳性率均为100%,见图3;谷红注射液低、高剂量组各滴度抗血清致皮肤被动过敏的阳性率显著低于阳性对照组(P=0.002);而谷红注射液低、高剂量组与阴性对照组比较,阳性率均为0,差异无统计学意义,见表3。

图3 谷红注射液大鼠皮肤被动过敏试验反应
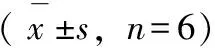
表3 大鼠皮肤被动过敏试验结果/mm
注:(1)括号内数字为阳性率;(2)*表示与阳性对照组比较,P=0.002;△表示与阴性对照组比较,阳性率均为0,差异无统计学意义。
4 讨论
临床上药物过敏反应常见迟发型过敏反应(Ⅳ型),但症状常常较轻,易于控制,而过敏性休克(属Ⅰ型过敏反应)一旦发生,若处置不当,常常危及生命。因此本研究着重考察谷红注射液导致Ⅰ型过敏反应发生的可能性。
研究以原国家食品药品监督管理局颁发的《化学药物刺激性、过敏性和溶血性研究技术指导原则》为依据,结合受试制剂具体情况,设计实验方案。全身主动过敏试验是根据药物初次进入体内,可刺激机体产生相应的抗体,当药物再次进入体内时与其抗体结合形成抗原抗体复合物,导致肥大细胞释放组胺等过敏介质,从而引起过敏反应。皮肤被动过敏试验(PCA)则是将致敏动物的血清皮内注射于正常动物,血清中IgE抗体与肥大细胞受体结合,使动物被动致敏,当应用致敏抗原激发时,引起局部肥大细胞释放过敏介质,从而使局部血管的通透性增加,激发时一同注入的染料可于皮内注射部位渗出,形成蓝斑。二者均可评价受试药品诱发动物产生Ⅰ型过敏反应的可能性。
通过豚鼠全身主动过敏试验及大鼠皮肤被动过敏试验研究受试制剂谷红注射液诱发动物产生Ⅰ型过敏反应的可能性,结果未发现谷红注射液诱发试验动物出现过敏反应现象,与阳性对照组比较差异有统计学意义,而与0.9%氯化钠溶液阴性对照组比较差异无统计学意义,表明该制剂诱发Ⅰ型过敏反应的风险较小。虽然谷红注射液引起变态反应的病例少见,但谷红注射液中的红花提取液本身成分复杂,含有鞣质、酶、皂苷、角质蛋白等多种大分子物质,静脉滴注后,上述物质作为抗原,具有高度致敏活性,易导致变态反应。因此,临床使用本品前应详细询问患者有无红花制剂过敏史;另外,对有过敏体质患者应慎用本品;并且在用药过程中,应密切观察,加强用药监护,防止过敏反应的发生,以保证用药安全。
[1] 张茁.谷红注射液治疗急性脑梗死有效性和安全性的多中心、随机、开放性临床观察[J].现代预防医学,2010,37(22):4382-4385.
[2] 王辉.中药注射剂致过敏性休克448例文献分析[J].中国药物应用与监测,2008,5(4):45-46,62.
[3] 金立军.金特佳注射液致皮肤瘙痒症2例分析[J].中国误诊学杂志,2007,7(19):4670-4671.
[4] 郑刚,张震,马军.谷红注射液致迟发性变态反应1例[J].现代中西医结合杂志,2006,15(24):3416.
[5] 李慧,刘顺良,尹晓飞.谷红注射液致过敏反应1例[J].药物流行病学杂志,2008,17(2):87.
[6] 杨玲,刘向龙,王玲勉.谷红注射液致迟发性过敏性休克1例[J].中国误诊学杂志,2006,6(20):4092.
[7] 彭均,金淑萍.谷红注射液不良反应[J].中国误诊学杂志,2009,9(33):8308.
[8] 国家食品药品监督管理局.化学药物刺激性、过敏性和溶血性研究技术指导原则[M].2005:13-14,19-21,25-27.
[9] 陈奇.中药药理研究方法学[M].北京:人民卫生出版社,1993:163-169.
[10] 孙敬方.实验动物方法学[M].北京:人民卫生出版社,2001:210.
[11] 徐叔云,卞如溓,陈修,等.药理实验方法学[M].第3版.北京:人民卫生出版社,2002:234-237,1407-1409.
[12] 国家食品药品监督管理局.中药、天然药物免疫毒性(过敏性、光过敏反应)研究的技术指导原则[M].2005:25.
AnaphylacticResponseofSafflowerExtractandAceglutamideInjection
ZHANG Bo-chen1,ZHANG Zhi2,ZHENG Xiang-lin2*
(1.ChemistryandChemicalEngineeringCollegeofShandongUniversity,Jinan250100,China;2.TonghuaguhongPharmaceuticalCompanyLimited,Meihekou135000,China)
Objective:To evaluate the probability of anaphylactic response induced by Safflower Extract and Aceglutamide Injection.Methods:In this study,every cavia cobaya was given the product 0.5 mL by intraperitoneal injection for sensitization,and excitation was performed 14 days later by intravenous injecting 0.2 mL the same product,to evaluate the risk of active systemic anaphylaxis(ASA); Every rat was given the product by intraperitoneal injection for sensitization,and its serum was collected 14 days later to give normal rats by intraperitoneal injection.The excitation of normal rats was done after 24 hours for evaluate the risk of passive cutaneous anaphylaxis(PCA).Results:No anaphylactic response induced by the product was found in this study.Conclusion:Safflower Extract and Aceglutamide Injection has little probability of anaphylactic response.
Safflower Extract and Aceglutamide Injection;ASA;PCA
2012-12-05)
*
郑湘临,E-mail:df-zhangxianglin@163.com
