美托洛尔基于循证的药物评价
2013-09-26刘晓琦劳海燕张建萍王映雪李桃黎月玲杨泽民
刘晓琦 劳海燕 张建萍 王映雪 李桃 黎月玲 杨泽民
(1广东省人民医院药学部,广东省医学科学院,广东广州510080;2暨南大学药学院,510632;3广州市红十字会医院,510220;4广东药学院附属第一医院,510080)
基本药物是20世纪70年代世界卫生组织(WHO)提出的理念,目的在于促进基本药物的公平可及、安全有效、合理使用。在我国,基本药物是指适应基本医疗卫生需求,剂型适宜,价格合理,能够保障供应,公众可公平获得的药品。根据我国《国家基本药物目录管理办法(暂行)》,我国基本药物遴选应该按照“防治必须、安全有效、价格合理、使用方便、中西药并重、基本保障、临床首选和基层能够配备”的原则。2009年版《国家基本药物目录》(以下简称2009年版目录)在遴选时虽然遵循了上述原则,对药品的有效性、安全性、质量、价格以及可获得性作了综合性分析,但目前尚未对目录中药品开展高质量证据支持的循证药物评价。本研究采用WHO及各国遴选基本药物时所依据的循证决策方法,对我国2009年版目录中抗心律失常药物美托洛尔进行综合评价,探索适合我国国情的基本药物遴选路径及评价方法,以促进基本药物制度的建立和完善。
1 材料与方法
1.1 临床问题的确定
美托洛尔是β受体阻滞剂,属于Ⅱ类抗心律失常药物,临床应用广泛,适应证包括窦性心动过速、围手术期心律失常、心房颤动伴快速心室反应、室性心动过速、交感神经兴奋引发的快速性心律失常,以及某些类型长QT综合征等。虽然目前认为此类药物是唯一能降低总死亡率的抗心律失常药物,但用药期间也可能出现一些不良反应,包括心率减慢、传导阻滞、血压降低、心衰加重、外周血管痉挛导致的四肢冰冷或脉搏不能触及、雷诺氏现象等,且美托洛尔为脂溶性药物,易透入中枢神经系统,故也可能出现中枢系统不良反应。为明确美托洛尔抗心律失常的疗效和安全性有必要对其进行循证评价。
1.2 文献入选及排除标准
入选标准:患者诊断为心律失常,干预组需接受美托洛尔治疗;研究结果包含疗效及安全性相关数据;入选研究为随机对照试验(RCT)。
排除标准:研究对象为动物或患者同时合并恶性肿瘤,血液疾病等;干预措施为联合用药。
主要结局指标(疗效)为全因死亡率、心律失常复发率,次要结局指标(安全性)为不良反应发生率,不良反应包括致心律失常、心动过缓、心动过速等。
1.3 检索策略与文献筛选
通过 Pubmed (1980-2012.11)、Cochrane Library、CNKI(1980-2012.11)等中英文数据库进行相关主题词检索,并搜索相关研究的参考文献。英文 检 索 策 略 : (“Metoprolol”[MeSH Terms]OR“Metoprolol” [All Fields])AND ((“Arrhythmias,Cardiac” [Mesh]AND “Anti-Arrhythmia Agents”[Mesh]) AND (((((((randomized controlled trial[Publication Type]OR controlled clinical trial[Publication Type]) OR randomized[Title/Abstract]) OR placebo[Title/Abstract])OR “clinical trials as topic”[MeSH MajorTopic])OR randomly[Title/Abstract]) OR trial[Title]) NOT (“animals”[MeSH Terms]NOT (“humans”[MeSH Terms]AND “animals” [MeSH Terms])))) AND (“loattrfree full text”[sb]AND “humans”[MeSH Terms])。 中文检索检索词为 “β受体阻滞剂”、“美托洛尔”、“抗心律失常”、“心律失常”、“临床试验”等。
1.4 数据提取与分析
提取每篇文献的基本信息,如题目、作者、患者情况、干预措施、治疗结果等,使用RevMan5.0软件对各项结局指标数据进行分析。采用推荐分级的评价、制定与评估 (grading of recommendations assessment,development,and evaluation,GRADE)方法[1]对各项证据的质量进行评价,形成证据概要表及结果总结表,最终形成美托洛尔是否纳入国家基本药物目录的推荐意见。
2 结果
2.1 文献检索结果
按照已制定检索策略检索相关数据库,根据纳入和排除标准最终纳入文献4篇[2-5]。文献筛选流程见图1,入选文献基本信息见表1。
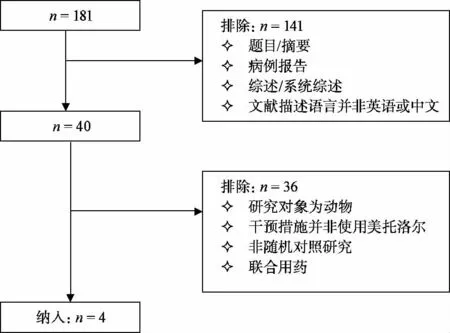
图1 文献筛选流程
2.2 全因死亡率
入选的4个研究异质性检验结果P=0.27(P>0.10),I2=24%,提示各项研究间并未存在异质性。 全因死亡率[RR=0.84,95%CI(0.52,1.35),P=0.47],见图 2。
2.3 心律失常复发率
3个研究异质性检验结果P=0.37(P>0.10),I2=0%,提示各项研究间并未存在异质性。心律失常复发率[RR=0.70,95%CI(0.61,0.82),P <0.000 01],结果显示美托洛尔能显著降低心律失常的复发率,见图3。
2.4 不良反应发生率
3个研究异质性检验结果P=1.00(P>0.10),I2=0%,提示各项研究间并未存在异质性。不良反应发生率[RR=5.39,95%CI(2.11,13.80),P=0.000 4],见图 4。

表1 纳入文献基本信息
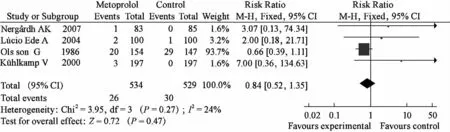
图2 美托洛尔vs.安慰剂全因死亡率
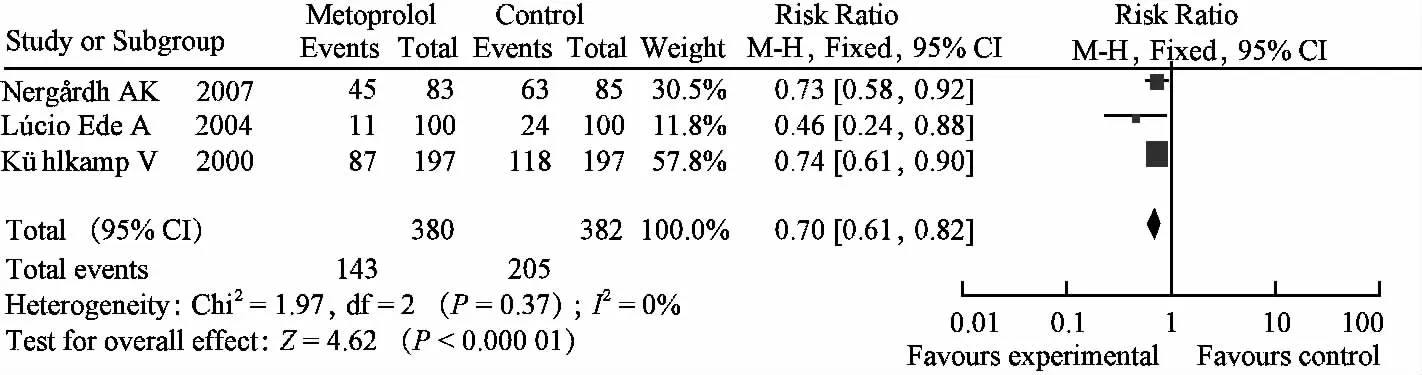
图3 美托洛尔vs.安慰剂心律失常复发率
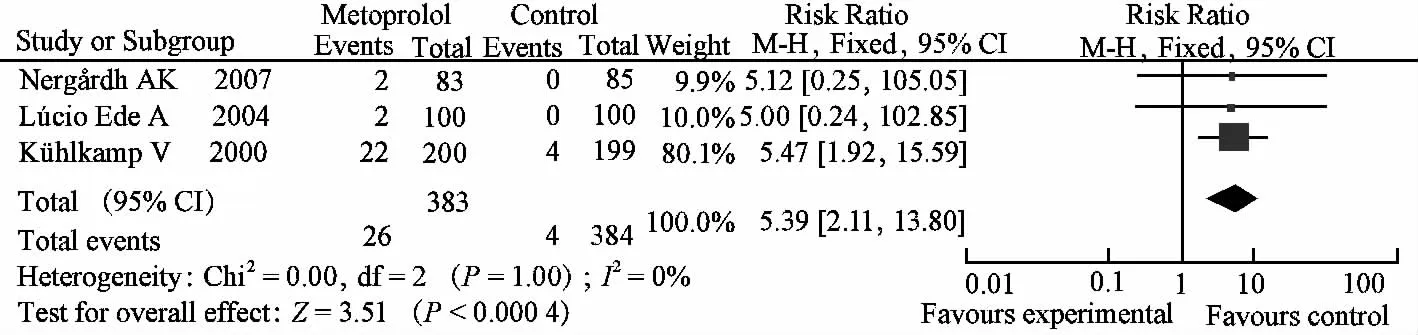
图4 美托洛尔vs.安慰剂不良反应发生率
2.5 证据质量评价
根据GRADE方法,本研究从证据质量、利弊结果的平衡、价值观与偏好、资源使用等方面对证据质量进行评价,评价原理见图5。各项结局指标GRADE评价证据概要及结果总结见表2、3。
2.6 形成推荐意见
通过对纳入研究的质量评价,显示美托洛尔能显著降低患者心律失常复发率,且未增加患者死亡风险,推荐美托洛尔继续保留在新版国家基本药物目录中。
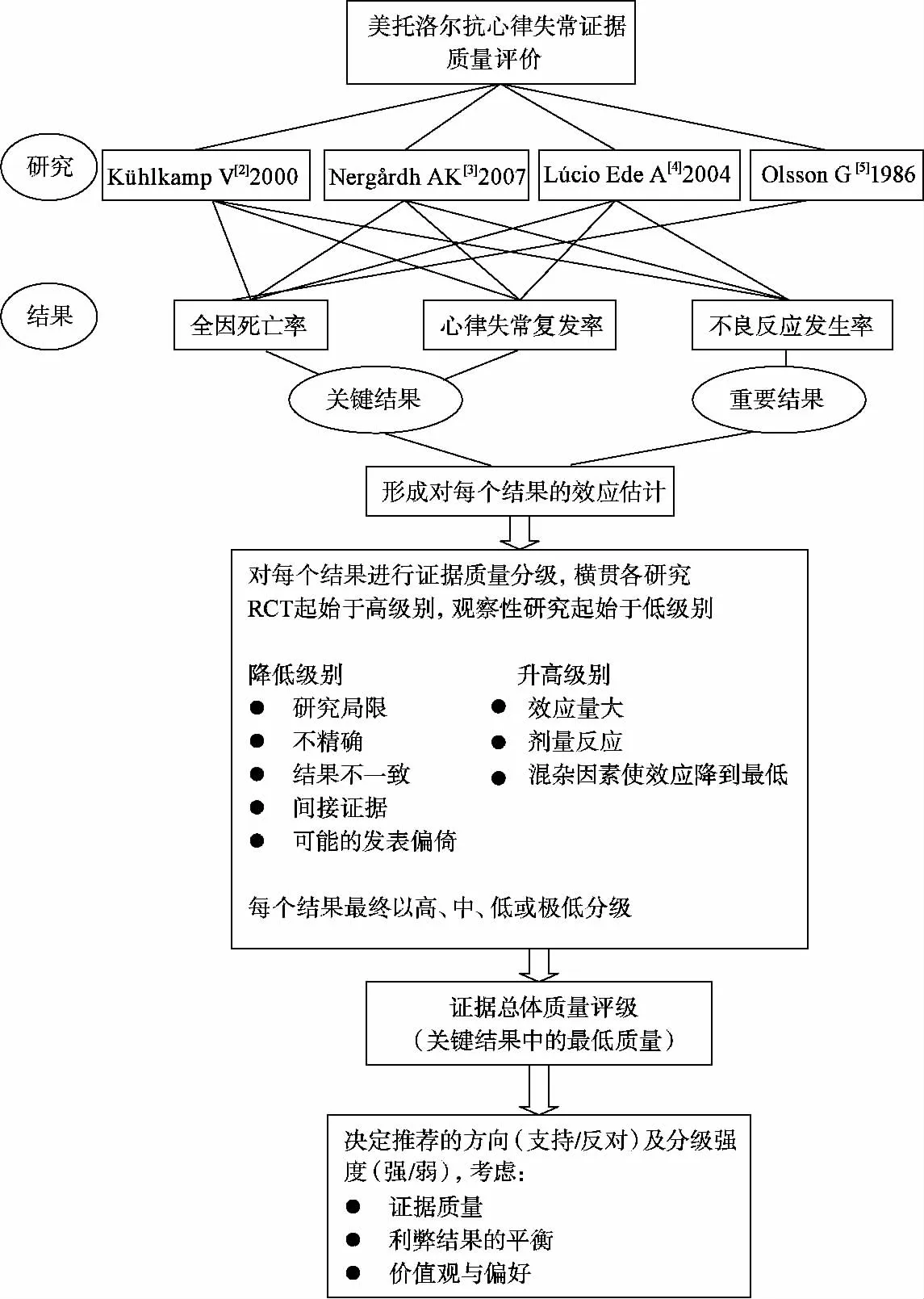
图5 证据质量评价原理
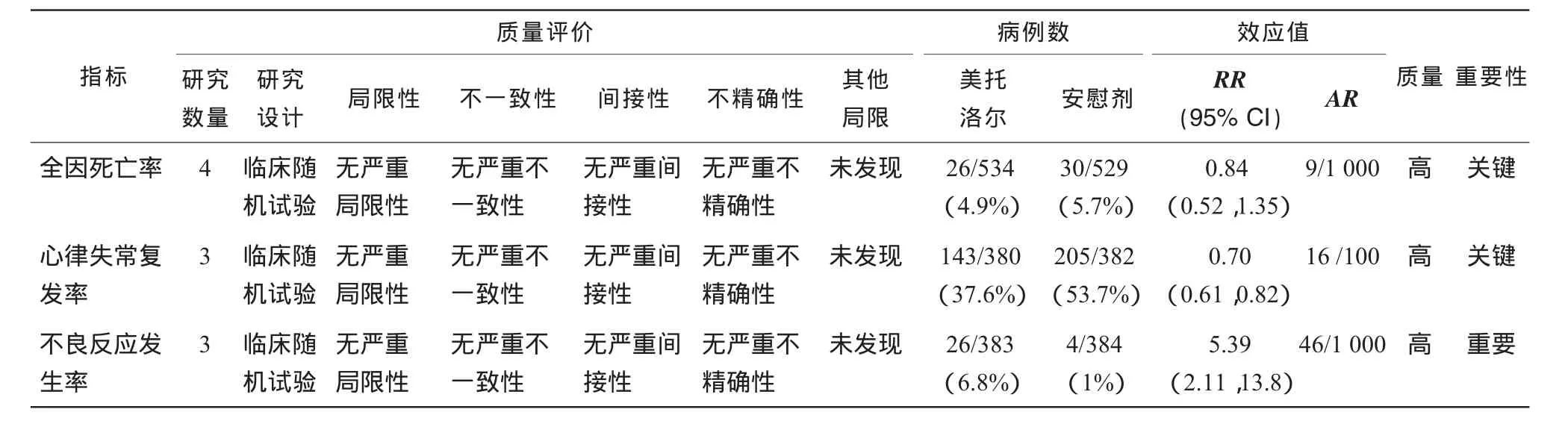
表2 美托洛尔抗心律失常评价的证据概要
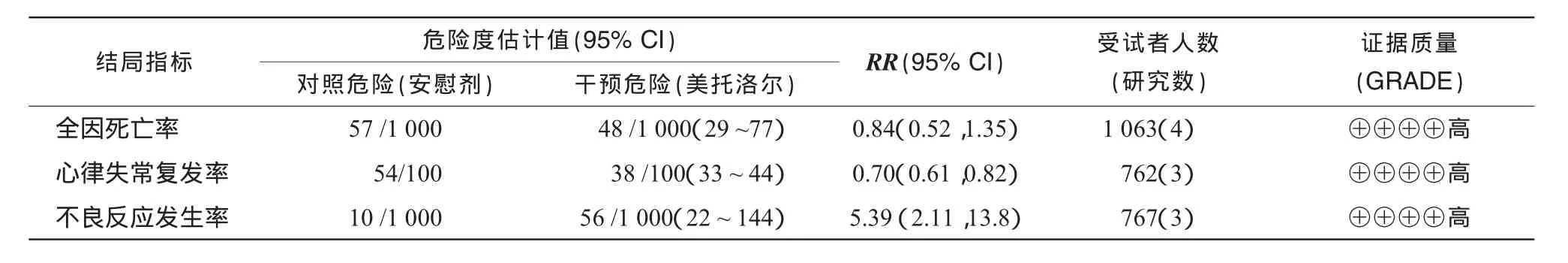
表3 美托洛尔抗心律失常的结果总结
3 讨论
本研究采用循证方法,对我国基本药物目录中抗心律失常药物的疗效及安全性进行评价:首先确定待评价药物美托洛尔,按确定的纳入/排除标准筛选文献后,综合评价药物安全性、有效性,并采用 GRADE方法对证据质量进行评价,最后根据结果形成推荐意见。
循证的理念及方法是WHO及各国遴选基本药物的依据,但我国目前在制定及调整基本药物目录时仍未系统开展对药物的循证评价。本研究首次运用循证方法对我国基本药物进行评价,此次实践可为今后基本药物的评价与目录调整提供参考。当然此次评价也存在不足,如重点在药物疗效及安全性,而缺乏可靠并充分的经济学指标,这与我国目前经济学研究尚不成熟,可参考数据有限相关。如何将安全、有效、经济等指标量化,按权重比例综合评价是今后基本药物评价的主要研究方向。
国家基本药物制度是保障人民群众基本用药的重要制度,而基本药物的遴选又是推行该制度的关键。以循证为核心的基本药物遴选,结合经济学研究能够满足基本药物遴选安全、有效、经济的要求,值得推广。
[1] 曾宪涛.如何正确理解及使用GRADE系统[J].中国循证医学杂志,2011,11(9): 985-990.
[2] Kühlkamp V,Schirdewan A,Stangl K,et al.Use of metoprolol CR/XL to maintain sinus rhythm after conversion from persistent atrial fibrillation: a randomized, double-blind, placebo-controlled study[J].J Am Coll Cardiol, 2000,36(1):139-146.
[3] Nergårdh AK,Rosenqvist M,Nordlander R,et al.Maintenance of sinus rhythm with metoprolol CR initiated before cardioversion and repeated cardioversion of atrial fibrillation:a randomized double-blind placebo-controlled study[J].Eur Heart J,2007,28(11):1351-1357.
[4] Lúcio Ede A,Flores A,Blacher C,et al.Effectiveness of metoprolol in preventing atrial fibrillation and flutter in the postoperative period of coronary artery bypass graft surgery[J].Arq Bras Cardiol,2004,84(1):42-46,37-41.
[5] Olsson G,Rehnqvist N.Evaluation of antiarrhythmic effect of metoprolol treatment after acute myocardial infarction:relationship between treatment responses and survival during a 3-year follow-up[J].Eur Heart J, 1986,7(4):312-319.
