聚3-己基噻吩的合成及表征
2013-09-19宫玉梅,夏令明,梁青,郭静,张鸿
宫 玉 梅,夏 令 明,梁 青,郭 静,张 鸿
(大连工业大学 纺织与材料工程学院,辽宁 大连 116034)
0 引 言
可溶性共轭聚合物因其良好的溶解性、低成本、易加工、环境稳定性等特点,已被广泛应用于有机薄膜太阳能电池、有机场效应晶体管、有机发光二极管、光学传感器等光电器件中[1-3]。在众多可溶性共轭聚合物中,有序聚3-己基噻吩(HTP3HT)作为聚噻吩类的一种,由于其烷基侧链的有序排列,使得共轭主链间能够有效地π-π堆积,使其具有较高的电荷载体迁移率而成为制备光伏材料时的首选聚合物。
聚3-己基噻吩的有序度、相对分子质量及其分布对光伏材料的导电性及其器件性能有着重要的影响。聚3-己基噻吩的有序度越高其结晶度也相应越高,从而能够有效提升光伏器件的性能。当大量非有序结构 HH(head-head)、TT(tailtail)存在时,聚3-己基噻吩的结晶性大幅降低,甚至不结晶,选作器件时性能将大大降低[4]。KLINE等[5]的研究表明在场效应晶体管中,聚3-己基噻吩(HT-P3HT)的相对分子质量从3 200增大到36 500时,其电荷载体迁移率相应从1.7×10-6cm2/Vs 增 加 到 9.4×10-3cm2/Vs。SCHILINSKY等[6]采用调控聚3-己基噻吩的相对分子质量分布从而优化了P3HT太阳能电池的性能。因而,制备有序、窄分布的P3HT对改善光伏器件的性能是一条有效途径。另外,KRASOVSKIY[7]等的研究发现,氯化锂可以有效地促进格氏试剂i-PrMgCl与富电子的卤代芳香化合物单体间的卤素-镁金属交换,提高反应速率。
本实验采用KCTP(chain growth Kumada catalyst-transfer polycondensation)法以 2,5-二溴-3己基噻吩为单体制备有序的聚3-己基噻吩(HT-P3HT)。考察了催化剂 Ni(dppp)Cl2用量对产物相对分子质量及其多分散系数的影响,并对促进剂氯化锂的使用对聚合物的有序度、相对分子质量及其多分散系数的影响进行了研究。
1 实 验
1.1 主要试剂
无水四氢呋喃、无水乙醇、甲醇、正己烷、无水氯化锂、邻二氯苯、盐酸、1-溴己烷均为分析纯;2,5-二溴-3-己基噻吩(纯度98%);Ni(dppp)Cl2。
1.2 聚3-己基噻吩的制备
1.2.1 己基溴化镁的制备
取适量金属镁,用2mol/L的稀盐酸去除表面氧化层,再用无水乙醇、无水THF清洗。将干燥后的镁放入100mL三口烧瓶中。抽真空并通氮气保护30min后加入30mL的无水THF搅拌。缓慢滴加适量1-溴己烷与5mL无水THF混合液。待反应结束后移取上清液备用。
1.2.2 聚3-己基噻吩(HT-P3HT)的合成
向已制备的己基溴化镁中缓慢滴加适量的单体2,5-二溴-3己基噻吩(1)与5mL无水THF混合液,60℃搅拌加热1.5h后加入适量Ni(dppp)Cl2与5mL THF混合液,60℃加热搅拌30min。反应结束后将溶液倒入200mL甲醇中沉淀、抽滤,产物用甲醇和正己烷索氏抽提12h。将提纯后的产物室温真空干燥得暗紫色固体。
1.2.3 等摩尔无水LiCl存在时聚3-己基噻吩(HT-P3HT)的合成
将适量无水LiCi 140℃真空干燥4h备用。向已制备的己基溴化镁中缓慢滴加适量的单体2,5-二溴-3己基噻吩(1)、无水 LiCl(与噻吩单体等摩尔)与10mL无水THF的混合溶液,60℃搅拌加热1.5h后,加入适量 Ni(dppp)Cl2与5mL THF的混合溶液。60℃加热搅拌30min。反应结束后将溶液倒入200mL甲醇中沉淀,抽滤。将产物用甲醇和正己烷索氏抽提12h。将提纯后的产物室温真空干燥得暗紫色固体。
2 结果与讨论
2.1 红外光谱分析
为了确定所得产物的分子结构,对未加促进剂LiCl时制备的P3HT进行了FT-IR分析,如图1所示。图1中,波数3 053cm-1为噻吩环上C — H 键的伸缩振动吸收峰,2 958、2 923、2 852cm-1为侧链烷基上 C— H 键的伸缩振动吸收峰,1 508、1 451cm-1为噻吩环上 —C═C — 双键的伸缩振动吸收峰。1 376cm-1为甲基弯曲振动吸收峰,819cm-1为噻吩环上 C— H 键面外弯曲振动吸收峰,723cm-1为甲基的面内摇摆振动吸收峰。由此可以推断所得产物为P3HT。

图1 有序聚3-己基噻吩的FT-IR图谱Fig.1 FT-IR spectrum of the synthesized HT-P3HT
2.2 1 H-NMR图谱分析
为了明确所得P3HT的噻吩单元间的排列方式,采用1H-NMR核磁图谱对其进行进一步分析。由于噻吩单元间不同的连接方式,噻吩环上的4位质子有4种不同的化学位移,分别为6.98(HT-HT)、7.00(TT-HT)、7.02(HT-HH)、7.05(TT-HH)。α亚甲基质子有2种化学位移,分别为2.80(HT)和2.58(HH)。β亚甲基质子有2种化学位移,分别为1.72(HT)和1.63(HH)。因而从噻吩环上4位质子、α亚甲基质子和β亚甲基质子的化学位移,可推断所制备P3HT分子链中单体间结构单元的排列方式,即有序度[8]。
图2为不使用LiCl时所制备的有序聚3-己基噻吩的核磁1H-NMR图谱。图2(a)显示δ=6.98的单峰,表示噻吩环上未被取代的4位H原子峰,而图2(b)显示为δ=2.80附近的三重峰,表示与芳香环直接相连的支链烷基的第1个亚甲基的H原子峰,而δ=1.72处的吸收峰,表示与芳香环直接相连的支链烷基的第2个亚甲基上H原子峰。因此可以判断结构单元HT-HT排列的聚3-己基噻吩已经形成,而表征非有序结构δ=7.00(HT-HH)、δ=7.02(HT-HH)、δ=7.05(TT-HH)等吸收峰并未在图谱中出现,可以推断在不使用LiCl时所制备的P3HT是高度有序的HT排列。

图2 无LiCl时 HT-P3HT的1 H-NMR图谱Fig.2 1 H-MNR spectra profile of HT-P3HT synthesized without LiCl
为了加快反应速率,制备P3HT时加入与单体等摩尔的LiCl作为促进剂,得到聚合物的1H-NMR图谱如图3所示。由图3(a)中箭头指示δ=7.05(TT-HH)、δ=7.02×10-6(HT-HH)和图3(b)中箭头指示δ=2.58(HH)的吸收峰,可以判定所制备的P3HT具有少量的无序链接结构。说明在促进剂氯化锂存在时所制备的P3HT的有序度有稍微的下降,存在一定的无序结构。
2.3 催化剂用量及促进剂LiCl对聚3-己基噻吩相对分子质量及其分布的影响
由图4(a)可以看出,随着单体(1)与催化剂用量摩尔比的增加,P3HT的相对分子质量成线性增大而多分散系数成线性下降。由此判断,可以通过改变单体与催化剂Ni(dppp)Cl2的摩尔比以获得不同相对分子质量及多分散系数的P3HT。由图4(b)可以看出,随着单体与催化剂摩尔比的增加,聚合物的相对分子质量及其多分散系数不再呈线性关系,并且与图4(a)比较发现,相同条件下当聚合过程中使用LiCl时,P3HT的相对分子质量增大,而多分散系数变小。

图3 加入LiCl产物HT-P3HT的1 H-NMR图谱Fig.3 1 H MNR spectra profile of the P3HT synthesized with LiCl
2.4 光性能
对制备的P3HT进行紫外-可见光吸收光谱分析。图5为有序聚3-己基噻吩在邻二氯苯溶液及其薄膜中的紫外-可见光吸收光谱。由图5可见,在邻二氯苯溶液中有序聚3-己基噻吩的λmax为459nm。而在薄膜中λmax为559nm,与溶液中相比,发生了100nm的红移,并且在薄膜中603nm处存在一个吸收肩峰,说明当成膜后高分子主链的刚性增强,有效共轭长度增大,链间堆积紧密,导致P3HT的能隙变小,使电子π-π跃迁所需能量降低[9],有利于后续薄膜光伏材料的制备。
3 结 论
采用KCTP法成功合成了有序聚3-己基噻吩(HT-P3HT)。研究表明催化剂 Ni(dppp)Cl2的用量对P3HT的相对分子质量及其多分散系数有重要的影响。随着单体与催化剂用量摩尔比的增加,P3HT的相对分子质量成线性增大,并且多分散系数成线性下降。当加入等摩尔LiCl作为促进剂时,随着单体与催化剂摩尔比的增加,P3HT的相对分子质量不再成线性增大并且多分散系数同样也不再成线性下降,产物的有序度有少许降低,但是产物的相对分子质量有所提高,分布变窄。
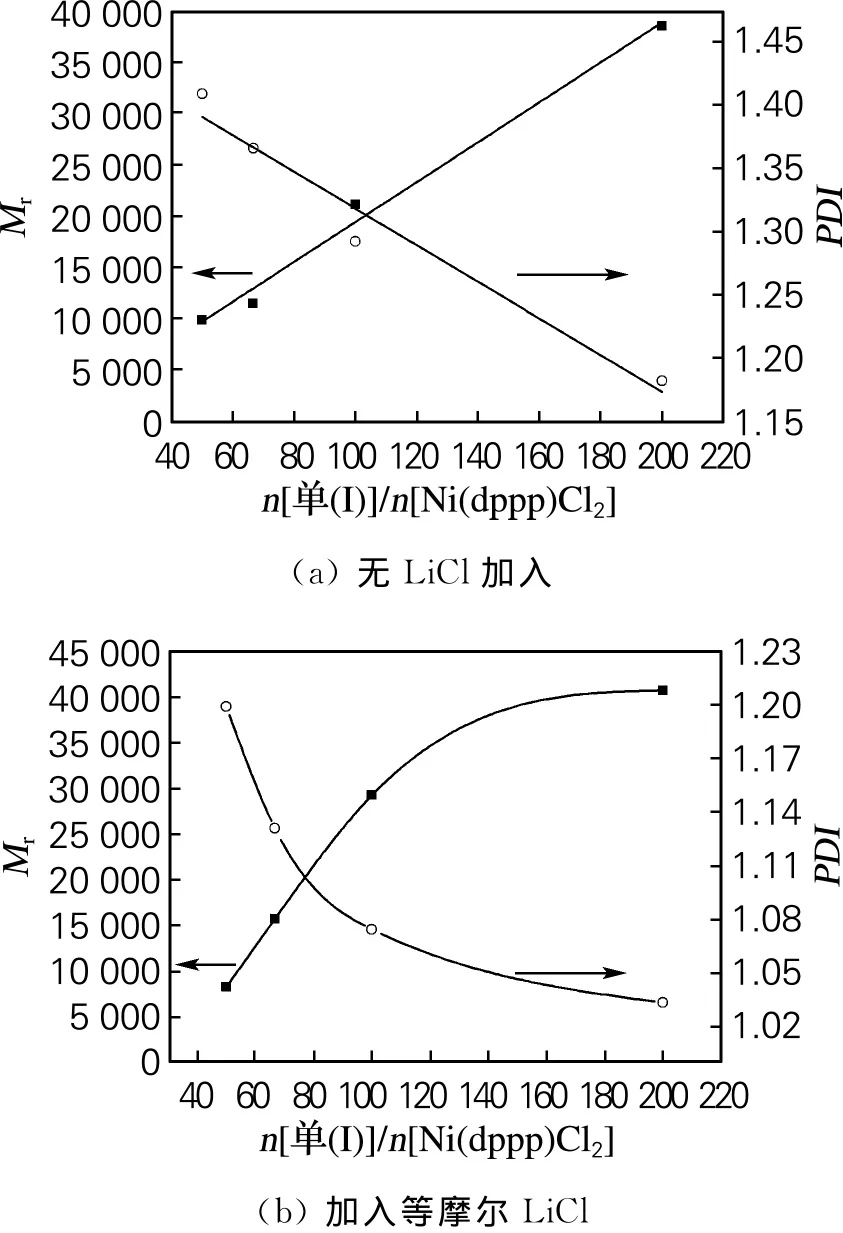
图4 单体与催化剂摩尔比与产物HT-P3HT的Mr及PDI的关系曲线Fig.4 Profiles of Mrand PDI of P3HT as a function of monomer and catalyst ratio
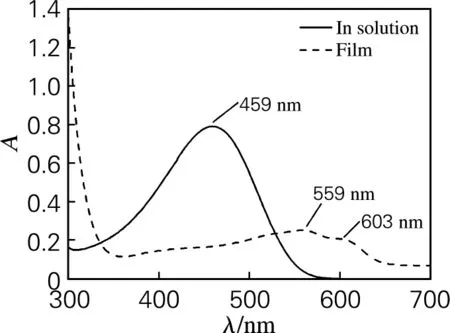
图5 HT-P3HT的邻二氯苯溶液中和薄膜中的UV-Vis吸收光谱Fig.5 UV-Vis adsorption spectra of the HT-P3HT in chloroben and film
[1]MURPHY A R,LIU Jinsong,LUSCOMBE C,et al.Synthesis,characterization,and field-effect transistor performance of carboxylate-functionalized polythiophenes with increased air stability[J].Chemistry of Materials,2005,17(20):4892-4899.
[2]DENNLER G,SCHARBER M C,BRABEC C J.Ploymer-fullerene bulk-heterojunction solar cells[J].Advanced Materials,2009,21:1323-1338.
[3]KLINE R J,MCGEHEE M D,KADNIKOVA E N,et al.Dependence of regioregular poly(3-hexylthiophene)film morphology and field-effect mobility on molecular weight[J].Macromolecules,2005,38(8):3312-3319.
[4]MAUER R,KASTLER M,LAQUAI F,et al.The impact of polymer regioregularity on charge transport and efficiency of P3HT:PCBM photovoltaic devices[J].Advanced Functional Materials,2010,20(13):2085-2092.
[5]KLINE R J,MCGEHEE M D,KADNIKOVA E N,et al.Controlling the field-effect mobility of regioregular polythiophene by changing the molecular weight[J].Advanced Materials,2003,15(18):1519-1522.
[6]SCHILINSKY P,ASAWAPIROM U,SCHERF U,et al.Influence of the molecular weight of poly(3-hexylthiophene)on the performance of bulk heterojunction solar cells[J].Chemistry of Materials,2005,17(8):2175-2180.
[7]KRASOVSKIY A,KONCHEL P.A LiCl-mediated Br/Mg exchange reaction for the preparation of functionalized Aryl-and Heteroarylmagnesium compounds from organic bromides[J].Angewandte Chemie,2004,43(25):3333-3336.
[8]CHEN Tianan,WU Xiaoming,RIEKE R D.Regiocontrolled synthesis of poly(3-alkylthiophenes)mediated by Rieke Zinc:their characterization and solidstate properties[J].Journal of the American Chemical Society,1995,117(1):233-244.
[9]CHANG Yi-ming,SU Wei-fang,WANG Leeyih.Influence of photo-induced degradation on the optoelectronic properties of regioregular poly(3-hexylthiophene)[J].Solar Energy Materials & Solar Cells,2008,92(7):761-765.
