乙酸预浸对玉米秸秆蒸汽爆破预处理的影响
2013-09-18赵鹏翔吴毅赵正凯
赵鹏翔,吴毅,赵正凯
(国网新源控股有限公司北京非粮醇电联产技术研发中心,北京 100053)
燃料乙醇属于生物质能源的一种,是清洁可再生能源,具有污染小,容易运输和贮藏的特点。木质纤维素在地球上含量大,分布广,可再生。因此,以纤维素生产燃料乙醇逐渐成为各国争相研究的热点。据测算,我国农作物秸秆资源总量约为6亿吨[1-2],可用作能源和生物质产品转化利用的秸秆约4亿吨,以稻草、玉米秸、麦秸为主,约占总量的3/4以上[3]。目前生产的大部分燃料乙醇是以玉米、小麦等粮食为原料。如果用我国10%的秸秆用来生产燃料乙醇,则可以生产1 000万吨纤维素乙醇,替代3 500万吨谷物,避免与人争粮的尴尬局面[4]。
木质纤维素主要由纤维素、半纤维素以及木质素构成,三者通过基团间的化学作用力相互结合在一起的,纤维素被木质素与半纤维素包裹在内部,从而阻碍了纤维素的水解糖化[5-6]。木质纤维素的结构特点决定了木质纤维素必须经过预处理来改变其完整有序的物理结构,以提高其水解性[7]。目前的预处理方法主要分为机械法、物化法、化学法以及生物法[8-9]。其中,蒸汽爆破法(STEX)是当下最常用的预处理方法之一,通过高压水蒸气的瞬间释放从内部破坏木质纤维素的物理结构[10-11]。同时,水在高温下作为酸性催化剂促进半纤维素水解为木糖等单糖[12]。但由于一定温度下水能提供的H+有限,通常需要较高的汽爆温度。而木糖在高温下会进一步分解为糠醛、乙酸等发酵抑制物,会乙醇发酵产生抑制作用[13]。
作者对STEX法进行了改良,在蒸汽爆破预处理前先用低浓度的乙酸对玉米秸秆进行预浸渍。乙酸为有机弱酸,可以提供一定量的H+作为催化剂,使得玉米秸秆中的半纤维素更容易在相对低温的蒸汽爆破条件下水解为单糖或者低聚糖,从而使得被包裹的纤维素暴露出来,达到增强纤维素的酶水解性。同时,减低蒸汽爆破预处理的温度还能减轻木糖等戊糖的进一步降解,减轻糠醛等副产物对后续乙醇发酵的抑制作用,提高玉米秸秆的利用率。目前,木质纤维素原料在蒸汽爆破预处理前进行乙酸预浸渍的研究在国内外还未见报道。
1 实验
1.1 实验材料
所用原料取自中国河北邯郸的玉米秸秆,含水量为19.8%。将其洗净干燥后用锤式破碎机将其粉碎至2~10 mm的小段,在38℃ 烘箱中烘干后取出备用,置于干燥处保存。
1.2 实验设计
1.2.1 预处理 本实验以质量分数为1.0% 的乙酸对玉米秸秆在常温下以固液比为1∶20(g∶mL)先预浸60 min,之后以27 MPa的压力将原料中的水分压至50%。然后在预处理反应器中分别以190℃(1.25 MPa)、200 ℃(1.55 MPa)、210 ℃(1.90 MPa)保持10 min 后,瞬间(小于0.5 s)释放压力。每个温度都设置一个空白对照组(水代替乙酸)。
1.2.2 酶水解 酶水解实验分别以玉米秸秆预处理后的整个草浆(包括液体与固体部分)为底物进行。其中,纤维素酶为Cellic CTec2(诺维信,丹麦),酶用量为每克底物10 FPU,底物浓度为5%,酶水解实验在温度45℃,pH值5的条件下进行96 h。
1.2.3 同步糖化发酵 同步糖化发酵的条件:底物浓度为10%,温度35℃,pH值5.5,发酵时间为96 h;酿酒酵母(Jästbolaget,瑞典)用量为每升发酵液3 g,纤维素酶为Cellic Ctec2,酶用量为每克底物10 FPU;培养液中(NH4)2PO3的浓度为0.5 g/L,MgSO4·7H2O 的浓度为0.025 g/L。
1.3 测定指标与方法
1.3.1 组成成分分析 玉米秸秆组成成分分析以及底物的固形物含量均采用NREL的相关方法进行测定[14]。
1.3.2 纤维素酶活测定 试管中放入1 cm×6 cm Whatman No.l滤纸(约50 mg)一条,加入0.5 mL适当稀释的纤维素酶液和1 mL柠檬酸钠缓冲液(pH值4.8),于50℃保温振荡30 min。空白试验中除酶液事先灭活外,其余条件不变。一个滤纸酶活力单位(FPU)等于酶促反应中每分钟生成1.0 μmol葡萄糖(以还原糖表示)所需的酶量[15]。
1.3.3 糖及抑制物浓度分析 单糖、乙醇以及抑制物用岛津Prominence LC-20AT高效液相色谱进行定量分析,检测器为折光检测器。其中,葡萄糖和木糖等单糖用色谱柱为Aminex HPX-87H(Bio-Rad,Hercules,CA,USA)分离,柱温85℃,以超纯水为流动相,流速0.5 mL/min。乙醇、糠醛、羟甲基糠醛以及乙酸用色谱柱Aminex HPX-87H(Bio-Rad,Hercules,CA,USA)进行分离,柱温为50℃,流动相为0.5 mmol/L的硫酸,流速为0.5 mL/min。HPLC分析前,所有测试样品以0.20 μm的微滤膜过滤。
1.4 计算方法

2 结果与分析
2.1 玉米秸秆预处理后的组成成分分析
实验所用玉米秸秆干物质组成为:纤维素33.6%,半纤维素22.8%,木质素14.1%,抽提物17.4%。其中,抽提物中主要含有的是一些油脂、蛋白质、淀粉等易溶于水或有机溶剂的物质。
按1.2.1节的预处理条件分别在190、200以及210℃ 下经乙酸预浸汽爆预处理10 min及未用乙酸预浸汽爆预处理玉米秸秆的成分分析见表1。可以明显看出,秸秆中的3种主要成分的质量分数发生了较大的变化,纤维素和木质素的质量分数得到了一定程度的提高,而半纤维素则有所下降。随着汽爆预处理温度的提高,各成分的质量分数变化的程度越大。当温度从190℃ 上升至210℃ 时,纤维素的质量分数从58.2% 上升至64.4%;半纤维素则从9.9% 下降至3.2%;而木质素则从26.9% 上升至33.1%。与未经乙酸预浸相比,玉米秸秆经乙酸预浸后,蒸汽爆破预处理对半纤维素的水解更为彻底,纤维素含量提升的程度更大。
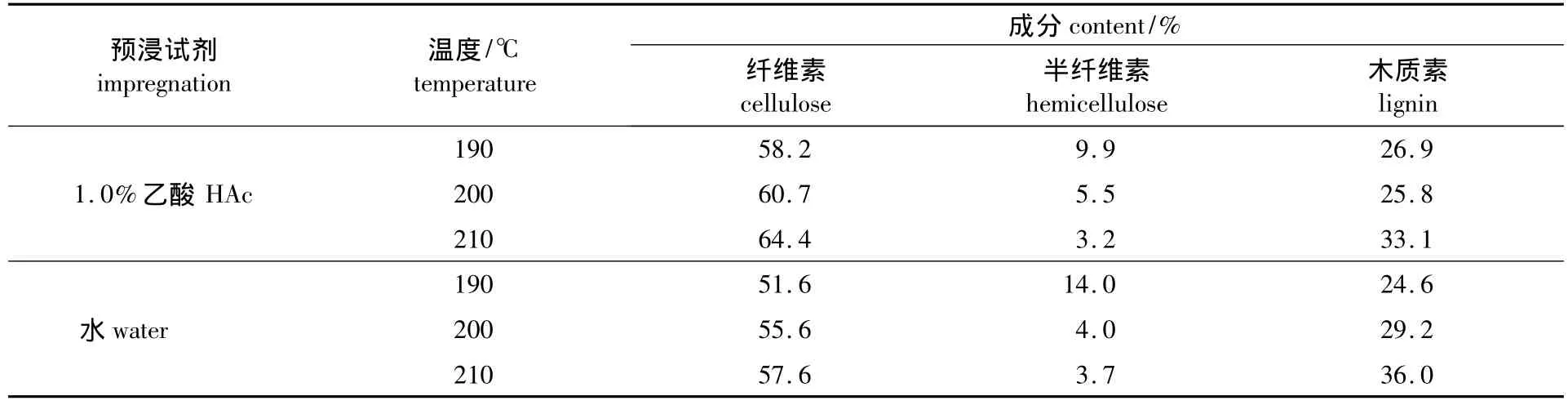
表1 玉米秸秆汽爆预处理后的组成成分分析Table 1 Composition analysis of pretreated corn stover
2.2 玉米秸秆预处理后的纤维素和半纤维素回收率分析
对按1.2.1节的预处理条件预处理后和纤维素和半纤维素回收率进行计算,结果见表2。从表2可以看出,蒸汽爆破预处理前不管是否经过乙酸预浸渍,对秸秆中葡萄糖的回收率几乎没有影响。而其回收率高于100%的原因,可能是秸秆中存在一定的淀粉。对于半纤维素而言,相较纤维素更容易被水解,大部分半纤维素被水解为单糖或低聚糖。随着预处理温度的提高,秸秆中残留的半纤维素越少,液体部分中的木糖回收率逐渐降低,说明温度的升高会促进木糖的进一步分解。乙酸预浸玉米秸秆中的半纤维素在相对低温的条件下更容易在汽爆过程中发生水解。以190℃为例,未经乙酸预浸秸秆中还残留57.3% 的木糖,而乙酸预浸秸秆中仅残留38.7%。此外,从水解液中的木糖回收率来看,前者仅为47.7%,后者为67.8%,说明乙酸预浸更有利于避免木糖的进一步分解。
Linde等[16]以0.2%H2SO4为预浸试剂,在190℃ 下维持10 min后蒸汽爆破,水解液中的木糖产量为75.9%,这说明强酸更有利于半纤维素的水解。

表2 玉米秸秆汽爆预处理后葡萄糖以及木糖回收率分析Table 2 Recovery of glucose and xylose in the solid and liquid fraction of pretreated corn stover
2.3 抑制物分析
图1显示了玉米秸秆预处理后的抑制物糠醛、羟甲基糠醛以及乙酸的生成情况。糠醛和羟甲基糠醛分别来源于木糖和葡萄糖的进一步分解,而乙酸则是由半纤维素侧链上的乙酰基生成。从图1可以看出,相比未经乙酸预浸,玉米秸秆经乙酸预浸汽爆预处理后产生的羟甲基糠醛没有明显增加。由于木糖在酸性条件下更容易继续分解,所以玉米秸秆经乙酸预浸汽爆预处理后产生的乙酸和糠醛的量有一定程度增加。随着预处理温度的提高,抑制物的产量也逐渐增加。当温度从190℃上升至210℃ 时,乙酸产量从每克原料24.1 mg增加至42.6 mg;糠醛则由每克原料 4.7 mg 上升至 13.2 mg。因此,为减少抑制物的生成,提高原料利用率,玉米秸秆更适合以乙酸为预浸试剂在相对较低的温度下进行汽爆预处理。
2.4 酶水解
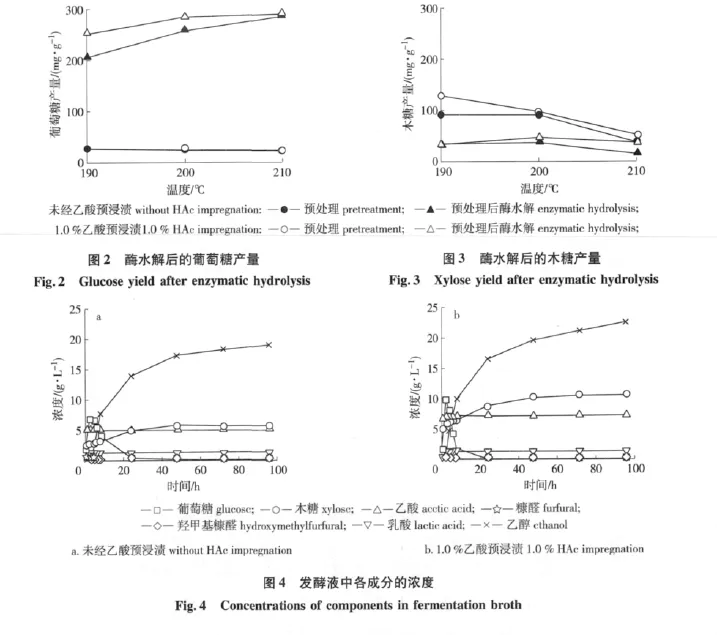
2.4.1 葡萄糖产量分析 从图2可以看出,未经乙酸预浸玉米秸秆分别以190、200以及210℃ 进行汽爆预处理后,酶水解得到的葡萄糖产量分别为每克原料207、258和284 mg,为理论值的55.5%、69.2% 和76.8%。可以看出,相应温度下1.0% 乙酸预浸汽爆玉米秸秆酶水解得到的葡萄糖产量分别为每克原料253、284以及290 mg,为理论值的67.8%、76.8% 和77.7%,均高于相同温度下的未经乙酸预浸玉米秸秆。乙酸预浸汽爆预处理的最佳温度为200℃,与未经乙酸预浸相比提高了10.2%。这可能是因为乙酸预浸汽爆预处理更大程度地增加了秸秆中纤维素的含量,使更多的纤维素暴露出来,增加了与纤维素酶的接触面积。
Varga等[17]采用两步预处理法,先以1% 的NaOH浸泡玉米秸秆,去除秸秆中的木质素;再以1%的H2SO4在120℃下蒸煮1 h后进行酶水解糖化,可以将95.7%的纤维素转化为葡萄糖。这是因为经过两步预处理后,秸秆中的木质素和半纤维素基本被完全去除,剩下的纤维素能够很容易在纤维素酶的作用下水解为葡萄糖。
2.4.2 木糖产量分析 由图3可以看出,未乙酸预浸玉米秸秆分别以190、200以及210℃进行汽爆预处理后,经酶水解获得的木糖产量分别为每克原料35、35和14 mg,为理论值的13.8%、13.8% 和5.5%。相应温度下乙酸预浸汽爆玉米秸秆酶水解得到的木糖产量分别为每克原料33、41和34 mg,为理论值的13.0%、16.2% 和13.4%。由于大部分半纤维素在蒸汽爆破预处理中已被水解为单糖,剩余秸秆固体纤维中只剩下小部分半纤维素。因此,是否经过乙酸预浸对酶水解后的木糖产量影响不大,但乙酸预浸后的总木糖产量更高。
2.5 同步糖化发酵
经过96 h的同步糖化发酵,从图4(a)可以看出,未经乙酸预浸汽爆预处理过的玉米秸秆的同步糖化发酵获得的乙醇浓度为19.0 g/L,相当于每克原料可以获得0.121 g乙醇,为理论值的60.1%。从图4(b)可以看出,以乙酸预浸汽爆预处理过的玉米秸秆草浆为底物进行的发酵并没有受到糠醛等抑制物的影响。发酵进行96 h后的乙醇浓度达到22.5 g/L,相当于每克原料可以获得0.143 g乙醇,为乙醇产率理论值的72%。这说明乙酸预浸可以提高汽爆预处理对玉米秸秆纤维素酶水解性的增强效果,导致更多的纤维素被水解为单糖,进而在发酵过程中被酿酒酵母转化为乙醇。
在Sassner等[18]的研究中,柳树枝经0.5%H2SO4预浸,200℃ 维持8 min汽爆后经过同步糖化发酵获得16 g/L的乙醇,为理论值的78%。虽然该研究获得的乙醇浓度并没有达到本研究的22.5 g/L,但是其乙醇产量却高于本研究的72%,相比未经乙酸预浸过的玉米秸秆,提高了11.9个百分点。究其原因,可能是玉米秸秆的纤维素含量高于柳树枝,酶水解糖化后获得的葡萄糖的量更大,导致其未能充分地被酿酒酵母利用。此外,也有可能是其所用的酵母产乙醇的能力更强。

图1 乙酸预浸前后各抑制物的产量Fig.1 Yields of inhibitors before and after HAc impregnation
3 结论
3.1 与未经乙酸预浸相比,在较低的汽爆温度下,乙酸预浸汽爆预处理玉米秸秆对半纤维素的水解程度更大,并且木糖回收率更高;此外,糠醛等发酵抑制物并没有明显增加。
3.2 综合考虑过程中的能耗以及发酵抑制物等因素,玉米秸秆乙酸预浸汽爆预处理的最佳温度为200℃。酶水解后每克原料葡萄糖产量为284 mg,相比未经乙酸预浸玉米秸秆提高了10.2%,为理论值的76.8%;由于大部分半纤维素已经在预处理过程中被水解,所以是否经过乙酸预浸渍对酶水解木糖产量的影响并不大。但是乙酸预浸可以获得更高的木糖总产量。
3.3 乙酸预浸玉米秸秆在200℃ 下汽爆预处理后的同步糖化发酵效果较好,经过96 h发酵,乙醇浓度达到22.5 g/L,为理论值的72%,相比未经乙酸预浸过的玉米秸秆,提高了11.9个百分点。说明乙酸预浸可以增强蒸汽爆破对玉米秸秆的预处理效果,提高原料利用率。
[1]任普鲜,蒋剑春,杨秀山.木质纤维素快速热解产物生产燃料乙醇研究进展[J].生物质化学工程,2009,43(3):47-51.
[2]BRIDGWATER A V.Catalysis in thermal biomass conversion[J].Applied Catalysis(A):Gen,1994,116:45-47.
[3]YANG Hai-ping,CENG Han-ping,WANG Xian-hua,et al.Progress of study on biomass pyrolysis[J].Gas & Heat,2006,26(5):18.
[4]HAHN B,GALBE M,GORWA M F,et al.Bio-ethanol:the fuel of tomorrow from the residues of today[J].Trends Biotechnol,2006,24:549-556.
[5]余世袁.植物纤维制备燃料乙醇的关键技术[J].生物质化学工程,2006,40(增刊):8-12.
[6]MOSIER N,WYMAN C,DALE B,et al.Features of promising technologies for pretreatment of lignocellulosic biomass[J].Bioresour Technol,2005,96:673-686.
[7]YANG Chang-jun,WANG Qin,ZHANG Guang-yue.Research progress in pretreatment techniques of lignocellulose[J].Liquor-making Science& Technology,2008(3):85-89.
[8]王堃,蒋建新,宋先亮.蒸汽爆破预处理木质纤维素及其生物转化研究进展[J].生物质化学工程,2006,40(6):37-42.
[9]GALBE M,ZACCHI G.Pretreatment of lignocellulosic materials for efficient bioethanol production[J].Adv Biochem Eng Biotechnol 2007,108:41-65.
[10]LI Da,ZHANG Xue,NIU Chun-hua.Advances in pretreatment technology of lignocellulose biomass[J].Academic Periodical of Farm Products Processing,2008(4):7-9.
[11]BALAT M,BALAT H,OZ C.Progress in bioethanol processing[J].Progress in Energy and Combustion Science,2009,34:551-573.
[12]TUCKE M P,KIM K H,NEWMAN M M.Effects of temperature and moisture on dilute-acid steam explosion pretreatment of corn stover and cellulase enzyme digestibility[J].Applied Biochemistry and Biotechnology,2003,105:165-177.
[13]KLINKE H B,THOMSEN A B,AHRING B K.Inhibition of ethanol-producing yeast and bacteria by degradation products produced during pretreatment of biomass[J].Applied Microbiology and Biotechnology,2004,66(1):10-26.
[14]SLUITER A,HAMES B,RUIZ R.Determination of structural carbohydrates and lignin in biomass[R].USA:National Renewable Energy Laboratory,2011.
[15]陈明.利用玉米秸秆制取燃料乙醇的关键技术研究[D].杭州:浙江大学博士学位论文,2007.
[16]LINDLE M,JAKOBSSON E L,GALBE M,et al.Steam pretreatment of dilute H2SO4-impregnated wheat straw and SSF with low yeast and enzyme loadings for bioethanol production[J].Biomass and Bioenergy,2008,32:326-332.
[17]VARGA E,SZENGYEL Z,RECZEY K.Chemical pretreatments of corn stover for enhancing enzymatic digestibility[J].Applied Biochemistry and Biotechnology,2002,98(100):73-87.
[18]SASSNER P,MARTENSSON C G,GALBE M,et al.Steam pretreatment of H2SO4-impregnated salix for the production of bioethanol[J].Bioresource Technology,2008,99:137-145.
