HPLC法同时测定龙血竭片中龙血素A和白藜芦醇
2013-09-17程维明杨晓洁黄琴伟陈慧敏张文婷
程维明, 杨晓洁, 施 贝, 黄琴伟, 陈慧敏, 张文婷*
(1.浙江省食品药品检验所,浙江杭州310004;2.浙江工业大学,浙江杭州310014)
龙血竭为龙舌兰科植物剑叶龙血树Dracaena cochinchinensis(Lour.)S.H.Chen的含脂木质部经提取加工制成的树脂,具有活血散瘀、消炎止痛、收敛止血、生肌敛疮、补血益气等功效[1-4],收载于《国家药品监督管理局药品标准》新药转正第二十二分册,在临床上用于治疗外科、妇科、内科、皮肤科等多种适应症[5],是名贵中药材之一。龙血竭片系龙血竭药材研细后加入适量辅料直接压片而成的,收载于国家中成药标准汇编内科气血津液分册,主要含黄酮类、芪类、甾醇类和皂苷类化合物等成分[6],其中龙血素A(loureirin A)和白藜芦醇 (resveratrol)等为主要活性成分,是其活血散瘀、生肌敛疮和补血益气等功效的物质基础,现代药理学研究也证实其均具有丰富的生物活性[7-10]。本实验采用高效液相色谱法,同时测定龙血竭片中龙血素A和白藜芦醇的量,该方法简便、准确、重复性好,可作为龙血竭片的质量控制方法研究。
1 仪器与试药
Agilent LC1200液相色谱仪 (美国安捷伦公司,配四元泵、智能柱温箱、自动进样器、VMD可变波长检测器),电子天平 (瑞士Metter公司,AE-163),超声波清洗器 (上海波龙公司,USC-802),高速冷冻离心机 (美国艾本德公司,Centriguge),所用仪器和量具均经校正和检定。
龙血素A和白藜芦醇对照品均购自中国药品生物制品检定所,批号分别为111660-200402、111535-200502;龙血竭片购自云南大唐汉方制药有限公司,批号为20120305;乙腈为色谱纯;水为超纯水;其余试剂为分析纯。
2 方法和结果
2.1 对照品溶液的制备
分别精密称取经五氧化二磷减压干燥24 h的龙血素A和白藜芦醇对照品适量,置于50.0 mL量瓶中,加乙腈溶解,并稀释至刻度,摇匀,制得各对照品贮备溶液。再分别精密量取1.0 mL龙血素A和白藜芦醇对照品贮备溶液置于5.0 mL量瓶中,用乙腈稀释至刻度,摇匀,配成质量浓度分别为21.24和23.24μg/mL的对照品混合溶液。
2.2 供试品溶液的制备
取龙血竭片20片,精密称定,研细,过4号筛,精密称约0.2 g,置50 mL量瓶中,加硅藻土0.1 g,混匀,加1%冰醋酸溶液-乙腈 (1∶1)混合溶液,超声处理15 min,放冷,定容,摇匀,取适量离心,即得供试品溶液。
2.3 色谱条件
Agilent Zorbax SB-C18色谱柱 (250 mm×4.6 mm,5μm);流动相为乙腈 (A)-1%冰醋酸(B)梯度洗脱 (0~55 min,20% ~45%A),体积流量1.0 mL/min;检测波长260 nm;进样量10 μL;柱温35℃。在上述色谱条件下,龙血素A和白藜芦醇的保留时间分别是50.7 min和14.8 min。见图1。
2.4 线性关系考察

图1 对照品 (A)和供试品 (B)色谱图Fig.1 HPLC chromatographs of reference substances(A)and sam p le(B)
取2.1项下制备的混合对照品溶液,按2.3项下色谱条件分别进样 1、2、5、10、15、20、30 μL测定,测定峰面积,将不同峰面积对各对照品进样量做线性回归,得回归方程,龙血素A为y=2 400.5x+17.44(r2=0.999 1);白藜芦醇为y=873.75x+6.45(r2=0.999 8)。结果表明,龙血素A和白藜芦醇分别在0.02~0.64μg和0.02~0.70μg内呈良好的线性关系。
2.5 精密度试验
取2.1项下制备的混合对照品溶液,按2.3项下色谱条件,连续进样6次,记录龙血素A和白藜芦醇的峰面积积分值,并计算它们的RSD值,分别为0.3%、0.3%,结果表明方法的精密度良好,符合方法学要求。
2.6 重复性试验
取同一份批号的龙血竭片6份,按2.2项下的方法制备供试品溶液,于2.3项色谱条件下测定,结果表明龙血素A的RSD为0.5%,白藜芦醇的RSD为0.6%,说明表明该方法的精密度良好,符合方法学要求。
2.7 稳定性试验
取同一份供试品溶液分别于0、1、2、4、8、12、24、48 h在2.3项色谱条件下进样测定,记录各对照品峰面积,结果表明龙血素A的RSD为1.8%,白藜芦醇的RSD为1.4%,说明供试品溶液在48 h内较稳定。
2.8 加样回收率试验
精密称取已知龙血素A和白藜芦醇量的供试品6份,分别精密加入龙血素A和白藜芦醇的对照品适量,按2.2项制备供试品溶液后测定,结果见表1。
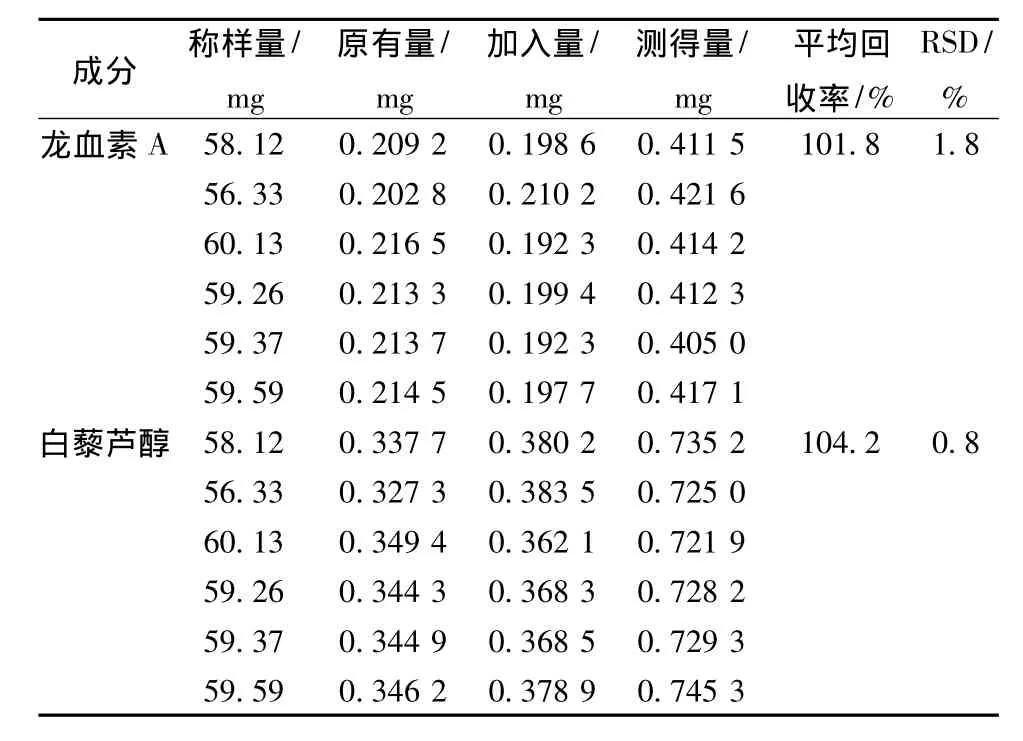
表1 加样回收率试验(n=6)Tab.1 Results of average revovery tests(n=6)
2.9 样品测定
各批号龙血竭片分别取3份,研细后,精密称取适量龙血竭粉末,按2.1项下方法制备供试品溶液,并在2.3项色谱条件下测定峰面积,结果见表2。

表2 样品测定结果Tab.2 Content determination of loureirin A and resveratrol in Longxuejie Tablets
3 讨论
实验中比较了不同柱温 (20℃、35℃、40℃)对这3种组分的分离效果的影响,结果表明,随着柱温的升高,各组分保留时间缩短,分离度基本保持一致,但为了保护柱子,延长使用寿命,最终确定柱温为35℃。
考察了回流提取和超声提取两种方法制备供试品溶液,实验结果无明显差异,但由于超声提取法具有效率高,操作简便等优点,所以采用超声提取法。在提取溶剂的选择上,分别考察了甲醇和1%冰醋酸溶液-乙腈 (1∶1)混合溶液提取,发现在相同条件下用后者提取所得的峰面积稍大,说明该溶剂提取效率稍好,故选用。同时,在用1%冰醋酸溶液-乙腈 (1∶1)混合溶液提取时,对不同超声时间 (10、15、25、30 min)进行了比较,结合指标成分的量,最终确定用1%冰醋酸溶液-乙腈 (1∶1)混合溶液在室温下超声提取15 min作为样品的处理方法。
考虑到不同色谱柱吸附性能等的差异,在耐受性试验中比较了Agilent Zorbax SB-C18(250 mm×4.6 mm,5μm)、Kromasil 100-5C18(250 mm ×4.6 mm)和 Extend-C18(250 mm×4.6 mm,5μm)3种色谱柱的分离效果,根据图谱的分离效果,选择了 Agilent Zorbax SB-C18进行深入的方法学考察研究。
[1]向金莲,程 睿,张路晗.血竭的活血和止血作用研究[J].华西药学杂志,2000,15(6):430-431.
[2]向金莲,张路晗,程 睿,等.血竭消炎止痛作用研究[J].时珍国医国药,2001,12(2):110-111.
[3]农兴旭.广西血竭的止血作用[J].中国中药杂志,1997,22(4):240242.
[4]陈德利,高青云,施伟民,等.中药中活血化瘀药对皮肤创伤愈合的影响[J].上海医学,2000,23(3):145-147.
[5]文东旭.龙血竭的研究进展[J].中草药,2001,11(32):1053-1054.
[6]陈军霞,邱碧菡,潘林梅,等.血竭的现代研究[J].现代中药研究与实践,2011,25(3):81-84.
[7]张天宝,吕敬慈,雍克岚,等.广西龙血竭中几种化学成分对血小板聚集影响的初步研究[J].天然产物研究与开发,2008,20:695-697.
[8]Wang S T,Chen S,Guo M,et al.Inhibitory effect of cochinchinenin B on capsaicin-activated responses in rat dorsal root ganglion neurons[J].Brain Res,2008,12(1):34-40.
[9]胡迎庆,屠鹏飞,李若瑜.剑叶龙血树中芪类化合物及其抗真菌活性的研究[J].中草药,2001,32(2):104-106.
[10]刘兆平,于 波.白藜芦醇的雌激素样作用研究[J].卫生研究,2002,31(3):188-190.
