不同剂量右美托咪定对全麻食道癌患者术后苏醒期的影响
2013-09-16汪延斌冯宇峰林梁
汪延斌 冯宇峰 林梁
不同剂量右美托咪定对全麻食道癌患者术后苏醒期的影响
汪延斌 冯宇峰 林梁
目的 观察不同剂量右美托咪定(Dexmedetomidine,Dex)用于食道癌患者全麻手术后苏醒期的影响。方法 选择开胸食道癌根治术患者120例,ASA I~Ⅱ级,随机双盲分为4组(n=30):D1组(Dex负荷剂量:0.6 μg/kg);D2组(Dex负荷剂量:0.6 μg/kg,维持剂量为 0.2 μg/(kg·h);D3组(Dex负荷剂量:0.8 μg/kg,维持剂量为 0.2 μg/(kg·h);C组(对照组泵注同等剂量的0.9%NS);插管成功后进行间歇正压通气,手术切皮前10 min开始泵注各组负荷剂量,15 min泵注完毕。记录四组患者入PACU时(T0)、拔管前(T1)、拔管后1 min(T2)、拔管后5 min(T3)和拔管后10 min(T4)的HR、MAP 和拔管时间;观察记录患者术中不良反应、在PACU时的Ramsay镇静及呛咳评分。结果 在T1~T4时点,C组的MAP、HR和明显高于D1、D2和D3组(P<0.05);Ramsay评分C组明显低于D1、D2和D3组(P<0.05),而在呛咳评分和躁动,C组明显高于D1、D2和D3组(P<0.05);C组和D1组在手术中低血压发生率和拔管时间上明显低于D2和D3组(P<0.05);D3组高血压发生率明显高于C组、D1组和D2组(P<0.05)。结论 术前单次泵注Dex负荷剂量0.6 μg/kg用于食道癌根治术患者,不仅提供有效的镇静、镇痛辅助,术中血流动力学平稳,不影响拔管时间且不良反应少。
右美托咪定;血流动力学;麻醉,全身;食管癌
食道癌根治手术创伤大,麻醉苏醒期患者因伤口剧烈疼痛可引起躁动、BP增高及HR加快,增加了发生并发症的风险。右美托咪定(Dexmedetomidine, Dex) 是一种新型的强效高选择性α2-肾上腺素能受体(α2-AR)激动剂,具有镇静、镇痛、抗焦虑、无呼吸抑制等优点,受到临床关注。作者将不同剂量的Dex用于全麻下食道癌根治术的患者,旨在评价Dex在此类手术后苏醒期间镇静、镇痛、抗焦虑的效果,并为临床应用Dex寻找最佳剂量。现报告如下。
1 资料与方法
1.1 一般资料 选择120例本院2012年1月至2013年05月择期全麻下行开胸食道癌根治术患者,ASAⅠ~Ⅱ级,男性78例,女性42例,年龄42~71岁,体重51~85 kg,身高 155~178 cm。随机双盲分为4组(n=30):D1组(Dex负荷剂量:0.6 μg/kg,15 min,泵注完毕);D2组(Dex负荷剂量:0.6 μg/kg,15 min。泵注完毕,维持剂量为 0.2 μg/(kg·h);D3组(Dex负荷剂量:0.8 μg/kg,15 min。泵注完毕,维持剂量为 0.2 μg/(kg·h);C组(对照组,泵注同等剂量的0.9%NS)。Dex为江苏恒瑞医药股份有限公司提供,批号:国药准字 H20090248。患者术前均无心动过缓、心脏传导阻滞、严重心肺肝肾功能异常及精神功能障碍。
1.2 麻醉方法 所有患者术前常规禁食,未使用术前药;入室常规监测SBP、DBP、MAP、HR、SpO2、ECG;局麻下行桡动脉和颈内静脉穿刺置管。麻醉诱导:咪达唑仑0.3 mg/kg、芬太尼0.2~0.5μg/kg、顺式阿曲库铵0.15 mg/kg、依托咪酯0.3 mg/kg静脉推注,5 min后经口置入双腔支气管导管,纤维支气管镜定位后接麻醉机行IPPV。麻醉维持:术中持续泵注竞安、瑞芬太尼,酌情静脉注射顺式阿曲库铵维持肌松。手术切皮前10 min开始泵注负荷剂量药物。关胸时静注芬太尼1.5 μg/kg。术毕将患者带气管导管送PACU观察,常规拮抗,酌情给予患者语言或轻微触动刺激。当患者自主呼吸潮气量>6 ml/kg,呼吸频率>10bpm,吸氧SpO2>95%,对指令有应答时,清除口咽腔分泌物后拔出气管导管。生命体征平稳,安全送回病房。
1.3 术中及在PACU观察指标 ①记录四组患者入PACU时的(T0)、拔管前(T1)、拔管后1 min(T2)、拔管后5 min(T3)和拔管后10 min(T4)的HR、MAP 和拔管时间。②Ramsay镇静评分:1分—焦虑,易激惹,烦躁;2分—睁眼、安静、合作、定向好;3分—仅对命令、轻触、正常声音有反应;4分—轻拍眉间或耳边大声刺激有迅速反应;5分—轻拍眉间或耳边大声刺激反应迟钝;6分—轻拍眉间或耳边大声刺激无反应。③呛咳评分:1分—无呛咳或仅在拔管时有呛咳;2分—恢复规律的自主呼吸,气管导管在位时即有呛咳;3分—患者在未恢复规律的自主呼吸时即有呛咳。④躁动评分:0分—安静、合作;1分—轻度烦躁,吸痰刺激时有肢体活动,间断呻吟;2分—无刺激时即有躁动,持续呻吟;3分—剧烈挣扎及喊叫,需外力按压四肢。

2 结果
2.1 四组患者一般情况:年龄、体重、性别、ASA分级、麻醉时间和手术时间,无统计学差异(P>0.05)。
2.2 四组患者麻醉苏醒时MAP和HR变化:T0时,各组MAP、HR差异无统计学意义(P>0.05),T0点MAP、HR明显小于T1~4时点(P<0.05);在T1~4时点,C组的MAP、HR明显高于D1、D2和D3组(P<0.05),D1组MAP、HR在T1~4时点略大于D2和D3组,但差异无统计学意义,见表1。
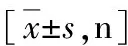
表1 四组患者苏醒期MAP、HR的比较
注:与T0时点比较,*P<0.05
2.3 四组患者拔管时间比较 C组和D1组明显短于D2和D3组(P<0.05),C组与D1组之间差异无统计学意义(P>0.05);镇静评分比较:C组明显低于D各组(P<0.05);呛咳评分和躁动比较:C组明显高于D各组(P<0.05)。见表3。
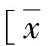
表3 四组患者拔管时间、镇静评分、呛咳评分、躁动比较±s,n=30]
注:与其他组比较,*P<0.05
2.4 四组患者不良反应比较 四组患者口干的发生率差异无统计学意义(χ2:5.49,P:0.139);术中高BP发生率:C组(1例)、 D1组(2例) 和D2组(3例)明显少于D3组(8例),差异有统计学意义(χ2:9.380,P:0.025);低BP发生率:C组(0例)和D1组(2例)明显少于D2组(5例)和D3组(6例),差异有统计学意义(χ2:7.850,P:0.049);术中窦性心动过缓的发生率:四组患者比较差异无统计学意义(χ2:3.405,P:0.333)。
3 讨论
麻醉苏醒期间,由于全身镇痛、镇静药物逐步消退,患者意识、痛觉和生理反射的恢复,对突如其来的机体和心理上的刺激难以耐受,引起交感兴奋和精神状态异常。而食道癌根治手术患者病情复杂、创伤较大,术前精神压力大,麻醉苏醒期疼痛剧烈,血流动力学变化大,更易增加术后恢复期并发症的发生和精神状态的异常。
Dex是高选择性α2-AR激动剂。蓝斑是中枢神经系统里α2-AR高度集中的区域,Dex通过激动蓝斑中的α2受体[1],抑制腺苷酸环化酶,减少cAMP生成,抑制了去甲肾上腺素的释放[2],从而调节抑制性γ-氨基丁酸(GABA)相关神经递质促睡眠通路,进而起到了镇静和抗焦虑作用。使用Dex镇静后,患者睡眠似自然睡眠,其脑电图表现和2期慢波睡眠类似,易被唤醒,配合度好,且不容易出现定向力障碍[3]。Dex半衰期为2 h左右,镇静作用呈剂量依赖性关系[4],单次输注0.25 μg/kg就能镇静2 h,2 μg/kg的镇静效应可达3 h以上[5]。本组资料中,Dex组Ramsay镇静评分明显高于C组,躁动发生率明显低于C组,而单次输注负荷剂量0.6 μg/kg D1组镇静评分和躁动发生率与有持续输注D2、D3组差异无统计学意义。Dex镇静程度与其使用剂量和时间正相关[6]。本研究C组和D1组未使用或使用少量的Dex,拔管时间明显短于持续泵注Dex的D2、D3组,也证实了长时间泵注有可能导致镇静过度而影响气管拔管[7]。
Dex在外周通过激动脊髓α2受体并抑制P物质的释放,还可对外周神经的C纤维和Aα纤维直接阻滞[8],从而达到镇痛抗伤害作用,因此,Dex可以和阿片类镇痛药产生协同作用,并可以减少其使用量[9],可减少使用阿片类药物30%左右[10]。本组资料C组患者在麻醉苏醒期血流动力学变化明显大于使用Dex组,呛咳的发生率明显高于使用Dex组。与Dex通过中枢神经系统的α2-AR激动,抑制了去甲肾上腺素的释放,抑制了神经系统的交感活性有关。
Dex对BP的影响是双向性的,静注Dex可先直接激活血管平滑肌中的α2-AR,使血管收缩,BP升高;继而,作用于中枢受体,抑制交感活性,使BP降低,HR减慢,中枢效用占主导地位[11]。本组资料显示:术中D3组发生短暂性高BP的例数大于其他各组;D2、D3组发生低BP和窦性心动过缓明显高于D1、C组。进一步说明,较大剂量、短时间输注Dex,可引起BP短暂性的升高,而持续泵注可产生抑制交感神经活性和增加迷走神经活性的作用[12]。
综上所述,在食道癌根治术中,术前Dex负荷剂量0.6 μg/kg15 min泵注完毕,可提供有效的镇静、镇痛辅助,术中血流动力学平稳,不影响拔管时间,术中和苏醒期不良反应少,是值得推荐的临床用药剂量。
[1] Okawa K, Ichinohe T, Kaneko Y. A comparison of propofol and dexmedetomidine for intravenous sedation: a randomized, crossover study of the effects on the central and autonomic nervous systems. Anesth Analg, 2010, 110(2):415-418.
[2] Chen BS,Peng H,Wu SN.Dexmedetomidine,an α2-adrenergic agonist,inhibits neuronal delayed-rectifier potassium current and sodium current.Br J Anaesth, 2009, 103 (2):244-254.
[3] Huupponen E,Maksimow A,Lapinlampi P,et al. Electroencephalogram spindle activity during dexmedetomidine sedation and physiological sleep. Acta Anaesthesiol Scand,2008,52(2):289-294.
[4] Angst MS,Ramaswamy B,Davies MF,et al. Comparative analgesic and mental effects of increasing plasma concentrations of dexmedetomidine and alfentanil in humans. Anesthesiology, 2004,101(3):744-752.
[5] Pypendop BH,Barter LS,Stanley SD,et al. Hemodynamic effects of dexmedetomidine in isoflurane-anesthetized cats.Vet Anaesth Analg, 2011, 38(6):555-567.
[6] Turgut N,Turkmen A,Gokkaya S,et al. Dexmedetomidine-based versus fentanyl-based total intravenous anesthesia for lumbar laminectomy. Minerva Anestesiol, 2008,74(9):469-74.
[7] Su F,Hammer GB. Dexmedetomidine: pediatric pharmacology,clinical uses and safety.Expert Opin Drug Saf, 2011,10 (1):55-66.
[8] Arain SR,Ruehlow RM,Uhrich TD,et al. The efficacy of dexmedetomidine versus morphine for postoperative analgesia after major inpatient surgery. Anesth Analg, 2004, 98(1):153-158.
[9] Dave J, Vaghela S. A comparison of the sedative,hemodynamic,and respiratory effects of dexmedetomidine and propofol in children undergoing magnetic resonance imaging. Saudi J Anaesth, 2011,5(3):295-9.
[10] Ngwenyama NE,Aanderson J,Hoernschemeyer DG, et al. Effects of dexmedetomidine on propofol and remifentanil infusion rates during total intravenous anesthesia for spine surgery in adolescents.Paediatr Anaesth,2008,18 (12):1190-1195.
[11] Norimasa O, Kotaro K, Kazuhiro S, et al. Recovery profiles from dexmedetomidine as a general anesthetic adjuvant in patients undergoing lower abdominal surgery. Anesth Analg, 2008,107(6):1871-1874.
[12] Saringcarinkul A,Punjasawadwong Y,Kongtonkul N,et al. Effect of Dexmedetomidine on hemodynamic responses during induction period,skull-pin application and skin incision in patients undergoing craniotomy. Eur J Anaesthesiol Suppl,2012,49: S1.
Clinical efficiency of dexmedetomidine with different doses during revival period of postoperative esophagus cancer in patients with general anesthesia
WANGYan-bin,FENGYu-feng,LINLang.
DepartmentofAnesthesiology,TheFirstAffiliatedHospitalofXiamenUniversity,Xiamen361003,China
Objective To observe the effects of dexmedetomidine (Dex) with different doses during revival period of postoperative esophagus cancer in patients with general anesthesia.Methods 120 patients, ASA grade I~II, undergoing radical resection of esophageal carcinoma under general anesthesia were randomly allocated to four groups with 30 cases each. Group D1, group D2, group D3and group C were respectively administered with Dex 0.6, 0.6, 0.8 μg/kg or 0.9% normal saline by micro-pump finished in 15 minutes before operation. Group D2and group D3kept injection the Dex at 0.2 μg/(kg·h) until operation finished. MAP, HR and Ramsay scores were monitored and recorded at the time points of just to the PACU (T0), before extubation (T1), after extubation 1 min (T2), after extubation 5 min (T3) and after extubation 10 min (T4). The extubation time and the incidences of adverse effects were observed and recorded. Results The values of MAP, HR at T1~T4, bucking scores and restlessness in group C were significantly higher than those in each group D(P<0.05). Ramsay scores in group C were lower than that in group D(P<0.05).The extubation time and the incidences of hypotension in group C and group D1were found significantly higher than those in group D2and group D3(P<0.05). The incidences of hypertension in group D3were significantly higher than that in others(P<0.05).Conclusion The single 0.6 μg/kg dose of Dex in 15 min used in patients with esophageal cancer by micro-pump before operation. It can provide obvious sedation, may keep stable perioperative hemodynamics and minimize the adverse effects without prolong the extubation time and recovery time.
Dexmedetomidine;Hemodynamics;Anesthesia, General;Esophagus cancer
361003厦门大学附属第一医院麻醉科
林梁
