CuZnAl催化剂甲醇水蒸气重整制氢催化性能研究
2013-09-15张文斌陈晓蓉
张文斌,梅 华,陈晓蓉,周 文
(1.南京工业大学化学化工学院,南京210009;2.防化研究院)
氢气除用作合成氨、石油炼制加氢装置的原料外,还广泛应用于冶金、精细化工、电子和浮法玻璃等行业[1-2]。天然气蒸汽转化制氢通常适合对氢需求量较大的用户;烃类蒸汽转化装置的工艺复杂,投资大,能耗高;电解水法制氢的能耗和生产成本较高;甲醇制氢技术的原料易得、工艺流程短、设备简单、投资和能耗低,制氢成本较低,适用于中小规模用氢企业[3-5]。此外,甲醇的氢含量高,运输和储存方便,因此成为车载制氢的理想燃料[6-8]。甲醇水蒸气重整制氢是甲醇制氢的主要方式,产品气中氢气含量高(约75%),反应条件温和(200~300 ℃)[9-11]。
常用的甲醇水蒸气重整制氢催化剂为Cu基催化剂。该类催化剂的低温活性高、选择性好、便宜易得[12-16]。甲醇制氢产品气提纯主要采用变压吸附技术(PSA),操作压力为1~2MPa,因此,工业上甲醇制氢操作压力为1MPa,产品气在进入变压吸附装置之前不需要进行增压[17]。本课题采用共沉淀法制备一系列CuZn和CuZnAl催化剂,通过BET,XRD,H2-TPR等技术表征催化剂的物化性质与还原性能,并在固定床反应器中对催化剂催化甲醇水蒸气重整制氢性能进行评价,考察催化剂中引入Al以及Cu/Zn比对催化反应活性的影响。
1 实 验
1.1 原料及仪器
硝酸铜,分析纯,上海新宝精细化工厂生产;硝酸锌,分析纯,西陇化工股份有限公司生产;硝酸铝,分析纯,上海新宝精细化工厂生产;无水碳酸钠,分析纯,上海凌峰化学试剂有限公司生产;甲醇,工业级,市售;氢气、氮气、氦气(纯度不小于99.99%),南京天泽气体有限公司生产。
D8AD-VANCE X射线衍射仪,德国Bruker公司生产;BelsorpⅡ吸附仪,荷兰Ankersmid公司生产;FEI QUANTA200扫描电镜,Philips公司生产;BELCAT-A型多用吸附仪,荷兰Ankersmid公司生产;GC-2014气相色谱仪,日本岛津公司生产;固定床反应器,自制;高压恒流泵,上海伍丰精密仪器有限公司生产。
1.2 催化剂的制备与表征
所有催化剂均采用共沉淀法制备。将配置好的Cu(NO3)2·3H2O,Zn(NO3)2·6H2O,Al(NO3)3·9H2O混合溶液置于一个分液漏斗中,将Na2CO3溶液置于另一个分液漏斗中,在不断搅拌下将两者并流滴加到三口烧瓶中,调节pH为7,控制温度为70℃,沉淀结束后搅拌老化2h,滤饼经过滤、洗涤、110℃隔夜烘干,在450℃下焙烧3h后制得CuZn或CuZnAl催化剂。CuZnAl催化剂按其所含氧化物质量分数命名,例如,Cu50Zn40Al10催化剂表示CuO,ZnO,Al2O3的质量分数分别为50%,40%,10%;Cu50Zn40催化剂表示 CuO 与ZnO的质量比为50∶40。
采用D8AD-VANCE X射线衍射仪分析样品物相,CuKα辐射,工作电压和电流分别为40kV和40mA,扫描范围2θ为10°~80°。在BelsorpⅡ吸附仪上采用N2吸附法测定催化剂的BET比表面积与孔体积,样品在测试之前先要在200℃下真空干燥5h,然后在液氮温度下吸附。采用FEI QUANTA200扫描电镜观察催化剂的表面形貌。H2程序升温还原在BELCAT-A型仪器上完成,将60mg催化剂在流动N2中于400℃下处理1 h,然后降至室温,切换为在10%H2/N2混合气中以10℃/min程序升温至400℃。Cu有效比表面积采用N2O脉冲吸附法测定,使用BELCAT-A型多用吸附仪,将200mg催化剂在流动He中于400℃下处理1h,并在250℃下10%H2/N2混合气中还原4h,然后切换为He吹扫0.5h以去除吸附的H2,再在50℃下用N2O脉冲吸附。采用催化剂表面形成的N2总量计算N2O吸附量,进而计算催化剂表面的Cu有效比表面积,反应方程式[18]如下:

1.3 催化剂活性评价
催化剂活性评价实验在固定床连续流动装置中进行,反应压力为0~1.5MPa。将10g催化剂置于固定床反应器恒温段,用N2置换系统内空气后,以120mL/min通入H2,以10℃/min升温至250℃,恒温还原5h。还原结束后关掉H2,使用高压恒流泵输入甲醇水溶液(n(H2O)/n(CH3OH)=1.5),VHSV(体积空速)=0.56h-1,将催化剂床层温度调至目标温度(220~250℃),压力调为设定压力,反应稳定2h后取样分析。产品气体采用岛津GC-2014气相色谱仪(TCD,色谱柱为5A分子筛)进行在线分析,以He为载气;液相产物采用岛津GC-2014气相色谱仪(FID)进行定量分析,柱温为60℃,进样口和检测器温度均为230℃。
2 结果与讨论
2.1 催化剂表征
表1列出了催化剂的比表面积、孔体积和Cu有效比表面积。从表1可以看出,将10%的Al2O3引入到Cu50Zn40催化剂中可以提高催化剂的比表面积。这主要是因为Al2O3的比表面积较大。此外,CuZnAl催化剂的比表面积还受CuO含量影响,在本实验考察范围内,比表面积先随CuO含量升高而升高,而当CuO含量达到60%之后,由于CuO在催化剂表面发生烧结,导致催化剂的比表面积急剧下降;催化剂表面的Cu有效比表面积随着CuO含量的变化显示出相同的规律。由Cu50Zn40和Cu50Zn40Al10的Cu有效比表面积可以看出,添加10% 的Al2O3可以提高Cu有效比表面积。
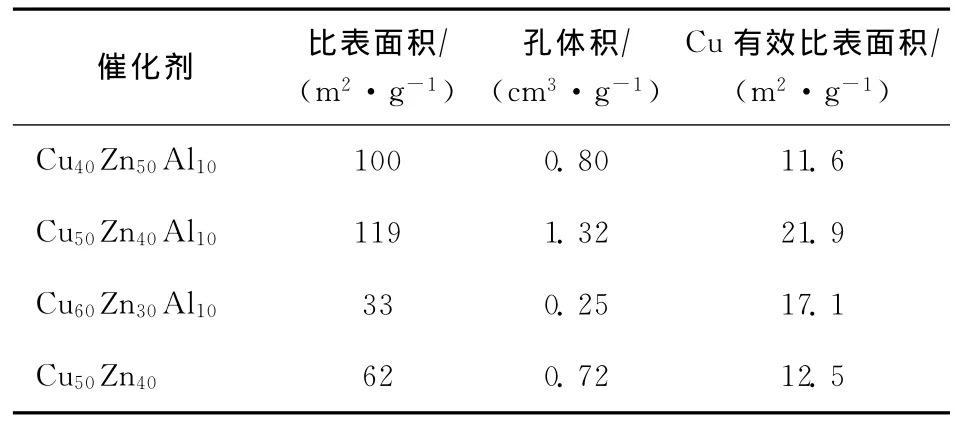
表1 CuZnAl催化剂的物化性质
图1为催化剂的XRD谱。由图1可以看出:对于Cu50Zn40催化剂,CuO的特征衍射峰在2θ为35.5°,38.7°,48.8°处,ZnO的主要特征衍射峰位于2θ为 32.8°,34.3°,36.1°处,且 峰 形 尖 锐;CuZnAl催化剂中CuO特征衍射峰随CuO含量的升高而逐渐尖锐,而ZnO特征衍射峰逐渐变弱和宽泛;向CuZn催化剂中引入Al可抑制CuO和ZnO晶体的生长,有利于CuO和ZnO在催化剂表面的分散;在所有CuZnAl催化剂的XRD谱中均没有观察到Al2O3衍射峰,这可能是由于Al2O3含量低,未达到其衍射阙值或者以无定形形式存在的缘故。
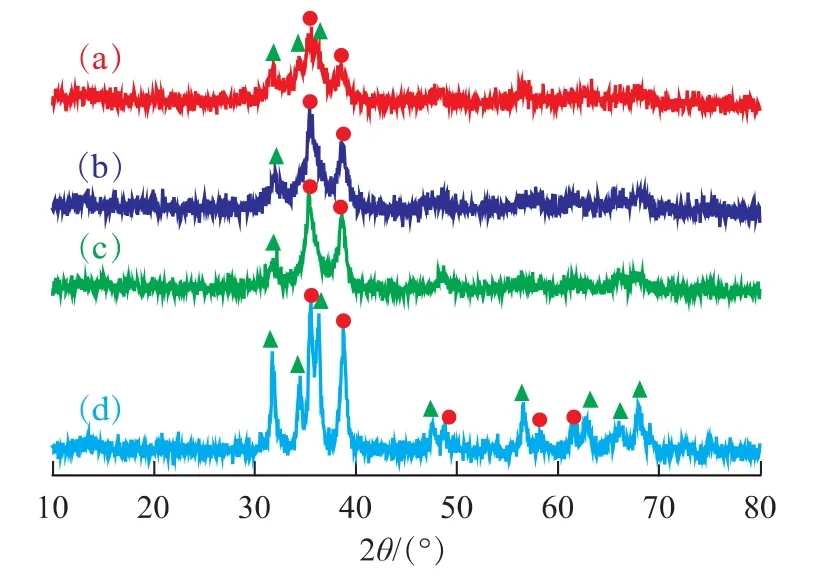
图1 催化剂的XRD谱▲—ZnO;●—CuO。(a)—Cu40Zn50Al10;(b)—Cu50Zn40Al10;(c)—Cu60Zn30Al10;(d)—Cu50Zn40
图2为催化剂的H2-TPR曲线。由图2可以看出:Cu50Zn40催化剂还原峰顶温度为240℃;当Al被引入到CuZn催化剂中时,使CuO晶粒变得更稳定,提高了还原温度,Cu40Zn50Al10的还原峰顶温度升高到250℃,Cu50Zn40Al10催化剂的还原峰顶温度升高到260℃;由于Cu60Zn30Al10催化剂表面CuO的烧结导致催化剂比表面积急剧降低,催化剂表面CuO难以被还原,还原峰顶温度升高到270℃。说明Cu50Zn40催化剂中引入Al有助于表面Cu物种的分散与稳定。
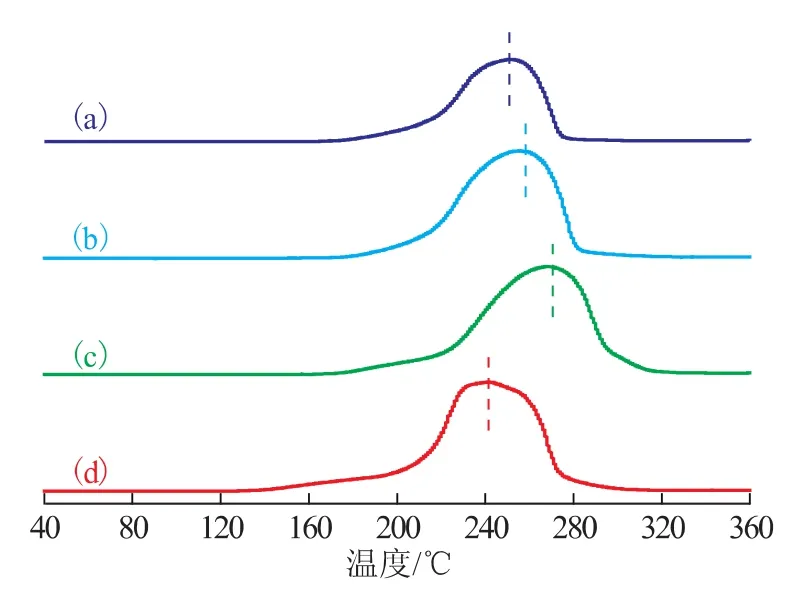
图2 催化剂的H2-TPR曲线(a)—Cu40Zn50Al10;(b)—Cu50Zn40Al10;(c)—Cu60Zn30Al10;(d)—Cu50Zn40
图3 为催化剂的SEM电镜照片。由于Cu40Zn50Al10与Cu50Zn40Al10催化剂的表面形貌呈松糕状,使得催化剂比表面积较大,与表1数据一致。Cu60Zn30Al10催化剂因其烧结严重,形貌呈块状结构,从而使催化剂比表面积急剧下降,Cu50Zn40催化剂中也可观察到明显的块状结构。说明Cu50Zn40催化剂中引入Al可提高比表面积,过高的Cu含量会促使氧化物烧结。
2.2 CuZnAl催化剂的甲醇水蒸气重整制氢催化性能
2.2.1 CuZn及CuZnAl催化剂上甲醇水蒸气重整制氢性能比较 CuZn及CuZnAl系列催化剂对甲醇水蒸气重整反应的催化性能如表2所示。由表2可以看出:CuO含量对CuZnAl催化剂活性有较大影响;Cu40Zn50Al10催化剂上甲醇转化率只有74.0%,H2产率为72.8%,是因为CuO含量较低,导致催化剂表面Cu活性位较少;而当CuO含量增加到50%时,由于催化剂表面Cu活性位增加,甲醇的转化率达到100%,H2产率为97.7%;进一步增大CuO含量,催化剂活性略有下降;不同CuZnAl催化剂上CO2选择性相近,产物中均有少量CO生成。

图3 催化剂的SEM电镜照片
在所考察的CuZnAl催化剂中,Cu50Zn40Al10催化剂的催化活性最高。Cu50Zn40催化剂上甲醇转化率为85.2%,低于Cu50Zn40Al10催化剂,主要原因是Al的添加提高了CuZn催化剂的比表面积与活性物种分散度,从而使催化活性升高。
2.2.2 反应温度的影响 在反应压力为1.0MPa、n(H2O)/n(CH3OH)=1.5、VHSV=0.56h-1的条件下,反应温度对Cu50Zn40Al10上甲醇水蒸气重整反应性能的影响见表3。甲醇水蒸气重整反应是吸热反应。由表3可知:甲醇转化率随反应温度升高而增加,在反应温度为220℃时,甲醇转化率为64.0%,H2产率为62.7%,CO2选择性为98.3%,CO选择性为1.7%;在反应温度升至250℃时,甲醇转化率达到100%,H2产率为97.7%,CO2选择性为97.5%,CO选择性为2.5%。很明显,升高温度有利于甲醇转化及提高H2产率,但CO2选择性略有下降,CO选择性略有增加。
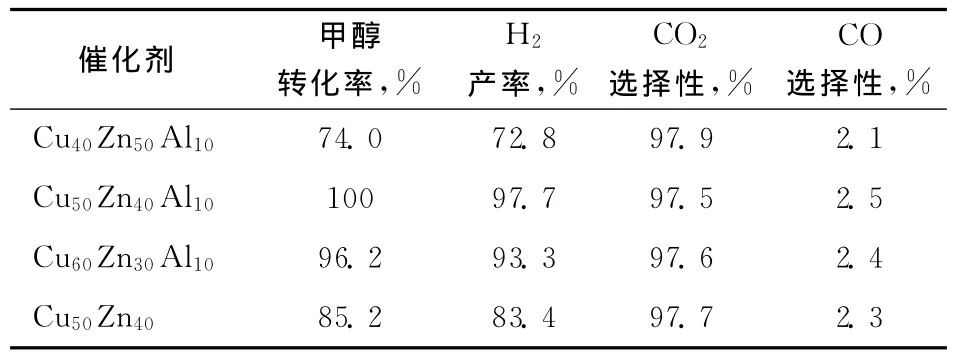
表2 CuZn及CuZnAl催化剂上甲醇水蒸气重整制氢性能比较
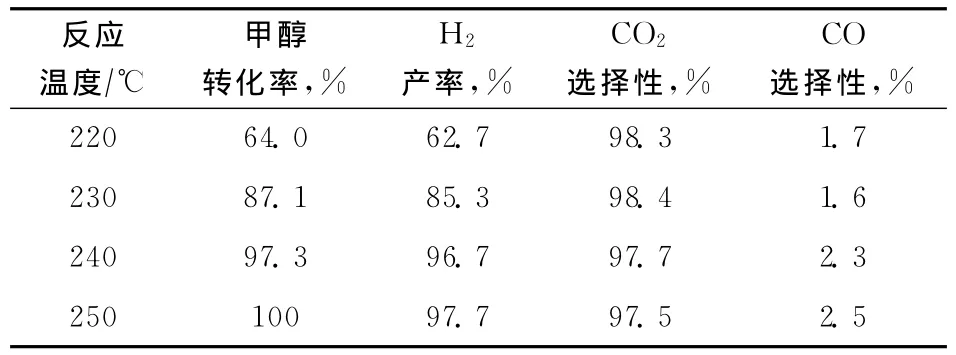
表3 反应温度对Cu50Zn40Al10上甲醇水蒸气重整制氢性能的影响
2.2.3 反应压力的影响 在反应温度为250℃、n(H2O)/n(CH3OH)=1.5、VHSV=0.56h-1的条件下,Cu50Zn40Al10催化剂在不同反应压力下催化甲醇水蒸气重整反应的性能见表4。由表4可知:反应压力对甲醇转化率影响很大,甲醇水蒸气重整制氢是体积增大的反应,提高反应压力会抑制反应;在反应压力为0~1.0MPa时,Cu50Zn40Al10催化剂上甲醇转化率达到100%,H2产率也保持在97.7%;当反应压力增加到1.5MPa时,甲醇转化率仅为89.7%,H2产率为87.5%;提高反应压力可降低CO选择性。综合比较,选定反应压力为1.0MPa。
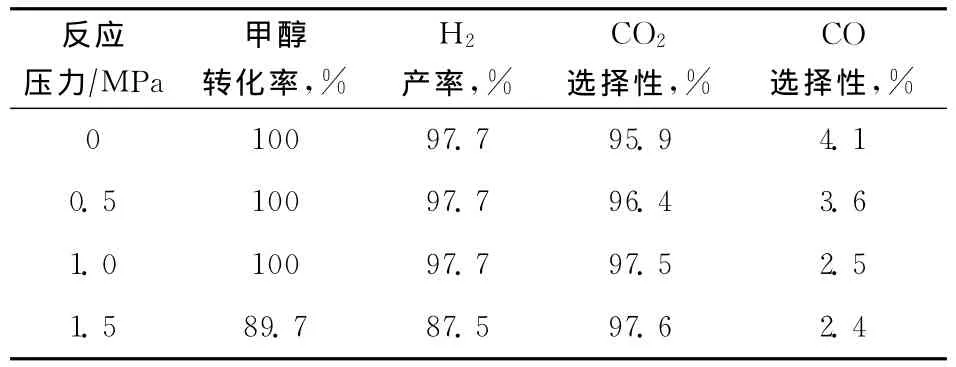
表4 反应压力对Cu50Zn40Al10上甲醇水蒸气重整制氢性能的影响
2.2.4 催化剂稳定性考察 图4为Cu50Zn40Al10与Cu50Zn40催化剂对甲醇水蒸气重整催化性能的稳定性考察结果,反应条件为:温度250℃,压力1.0MPa,n(H2O)/n(CH3OH)=1.5,VHSV=0.56h-1,反应时间200h。由图4可知:Cu50Zn40Al10催化剂上甲醇初始转化率为100%,随着反应的进行,催化活性略有下降,50h后催化剂的活性基本保持不变,甲醇转化率稳定在97%;Cu50Zn40催化剂在200h的反应过程中甲醇转化率一直呈下降趋势,甲醇初始转化率为85.2%,反应200h后,甲醇转化率降至70%。上述结果表明,向Cu50Zn40催化剂中引入Al可使催化剂活性稳定。
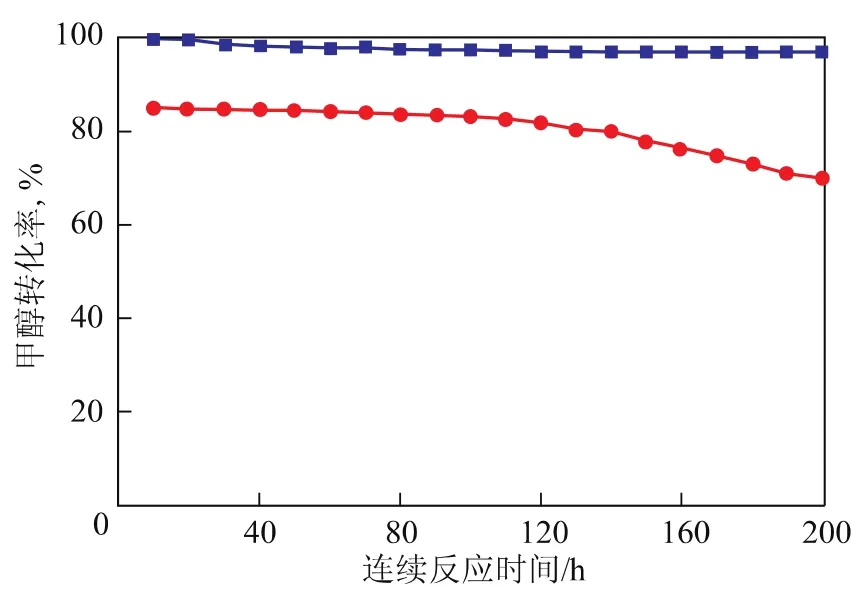
图4 Cu50Zn40Al10与Cu50Zn40催化剂稳定性实验结果■—Cu50Zn40Al10;●—Cu50Zn40
3 结 论
(1)向CuZn催化剂中引入Al可以增大催化剂比表面积,提高活性组分的分散度和稳定表面活性物种,从而提高催化剂的活性与稳定性。
(2)Cu50Zn40Al10催化剂对甲醇水蒸气重整制氢反应催化活性较高,在温度250℃、压力1.0 MPa、n(H2O)/n(CH3OH)=1.5、VHSV=0.56h-1的条件下,甲醇转化率达到100%,氢气产率达到97.7%,CO2选择性高达97.5%。连续反应200h后催化剂的活性稳定,有较好的工业应用前景。
[1] Agarwal V,Patel S,Pant K K.H2production by steam reforming of methanol over Cu/ZnO/Al2O3catalysts:Transient deactivation kinetics modeling[J].Appl Catal A,2005,279(1/2):155-164
[2] Eliezer D,Eliaz N,Senkov O N,et al.Positive effects of hydrogen in metals[J].Mater Sci Eng A,2005,280(1):220-224
[3] 冯钰.甲醇裂解-变压吸附联合制氢技术的应用[J].化工矿物与加工,2001,6(12):13-14
[4] 刘京林,孙党莉.甲醇蒸汽转化制氢和二氧化碳技术[J].甲醛与甲醇,2005,2(1):31-33
[5] 赵明正.甲醇裂解制氢装置的运用[J].石油与天然气化工,2003,32(5):278-280
[6] Chiu K L,Kwong F L.Oxidation states of Cu in the CuO/CeO2/Al2O3catalyst in the methanol steam reforming process[J].Curr Appl Phys,2012,12(4):1195-1198
[7] Yang Hungming,Chen Minke.Steam reforming of methanol over copper-yttria catalyst supported on praseodymium-aluminum mixed oxides[J].Catal Commun,2011,12(15):1389-1395
[8] Choi Y,Stenger H G.Fuel cell grade hydrogen from methanol on a commercial Cu/ZnO/Al2O3catalyst[J].Appl Catal B,2002,38(4):259-269
[9] Sanches S G,Huertas Flores J,Avillez R R,et al.Influence of preparation methods and Zr and Y promoters on Cu/ZnO catalysts used for methanol steam reforming[J].Int J Hydrogen Energy,2012,37(8):6572-6579
[10]Kniep B L,Girgsdies F,Ressler T.Effect of precipitate aging on the microstructural characteristics of Cu/ZnO catalysts for methanol steamreforming[J].J Catal,2005,236(1):34-44
[11]Turco M,Cammarano C,Bagnasco G,et al.Oxidative methanol steam reforming on a highly dispersed CuO/CeO2/Al2O3catalyst prepared by a single-step method[J].Appl Catal B,2009,91(1/2):101-107
[12]Mierczynski P,Maniecki T P,Chalupka K,et al.Cu/ZnxAlyOzsupported catalysts(ZnO∶Al2O3=1,2,4)for methanol synthesis[J].Catal Today,2011,176(1):21-27
[13]余力挺,马建新.CuZnAlZr催化剂上甲醇氧化水蒸气重整制氢催化剂组成的优化[J].催化学报,2004,25(7):523-528
[14]Lindstrom B,Pettersson L J.Hydrogen generation by steam reforming of methanol over copper-based catalysts for fuel cell applications[J].Int J Hydrogen Energy,2001,26(9):923-933
[15]Agrell J,Birgersson H,Boutonnet M,et al.Production of hydrogen from methanol over Cu/ZnO catalysts promoted by ZrO2and Al2O3[J].J Catal,2003,219(2):389-403
[16]Reppley B A,Amphlett J C,Kearns L M,et al.Methanolsteam reforming on Cu/ZnO/Al2O3.Part 1:The reaction network[J].Appl Catal A,1999,179(1):21-29
[17]Sircar S,Waldron W E,Rao M B,et al.Hydrogen production by hybrid SMR-PSA-SSF membrane system[J].Sep Purif Technol,1999,17(1):11-20
[18]Hinrichsen O,Genger T,Muhler M.Chemisorption of N2O and H2for the surface determination of copper catalysts[J].Chem Eng Technol,2000,23(1):956-959
