非负载型NiMoW催化剂催化萘一步加氢合成十氢萘
2013-09-15殷长龙刘晨光
殷长龙,刘 欢,张 胜,2,刘晨光
(1.中国石油大学 重质油国家重点实验室CNPC催化重点实验室,山东 青岛266580;2.中国石化金陵分公司)
随着化石燃料的逐渐枯竭及燃烧引起的环境问题[1-2],人类对清洁替代燃料的需求越来越迫切。十氢萘作为一种被寄予厚望的燃料电池储氢材料,具有较高的储氢能力,可提供的有效氢量为7.3%,而单位体积氢的质量高达64.8kg/m3,高于国际能源署(IEA)提出的有效氢量6.5%或单位体积氢质量62.0kg/m3的理想标准[3]。同时十氢萘也是一种优良的高沸点有机溶剂,能溶解某些高分子化合物,比如十氢萘可作为超高相对分子质量聚乙烯的溶剂,还可用作涂料的溶剂,用于提取脂肪和蜡,代替松节油用于鞋油、地板蜡的制造等。因此,十氢萘的合成制备技术一直备受关注[3-7]。
虽然十氢萘可以通过Diels-Alder和双Michael环加成、电环化二烯等来合成,但目前研究较多的仍是通过萘加氢合成十氢萘[5,7],主要集中在催化剂的研制开发及改性、反应工艺条件的优化等方面[5,8-9]。Pawelec等[6,10-12]研 究 了 活 性 组 分 为 Pd-Pt-Au的催化剂催化萘加氢体系,发现在此过程中AuPd合金的生成,对活性物种的电子及几何特性进行了修饰及改性,不仅有利于改善Pt/Pd物种在载体表面的暴露程度,同时也对载体的酸性进行了修饰,提高了加氢反应活性,并抑制了因结焦导致的催化剂失活。Shirai等[7,13]采用碳负载的Rh催化剂,在超临界CO2作为溶剂的条件下,催化萘加氢合成十氢萘,反应产物十氢萘的收率较高,主要是超临界CO2流体可以溶解更多的氢气,并能有效地降低反应温度所致。
尽管贵金属催化剂能较为有效地催化萘加氢合成十氢萘,但原料萘中携带的硫对贵金属的毒害作用[10,14]、贵金属 因结焦导致催化剂失活[8]及贵金属昂贵的价格极大地限制了其应用。而过渡金属硫化物不仅具有较高的加氢性能[15-16],同时对原料中的硫有较强的抵抗作用,且价格低廉。然而传统方法制备的负载型催化剂由于受到活性组分含量的限制,催化活性较低,难以将萘一步加氢合成十氢萘,主要是用来生产四氢萘[17-19]。而非负载型催化剂由于不使用载体,克服了活性组分含量的限制,催化反应活性有了较大的提高[15-16,20]。
本课题采用水热反应法制备一种多孔NiMoW复合氧化物,并以此为前驱体制备硫化态非负载型NiMoW催化剂,探索其催化萘加氢合成十氢萘反应,并对反应工艺条件进行优化。
1 实 验
1.1 试验材料
碱式碳酸镍 NiCO3·2Ni(OH)2·4H2O、七钼酸铵(NH4)6Mo7O24·4H2O、偏钨酸铵(NH4)6W7O24·6H2O、拟薄水铝石均取自中国石油抚顺催化剂厂,工业级试剂。反应助剂乙二醇、萘均购自国药集团化学试剂有限公司,分析纯。
1.2 非负载型NiMoW催化剂的制备
将一定比例的碱式碳酸镍、七钼酸铵、偏钨酸铵混合,形成悬浊液,与一定量的助剂置于高压釜中,将上述配好的液体加入到高压釜中并在150℃下反应10h后,冷却,抽滤,将得到的滤饼置于烘箱中于120℃下烘干10h,即得到NiMoW复合金属氧化物。将拟薄水铝石与合成的NiMoW复合氧化物粉末混合(以氧化物计,按活性金属质量分数占催化剂的75%添加),缓慢滴加适量的胶溶剂和去离子水,混合挤条成形。成形之后先在红外灯下烘干,再转移至烘箱中于80℃下干燥12h,最后在马福炉中于375℃焙烧4h,即得非负载型NiMoW催化剂。
采用传统浸渍法制备NiMoW/Al2O3负载型催化剂(金属氧化物质量分数为30%)作为参比催化剂。
1.3 催化剂的表征
采用荷兰Panalytical公司生产的X’Pert Pro MPD型X射线衍射仪测定硫化态NiMoW催化剂的晶型结构。测定条件为:CuKα(λ=1.54 060nm)衍射源,管电压45kV,管电流40mA,检测器为闪烁计数器,扫描范围5°~75°,扫描速率5(°)/min,发散狭缝1°,接收狭缝0.3mm。
硫化态NiMoW催化剂活性组分的分散状态在日本电器公司生产的JEM2010型高分辨透射电镜上进行观测,电镜加速电压200kV,采用LaB6灯丝。
1.4 催化剂的硫化及活性评价
硫化态NiMoW催化剂的萘加氢活性评价在10mL高压加氢微反装置上进行,反应器为Ф15 mm×650mm的不锈钢管,催化剂装量5mL。反应原料为10%(w)萘-环己烷溶液。实验前用含3%(w)CS2-环己烷溶液对催化剂进行预硫化,预硫化条件为:硫化温度280℃,氢气压力3.0MPa,体积空速3.0h-1,预硫化时间6h。催化反应之后得到的产物经冷凝气液分离后,采用Varian3800气相色谱(OV101毛细管柱,50m,FID检测器,面积由归一法计算)分析液相产物组成。
2 结果与讨论
2.1 硫化态NiMoW催化剂的表征
制备的硫化态NiMoW催化剂的XRD表征结果见图1。从图1可以看到,所制备的硫化态非负载型NiMoW催化剂的衍射峰较多,主要归属于Ni3S2和MoS2/WS2。Ni3S2的特征衍射峰较为明显,分别在2θ为21.8°,31.1°和50.1°处;而 MoS2和 WS2特征衍射峰非常接近,分别在14.4°、39.5°和14.3°、39.6°处,故不予区分,均记为 MoS2/WS2。这与传统浸渍法制备的负载型NiMoW催化剂存在明显的区别,传统浸渍法制备的负载型NiMoW催化剂由于金属含量低,在XRD谱图中难以辨识出硫化态金属的衍射峰,尤其是 MoS2/WS2在2θ为14.4°的特征衍射峰。
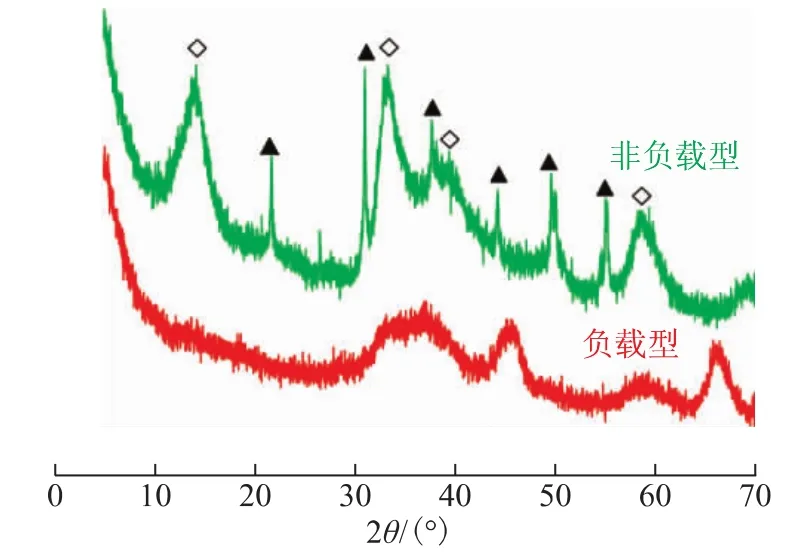
图1 硫化态NiMoW催化剂的XRD谱
硫化态NiMoW催化剂的HRTEM照片见图2。从图2(a)可以看出,硫化态非负载型NiMoW催化剂的MoS2/WS2片晶具有较长的长度及较高的堆叠层数。经计算统计得知,MoS2/WS2片晶长度主要集中在5~10nm范围内,而堆积层数主要集中在3~5层;从图2(b)可以看出,硫化态负载型NiMoW催化剂的MoS2/WS2片晶长度及堆积层数主要集中在3~5nm和1~3层。根据Topsøe等[21-22]提出的“活性相”模型,结合得到的实验数据及分析可以推断,制备的硫化态非负载型NiMoW催化剂是具有“TypeⅡ”活性相的催化剂,因此具有较为优异的催化反应性能。
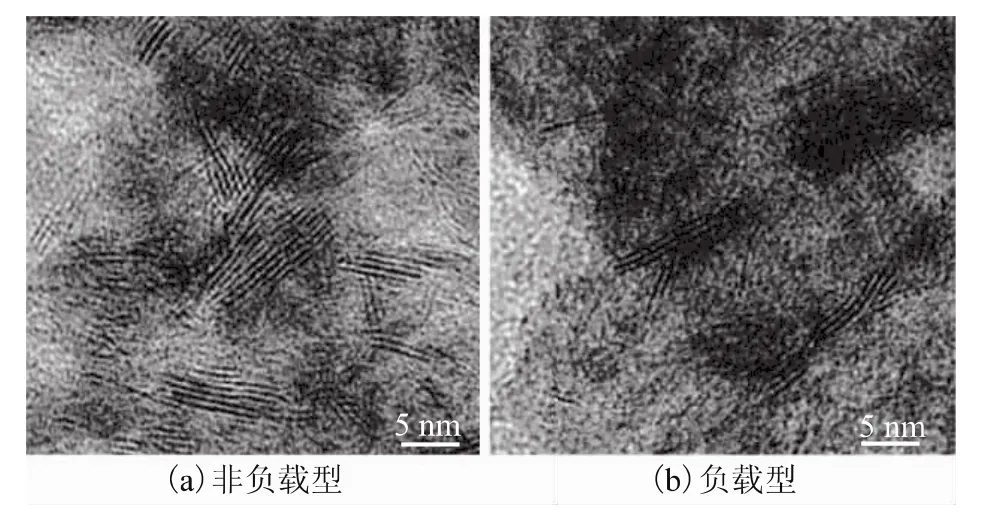
图2 硫化态NiMoW催化剂HRTEM照片
2.2 萘加氢产物
对萘加氢产物进行质谱分析的结果见图3。从图3可以看出,萘加氢之后的主要产物为四氢萘、顺式十氢萘和反式十氢萘,也有少量的加氢中间产物八氢萘。同时,由于加氢产物及加氢中间产物也发生了其它复杂的反应,如裂化、异构化等[4,23-24],因 此 也 检 测 到 了 其 它 的 反 应 产 物 如 乙苯、乙基环己烷、二联环戊烷、甲苯等。非负载型加氢催化剂由于加氢活性高,而裂化及异构化活性低,其裂化开环及异构化产物含量相对较低,一般不超过1%,因此,主要考虑反应原料萘与四氢萘、十氢萘含量的相对关系,其它中间产物未列出。
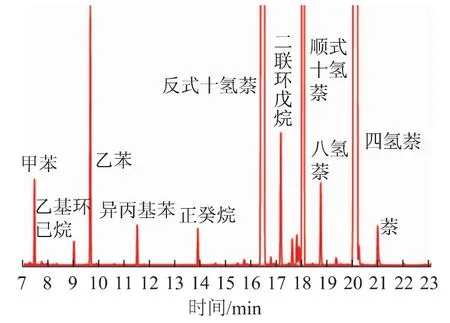
图3 萘加氢产物分析
2.3 工艺条件对萘加氢合成十氢萘的影响
2.3.1 反应温度 采用硫化态非负载型NiMoW催化剂,在反应压力6.0MPa、体积空速1.0h-1的条件下,考察反应温度对萘加氢合成十氢萘反应的影响,结果见图4。从图4可以看出,当反应温度较低(200℃)时,萘的转化率较高,可以达到99.7%,但是此时十氢萘的选择性较低;继续升高反应温度至220℃时,萘的转化率可以达到100%;当反应温度升高至240℃时,萘的转化率也达到100%。因此,当反应温度超过220℃,反应原料中的萘可以完全转化。同时也观察到随着反应温度的升高,十氢萘的选择性也随之升高,当反应温度为240℃时,产物十氢萘的选择性达到99.1%。Egan[25]的研究结果表明,萘加氢至四氢萘,进一步加氢合成十氢萘为可逆放热过程,因此,反应温度的升高不利于萘的加氢反应,而文中观察到十氢萘产物的选择性随着温度的提高呈现上升的趋势,这可能与硫化态催化剂所需的催化反应温度较高有关[2]。
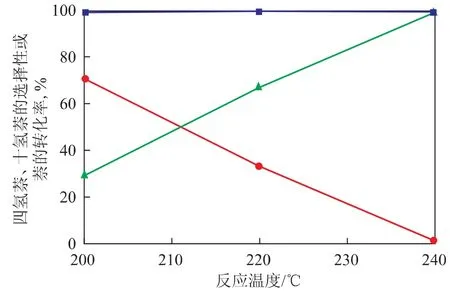
图4 反应温度对萘的转化率和产物选择性的影响●—四氢萘选择性;▲—十氢萘选择性;■—萘的转化率
对于十氢萘,因为两个环的稠合方式不同,分为顺、反两种异构体,且反式十氢萘比顺式十氢萘的热力学稳定性更高[25],反、顺十氢萘的质量比随反应温度的变化见图5。从图5可以看出,在考察的反应温度范围(200~240℃)内,反式十氢萘的比例高于顺式十氢萘,两者之间的比值在3.4~3.6范围内。Song等[26]的实验结果表明,当反应温度为548K时,处于热力学平衡状态下的反、顺十氢萘的质量比为11,而Dokjampa等[27]进一步指出,催化剂的类型对反、顺十氢萘的比值影响较大,且活性组分为Ni时,有助于降低反、顺十氢萘的质量比。从图5还可以看出,随着反应温度的升高,反、顺十氢萘的质量比呈现先增加后降低的趋势,在反应温度为220℃时,观察到反式十氢萘的选择性最高,达到了78.1%,继续升高温度,反、顺十氢萘的质量比呈现下降的趋势,这可能是由顺、反十氢萘生成及异构化速率的差异引起的[27-28],导致顺式十氢萘的总生成速率增加,而反式十氢萘的总生成速率降低。
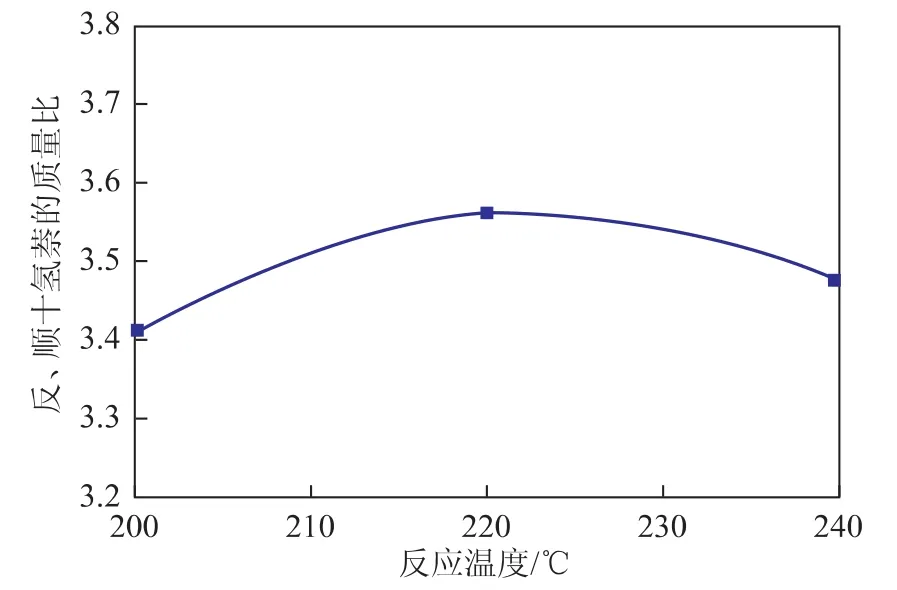
图5 反应温度对反、顺十氢萘质量比的影响
2.3.2 反应压力 采用硫化态非负载型NiMoW催化剂,在反应温度220℃、体积空速1.0h-1的条件下,考察反应压力对萘加氢合成十氢萘反应的影响,结果见图6。从图6可以看出:当反应压力为4.0MPa时,萘的转化率可以达到99.9%,十氢萘的选择性达到49.8%;随着反应压力继续升高,反应原料萘可以100%转化,同时产物中十氢萘的比例逐渐升高;当反应压力为7.5MPa时,十氢萘的选择性达到了86.8%。
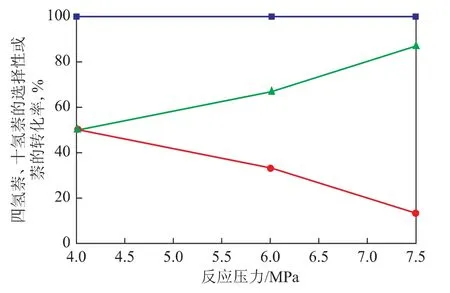
图6 反应压力对萘的转化率和产物选择性的影响●—四氢萘选择性;▲—十氢萘选择性;■—萘转化率
2.3.3 反应空速 采用硫化态非负载型NiMoW催化剂,在反应温度240℃、压力6.0MPa的条件下,考察空速对萘加氢合成十氢萘反应的影响,结果见图7。从图7可以看出,在选定的空速范围内,萘的转化率均达到100%。同时也观察到,随着空速的增加,十氢萘选择性下降,由体积空速为1.0h-1时的99.7%降低至2.0h-1时的34.7%,四氢萘选择性上升。这可能是由于空速的提高,减少了反应原料萘、反应中间产物四氢萘与催化剂的接触时间,不利于萘与四氢萘的加氢,因为相对于萘加氢至部分加氢产物四氢萘、进一步加氢至全加氢产物十氢萘的过程,第二步为速率控制步骤,因此其受空速的影响更为明显[26]。
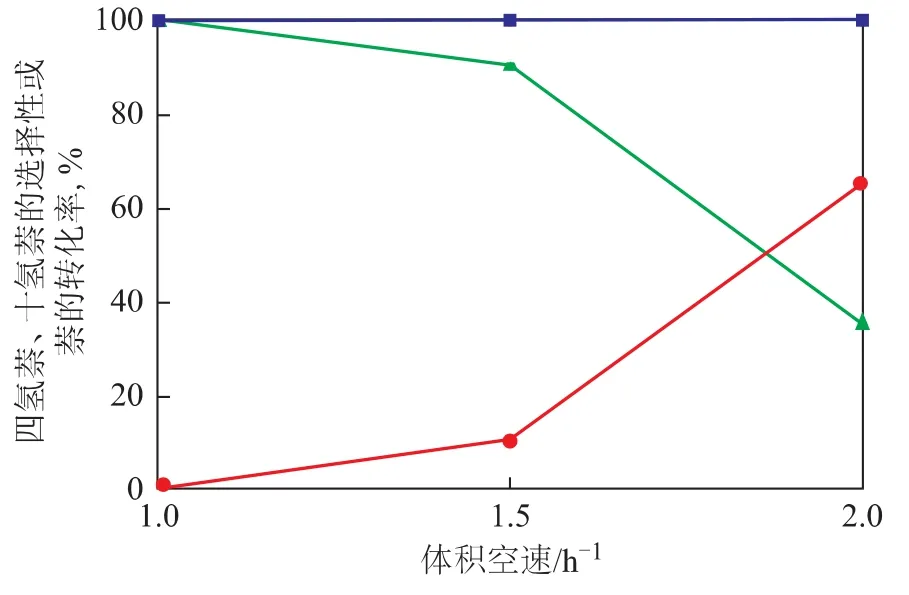
图7 空速对萘的转化率和产物选择性的影响●—四氢萘选择性;▲—十氢萘选择性;■—萘转化率
2.4 催化剂反应活性
在反应温度240℃、反应压力6.0MPa、体积空速1.0h-1的条件下,分别考察采用硫化态非负载型NiMoW催化剂和浸渍法制备的硫化态负载型NiMoW参比催化剂对萘加氢合成十氢萘反应的影响,结果见表1。从表1可以看出,硫化态非负载型NiMoW催化剂可以将原料萘100%转化,目标产物十氢萘的选择性达到99.1%以上。而参比催化剂的加氢性能相对较差,萘的转化率只有88%,而且目标产物十氢萘的选择性只有46.2%。
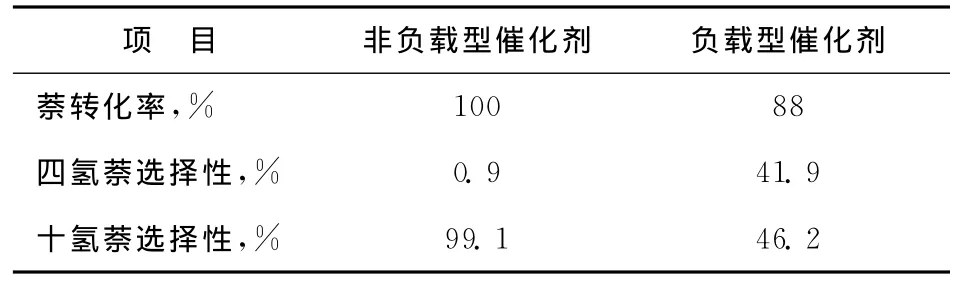
表1 不同催化剂对萘加氢合成十氢萘反应的影响
从以上实验结果及分析可知,硫化态非负载型NiMoW催化剂具有较高的催化加氢性能,可以有效地催化萘加氢合成十氢萘,这可能与其含有的 Ni3S2、MoS2/WS2等 有 关。Delmon 等[29-31]认为,NiS物种(如Ni3S2)有助于实现反应气体氢气的吸附及解离,而 Tuxen等[21-22]通过扫描隧道显微镜(STM)发现,含有芳环类的反应物在催化剂表面的吸附主要是通过“π”吸附的方式与表面的Mo/W边进行键合,而这就需要在表面暴露更多的MoS2/WS2。通过XRD及HRTEM表征结果可知,制备的硫化态非负载型NiMoW催化剂具有较为明显的 Ni3S2、MoS2/WS2特征衍射峰,且MoS2/WS2片晶的堆垛层数主要集中在3~5层之间,这些因素均有助于提高硫化态非负载型NiMoW催化剂的加氢性能,使得萘加氢转化率达到100%,而十氢萘的选择性最高可达到99.1%。与之对应的是,通过传统的浸渍法制备的NiMoW催化剂,在XRD谱图分析中并没有明显观察到具有较高催化反应活性的Ni3S2、MoS2/WS2等活性物种的特征衍射峰,且其MoS2/WS2的堆垛层数较低、片晶较短,催化反应活性较低。因此,硫化态非负载型NiMoW催化剂具有较好的催化加氢反应性能,可以较为有效地催化萘加氢一步反应生成十氢萘。
3 结 论
(1)制备的硫化态非负载型NiMoW催化剂具有明显的 Ni3S2、MoS2/WS2特征衍射峰,且MoS2/WS2片晶长度主要集中在5~10nm,堆垛层数为3~5层。
(2)与传统浸渍法制备的负载型NiMoW催化剂相比,硫化态非负载型NiMoW催化剂能更为有效地催化萘加氢合成十氢萘,萘的转化率达到100%,十氢萘的选择性最高可达99.1%。
(3)温度及压力的升高及空速的降低,有利于提高萘的转化率及十氢萘的收率。
[1] Meher L,Vidyasagar D,Naik S.Technical aspects of biodiesel production by transesterification—A review[J].Renewable and Sustainable Energy Reviews,2006,10(3):248-268
[2] Song Chunshan.An overview of new approaches to deep desulfurization for ultra-clean gasoline,diesel fuel and jet fuel[J].Catalysis Today,2003,86(1/2/3/4):211-263
[3] Hodoshima S.Catalytic decalin dehydrogenation/naphthalene hydrogenation pair as a hydrogen source for fuel-cell vehicle[J].International Journal of Hydrogen Energy,2003,28(11):1255-1262
[4] 杨平,辛靖,李明丰,等.四氢萘加氢转化研究进展[J].石油炼制与化工,2011,42(8):1-6
[5] Kirumakki S,Shpeizer B,Sagar G,et al.Hydrogenation of naphthalene over NiO/SiO2-Al2O3catalysts:Structure-activity correlation[J].Journal of Catalysis,2006,242(2):319-331
[6] Pawelec B,Parola V,Thomas S,et al.Enhancement of naphthalene hydrogenation over PtPd/SiO2-Al2O3catalyst modified by gold[J].Journal of Molecular Catalysis A:Chemical,2006,253(1/2):30-43
[7] Shirai M,Rode V,Mine E,et al.Ring hydrogenation of naphthalene and 1-naphthol over supported metal catalysts in supercritical carbon dioxide solvent[J].Catalysis Today,2006,115(1/2/3/4):248-253
[8] Pawelec B,Venezia M,Parola V,et al.AuPd alloy formation in Au-Pd/Al2O3catalysts and its role on aromatics hydrogenation[J].Applied Surface Science,2005,242(3/4):380-391
[9] Lu Chunmei,Lin Yuming,Wang Ikai.Naphthalene hydrogenation over Pt/TiO2-ZrO2and the behavior of strong metalsupport interaction(SMSI)[J].Applied Catalysis A:General,2000,198(1/2):223-234
[10]Pawelec B,Cano-Serrano E,Campos-Martin M,et al.Deep aromatics hydrogenation in the presence of DBT over Au-Pd/γ-alumina catalysts[J].Applied Catalysis A:General,2004,275(1/2):127-139
[11]Barrio L,Arias L,Cambra F,et al.Aromatics hydrogenation on silica-alumina supported palladium-nickel catalysts[J].Applied Catalysis A:General,2003,242(1):17-30
[12]Venezia A,Parola V,Pawelec B,et al.Hydrogenation of aromatics over Au-Pd/SiO2-Al2O3catalysts:Support acidity effect[J].Applied Catalysis A:General,2004,264(1):43-51
[13]Hiyoshi N,Yamaguchi A,Rode C,et al.Graphite-supported rhodium catalysts for naphthalene hydrogenation in supercritical carbon dioxide solvent[J].Catalysis Communications,2009,10(13):1681-1684
[14]Lin S,Song C.Noble metal catalysts for low-temperature naphthalene hydrogenation in the presence of benzothiophene[J].Catalysis Today,1996,31(1/2):93-104
[15]Chianelli R,Berhault G,Torres B.Unsupported transition metal sulfide catalysts:100years of science and application[J].Catalysis Today,2009,147(3/4):275-286
[16]Eijsbouts S,Mayo S,Fujita K.Unsupported transition metal sulfide catalysts:From fundamentals to industrial application[J].Applied Catalysis A:General,2007,322:58-66
[17]Egorova M,Prins R.Competitive hydrodesulfurization of 4,6-dimethyldibenzothiophene,hydrodenitrogenation of 2-methylpyridine,and hydrogenation of naphthalene over sulfided NiMo/γ-Al2O3[J].Journal of Catalysis,2004,224(2):278-287
[18]Montesinos-Castellanos A,Zepeda T.High hydrogenation performance of the mesoporous NiMo/Al(Ti,Zr)-HMS catalysts[J].Microporous and Mesoporous Materials,2008,113(1/2/3):146-162
[19]Beltramone A,Resasco D,Alvarez W,et al.Simultaneous hydrogenation of multiring aromatic compounds over NiMo catalyst[J].Industrial & Engineering Chemistry Research,2008,47(19):7161-7166
[20]Nava H,Pedraza F,Alonso G.Nickel-molybdenum-tungsten sulfide catalysts prepared by in situ activation of tri-metallic(Ni-Mo-W)alkylthiomolybdotungstates[J].Catalysis Letters,2005,99(1/2):65-71
[21]Tuxen A,Gøbel H,Hinnemann B,et al.An atomic-scale investigation of carbon in MoS2hydrotreating catalysts sulfided by organosulfur compounds[J].Journal of Catalysis,2011,281(2):345-351
[22]Lauritsen J,Bollinger M,Lægsgaard E,et al.Atomic-scale insight into structure and morphology changes of MoS2nanoclusters in hydrotreating catalysts[J].Journal of Catalysis,2004,221(2):510-522
[23]Flinn R,Larson O,Beuther H.The mechanism of catalytic hydrocracking[J].Industrial and Engineering Chemistry,1960,52(2):153-156
[24]Lylykangas M,Rautanen P,Krause A.Liquid-phase hydrogenation kinetics of multicomponent aromatic mixtures on Ni/Al2O3[J].Industrial & Engineering Chemistry Research,2002,41(23):5632-5639
[25]Egan C.Heat and free energy of formation of the cis-and transdecalins,naphthalene and tetralin,from 298to 1 000K[J].Journal of Chemical and Engineering Data,1963,8(4):532-533
[26]Wei C,Song C.Conformational isomerization of cis-decahydronaphthalene over zeolite catalysts[J].Catalysis Today,1996,31(1/2):171-181
[27]Dokjampa S,Rirksomboon T,Osuwan S,et al.Comparative study of the hydrogenation of tetralin on supported Ni,Pt,and Pd catalysts[J].Catalysis Today,2007,123(1/2/3/4):218-223
[28]Schucker R.Chemical equilibria in condensed-ring systems.Isomerization equilibria of cis-and trans-decalin[J].Journal of Chemical and Engineering Data,1981,26(3):239-241
[29]Baeza P,Villarroel M,ávila P,et al.Spillover hydrogen mobility during Co-Mo catalyzed HDS in industrial-like conditions[J].Applied Catalysis A:General,2006,304:109-115
[30]Baeza P,Ureta-Zañartu M,Escalona N,et al.Migration of surface species on supports:A proof of their role on the synergism between CoSxor NiSxand MoS2in HDS[J].Applied Catalysis A:General,2004,274(1/2):303-309
[31]Li Yongwang,Pang Xianyong,Delmon B.Role of hydrogen in HDS/HYD catalysis over MoS2:An ab initio investigation[J].Journal of Molecular Catalysis A:Chemical,2001,169(1/2):259-268
