一对手性Salen 型席夫碱对映体的合成、结构与生物活性
2013-08-20郝洪庆
郝洪庆 李 鑫 孙 静
(1 嘉应学院化学与环境学院,梅州 514015)
(2 广东医学院药学院,东莞 523808)
0 引 言
手性化合物在不对称催化、功能材料、液晶等领域具有重要应用[1-6]。由于席夫碱化合物在结构上的多样性、可调控性[14-17],以及席夫碱及其配合物具有的抑菌、抗癌、抗病毒、杀霉等生物活性[7-8],手性席夫碱化合物的合成及其化学生物学和医药开发[9-13]等研究一直倍受关注。
目前报道的Salen 型手性席夫碱通常呈对称结构,它们多是由1 个几何结构上左右对称的手性二胺(如1, 2-环己二胺、1, 2-二苯基乙二胺等) 上的2个氨基与2 个相同的有机基团缩合而得。以上述手性二胺的2 个氨基与2 个不同基团反应合成结构上左右不对称的手性席夫碱难度较大,相关报道较少。据文献报道,二胺与羰基化合物缩合制备三齿或四齿非对称席夫碱的方法主要有条件控制分步反应法与金属模板法。前者是指严格控制反应条件,如反应温度、时间、溶剂或反应物物质的量之比和浓度等先得到中间产物,进一步制备二胺与2 个不同羰基缩合的席夫碱; 金属模板法则是将金属离子作为模板剂,利用金属离子对N 原子的较强亲合力,特别适合于促使小分子有机物定向缩合成较大分子的有机配体并形成配合物,除去配合物中的金属离子后,最终得到席夫碱配体[18-20]。
本文通过改变溶剂,降低胺解反应速度的措施,利用手性1R, 2R-环己二胺(或1S, 2S-环己二胺)与水杨酸苯酯、2-羟基萘甲醛分步反应合成了一对手性Salen 型席夫碱对映体,并对其结构与性质进行了表征。
1 实验部分
1.1 仪器与试剂
实验所需的试剂均为AR 级,使用前未经特殊处理。Nicolet AVATAR FT-IR360 型红外光谱仪,Flash EA 1110 型元素分析仪,Brucker Smart Apex CCD 衍射仪,JASCO J-810 型圆二色分光偏振仪。
1.2 合成方法
将1.32 g 1R, 2R-环己二胺酒石酸盐(5 mmol)或1S, 2S-环己二胺酒石酸盐(5 mmol),0.74 g Ca(OH)2(10 mmol)和4 mL 蒸馏水混合,40 ℃下搅拌10 h,抽滤,冷却。
称取1.07 g 水杨酸苯酯(5 mmol)与上述滤液在20 mL 异丙醇中加热回流40 min 后,自然冷却至室温,得到浅黄色溶液,将其过滤,浓缩,用乙醇洗涤,真空干燥,即可得到中间产物。将0.235 g 中间产物(1 mmol)溶解在20 mL 乙醇中,加入0.172 g 2-羟基萘甲醛(1 mmol),所得混合溶液回流2.5 h,冷却后置于冰箱缓慢挥发,所得油状物用乙醚洗涤,抽滤,真空干燥,再用乙醇重结晶3 次,最后得到黄色块状晶体1a 或1b(合成路线如Scheme 1)。

Scheme 1 Synthesis of 1a and 1b
1a 的元素分析结果(%):C, 74.21(74.15); H, 6.23(6.28); N, 7.21(7.30);1b 的 元 素 分 析 结 果(%):C,74.18(74.15); H, 6.25(6.28); N, 7.28(7.30) %(括 号 内数据为按C24H24N2O3,Mr=388.45 计算的理论值)。
1a 和1b 的红外光谱(KBr, 4 000~400 cm-1): 3 246(νO-H), 3 061(νC-H), 2 933, 2 855(νC-H), 1 629, 1 593(νC=N), 1 244(νC-O), 1 185(νC-N)[24]。
1.3 单晶结构的测定
挑 选0.22 mm×0.18 mm×0.15 mm(1a)和0.20 mm×0.13 mm×0.11 mm (1b)大小的晶体,将其粘在玻璃丝纤维上,进行X-射线单晶衍射。在298 K 下,用Bruker Smart Apex CCD 衍射仪,以石墨单色化的Cu Kα 射线(λ=0.154 178 nm)为辐射源φ-ω 扫描方式,收集衍射点。强度数据先用SAINTPLUS 程序进行还原校正[21],然后采用SADABS 程序进行半经验吸收校正[22]。利用SHELXS-97 程序包解析得到初结构,然后利用全矩阵最小二乘法修正这些结构,并用差值Fourier 合成法完善,得到最后结构[23]。所有非氢原子都做各向异性精修,氢原子位置由理论计算确定。
化合物1a 和1b 同属正交晶系,P212121空间群。1a 的晶胞参数为a=1.630 06(3) nm,b=1.819 79(3)nm,c=2.090 11(4) nm,V=6.200 0(2) nm3,Flack parameter x=0.09(15);1b 的 晶 胞 参 数 为a=1.629 52(1)nm,b=1.820 29(1)nm,c=2.090 23(2)nm,V=6.200 04(8)nm3, Flack parameter x=0.21(14)。
CCDC:932330,1;932331,2。
2 结果与讨论
2.1 合成讨论
两个氨基与不同基团缩合的手性Salen 型席夫碱合成比较困难,需要严格地控制反应条件。因为氨基与醛的缩合在乙醇中通常反应较快,易生成2 个氨基缩合相同基团的产物,而在氯仿、异丙醇等溶剂中缩合反应较慢,利于形成2 个氨基缩合不同基团的席夫碱。因此,首先选择异丙醇作为溶剂,有利于得到部分缩合的中间产物,避免结构上左右对称的副产物[1]。本实验正是采取分步反应的策略,将等物质的量的水杨酸苯酯和环己二胺在异丙醇中首先胺解,得到单氨基缩合的中间产物,中间产物与等物质的量的2-羟基萘甲醛在乙醇中进一步缩合后得到氨基缩合不同基团的一对手性Salen 型席夫碱对映体。
2.2 结构描述
如图1 和图2 所示,在化合物1a 和1b 的结构单元中都含有3 个独立的分子; 每个分子上有1 个酰胺基N、1 个亚胺基、1 个酰胺和2 个酚羟基,是一种五齿的氮氧配体,环己烷上的2 个氮原子均呈反式排列。化合物1a 中,手性的C1 和C6 都是R 构型;苯环和萘环分列在环己二胺基团的两侧,二面角为88.731°,N1-C1-C6-N2 的扭角为61.4(7)°。化合物1b 中,手性的C1 和C6 均为S 构型。
在1a 的结构单元中,d(C17-N1)=0.130 3(3) nm,d(C18-O2)=0.124 6(3) nm,d(C1-N1)=0.145 6(3) nm,d(C6-N2)=0.145 4(3) nm,d(C23-O1)=0.135 1(3) nm,d(C8-O3)=0.128 4 (3) nm。在1b 的结构单元中,d(C17-N1)=0.130 4 (3) nm,d(C18-O2)=0.124 9(2)nm,d (C1-N1)=0.145 6 (3) nm,d(C6-N2)=0.145 3(3)nm,d(C23-O1)=0.134 8(3) nm,d(C8-O3)=0.128 8(3)nm。
此外,在化合物1a 和1b 固体结构中,还存在着丰富的分子内氢键和分子间氢键。以1a 为例,在O…H…O 之间(O1-H…O2,O4-H…O5 与O7-H…O8)和O…H…N 之间(O3-H…N1,O6-H…N3 与O9-H…N5)存在明显的分子内氢键(图3);N-H…O 之间(N2-H…O6, N4-H…O9#1 和N6#2-H…O3)存在明显的分子间氢键,每个分子和相邻的2 个分子通过分子间氢键组装成超分子链(图4)。
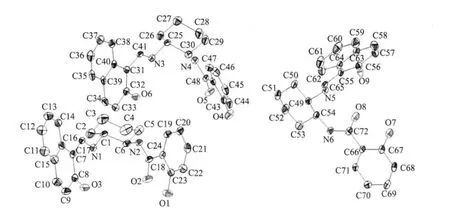
图1 化合物1a 的分子结构Fig.1 Molecular structure with 30% probability displacement ellipsoids in 1a

图2 化合物1b 的分子结构Fig.2 Molecular structure with 30% probability displacement ellipsoids in 1b
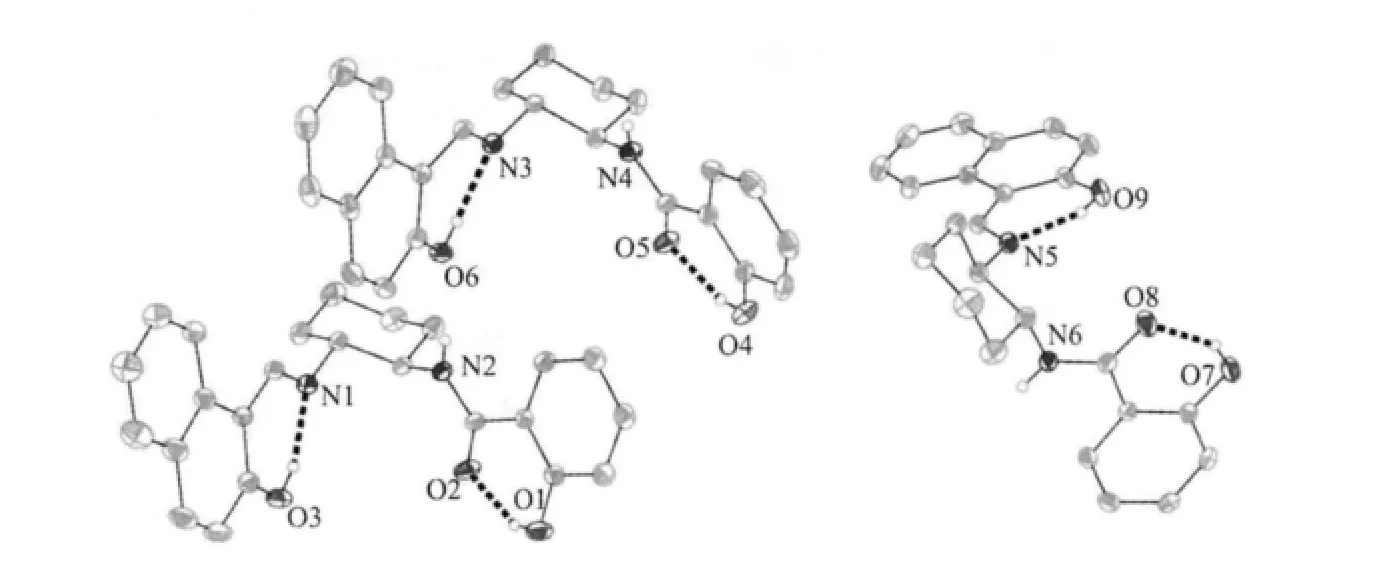
图3 化合物1a 的分子内氢键Fig.3 Intramolecular hydrogen bonds of 1a
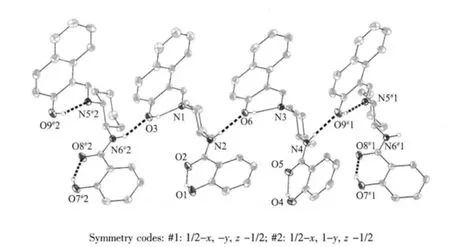
图4 化合物1a 的分子间氢键Fig.4 Intermolecular hydrogen bonds of 1a
2.3 CD 光谱
我们对化合物1a (1b)的甲醇溶液进行了CD 光谱表征(图5),其CD 光谱在257 nm(263nm)、315 nm(318 nm)、400 nm(405 nm)、417 nm(424 nm)处出现了明显的Cotton 效应[25],证明化合物1a 和1b 确为手性分子且互为对映异构。

图5 化合物1a 和1b 的CD 光谱Fig.5 Solution CD spectra of 1a and 1b
2.4 生物活性
用滤纸片法测试化合物1a 的抑菌活性:真菌以马铃薯葡萄糖为培养基,细菌以牛肉膏蛋白胨为培养基,培养基斜面经灭菌后接活化菌种,培养的指示菌分别与灭菌后的马铃薯葡萄糖、 牛肉膏蛋白胨培养基混合,倒入培养皿制平板;将1a 的溶液(10 μg·mL-1)注射到灭菌的滤纸片上,吹干后贴到平板上;倒置培养皿于37 ℃培养箱,真菌培养两天,细菌培养一天后,测量抑菌圈直径。生物实验显示1a 对白色假丝酵母、 黑曲霉几乎无抑制(抑菌圈直径均<7 mm),但对枯草杆菌(9 mm)、大肠杆菌(10 mm)和金色葡萄球菌(11 mm)具有一定的抑制活性。
3 结 论
以1R,2R-环己二胺或1S,2S-环己二胺、 水杨酸苯酯和2-羟基萘甲醛为原料,采取分步反应策略合成了一对手性Salen 型席夫碱对映体:1R-(2-羟基苯甲酰亚胺)-2R-(2-羟基萘甲亚胺)环己烷(1a)和1S-(2-羟基苯甲酰亚胺)-2S-(2-羟基萘甲亚胺) 环己烷(1b),对其进行了元素分析、红外、X 射线单晶衍射、CD 光谱及生物活性测试。CD 光谱与单晶结构表明化合物1a 和1b 均具有手性且对映异构。生物实验显示1a 对枯草杆菌、大肠杆菌和金色葡萄球菌均有一定的抑菌活性。
[1] YOU Xiao-Zeng(游效曾), MENG Qing-Jin(孟庆金), HAN Wan-Shu(韩 万 书). Progress of Coordination Chemistry (配位 化 学 进 展). Beijing: Higher Education Publishing House,2000.
[2] Vaidhyanathan R, Bradshaw D, Rebilly J, et al. Angew.Chem. Int. Ed., 2006,45(39):6495-6499
[3] HU Guo-Hang(胡国航), RUAN Wen-Juan(阮文娟), ZhANG Yu-Ling( 张 玉 玲), et al. Acta Phys.-Chim. Sin. (Wuli Huaxue Xuebao), 2003,19(4):320-325
[4] Christoph J. Dalton Trans., 2003(14):2781-2804
[5] Feringa B L, Van-Delden R A. Angew. Chem. Int. Ed., 1999,38(23):3418-3438
[6] Perez-Garcia L, Amabilino D B. Chem. Soc. Rev., 2002,31(6):342-356
[7] Hodnett E M, Mooney P D. J. Med. Chem., 1970,13(4):768-770
[8] WANG Jian-Hua(王建华), LEI Wen(雷文), WANG Yuan-Liang( 王 远 亮). Chin. Chem. Bull. (Huaxue Tongbao),2002,65:w035
[9] Ganter C. Chem. Soc. Rev., 2003,32(3):130-138
[10]Zhang H, Yang C B, Li Y Y, et al. Chem. Commun., 2003(1):142-143
[11]Amendola V, Fabbrizzi L, Mangano C, et al. Inorg. Chem.,2000,39(25):5803-5806
[12]Gennari C, Piarulli U. Chem. Rev., 2003,103(8):3071-3100
[13]ZHAO Jian-Zhang(赵建章), ZHAO Bing(赵冰), XU Wei-Qing(徐蔚青),et al.Chemical Journal of Chinese Universities(Gaodeng Xuexiao Huaxue Xuebao), 2001,22(6):971-975
[14]Cozzi P G. Chem. Soc. Rev., 2004,33(7):410-421
[15]YU Yun(俞芸), LIN Li-Rong(林丽榕), YANG Kai-Bing(杨 开 冰), et al. Chin. J. Org. Chem.(Youji Huaxue), 2006,26(7):933-936
[16]WANG Yu-Jia(王雨嘉), LUO Geng-Geng(骆耿耿), YU Yun(俞 芸), et al. Chin. J. Org. Chem.(Youji Huaxue), 2008,28(5):903-906
[17]ZHANG Hui(章慧), CHEN Yuan-Chuan(陈渊川), WANG Fang(王 芳), et al. Acta Phys.-Chim. Sin. (Wuli Huaxue Xuebao), 2006,22(6):666-671
[18]Sigman M S, Jacobsen E N. J. Am. Chem. Soc., 1998,120(19):4901-4902
[19]Kureshy R I, Khan N H, Abdi S, et al. Polyhedron, 1999,18(12):1773-1777
[20]Costes J P, Dahan F, Donnadieu B, et al. Inorg. Chem.,2004,43(8):2736-2740
[21]Bruker. SAINT and SMART. Bruker AXS Inc, Madison,Wisconsin, USA, 2001.
[22]Sheldrick G M. SADABS. University of Gttingen, Germany,1996.
[23]Sheldrick G M. SHELXS97 and SHELXL97. University of Gttingen, Germany, 1997.
[24]Pretsch E, Bühlmann P, Affolter C, Translated by RONG Guo-Bin(荣国斌), ZHU Shi-Zheng(朱士正). Structure Determination of Organic Compounds Tables Spectral Data(波谱数据表——有机化合物的结构解析). Shanghai:East China University of Science and Technology Press,2002.
[25]Pasini A, Gullotti M, Ugo R. Dalton Trans., 1977(4):346-356
