胃癌穿孔的临床病理分期特点和手术方式的相关性研究
2013-08-14孙德利解寒冰杨大勇
孙德利,解寒冰,杨大勇
(郑州人民医院普通外科 450000)
胃癌穿孔患者往往同时伴有腹腔污染等相关并发症状,死亡率较高[1]。据有关治疗研究表明,诸多胃癌穿孔患者处于临床病理分期的进展期阶段[2],根本性治疗难度大,目前关于不同临床病理分期的胃癌穿孔确定性治疗措施的研究存在争议[3]。为了进一步了解胃癌穿孔的临床病理分期表现,并有效分析与手术方式的相关性,现将本院收治的该疾病的患者的临床病理分期特点进行分析,取得显著的研究结果,现报道如下。
1 资料与方法
1.1 一般资料 本院于2007年1月至2012年1月期间共收治并经确诊为胃癌穿孔患者共50例。其中,男32例,女18例,年龄47~85岁,平均(69.5±6.3)岁。患者在临床上主要表现为突发的腹痛和腹膜炎体征等表现。
1.2 方法
1.2.1 手术方式 50例患者均行剖腹探查术,术前均补液抗感染治疗,其中合并休克患者术前积极抗休克治疗症状部分缓解后急诊行剖腹探查[4],术中行快速冰冻,考虑良性病变而行胃大部切除术者,若证实为胃癌症状,则均进行姑息性手术治疗。针对于腹腔污染严重或者出现合并感染性休克症状的患者,依照损伤控制外科(damage control surgery,DCS)原则[5],进行穿孔修补引流手术治疗,术后2周内恢复后行根治性切除术,即为二期根治性切除手术。
1.2.2 研究方法 对本次研究的50例患者临床病理分期的例数进行统计,并对不同分期采用何种手术方式进行探讨。其中,胃癌的临床病理分期标准按卫生部胃癌诊疗规范标准进行分期[6]。对手术治疗30d内出现死亡患者的例数进行统计分析,并探讨不同临床病理分期患者的表现分布结果以及其与不同手术方式的相关性关系。
1.3 统计学处理 采用SPSS17.0为统计学分析软件对数据进行分析处理。计量资料采用表示,采用t检验、χ2检验以及秩和检验,检验水准α=0.05,以P<0.05为差异有统计学意义。
2 结 果
2.1 患者不同临床病理分期 本次研究的50例出现胃癌穿孔的患者,大多数处于进展期阶段,占96%,且均出现侵犯患者浆膜或浆膜外组织与器官。临床病理分期:Ⅱ~Ⅳ期,其中Ⅱ期(T4aN0M0)2例、Ⅲ期19例(T4aN1-2M05例,T4bN0-1M014 例 )、Ⅳ 期 29 例 (T4aN1-3M13 例,T4bN1-3M116例)。
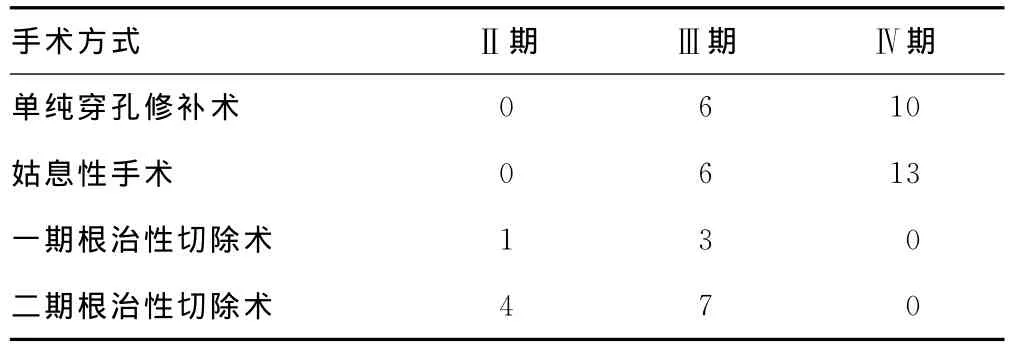
表1 不同临床病理分期手术方式的选择表(n)
2.2 病理分期与手术方式的相关性 16例(32.0%)行单纯穿孔修补术;19例(38.0%)行姑息性手术;4例(8%)一期根治性切除术;另外11例(22.0%)行二期根治性胃切除术,见表1。不同手术治疗后,共死亡17例,存活33例,患者的围术期死亡与存活情况比较差异有统计学意义(P<0.05),见表2。
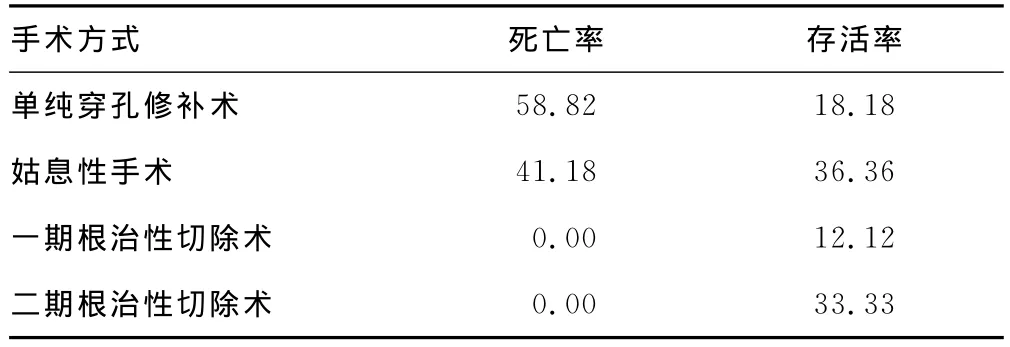
表2 不同手术方式死亡与存活情况(%)
3 讨 论
胃癌穿孔症状在胃癌患者中比较少见,属于胃癌的一种严重并发症状之一[7]。据相关统计研究资料表明,胃癌穿孔患者在胃癌中的发病率约为0.3%~3.9%[8],并且大多数胃癌穿孔患者处于临床病理分期的进展期阶段,患者的侵犯浆膜或浆膜外组织与器官会受到不同程度的损害[9],出现严重的胃癌穿孔症状最为常见[10],但这并不排除早期的胃癌患者不会发生的可能性[11]。而腹膜炎相关的组织发炎症状可以导致外科医生高估肿瘤和淋巴结转移的范围,进而影响诊断效果的准确性与可靠性[12]。
本次研究的50例出现胃癌穿孔的患者,大多数处于进展期阶段,占96%,且均出现侵犯患者浆膜或浆膜外组织与器官。临床病理分期:Ⅱ~Ⅳ期,其中16例(32.0%)行单纯穿孔修补术;19例(38.0%)行姑息性手术;4例(8%)一期根治性切除术;另外11例(22.0%)按损伤控制外科(DCS)原则行简单修补术后2周内行根治性胃切除术,且不同手术治疗后,共死亡17例,存活33例,患者的围术期死亡与存活情况比较差异有统计学意义(P<0.05),说明胃癌患者不同临床病理分期与手术方式的选择具有一定的相关性关系。而在李立涛等[12]研究中提到,对临床病理分期患者关于手术方式、年龄、性别以及是否出现术前并发症与感染症等方面进行统计学分析,发现不同手术方式存在差异性,在一定程度上支持了本文研究结论。而不同手术治疗方式与临床分期的关系研究较多,大多数研究认为单纯穿孔修补术适用于年纪大,穿孔时间长、手术耐受性差的晚期胃癌患者[13];姑息性手术,适用于可耐受较大手术而不能完整切除肿瘤患者;根治性切除手术,适用于一般情况患者[14];二期根治性手术,适用于肿瘤临床分期不超过Ⅳ期,但一期根治手术耐受性差、风险大的患者。
综上所述,胃癌患者在临床病理分期的进展期中比较容易发生胃癌穿孔症状,治疗该疾病的手术方式的选择与患者临床病理不同分期的具体表现有较大的相关性,对该疾病患者进行综合、科学的判断,再选择合适的手术治疗方式,具有延长患者生存时间,提高部分患者根治的可能性,值得临床上进一步研究与推广。
[1]董艳军,吴强.胃癌急性穿孔手术治疗临床分析[J].中国医药,2011,6(1):69-70.
[2]曹文彬,周昊,周利人,等.20例胃癌急性穿孔的外科治疗体会[J].实用临床医学,2009,10(4):16.
[3]李振军.胃癌急性穿孔的外科治疗分析[J].医学理论与实践,2012,25(16):1999-2000.
[4]张昊,高黎黎,薛会朝,等.胃癌穿孔患者术后预后影响因素分析[J].中国全科医学,2012,15(2):172-174.
[5]黄国民,郑连文,房学东,等.胃癌穿孔的外科治疗[J].中国普通外科杂志,2009,18(10):1027-1029.
[6]王江红,项颖.早期胃癌的筛查现状及诊断进展[J].重庆医学,2009,38(20):2634-2636.
[7]时云飞,刘翠苓,周春菊,等.原发系统型问变性大细胞淋巴瘤问变性淋巴瘤激酶基因异常与其融合蛋白表达及预后分析[J].北京大学学报:医学版,2008,40(4):380-381.
[8]宋晓斌,董强,侯波,等.腹腔CEA mRNA检测在胃癌穿孔治疗中的意义[J].中国老年学杂志,2010,30(23):3567-3569.
[9]崔莲,王志津,张金萍,等.胃癌伴弥散性血管内凝血一例[J].中华临床医师杂志:电子版,2011,5(20):6189-6190.
[10]林萍,李玮.135例晚期恶性肿瘤合并DIC临床分析[J].中华医院感染学杂志,2010,20(17):2597-2598.
[11]Wang FH,Li YH,Zeng J,et al.Clinical analysis of primary systemic anaplastic large cell lymphoma:a report of 57 cases[J].Chin J Cancer,2009,28(1):49-53.
[12]李立涛,王华丽,司丕成,等.胃癌急性穿孔临床病理分期的特点以及手术方式[J].岭南现代临床外科,2012,12(3):181-183.
[13]Ohtsuka T,Sato S,Kitajima Y,et al.False-positive findings for tumor markers after curative gastrectomy for gastric cancer[J].Dig Dis Sci,2008,53(1):73-79.
[14]Jung M,Jeung HC,Lee SS,et al.The clinical significance of ascitic fluid CEA in advanced gastric cancer with ascites[J].J Cancer Res Clin Oncol,2010,136(4):517-526.
