多发性硬化的诊断
2013-08-14张星虎
张星虎
多发性硬化(multiple sclerosis,MS)是中枢神经系统炎性脱髓鞘疾病,好发于20~40岁,女性多见,其显著特点为时间上的多发性(多次发作)及空间上的多发性(多个病变部位),呈慢性发作性病程,晚期病情进展较快,是致残率较高的疾病,严重影响患者生活质量。近年来,新的免疫治疗药物如干扰素-β用于治疗MS,该药能降低MS的复发次数[1],特别是其用于临床孤立综合征(clinically isolated syndrome,CIS)能够降低CIS的临床确诊MS(clinically definite MS,CDMS)转化率[2]。这些结果表明,早期诊断、早期治疗MS能够改善预后,而MS的早期正确诊断是核心。即使MRI新技术的应用以及MS诊断标准的不断修订,临床上仍然大量存在将MS误诊为其他疾病以及将其他疾病误诊为MS的情况,说明MS诊断的难度较大。其主要根源是MS临床表现的多样性以及缺乏特异性生物学检测指标。基于此,MS诊断仍然应强调临床诊断,特别应该强调排除其他疾病[3]。
1 MS的临床特点
MS的病理改变主要为脑、脊髓及视神经(因为其髓鞘形成细胞为少突胶质细胞)的髓鞘脱失导致相应的神经传导功能障碍。由于脱髓鞘病变的空间多发性,导致临床表现的多样性,临床症状及体征取决于CNS受累的部位(大脑半球白质、中脑、脑桥、延髓、脊髓、视神经)。MS常见表现有视力下降(单眼或双眼)、复视、共济失调、肢体麻木无力、二便障碍等;因为病变主要累及白质,很少出现如癫痫、失语、智能减退等灰质或核团受累的表现。MS患者在疾病晚期也可以伴有情感或认知障碍。特别应强调的是,患者在发生髓鞘脱失的同时,机体也启动髓鞘修复机制,这点对临床诊断MS也很重要。临床常遇到患者自述曾经出现过神经功能障碍,未给予治疗或按其他疾病治疗而症状减轻或消失,本次以典型的脱髓鞘事件就诊,医生应慎重考虑前次表现是否为脱髓鞘事件。因此,在临床诊断MS采集病史时应仔细甄别既往神经功能障碍是否为脱髓鞘事件,有助于确定是否为炎性脱髓鞘病及相关分型。
2 MS相关实验室检查
MS的实验室检查有助于支持临床诊断,但不能过分夸大其诊断价值,特别是应杜绝仅凭影像学表现或脑脊液检测结果进行MS诊断的情况。通常情况下,MS的实验室检查包括3个方面:支持诊断检查、排他诊断检查及治疗评价相关检查。支持诊断检查包括头或脊髓MRI、诱发电位〔视觉诱发电位(VEP)、脑干诱发电位和体感诱发电位(SEP)〕、脑脊液免疫学检查〔寡克隆区带(OB)或24h鞘内IgG合成率〕等。排他诊断检查项目很多,主要应强调与视神经脊髓炎(NMO)相关的水通道蛋白4(AQP4)抗体检测,与系统性自身免疫病(包括干燥综合征、白塞病或系统性红斑狼疮等)相关的自身抗体检测。治疗相关检查又分有效性检查及安全性检查,前者包括 MRI、诱发电位、OCT等,后者包括血常规、血生化(肝肾功能)等。
MRI在MS诊断中具有非常重要的价值。它不仅有助于MS的诊断,也有助于了解病灶的活动性,是新药临床试验的重要评价指标。MS在MRI典型表现:病灶大小>3mm(T2W),圆形或椭圆形,分布于近皮层、天幕下、脑室周围,多发T2W高信号病灶,部分病灶伴有Gd强化,强化呈环状或半环状。2003年,美国神经病学学会(AAN)指南介绍了MRI在可疑 MS患者的使用价值[4]:在CIS患者,MRI T2像发现3个以上白质病灶是未来7~10年发展为CDMS的极为敏感的预测指标(A级推荐);CIS后(及基线 MRI评价后)3个月以上出现新的T2病灶或Gd-增强病灶对以后发展为CDMS具有高度预测价值(A级推荐);具有以上MRI异常表现的CIS患者,诊断为其他疾病而非MS的可能性很低(A级推荐)。
诱发电位可以发现亚临床病灶,也是MS常用的检查手段。2000年,AAN指南介绍了诱发电位在 MS诊断中的应用价值[5]:(1)VEP检查很可能对发现患者发展为CDMS的危险性增加有帮助(ANN指南,Ⅱ级证据)。(2)SEP检查可能对发现患者发展为CDMS的危险性增加有帮助(可选用,Ⅱ级证据)。(3)目前证据尚不能推荐脑干听觉诱发电位(BAEP)作为一项判断患者发展为CDMS的危险性增加的有用检查(ANN指南,Ⅱ级证据)。
CSF检查对MS诊断及鉴别诊断均有帮助。一般而言,MS患者CSF白细胞<50个/mm3,蛋白<100mg/dL,OB可为阳性,24h鞘内IgG合成率增加。值得注意的是,OB并非MS的特异性指标,其他慢性感染也可以阳性,在临床高度怀疑MS的患者,OB阳性更支持诊断。然而,亚洲报道的MS OB阳性率低。
3 MS诊断标准的演变
1983年制定了Poser诊断标准[6],该标准将诊断分为4种情况:临床确定、实验室确定、临床可能、实验室可能。该标准引入诱发电位、脑脊液免疫学指标作为重要的诊断依据,应用较为广泛,但是在亚洲地区,OB阳性率低,对实验室确定MS及实验室可能MS的诊断帮助不大。
随着MRI技术的广泛使用,MS的诊断更加依赖MRI。基于此,2001年制定了 McDonald诊断标准[7],该标准将诊断分为确诊 MS(完全符合标准,其他疾病不能更好的解释临床表现)、可能MS(不完全符合标准,临床表现怀疑MS)及非MS(在随访和评估过程中发现其他能更好解释临床表现的疾病诊断)。该诊断标准的特点是突出了MRI在MS诊断中的作用,特别是MRI病灶在时间及空间上的多发性,对于MS早期诊断更有价值,而且该标准中特别提出了原发进展型MS的诊断。与Poser标准相似,McDonald标准将发作定义为具有MS所见到的神经功能障碍,临床表现包括主观描述或客观体征,最少持续24h,应排除假性发作或单次发作性表现。两次发作间隙>30d。MRI空间多发性的证据(必须具备下述4项中的3项):(1)1个Gd强化病灶或9个长T2信号病灶(若无 Gd强化病灶);(2)1个以上幕下病灶;(3)1个以上邻近皮层的病灶;(4)3个以上室旁病灶(1个脊髓病灶等于1个脑部病灶)。MRI病灶在时间上呈多发性的证据:(1)临床发作后至少3个月行MRI检查在与临床发作病灶不同的部位发现Gd强化病灶;或(2)在3个月检查无Gd强化病灶,之后3个月复查显示Gd强化病灶或新发现的T2病灶。
2005年,对2001年颁布的McDonald标准进行了修订[8]。首先在MRI病灶中,将脊髓病灶与天幕下病灶视为具有同等价值,1个脊髓增强病灶等同于1个脑部增强病灶,1个脊髓T2病灶可代替1个脑内病灶;其次,对于MRI时间多发性的证据,临床发作30d后出现新的T2病灶;其三,病灶大小必须≥3mm;最后,CSF阳性不再作为原发进展型 MS(primary-progressive MS,PPMS)必不可少的条件。
2010年修订的McDonald诊断标准能够较为快速诊断 MS[9](表1),与过去诊断标准相比其敏感性及特异性相同,但简化了诊断过程,所要求的MRI检查次数减少(取消了MRI检查时间间隔的限制),对MRI时间上及空间上多发性的标准也进行了修改。
4 MS与NMO的关系
NMO最早是由Devic于1894年提出,是指双侧视神经炎和脊髓炎在短期内相继发生的单相性疾病。对NMO是独特的脱髓鞘疾病还是MS的一个亚型一直存在争议。日本学者曾提出视神经脊髓型 MS(OSMS)的概念,但西方学者仍提出NMO应独立于经典的MS。1999年Wingerchuk等[10]提出了 NMO 诊断 标准。Misu等[11]于2002年提出的NMO诊断标准:临床上选择性累及脊髓和视神经;随访超过5年重复MRI检查未发现视神经和脊髓之外的病变。近年来,对NMO又有一些新的认识,首先NMO也可以出现视神经和脊髓以外其他中枢神经系统结构的累及,包括脑干、小脑、大脑半球等,但不满足MS MRI标准[12]。有学者提出,NMO-IgG已经被证实是NMO较为特异的一项免疫标记物[13]。因此2006年 Wingerchuck等[14]对1999年提出的NMO诊断标准进行了修改(表2)。
2007年,Wingerchuck等[15]在NMO基础上提出了 NMO谱系疾病(NMO spectrum disorders)的概念,包括的疾病有复发性脊髓炎(MRI病灶≥3个脊柱节段)、复发性视神经炎、伴系统性自身免疫病的视神经炎或脊髓炎、伴脑部病灶(下丘脑、胼胝体、脑室旁或脑干)的视神经炎或脊髓炎。
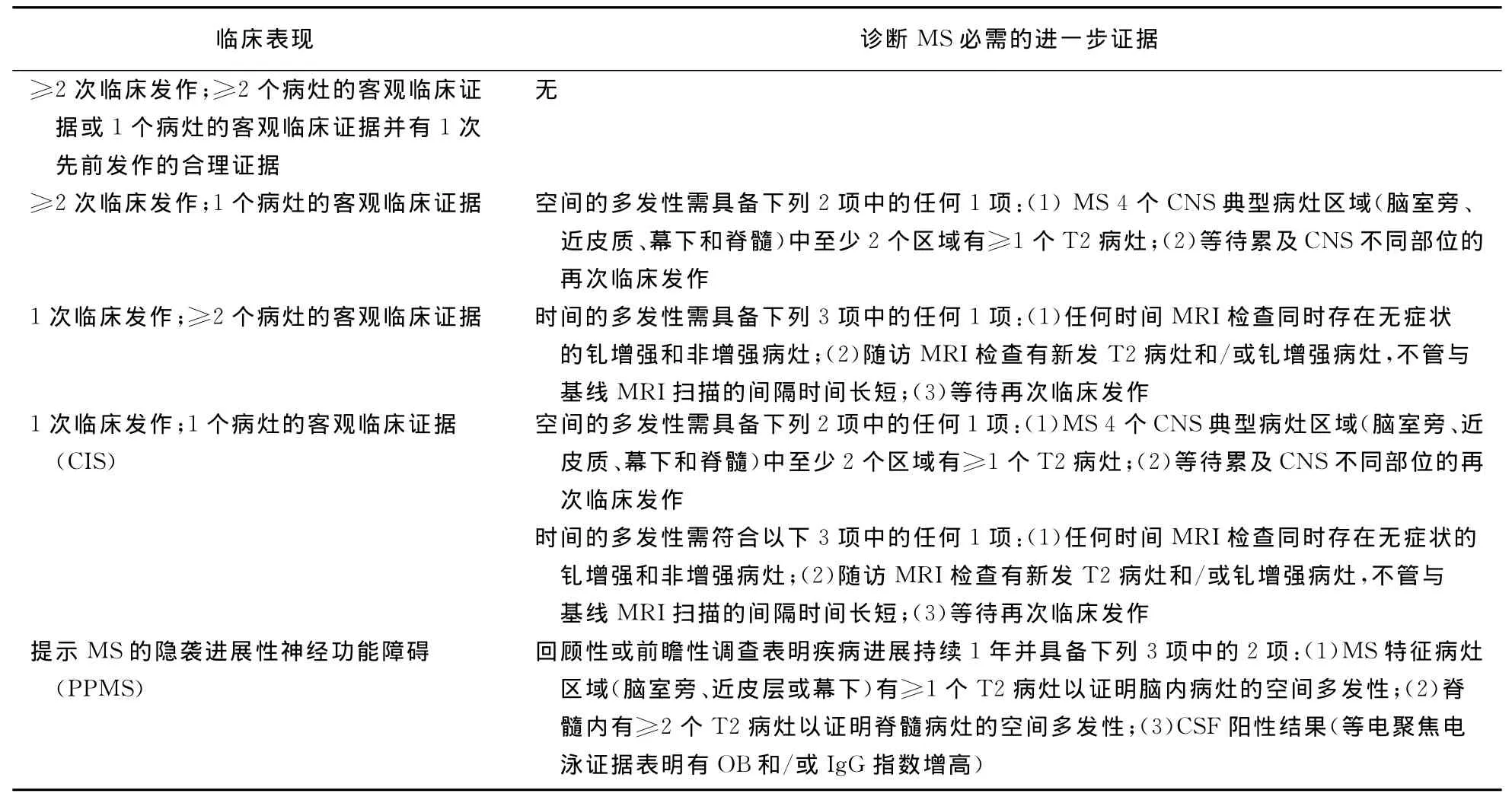
表1 McDonald诊断标准(2010)

表2 Wingerchuk等提出的NMO诊断标准(2006)
5 CIS
CIS概念的提出与近年来疾病修正治疗(disease modifying treatment,DMT)的使用密切相关,研究显示对于CIS患者早期使用DMT可明显降低CIS转变为CDMS的比率,并改善预后[16]。
CIS系指首次因中枢神经系统炎性脱髓鞘事件而导致的一组临床综合征,临床既可表现为孤立的视神经炎、脑干脑炎、脊髓炎,亦可出现多部位同时受累的复合临床表现。病灶特点为时间上的孤立,并且临床症状持续24h以上。据资料显示一半以上的CIS患者最终发展为MS。CIS患者中,易发展为MS的表现包括运动系统受累、共济失调、MRI显示颅内多发病灶,预后良好者多表现为只有感觉症状、临床症状完全缓解、5年后仍没有活动障碍、MRI表现正常等。
6 MS诊断中应注意的问题
综上所述,在MS诊断中应该强调如下几点:(1)脑内病灶的数目是观察的一个方面,更重要的是观察病变的分布、病灶的活动性及病灶特点,病灶有时间上或空间上多发,不能用其他病因来解释,尤其要重点观察近皮层病灶、脑室旁病灶、幕下病灶、胼胝体病灶;(2)CSF OB/24hIgG合成率应统一检测方法,实现检测标准化,使患者之间资料具有可比性;(3)为了减少误诊,应全面进行相关方面的检查包括自身抗体、ANCA、RF、抗“O”、ACE、ESR、特殊感染检查(包括HIV、梅毒、HBV、HCV)、脑血管病相关检查〔经颅多普勒(TCD)、血脂、血糖、血管B超、数字减影血管造影(DSA)〕等;(4)加强随访,关注病情演变并根据病情不断修订诊断。
[1]Goodin DS,Frohman EM,Garmany GP,et al.Disease modifying therapies in multiple sclerosis.Report of the therapeutics and technology assessment subcommittee of the American academy of neurology and the MS council for Clinical Practice Guidelines[J].Neurology,2002,58(2):169-178.
[2]Doggrell SA.Good results for early treatment of clinically isolated syndrome prior to multiple sclerosis with interferon beta-1band glatiramer group[J].Expert Opin Pharmacother,2010,11(7):1225-1230.
[3]Rolak LA,Fleming JO.The differential diagnosis of multiple sclerosis[J].Neurologist,2007,13(2):57-72.
[4]Frohman EM,Goodin DS,Calabresi PA,et al.The utility of MRI in suspected MS:Report of the therapeutics and technol-ogy Assessment Subcommittee of the American Academy of Neurology and The Practice Committee of the Child Neurology Society[J].Neurology,2003,61(5):602-611.
[5]Gronseth GS,Ashman EJ.The usefulness of evoked potentials in identifying clinically silent lesions in patients with suspected multiple sclerosis (an evidence-based review):Report of the Quality Standards Subcommittee of the American Academy of Neurology[J].Neurology,2000,54(9):1720-1725.
[6]Poser CM,Paty DW,Scheinberg L,et al.New diagnostic criteria for multiple sclerosis:guidelines for research protocols[J].Ann Neurol,1983,13:227-231.
[7]McDonald WI,Compston A,Edan G,et al.Recommended diagnostic criteria for multiple sclerosis:Guidelines from the international panel on the diagnosis of multiple sclerosis[J].Ann Neurol,2001,50:121-127.
[8]Polman CH,Reingold SC,Edan G,et al.Diagnostic criteria for multiple sclerosis:2005revision to the“McDonald criteria”[J].Ann Neurol,2005,58:840-846.
[9]Miller A.Revised diagnostic criteria for multiple sclerosis[J].Ann Neurol,2011,69:292-302.
[10]Wingerchuk DM,Hogancamp WF,O’Brien PC,et al.The clinical course of neuromyelitis optica(Devic’s syndrome)[J].Neurology,1999,53(5):1107-1114.
[11]Misu T,Fujihara K,Nakashima I,et al.Pure optic-spinal form of multiple sclerosis in Japan[J].Brain,2002,125(11):2460-2468.
[12]Pittock SJ,Lennon VA,Krecke K,et al.Brain abnormalities in neuromyelitis optica[J].Arch Neurol,2006,63:390-396.
[13]Lennon VA,Wingerchuck DM,Kryzer TJ,et al.A serum antibody marker of neuromyelitis optica:distinction from multiple sclerosis[J].Lancet,2004,364:2106-2112.
[14]Wingerchuk DM,Lennon VA,Pittock SJ,et al.Revised diagnostic criteria for neuromyelitis optica[J].Neurol,2006,66:1485-1489.
[15]Wingerchuk DM,Lennon VA,Lucchinetti CF,et al.The spectrum of neuromyelitis optica[J].Lancet Neurol,2007,6:805-815.
[16]Miller DH,Chard DT,Ciccarelli O.Clinically isolated syndromes[J].Lancet Neurol,2012,11:157-169.
