离子液体萃取精馏制取乙醇的计算机过程模拟与优化
2013-08-08王宝华任佳伟冉晓萌
王宝华 ,任佳伟 ,冉晓萌 ,邵 露 ,李 洁 ,王 妍,鲁 冰
(1 北京中医药大学,北京 100102;2 华北电力大学,北京 102206)
无水乙醇由于乙醇-水形成恒沸而无法采用普通精馏方法得到。在无水乙醇的生产方法中,萃取精馏是应用较多的一种,常用萃取剂有乙二醇、甘油、乙酸钾等[1-3]。离子液体与常见萃取剂相比,可通过对正、负离子的设计在相当大的范围内调控离子液体的理化性质,被称为“绿色溶剂”[4-5]。选择离子液体作夹带剂,集合了分离能力高、产物纯度高等优点,相对于其它液态夹带剂或固态无机盐有着更大的实际优势[6]。关于醇-水-复合萃取剂物系的模拟计算及加盐萃取精馏制备回收乙醇的实验报道较少。
本文作者对乙醇-水-[MMIM]+[DMP]-萃取精馏采用Aspen Plus 进行模拟,选用质量分数为95.0%的乙醇-水混合溶液作原料,选用[MMIM]+[DMP]-为萃取剂,通过模拟计算得出了最佳回流比、原料最佳进料位置、萃取剂进料量等数据。
1 流程模拟
1.1 离子液体参数的确定
离子液体的安东尼方程常数利用Rudkin 提出的方法进行估算,等压液体热容由José等[7]基团贡献模型提供计算值。

cp为定压摩尔热容,J/(mol·k),见式(2)。

离子液体的临界性质(包括临界温度、压力、体积等)的估算利用Valderrama等[8]提出的基团贡献理论。利用计算机也可以估算出离子液体的一些性质,如表1、表2所示。
1.2 热力学模型的选取
本研究根据李群生等[9]测定的乙醇-水-[MMIM]+[DMP]-体系的汽液平衡数据,利用Aspen Plus 提供的参数回归模块对NRTL 模型的二元交互作用参数值进行回归(表3)。乙醇-水的萃取剂选择1,3-二甲基咪唑二甲酯磷酸[MMIM]+[DMP]-进行模拟。
1.3 剩余曲线对萃取精馏的可行性分析
本文利用Aspen Plus 软件,选取NRTL 方程绘制了所要考察的体系在常压下的剩余曲线,如图1所示。

表1 基团贡献模型参数
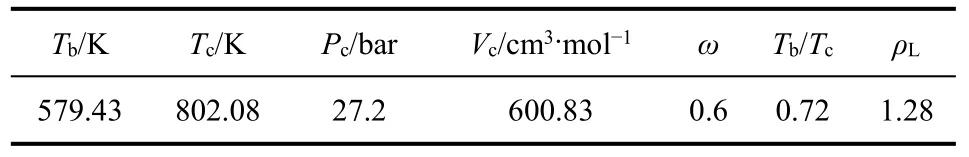
表2 官能团贡献理论计算的离子液体[MMIM]+[DMP]-临界性质
从图1 看出,对于含离子液体的三元体系,只有乙醇和水存在着共沸点,离子液体和乙醇、水之间并无共沸点存在,乙醇和水的共沸点为不稳定节点,并且为体系的最低沸点处,所有剩余曲线从乙醇和水的共沸点处出发,指向离子液体边线,并无精馏边界的存在,根据剩余曲线的原理,所有剩余曲线的汇聚点是稳定节点,意味着原料的蒸馏结果会是高纯度的乙醇。这说明本文采用离子液体[MMIM]+[DMP]-做萃取剂,通过萃取精馏分离乙醇和水是可行的。
1.4 流程叙述
图2为采用Aspen Plus 进行萃取精馏模拟流程图。

表3 NRTL 关联乙醇(1)-水(2)-[EMIM]+[BF4]-(3)三元体系所得到的二元交互参数

图1 三元体系乙醇(1)+水(2)+[MMIM]+[DMP]-(3)的剩余曲线图

图2 采用离子液体作萃取剂时的Aspen Plus 流程图
由萃取精馏塔、闪蒸罐和换热器组成的萃取精馏流程,原料经过换热后以饱和液体的状态进入精馏塔(T1)中,在精馏塔的塔顶得到高纯度的乙醇,塔底出料为萃取剂和水、少量乙醇的混合物,塔底出料(B1) 经过换热器(H1)后进入闪蒸罐进行减压操作达到汽液相分离的目的,闪蒸罐的底部采出离子液体通过泵(P1)、换热器(H2)返回精馏塔T1 循环使用,流程图中的B1、B2为温度不同的同一物流,B3、B4为压力不同的同一物流,IL为经过闪蒸分离后得到的高纯度的离子液体。
1.5 模拟操作条件
乙醇质量分数为95%的乙醇-水混合溶液作为原料,离子液体1,3-二甲基咪唑二甲酯磷酸盐[MMIM]+[DMP]-作为乙醇-水精馏的萃取剂进行萃取精馏的模拟计算,萃取精馏塔模拟条件如表4所示。

表4 萃取精馏塔模拟条件
2 模拟结果与讨论
2.1 萃取剂进料量FS对塔顶产品组成影响
萃取剂进料位置NSF=3,原料进料位置NF=21,回流比R=3.5,利用灵敏度分析做出塔顶乙醇质量分数w随萃取剂加入量的关系曲线,如图3所示。由图3 中曲线可知,随着萃取剂加入量的增加,塔顶产品质量分数随之增大,这主要是因为随着萃取剂加入量的增加,待处理物系乙醇-水的相对挥发度也随之增大,但离子液体加入量过大,会增加塔釜再沸器的负荷,且离子液体的价格比较昂贵,在实际工业应用中,故离子液体的加入量选30~40 kg/h为宜。
2.2 回流比对塔顶产品组成的影响
FS=35 kg/h,NSF=3,NF=21时,考察R对塔顶乙醇含量的影响,关系曲线如图4所示。图4 中显示了最佳回流比的存在,由于萃取剂的加入提高了待处理物系的挥发度。精馏塔的塔板上需要有充足的离子液体作萃取剂,若回流比过大会稀释塔板上的离子液体,不利于共沸物系的分离。萃取精馏的最佳回流比受回流量和溶剂的浓度的影响。
2.3 萃取剂进料位置NSF对塔顶产品组成的影响
考察萃取剂进料位置对塔顶产品组成的影响,见图5所示。随着萃取剂进料位置的增加,塔顶产品质量分数反而减小,随着离子液体加料位置的增加,塔内的共沸物系与离子液体的接触时间变短的缘故。因此离子液体的加料位置应该在塔体的上部。
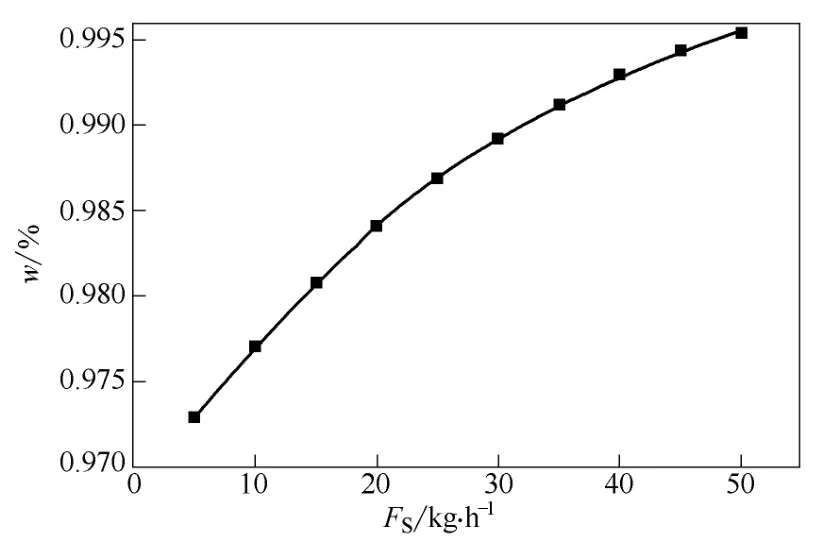
图3 萃取剂进料量对塔顶产品组成的关系曲线

图4 回流比对塔顶产品组成的关系曲线
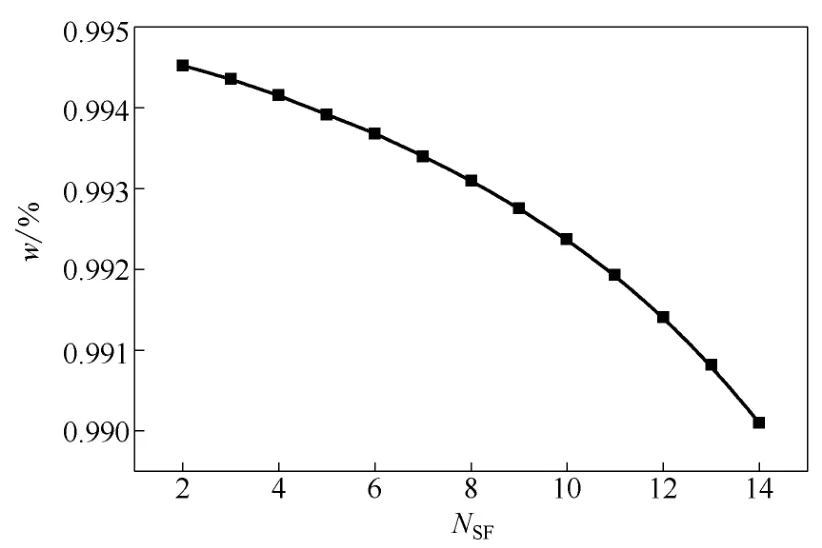
图5 萃取剂进料位置对塔顶产品组成的关系曲线
2.4 NF对塔顶产品组成的影响
考察原料进料位置对塔顶产品组成的影响,见图6所示。在其它条件相同的条件下,原料进料位置的不同,会影响塔顶、塔釜产品组成,从而也可以影响冷凝器和再沸器的热负荷。萃取精馏塔进料位置在23 块塔板附近达到最佳。
2.5 萃取精馏塔内汽液分布

图6 原料进料位置对塔顶产品组成影响
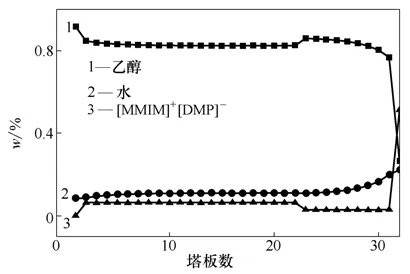
图7 塔内各塔板上液相浓度分布

图8 塔内各塔板上气相浓度分布
萃取精馏塔内汽液分布如图7和图8所示。由于第23 层塔板上有原料液的加入,使得离子液体含量明显下降,但到第32 层塔板,即再沸器中的离子液体含量突然提高,这是因为进入塔器内部的离子液体完全从塔釜采出。由此可以看出,塔顶、各塔板及塔釜中的离子液体含量不同,在设计塔板的时候,不能根据塔顶及塔釜中的离子液体含量来衡量各塔板上的离子液体含量。另外,由于各塔板上都有离子液体的存在,故乙醇对水的挥发度都不同程度的提高,从而达到了二者的分离。在精馏段,乙醇实现了增浓,而在提馏段,水实现了增浓。
2.6 萃取精馏塔内温度分布
灵敏板即精馏塔中温度变化最显著的塔板,通常可以通过测量该塔板上的温度变化来监控整个全塔的操作状况,这样有利于对精馏塔进行有预见性的调节。
萃取精馏塔内各塔板上温度分布见图9所示。通过分析温度变化发现,只是在萃取剂进料板、原料进料板和塔釜有显著的温度变化,这3个主要变化的拐点主要是因为离子液体的含量变化使得温度发生变化,其它塔板温度变化很小,故以离子液体作为萃取剂的萃取精馏塔的灵敏板较难确定。
2.7 萃取精馏塔各塔板上汽液相流率

图9 塔内各塔板上温度分布

图10 各塔板上汽液相流率
图10 反映了离子液体作为萃取剂的塔内各塔板汽液相流率分布情况,可以看出汽、液相流率的变化趋势是相同的。由于塔顶全凝,汽相流率从零开始,原料进料板处加入了乙醇-水原料液,所以汽液相流率均发生了突变。液体加料使得液相流率的变化较汽相流率的变化要显著。同时第2块塔板是离子液体加料板,所以在第2 块塔板处汽液相流率也增加。对于以离子液体作为萃取剂的精馏过程计算,应注意萃取剂进料板、原料液进料板和塔釜的浓度发生突变的情况。
2.8 各塔板汽液平衡常数的K值分布情况
萃取精馏塔内各塔板上温度分布见图11所示。由图11 可知,在全塔范围内,乙醇的平衡常数总大于水,并且在精馏段,乙醇的平衡常数有不断增长趋势,在原料进料板处发生突变,但随着板数增加,乙醇平衡常数又不断增加,到再沸器处,因为离子液体含量很大,所以其平衡常数达到最大值。而随着塔板数的增加,水的平衡常数一直减小。从而保证了乙醇和水在塔板上分离。
3 结论
(1)利用剩余曲线,分析了离子液体[MMIM]+[DMP]-作为乙醇-水精馏的萃取剂的可行性。

图11 各塔板上汽液平衡常数的K值分布情况
(2)对[MMIM]+[DMP]-作为萃取剂用于乙醇-水物系的萃取精馏过程采用Aspen Plus 软件进行了流程模拟,进一步考察了[MMIM]+[DMP]-用于乙醇-水萃取精馏的可行性。经过模拟得出了最优条件:原料进料位置为第23 块塔板,萃取剂进料量35 kg/h,R=1,萃取剂进料位置为第2 块塔板,塔顶产品浓度可达到99.6%,为[MMIM]+[DMP]-用于乙醇-水萃取精馏的实验研究提供了设计及操作参数。
[1]王洪海,李春丽,方静,等.加盐萃取精馏制取无水乙醇过程的模拟[J].石油化工,2008,37(3):258-261.
[2]李沫林,陈砺,严总诚,等.燃料乙醇脱水工艺的研究与展望[J].食品工业科技,2010,31(5) :410-413.
[3]Benedict M,Runin R L.[J].Trans.Am.Inst.Chem.Eng.,1945,41:353-370.
[4]李汝雄,王建基.绿色溶剂离子液体的制备与应用[J].化工进展,2002,21(1):43-48.
[5]Welton T.Room-temperature ionic liquids solvents for synthesis and catalysis[J].Chem.Rev.,1999,99(8):2071-2083.
[6]Orchille’s A V,Miguel P J,Vercher E.Ionic liquids as entrainers in extractive distillation :Isobaric vapor-liquid equili-bria for acetone+methanol+l-ethyl-3-methylimidazolium trifluoromethane sulfonate[J].Journal of Chemical and Engineering Data,2007,52(1):141-147.
[7]Valderrama J O,Toro A,Rojas R E.Prediction ofthe heat capacity of ionic liquids using the mass connectivity index and a group contribution metbod[J].Chem.Thermodynamics,2011,43:1068-1073.
[8]Valderrama J O,Robles P A.Critical properties,normal boiling temperatures and acentric factors of fifty ionic liquid[J].Ind.Eng.Chem.Res.,2007,46:1338-1344.
[9]李群生,王海川,冉晓萌,等.乙醇-水-离子液体三元体系的气液平衡测定及其萃取精馏试验[J].现代化工,2012,32(2):69-73.
