脱氢枞胺磷钨酸盐催化1-辛烯的氧化反应研究
2013-07-18王小淑黄道战朱守记蓝虹云
颜 芳,王小淑,黄道战,朱守记,蓝虹云
(广西民族大学化学化工学院广西林产化学与工程重点实验室,广西南宁530008)
脱氢枞胺磷钨酸盐催化1-辛烯的氧化反应研究
颜 芳,王小淑,黄道战,朱守记,蓝虹云
(广西民族大学化学化工学院广西林产化学与工程重点实验室,广西南宁530008)
以脱氢枞胺(DHA)与Keggin型磷钨酸(HPW)反应制备脱氢枞胺磷钨酸盐(DHPW),运用红外光谱、紫外光谱对其结构进行表征,并以催化H2O2氧化1-辛烯为探针反应,考察脱氢枞胺磷钨酸盐的催化性能。结果表明,脱氢枞胺磷钨酸盐具有氧化-酸双功能催化作用,能催化H2O2氧化1-辛烯生成1,2-环氧辛烷、1,2-二羟基辛烷和2-羟基辛烷;在无溶剂或极性溶剂中,1,2-环氧辛烷易发生环氧开环水解反应,选择性较低;在非极性溶剂中,1,2-环氧辛烷的选择性较高,在1,2-二氯乙烷用量为5 m L、1-辛烯用量为5 mmol、催化剂用量为0.075 g、H2O2用量为5.0 mmol、反应温度为30℃、反应时间为3 h的条件下,1,2-环氧辛烷的选择性最高,达到90.0%。
脱氢枞胺磷钨酸盐;1-辛烯;过氧化氢;催化氧化
杂多化合物包括杂多酸及其盐,是兼具酸性、氧化还原特性的环境友好型多功能催化剂,且其组成和性质易于调变[1],如以有机胺[2-4]、有机季铵阳离子[5-9]、金属阳离子[10-12]等对杂多化合物进行结构修饰,可调变其催化性能,实现均相、两相以及多相催化过程。目前杂多化合物的结构修饰与应用研究已成为多酸化学和催化材料研究的热点。
脱氢枞胺(DHA)是可再生林产资源松香的深加工衍生物,拥有亲脂性好、性质稳定的三元菲环骨架结构,以及化学活性的胺基官能团。研究脱氢枞胺与杂多酸的反应,探讨其对杂多酸的结构、性质以及催化性能的影响,对拓展松香深加工产品应用途径,开发新的杂多化合物催化材料,具有理论和实际应用价值。
作者首次以脱氢枞胺与Keggin型磷钨酸(HPW)反应制备脱氢枞胺磷钨酸盐(DHPW),研究脱氢枞胺对磷钨酸的结构、性质的影响,并以催化H2O2氧化1-辛烯为探针反应,考察了脱氢枞胺磷钨酸盐的催化性能。
1 实验
1.1 脱氢枞胺磷钨酸盐的制备
称取1.5 g磷钨酸,加入5 m L 95%乙醇溶解,在搅拌下滴加到由0.4 g脱氢枞胺和20 m L 95%乙醇配成的溶液中;滴加完毕,继续搅拌反应2 h,过滤,在60℃、0.9 Pa的真空条件下干燥,得淡黄色固体粉末,即脱氢枞胺磷钨酸盐。
1.2 脱氢枞胺磷钨酸盐催化1-辛烯的氧化反应
向装有回流冷凝管的恒温磁力搅拌夹套反应器中依次加入5 mmol 1-辛烯、适量的溶剂、催化剂和30% H2O2,在设定温度下搅拌反应;反应结束后,反应混合物冷却至室温,静置分层;分出有机相,用气质联用仪进行定性分析,用气相色谱测定反应混合物各组分的含量,计算1-辛烯的转化率和产物的选择性。
1.3 测试与表征
(1)红外光谱用Nicolet 550型红外光谱仪测定, KBr压片,扫描范围400~4000 cm-1。
(2)紫外光谱用GBC 916型紫外可见分光光度计测定,波长范围190~400 nm。
(3)气相色谱用Shimadzu GC-14B型气相色谱仪测定,色谱条件:DB-5型弹性石英毛细管色谱柱(30 m×0.25 mm×0.25 mm),N2为载气,FID检测器,进样口和检测器温度均为230℃,程序升温:初温60℃,保持0.5 min;以5℃·min-1升温到80℃,保持0.5 min;以20℃·min-1升温到140℃,保持0.5 min;以4℃·min-1升温到180℃,保持0.5 min;以2℃·min-1升温到230℃,保持5 min。
(4)反应混合物的组成用PE Clarus500型气质联用仪测定,色谱条件与气相色谱分析条件相同。
2 结果与讨论
2.1 脱氢枞胺磷钨酸盐的结构表征
2.1.1 紫外光谱
以无水乙醇为溶剂,脱氢枞胺、磷钨酸和脱氢枞胺磷钨酸盐的紫外光谱如图1所示。
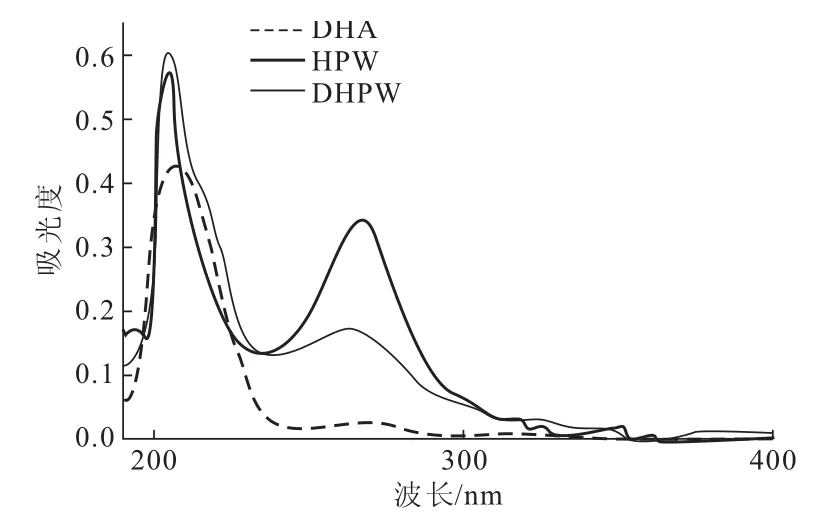
图1 脱氢枞胺、磷钨酸和脱氢枞胺磷钨酸盐的紫外光谱Fig.1 Ultraviolet spectra of dehydroabietyl amine(DHA), phosphotungstic acid(HPW)and dehydroabietyl ammonium phosphotungstate(DHPW)
由图1可见,3种化合物在266 nm处都存在明显的吸收峰,但吸收峰的强度和归属不同:脱氢枞胺的紫外吸收特征峰较弱,属于脱氢枞基中苯环的共轭双键π-π电子跃迁;磷钨酸的特征峰较强,属于Ob→W和Oc→W的荷移跃迁,是Keggin结构POM的特征峰[13];脱氢枞胺磷钨酸盐的吸收峰强度介于脱氢枞胺和磷钨酸之间,但吸收峰没有发生明显位移,表明脱氢枞胺与磷钨酸反应生成的脱氢枞胺磷钨酸盐仍保持Keggin杂多酸的结构特征,即脱氢枞胺的引入没有改变磷钨酸阴离子的内部结构。
2.1.2 红外光谱
脱氢枞胺、磷钨酸和脱氢枞胺磷钨酸盐的红外光谱如图2所示。
由图2可见,脱氢枞胺磷钨酸盐在700~1100 cm-1范围出现代表Keggin型磷钨酸阴离子的4个特征吸收峰[13]:1080 cm-1处为磷与内氧键P-Oa的伸缩振动吸收峰,961 cm-1处为金属端氧键W=Od的伸缩振动吸收峰,894 cm-1处为金属桥氧键W-Ob-W的伸缩振动吸收峰,818 cm-1处为金属角氧键WOc-W的伸缩振动吸收峰;与Keggin型磷钨酸的特征吸收峰相比,W=Od、P-Oa和W-Ob-W三个吸收峰的强度明显减弱,W-Oc-W吸收峰强度变化不大,此外,W=Od吸收峰发生了蓝移。这进一步表明,脱氢枞胺的引入不改变磷钨酸阴离子的内部结构,但会影响金属簇之间的结合情况,使部分金属簇的原子键间结合力增强,键的振动频率降低,对应961 cm-1处的红外吸收峰发生了蓝移。

图2 脱氢枞胺、磷钨酸和脱氢枞胺磷钨酸盐的红外光谱Fig.2 Infrared spectra of dehydroabietyl amine(DHA), phosphotungstic acid(HPW)and dehydroabietyl ammonium phosphotungstate(DHPW)
2.2 1-辛烯氧化产物的分布特征
质谱分析表明,以乙酸乙酯为溶剂,脱氢枞胺磷钨酸盐催化H2O2氧化1-辛烯的反应,生成了1,2-环氧辛烷(Ⅰ)、1,2-二羟基辛烷(Ⅱ)和2-羟基辛烷(Ⅲ)等氧化产物,其中主要的氧化产物是1,2-环氧辛烷,产物各组分的质谱均与标准品的质谱相符。这表明,脱氢枞胺磷钨酸盐具有氧化-酸双功能催化作用,首先催化H2O2氧化1-辛烯生成1,2-环氧辛烷,再经环氧开环水解反应生成1,2-二羟基辛烷或2-羟基辛烷,反应式如图3所示。
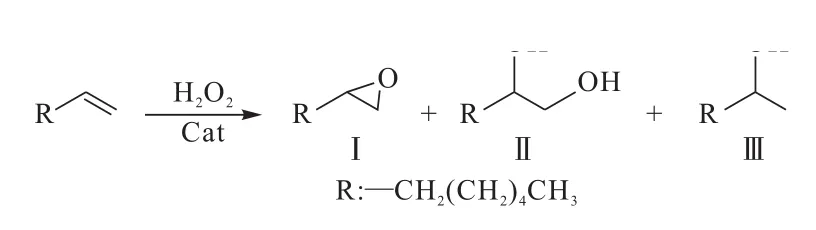
图3 1-辛烯的氧化反应式Fig.3 Oxidation reaction of 1-octene
2.3 脱氢枞胺磷钨酸盐催化1-辛烯氧化反应条件的优化
2.3.1 溶剂对1-辛烯氧化反应的影响(表1)
由表1可知,溶剂对1-辛烯的氧化反应有较大影响。在无溶剂条件下,1-辛烯的转化率较高,达到43.9%,氧化产物1,2-环氧辛烷的选择性为21.9%;而在有机溶剂条件下,1-辛烯的转化率降低,但1,2-环氧辛烷的选择性明显升高,且溶剂极性越小,升幅越大;在非极性溶剂1,2-二氯乙烷中,1,2-环氧辛烷的选择性高达88.3%,环氧开环水解反应产物极少。有机溶剂对1,2-环氧辛烷选择性影响的顺序为:1,2-二氯乙烷>氯仿>乙酸乙酯。这是由于,在有机溶剂条件下,反应体系被稀释,底物、催化剂、氧化剂和氧化产物之间的接触碰撞程度减弱,氧化反应速度减慢,1-辛烯的转化率降低;在非极性溶剂中,催化剂的“B酸位点”释放质子的能力减弱,环氧开环、水解反应被抑制,1, 2-环氧辛烷的选择性较高。因此,后续实验以1,2-二氯乙烷作为溶剂。
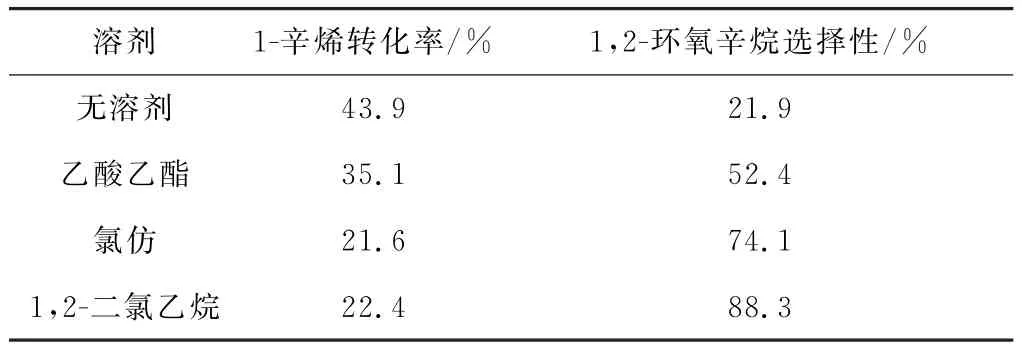
表1 溶剂对1-辛烯转化率和1,2-环氧辛烷选择性的影响Tab.1 Effect of solvent on conversion rate of 1-octene and selectivity of 1,2-epoxy octane
2.3.2 催化剂用量对1-辛烯氧化反应的影响(表2)
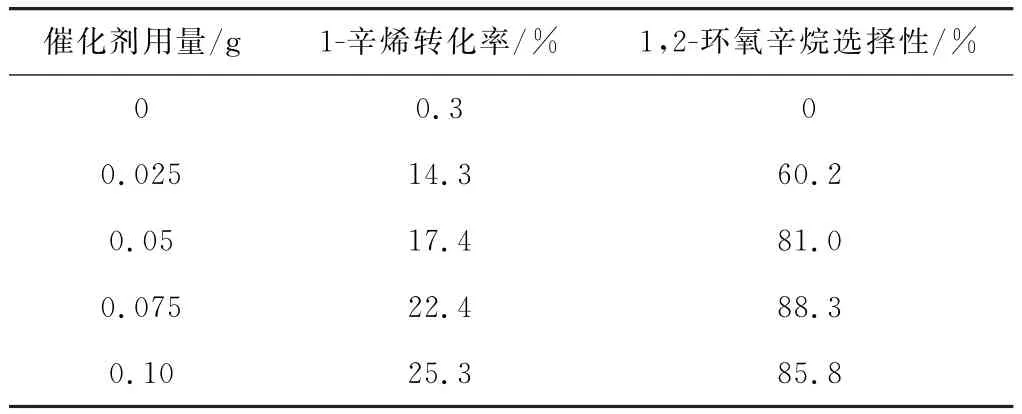
表2 催化剂用量对1-辛烯转化率和1,2-环氧辛烷选择性的影响Tab.2 Effect of catalyst dosage on conversion rate of 1-octene and selectivity of 1,2-epoxy octane
由表2可知,不加催化剂时,1-辛烯的转化率极低,仅为0.3%;加入脱氢枞胺磷钨酸盐催化剂后, 1-辛烯的转化率随着催化剂用量的增加而逐渐升高,同时1,2-环氧辛烷的选择性明显提高;当催化剂用量为0.075 g时,1,2-环氧辛烷的选择性最高,为88.3%;催化剂用量继续增加,环氧选择性降低。因此,催化剂用量选择0.075 g为宜。
2.3.3 H2O2用量对1-辛烯氧化反应的影响(表3)
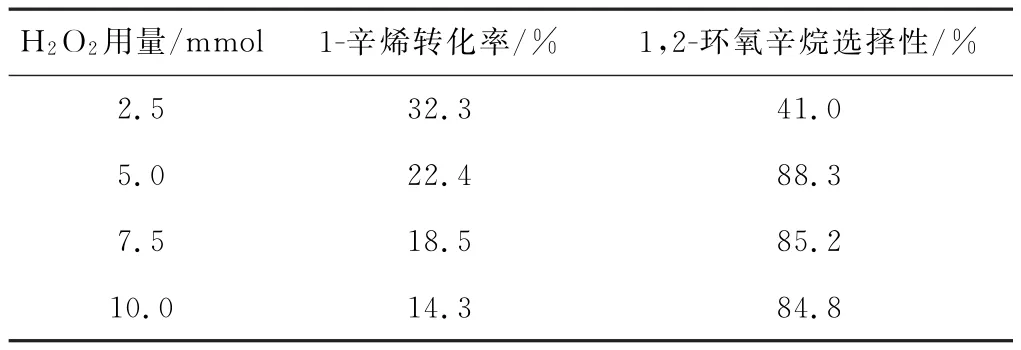
表3 H2O2用量对1-辛烯转化率和1,2-环氧辛烷选择性的影响Tab.3 Effect of H2O2amount on conversion rate of 1-octene and selectivity of 1,2-epoxy octane
由表3可知,当H2O2用量为5.0 mmol时,1-辛烯的转化率较高,1,2-环氧辛烷的选择性最高,为88.3%;此后随着H2O2用量的增加,1-辛烯的转化率反而降低,这可能是由于H2O2用量超过一定值后,其单位时间内生成的分子氧的量相应增多,从而导致反应底物、催化剂与氧化剂之间的反应点相应减少。因此,H2O2用量选择5.0 mmol为宜。
2.3.4 反应温度对1-辛烯氧化反应的影响(表4)

表4 反应温度对1-辛烯转化率和1,2-环氧辛烷选择性的影响Tab.4 Effect of reaction temperature on conversion rate of 1-octene and selectivity of 1,2-epoxy octane
由表4可知,随着反应温度的升高,1-辛烯的转化率逐渐升高;当反应温度为30~50℃时,1,2-环氧辛烷的选择性较高,均超过88%,且反应温度的升高对1,2-环氧辛烷的选择性影响不明显;当反应温度升高至60℃时,1,2-环氧辛烷的选择性反而降低至62.7%。这表明,反应温度低于60℃,1-辛烯的氧化反应较温和,以环氧化反应为主;反应温度高于60℃, 1-辛烯的氧化反应加剧,并伴随着1,2-环氧辛烷的开环、水解反应的发生。因此,为确保较高的环氧化反应的选择性,反应温度选择30℃为宜。
3 结论
(1)在乙醇溶剂中,脱氢枞胺与磷钨酸反应制备脱氢枞胺磷钨酸盐,脱氢枞胺的引入没有改变磷钨酸阴离子的内部结构。
(2)脱氢枞胺磷钨酸盐具有氧化-酸双功能催化作用,能够催化H2O2氧化1-辛烯,反应工艺条件对脱氢枞胺磷钨酸盐的催化性能有较大的影响:在无溶剂或极性溶剂条件下,脱氢枞胺磷钨酸盐的酸催化作用增强,1-辛烯的氧化反应速度加快,但1,2-环氧辛烷易发生环氧开环、水解反应;在非极性溶剂条件下,脱氢枞胺磷钨酸盐主要表现为环氧催化作用,酸催化作用较弱,而且氧化反应速度较慢,1-辛烯转化率较低,但1, 2-环氧辛烷的选择性较高。
(3)在非极性溶剂1,2-二氯乙烷用量为5 m L、1-辛烯用量为5 mmol、催化剂用量为0.075 g、H2O2用量为5.0 mmol、反应温度为30℃、反应时间为3 h的条件下,1,2-环氧辛烷的选择性最高,达到90.0%。
[1] 王德胜,闫亮,王晓来.杂多酸催化剂研究进展[J].分子催化, 2012,26(4):366-375.
[2] 周长江,葛汉青,冷炎,等.用于苯与分子氧羟基化制苯酚的长链脂肪胺修饰的杂多酸催化剂[J].催化学报,2010,31(6):623-625.
[3] 柳士忠,张贞文,王俊,等.十八胺杂多阴离子杂化LB膜的制备与表征[J].无机化学学报,2001,17(1):96-100.
[4] 王丽丽,武启华,王向宇.(+)-α-苯乙胺磷钨杂多化合物的合成、表征和催化不对称环氧化性能[J].催化学报,2008,29(10):992-996.
[5] 张予辉,叶天旭,孙颖.相转移催化剂/过氧化氢催化氧化降低流化催化裂化汽油烯烃的性能研究[J].精细石油化工,2011,28 (3):5-9.
[6] 李学超,吴学明,唐安斌.二氧化双环戊二烯的无溶剂催化合成[J].精细化工中间体,2010,40(1):54-57.
[7] 李超,吾满江·艾力,哈丽丹·买买提.过氧化磷钨杂多酸季铵盐催化氧化苯乙烯的研究[J].化学与生物工程,2008,25(5):16-19.
[8] 冯树波,杨华,郑二丽,等.磷钨杂多酸季铵盐催化脂肪酸甲酯环氧化[J].分子催化,2010,24(3):222-227.
[9] Hua Hui,Ma Bao-chun,Tong De-jie,et al.[π-C5H5N(CH2)15CH3]3[PMoW3O24]:A heteropolyoxomolybdotungstate catalyst for efficient and recyclable epoxidation of 1-octene with 30% H2O2using environmentally friendly solvent[J].Journal of Molecular Catalysis,2009,23(2):97-105.
[10] Fan Zong-liang,Wang Xiao-rui,Li Gui-xian,et al.Catalytic oxidation of toluene to benzaldehyde over Dawson-type heteropoly acid neodymium salt[J].Journal of Molecular Catalysis,2012,26 (1):32-38.
[11] 范宗良,张彩霞,李贵贤.Keggin型多金属氧酸盐催化醛与乙酸酐合成1,1-二乙酸酯[J].分子催化,2011,25(1):64-68.
[12] 许招会,廖维林,王牲.磷钨酸镧催化合成缩醛(酮)的研究[J].分子催化,2008,22(1):39-43.
[13] 王恩波,胡长文,许林.多酸化学导论[M].北京:化学工业出版社,1988.
Study on Catalytic Oxidation of 1-Octene with Hydrogen Peroxide by Dehydroabietyl Ammonium Phosphotungstate
YAN Fang,WANG Xiao-shu,HUANG Dao-zhan,ZHU Shou-ji,LAN Hong-yun
(Guangxi Key Laboratory of Chemistry and Engineering of Forest Products,College of Chemistry and Chemical Engineering,Guangxi University for Nationalities,Nanning 530008,China)
Dehydroabietyl ammonium phosphotungstate(DHPW)synthesized from dehydroabietyl amine (DHA)and Keggin-type phosphotungstic acid(HPW)has been structurally characterized by IR and UV spectroscopy,and then its catalytic performance on oxidation of 1-octene is investigated with aqueous 30%hydrogen peroxide under different conditions.The results show that DHPW has an oxidative-acidic bifunctional catalysis for the conversion of 1-octene in the presence of hydrogen peroxide to 1,2-epoxy octane,1,2-dihydroxy octane and 2-hydroxy-octane,the selectivity of 1,2-epoxy octane in non-polar solvents is relatively high and decreases in free-solvents or polar solvents because 1,2-epoxy octane can be decomposed by the ring-opening of epoxide. Under the reaction conditions as follows:1,2-dichloroethane amount is 5 m L,DHPW dosage is 0.075 g,1-octene amount is 5 mmol,hydrogen peroxide amount is 5.0 mmol,the reaction temperature is 30℃,the reaction time is 3 h,the selectivity of 1,2-epoxy octane reaches the maximum value of 90.0%.
dehydroabietyl ammonium phosphotungstate;1-octene;hydrogen peroxide;catalytic oxidation
TQ 203.5
A
1672-5425(2013)03-0046-04
10.3969/j.issn.1672-5425.2013.03.012
广西自然科学基金资助项目(2011GXNSFA018057),广西教育厅科研项目(201010LX083),广西民族大学引进人才科研启动项目(2010QD020)
2012-12-06
颜芳(1987-),女,湖南娄底人,硕士研究生,研究方向:天然产物开发与应用;通讯作者:黄道战,高级实验师,E-mail: huangdaozhan@gxun.cn。
