中国朝鲜族人群MDR1基因多态性与环孢素A谷浓度的相关性研究
2013-05-22唐哲孙玉坤杨媛媛何伟张敬一武警辽宁省总队医院药剂科沈阳004沈阳市苏家屯区中医医院药剂科沈阳00沈阳军区总医院药剂科沈阳006
唐哲,孙玉坤,杨媛媛,何伟,张敬一(.武警辽宁省总队医院药剂科,沈阳 004;.沈阳市苏家屯区中医医院药剂科,沈阳 00;.沈阳军区总医院药剂科,沈阳 006)
环孢素A(Cyclosporine A,CsA)为免疫抑制剂,是由11个氨基酸组成的中性环状多肽,属钙调磷酸酶抑制剂家族。有报道[1]指出,CsA在药动学、毒理学、敏感性和耐受性等方面存在着明显的个体差异,而且治疗指数较窄,引起这种差异的原因目前尚不十分清楚。临床上,监测免疫抑制剂的药物浓度,可以更好地调整药物使用剂量,以及减少药品不良反应发生。CsA的体内药物浓度和治疗效果存在相关性[2],因此,临床上对其血药浓度监测是十分必要的。
P糖蛋白(P-gp)是由多药耐药基因(MDR1)编码的一种产物,是一个膜蛋白,属三磷酸腺苷(ATP)结合家族。P-gp主要作用为能量依赖性地将作用底物由细胞膜内转运至细胞膜外,起跨膜渗透泵的作用。当P-gp活性增加时,底物将大量被转运至膜外,反之亦然。现有文献提示MDR1基因具有48个单核苷酸多态性(SNP),其中,有重要的功能意义的为第26外显子C3435 T位点上的基因多态性,且不同种族间差异较大[3]。近年来,有关C3435 T基因多态性与CsA体内代谢的相关性的报道已有很多,但有关中国朝鲜族肾移植术后患者CsA谷浓度与MDR1C3435 T位点的基因多态性之间的关联性尚无报道。本文以75例肾移植术后患者(中国朝鲜族)为探讨对象,采用聚合酶链反应(PCR)扩增MDR1 C3435 T基因,利用DNA限制性片段长度多态性(Restriction fragment length polymorphism,RFLP)方法检测了C3435 T的多态性,并探讨了CsA的谷浓度与MDR1 C3435 T基因位点多态性之间的相关性,希望为临床个体化用药提供依据。
1 材料
1.1 仪器
ABI 2720 PCR扩增仪、紫外凝胶成像系统(Gene Company);TDxFLx/TDx免疫分析仪(珠海健民医用科技有限公司);Eppendorf 5804 R冷冻离心机(Gene Company);DYY-6 C电泳仪(上海笛柏实验设备有限公司);HH-S恒温水浴锅(郑州佳创仪器设备有限公司);V-32涡旋混合器(上海凌初科学仪器有限公司)。
1.2 药品与试剂
提取基因组DNA试剂盒(广州健仑生物科技有限公司);引物(广州健仑生物科技有限公司);限制性内切酶MboI与Taq酶(郑州博美生物技术有限公司);硼酸(优级纯,国药集团化学试剂北京有限公司);琼脂糖凝胶、溴化乙锭(EB)(北京奇松生物科技有限公司);乙二胺四乙酸二钠盐(EDTA-Na2,纯度>99.0%)、无水乙醇(纯度为99.7%)(北京索莱宝科技有限公司)。
2 方法
2.1 研究对象
75例肾移植术后患者均为沈阳军区总医院门诊随访患者(中国朝鲜族),患者接受肾移植手术时间范围为2001-2011年,全部为首次肾移植术。其中,男性42例,女性33例;年龄18~65岁,平均年龄(42.5±10.6)岁;体质量41~106 kg,平均体质量(67±9.8)kg。所有入组的患者均同时口服麦考酚酸吗乙酯和CsA抗排斥治疗,未出现严重感染或排斥反应,手术时间>0.5年。入选的患者在2周内没有服用过可能对CsA体内代谢有影响的药物,如促胃动力药、H1受体拮抗药、钙离子拮抗药、抗结核类药、抗癫痫药、大环内酯类及四环素类抗生素等。
2.2 基因分型
提取人类基因组DNA:抽取200 μl静脉血液,按照试剂盒说明提取DNA。MDR1 C3435 T基因序列的扩增:向反应体系中加入10×Buffer 5 μl、dNTP 5 μl,根据文献合成的引物[4],即:10Pmol/μl上游与下游引物各2μl(上游引物:5′-TGCTGGTCCTGAAGTTGATCTGTGAAC-3′;下游引物:5′-ACATTA GGCAGTGACTCGATGAAGGCA-3′)、DNA 样品 2.5μl、Taq酶0.2 μl、双蒸水18.3 μl,总体积30 μl。PCR反应条件为:94℃预变性3 min,然后94℃变性30 s,60℃复性30 s,72℃延伸1 min,共35个循环,最后72℃再延伸5 min。扩增的产物长度为248 bp,经限制性内切酶MboI 37℃酶切4 h,65℃水浴灭活20 min。以2.0%琼脂糖凝胶电泳分离,EB染色,紫外成像系统观察结果。
2.3 数据分析
3 结果
MDR1 C3435 T基因片段PCR扩增后的产物为248 bp,电泳显示结果如图1。MDR1 C3435 T基因片段PCR扩增后的酶切产物如图2[1、2、6、7为野生型等位基因(C/C型),产生172、60、16 bp 3个片段;3、4、5、8为杂合型(C/T型),产生238、172、60、16 bp 4个片段;9为突变型等位基因(T/T型),产生248、16 bp 2个片段;由于16 bp片段太短,已泳出凝胶板,故未能在图中观察到]。M为DNA标准品(Marker)。75例患者的基因分布频率为C/C 31例(41.3%)、C/T 37例(49.3%)、T/T 7例(9.3%),等位基因频率分别为C66%、T34%,具体见表1。患者的MDR1C3435 T各基因型频率经Hardy-Weinberg遗传平衡检验,结果均符合遗传平衡定律,说明研究对象符合群体代表性。
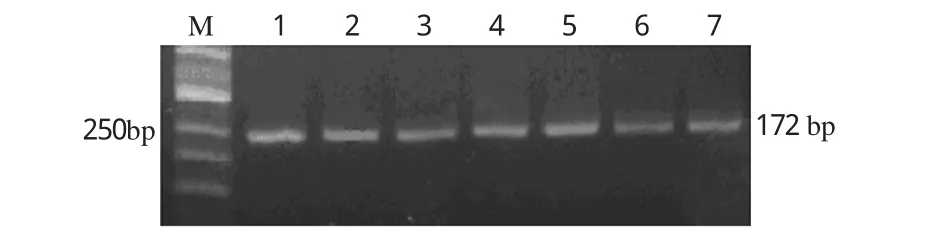
图1 MDR1C3435T基因多态性经PCR后电泳图M.Marker;1~7.PCR产物Fig 1 Electrophoretogram of MDR1 C3435T gene polymorphism by PCRM.Marker;1-7.PCR products
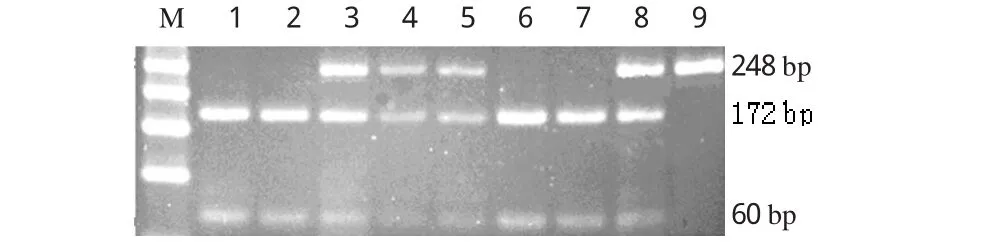
图2 MDR1C3435T基因多态性经PCR-RFLP电泳图M.Marker;1~9.PCR-RFLP产物Fig 2 Electrophoretogram of MDR1 C3435T gene polymorphism by PCR-RFLPM.Marker;1-9.PCR-RFLP products
在对表1分析中发现,P值均>0.05,因此认为中国朝鲜族肾移植术后患者的MDR1C3435 T基因多态性对服药剂量、CsA谷浓度及调整剂量浓度没有显著性影响。
4 讨论
C3435 T基因多态性是最早进行研究的,也是目前为止认为最有可能影响MDR1编码的P-gp功能表达,进而影响药物在体内的代谢。国外有学者认为,口服CsA吸收不完全、个体间吸收的差异大,主要与MDR1多态性有关[5-6]。由于免疫抑制剂CsA治疗窗范围较窄而药动学参数的个体间差异较大,因此对器官移植患者服用CsA血药浓度的监测是有必要的。CsA的血药浓度变化除了与个体的生理、病理因素有关外,还与遗传(种族、性别、基因多态性)和环境(食物或联合用药)等因素有关[7]。有研究表明,80%的口服CsA血药浓度的差异与肝脏细胞色素P4503 A(CYP3 A)和小肠P-gp的活性差异有关[3]。现已证明C3435 T的SNP与P-gp的表达最为密切,Hoffmeyer S等[8]首先报道具有T/T型的健康白种人群中,P-gp的表达比其他基因型降低了2倍。国外对MDR1基因型和表型的关系进行了很多研究,但结论并不一致。法国学者采用大样本肾移植病例研究显示[9],C1236 T对服用不同剂量CsA患者的ρmax、AUC0-4h有影响,统计学呈显著性差异;而CYP3 A5*3、C3435 T、G2677 T/A和MDR1-129 T>C则对不同剂量CsA的谷浓度、AUC0-12h、ρmax和AUC0-4h无显著影响。亚洲人心脏移植病例的研究提示[10],MDR1G2677 T/A、C3435 T、C1236 T对CsA谷浓度、AUC0-12h、AUC0-4h和ρmax无明显影响;而CsA的剂量与基因类型的相关性却存在于单倍体型TT-TT-TT、CC-GG-CC和CT-GT-CT之间,即CsA谷浓度、AUC0-12h、AUC0-4h和ρmax按照野生型纯合子、杂合子、突变型纯合子顺序,依次增高[11]。因此,服用不同剂量CsA的谷浓度是否会受到MDR1、CYP3 A5和CYP3 A4等基因多态性的影响,意见还不统一,这可能与人种差异、性别、药物剂量、剂型、疾病状况等综合因素影响有关。
表1 MDR1C3435T不同基因型患者各项参数比较()Tab 1 Comparison of parameters in different C3435T gene types()
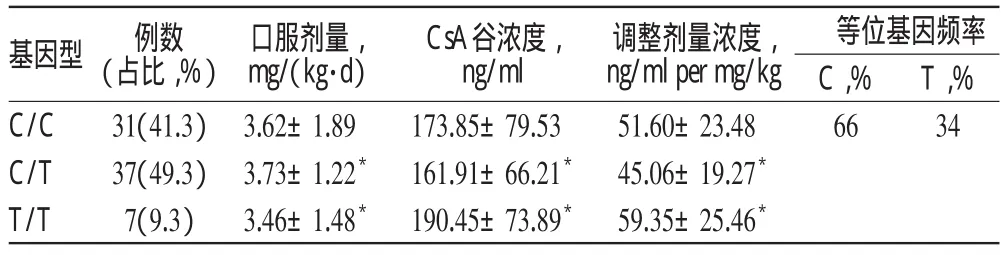
表1 MDR1C3435T不同基因型患者各项参数比较()Tab 1 Comparison of parameters in different C3435T gene types()
与C/C基因型比较:*P>0.05vs.C/C gene type:*P>0.05
基因型C/C C/T T/T例数(占比,%)31(41.3)37(49.3)7(9.3)口服剂量,mg/(k g·d)3.62±1.893.73±1.22*3.46±1.48*Cs A谷浓度,n g/ml 173.85±79.53161.91±66.21*190.45±73.89*调整剂量浓度,n g/ml p e r mg/k g 51.60±23.4845.06±19.27*59.35±25.46*等位基因频率C,%66 T,%34
C3435 T基因型的分布频率在不同的人种中存在差异,Wang Y等[12]研究112例中国汉族人群C3435 T位点C/C、C/T和T/T型的分布频率分别为37.5%、48.2%和14.3%,C等位基因频率为61.6%,T等位基因频率为38.4%。这与本研究结果相近,说明中国朝鲜族人群与中国汉族人群C3435 T基因多态性没有很大差别。Ameyaw MM等[4]研究发现非洲人群C等位基因频率明显增高,这可能与非洲人群处于胃肠道疾病易感地区有关,是自然选择的优势。
本文首次以中国朝鲜族肾移植术后患者为研究对象,考察了此人群MDR1中26外显子C3435 T多态性与CsA谷浓度的关系。试验结果提示,在现有采集样本下,未发现MDR1 C3435 T基因多态性对CsA谷浓度有显著性影响。这一结果与Wang Y等[12]就MDR1 C3435 T多态性对CsA剂量调整的谷浓度影响的研究结论相似,可以认为MDR1 C3435 T基因多态性可能不是影响CsA谷浓度的主要因素。
[1]王国俊,张青碧,孔伶俐.肾移植术后环孢素血药浓度与患者体内因素相关性分析[J].中国药房,2008,19(23):1795.
[2]王莉,卢一平,石明,等.肾移植术后应用2种不同剂量环孢素A的临床对照研究[J].中国药房,2008,19(11):844.
[3]Lown KS,Mayo RR,Leichtman AB,et al.Role of intestinal P-glycoprotein(mdr1)in interpatient variation in the oral bioavailability of cyclosporine[J].Clin Pharmacol Ther,1997,62(3):248.
[4]Ameyaw MM,Regateiro F,Li T,et al.MDR1pharmacogenetics:frequency of the C3435 T mutation in exon 26is significantly influenced by ethnicity[J].Pharmacogenetics,2001,11(3):217.
[5]Wählby U,Jonsson EN,Karlsson MO.Comparison of stepwise covariate model building strategies in population pharmacokinetic-pharmacodynamic analysis[J].AAPS Pharm Sci,2002,4(4):27.
[6]Zhang Y,Benet LZ.The gut as a barrier to drug absorption:combined role of cytochrome P4503 A and P-glycoprotein[J].Clin Pharmacokinet,2001,40(3):159.
[7]Hashida T,Masuda S,Uemoto S,et al.Pharmacokinetic and prognostic significance of intestinal MDR1expression in recipients of living-donor liver transplantation[J].Clin Pharmacol Ther,2001,69(5):308.
[8]Hoffmeyer S,Burk O,von Richter O,et al.Functional polymorphisms of the human multidrug-resistance gene:multiple sequence variations and correlation of one allele with P-glycoprotein expression and activity in vivo[J].Proc Natl Acad Sci USA,2000,97(7):3473.
[9]Anglicheau D,Thervet E,Etienne I,et al.CYP3 A5and MDR1genetic polymorphisms and cyclosporine pharmacokinetics after renal transplantation[J].Clin Pharmacol Ther,2004,75(5):422.
[10]Chowbay B,Cumaraswamy S,Cheung YB,et al.Genetic polymorphisms in MDR1and CYP3 A4genes in Asians and the influence of MDR1 haplotypes on cyclosporin disposition in heart transplant recipients[J].Pharmacogenetics,2003,13(2):89.
[11]Anglicheau D,Verstuyft C,Laurent-Puig P,et al.Association of the multidrug resistance-1gene single-nucleotide polymorphisms with the tacrolimus dose requirements in renal transplant recipients[J].J Am Soc Nephrol,2003,14(7):1889.
[12]Wang Y,Wang C,Li J,et al.Effect of genetic polymorphisms of CYP3 A5and MDR1on cyclosporine concentration during the early stage after renal transplantation in Chinese patients co-treated with diltiazem[J].Eur J Clin Pharmacol,2009,65(3):239.
