临床药师对1例骨科术后感染患者抗感染治疗的药学监护
2013-05-22文海岸青海大学附属医院临床药学科西宁810001
文海岸(青海大学附属医院临床药学科,西宁 810001)
骨科手术术后感染并不少见,常威胁到患者的术后康复和生命安全,因此,术后感染治疗方案和药物的选择是临床医师非常关注的问题。临床药师可利用自己的药学专业优势,参与术后感染患者药物的选择,提高合理用药水平。本文以1例骨科术后感染患者为例,探讨临床药师在骨科手术术后感染中如何发挥药学优势、促进患者康复。
1 病例资料
患者,男性,45岁,因“外伤致右膝疼痛,活动受限4 h”,于2012年6月29日收住我院骨科,诊断为“右侧胫骨平台骨折”。6月30日,血常规示:白细胞计数(WBC)14.19×109L-1,中性粒细胞百分比(N%)89.4%,中性粒细胞计数(N)12.70×109L-1;体温最高时为37.4℃。7月2日行“胫骨平台骨折切开复位内固定术”。7月4日,患者切口有持续渗出,并且WBC、C反应蛋白(CRP)、红细胞沉降率(ESR)、体温均较高,术后切口引起感染。给予头孢西丁抗感染治疗9 d,感染并未得到完全控制,遂将抗感染药物头孢西丁更换为使用万古霉素治疗5 d,感染得到有效控制。
由于患者术后发生感染导致内固定失效,遂于8月1日行“清创+胫骨平台骨折再次切开内固定术”,8月2日患者胃部不适,吐出黄色黏性液体30 ml,血常规示:WBC 19.98×109L-1,N%89.0%,N 17.80×109L-1。8月4日,患者腹痛、腹胀症状明显,考虑腹膜炎感染可能,给予头孢哌酮/舒巴坦钠联合甲硝唑进行治疗。8月5日行“阑尾切除术、后腹膜切开引流术”,并进行胸腔穿刺,置管引流。使用头孢哌酮/舒巴坦钠联合比阿培南抗感染治疗。8月9日,考虑到患者可能有真菌感染,给予卡泊芬净抗真菌治疗,给予利奈唑胺加强对革兰阳性球菌的作用。8月11日,患者既往有十二指肠溃疡,此次创伤应激后引起溃疡穿孔,并发后腹膜感染。根据相关检查和体征,考虑存在升结肠坏死穿孔,即刻行手术治疗,清除腹腔感染,行胃造口、空肠造口(肠内营养)、回肠造口、后腹膜充分引流,进行腹腔引流管持续冲洗引流。8月12日,患者腹胀症状较前好转。8月14日,粪便检出:热带假丝酵母菌。8月16日引流液检出:热带假丝酵母菌。经过积极治疗和引流,8月25日后体温正常。
2 临床药师参与药学监护情况
2.1 术后抗感染药物的调整
患者入院后完善相关检查,患者手术指征明确,且无明显手术禁忌证。于7月2日在全麻下行“胫骨平台骨折切开复位内固定术”。术前30 min给予头孢硫脒1 g静脉推注,术后给予头孢硫脒2 g,bid,ivgtt,预防用药1 d。
7月4日,患者引流出血性液体50 ml,手术切口持续有渗出,血常规示:WBC 22.03×109L-1,N%88.9%,N 19.60×109L-1;CRP 262.0mg/L,ESR 56mm/h;体温最高时达38.4℃。考虑手术后切口感染,给予头孢西丁2 g,bid,ivgtt治疗切口感染;并送细菌培养+药敏,细菌培养24 h无细菌生长。此后,患者体温波动在37.0~37.8℃之间。7月13日患者体温最高为38.2℃,血常规示:WBC 15.96×109L-1,N%85.2%,N 13.60×109L-1。已使用头孢西丁抗感染治疗9 d,手术切口感染控制效果不佳。临床药师参与会诊,建议更换为万古霉素抗感染治疗,万古霉素有肾毒性和耳毒性,请医师注意监测患者的肾功和听力。医师接受建议,遂于7月14日将抗感染药物头孢西丁更换为使用万古霉素1 g,bid,ivgtt。7月18日患者体温正常,血常规示:WBC 7.2×109L-1,N%73.1%,N 5.27×109L-1,感染得到有效控制。
2.2 继发腹膜炎的治疗
7月31日复查膝关节X线提示:右侧胫骨平台骨折术后,原骨折内固定失效,内外侧平台塌陷。由于患者术后发生感染导致内固定失效,原骨折明显移位。遂于8月1日行“清创+胫骨平台骨折再次切开内固定术”。8月2日患者胃部不适,吐出黄色黏性液体30ml,血常规示:WBC 19.98×109L-1,N%89.0%,N 17.80×109L-1。8月4日,患者腹痛、腹胀症状明显,考虑腹膜炎感染可能。临床药师参与会诊,认为腹膜炎感染可能的病原菌有革兰阴性杆菌和厌氧菌,建议使用头孢哌酮/舒巴坦钠联合甲硝唑进行治疗。医师接受建议,给予头孢哌酮/舒巴坦钠3 g,bid,ivgtt;甲硝唑0.5 g,bid,ivgtt。 8月5日行“阑尾切除术、后腹膜切开引流术”,并进行胸腔穿刺,置管引流。8月6日患者转入重症监护病房(ICU)进行治疗,血常规示:WBC 15.93×109L-1,N%92.7%,N 14.77×109L-1。考虑为混合菌感染可能,ICU医师给予比阿培南联合头孢哌酮/舒巴坦钠抗感染治疗。临床药师参与会诊,指出比阿培南与头孢哌酮/舒巴坦钠作用机制相同,均抑制细菌细胞壁合成,且抗菌谱重复,仅使用比阿培南即可。为加强对革兰阴性菌和厌氧菌的作用,建议医师使用比阿培南联合阿米卡星和甲硝唑。医师未采纳临床药师建议。
8月7日分泌物微生物鉴定:肺炎克雷伯菌。8月9日腹水微生物鉴定:肺炎克雷伯菌,胸水微生物鉴定:人葡萄球菌人亚种;血常规示:WBC 21.06×109L-1,N%92.34%,N 19.44×109L-1;患者最高体温38.7℃,感染未得到有效控制。临床药师参与会诊,建议后腹膜引流液做真菌培养,再根据真菌培养结果考虑是否使用抗真菌药。医师考虑有真菌感染可能,使用卡泊芬净每日70 mg,ivgtt。8月10日改为卡泊芬净每日50 mg,ivgtt。8月11日,考虑患者既往有十二指肠溃疡,此次创伤应急后引起溃疡穿孔。并发后腹膜感染,根据相关检查和体征,考虑存在升结肠坏死穿孔。即刻行手术治疗,清除腹腔感染,行胃造口、空肠造口(肠内营养)、回肠造口、后腹膜充分引流,进行腹腔引流管持续冲洗引流。8月12日,患者腹胀症状较前好转。8月14日,粪便检出:热带假丝酵母菌。8月16日引流液检出:热带假丝酵母菌。抗真菌治疗17 d,8月25日后体温正常。
患者入院后WBC、N及ESR变化见表1,抗感染药物使用情况见表2。
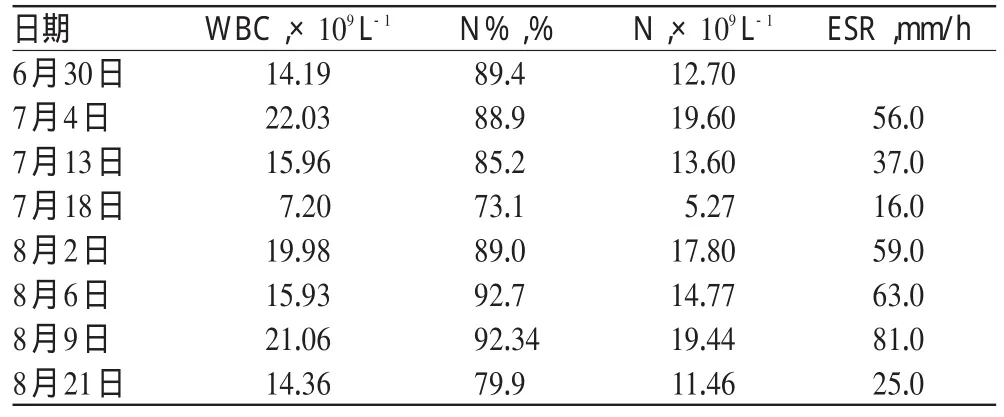
表1 患者白细胞、中性粒细胞及血沉变化Tab 1 Change of WBC,neutrophile granulocyte and ESR in patinet
2.3 肝肾功能损害的监测和防治
患者术后感染使用头孢西丁6 d后,7月10日患者血生化示:丙氨酸氨基转移酶(ALT)696.0U/L,碱性磷酸酶(ALP)317.0 U/L,转肽酶(GGT)518 U/L,总胆红素(TBIL)19.0 μmol/L,直接胆红素(DBIL)7.2 μmol/L,结合出现肝功能异常及肝损害,因此不排除患者的肝功能变化与使用头孢西丁有关。7月11日开始给予异甘草酸镁注射液0.1 g,qd,ivgtt和注射用还原型谷胱甘肽2 g,qd,ivgtt进行保肝治疗,并停用头孢西丁。7月30日患者生化示:ALT 39.0 U/L,ALP 222.0 U/L,GGT 145.0 U/L,TBIL 13.7 μmol/L,DBIL 4.0 μmol/L,肝功能恢复正常。
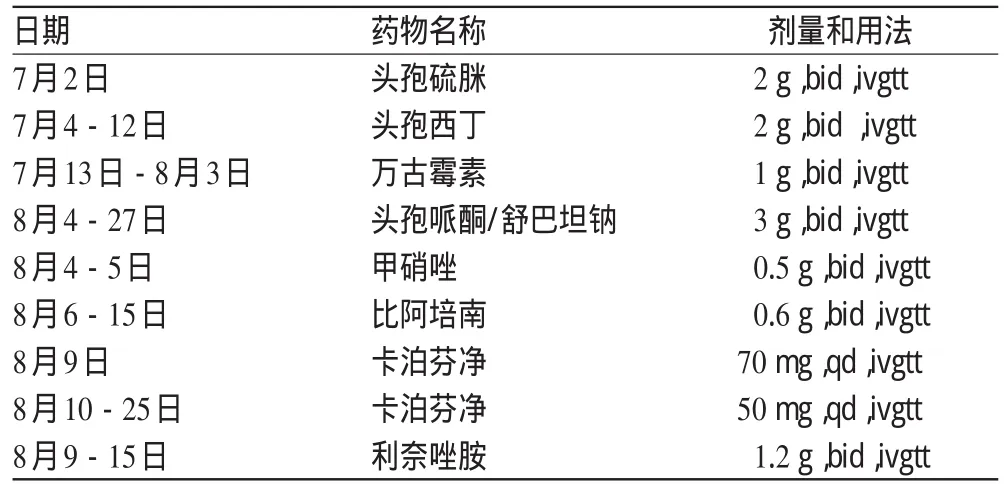
表2 抗感染药物使用情况Tab 2 The application of anti-infective drug
万古霉素不良反应主要为肾损害。本患者在使用万古霉素22 d后,患者的肾功能出现异常。8月3日患者血生化示:血肌酐(Scr)189.0 μmol/L,血尿素氮(BUN)11.50 μmol/L。考虑为万古霉素引起的肾损害,停用万古霉素。8月8日患者生化示:Scr 60.0 μmol/L,BUN 5.14 μmol/L,患者肾功能恢复正常。
患者入院后肾功能和肝功能变化的指标见表3。
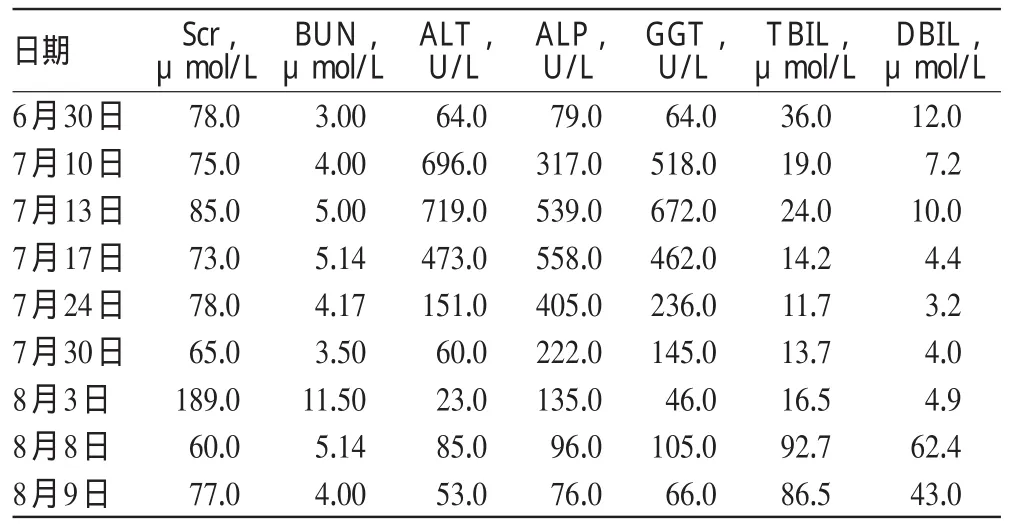
表3 患者肾功能和肝功能变化Tab 3 Changes of patinet’s renal and live function
3 分析与讨论
3.1 抗感染治疗药学监护分析
造成手术切口感染的原因有许多,包括手术室的环境条件、无菌操作执行情况、预防用药的选择和时机,手术本身的侵袭性操作亦可使患者抵抗力降低,是造成骨科手术切口感染的因素之一。骨科手术切口感染可能的病原菌有革兰阴性杆菌,如大肠埃希菌、肺炎克雷伯菌、铜绿假单胞菌、鲍曼不动杆菌等;阳性球菌可能有金黄色葡萄球菌、表皮葡萄球菌、溶血葡萄球菌等;骨科手术切口真菌引起的感染所占比例极低。因此,须根据患者手术部位病原学检测结果和相关抗菌药物特点制订用药方案。
该患者手术后引起手术切口感染,使用头孢西丁治疗切口感染,但效果不佳。手术切口分泌物多次送细菌培养,细菌培养24 h无细菌生长。临床药师参与会诊,指出我院葡萄球菌中耐甲氧西林金黄色葡萄球菌(MRSA)所占比例较高,此次感染细菌可能为MRSA引起的感染。MRSA对利奈唑胺和万古霉素高度敏感,利福平、呋喃妥因、氯霉素及复方磺胺甲唑对MRSA有一定敏感性,其他抗菌药物均对MRSA高度耐药[1]。该患者肾功能正常,因此建议更换为万古霉素进行抗感染治疗,医师接受建议。遂将抗感染药物头孢西丁更换为万古霉素,使用5 d后,感染得到控制。
随后患者引起溃疡穿孔,继发腹膜后感染。继发性腹膜炎多由空腔脏器穿孔或坏死(跨壁感染)或细菌在腹壁内接种引起。在上消化道以肠道杆菌科细菌为主,非发酵菌如铜绿假单胞菌和不动杆菌也多见;下消化道穿孔或破裂,细菌污染要严重得多,有厌氧菌(主要是脆弱类杆菌)参与的混合感染机会也很大。需氧菌主要是引起急性炎症和全身脓毒症状,厌氧菌则主要在后期引起脓肿形成。多种细菌的同时存在可发生协同的病理作用,极大地增加了感染的严重性。考虑为混合菌感染可能,医师给予比阿培南联合头孢哌酮/舒巴坦钠抗感染治疗。临床药师参与会诊,指出比阿培南与头孢哌酮/舒巴坦钠作用机制相同,均抑制细菌细胞壁合成,且抗菌谱重复,头孢哌酮/舒巴坦钠可不必使用。患者行阑尾手术,考虑有厌氧菌感染可能,虽然比阿培南对厌氧菌有一定的抗菌作用,但作用不及甲硝唑。甲硝唑为硝基咪唑类抗菌药物,除抗滴虫、阿米巴原虫作用外,还具有很强的抗脆弱类杆菌等厌氧菌作用。世界卫生组织将其定为抗厌氧菌感染的基本药物,主要用于对厌氧菌的防治[2]。对于厌氧菌引起的严重感染可加用甲硝唑,为加强对革兰阴性菌的作用可联合使用阿米卡星。因此建议使用比阿培南联合阿米卡星和甲硝唑。医师未采纳临床药师建议。
后腹膜感染使用比阿培南联合头孢哌酮/舒巴坦钠抗感染治疗5 d后,治疗效果不佳。临床药师考虑到患者使用抗菌药物时间较长,且患者又经过3次手术,损伤了机体的防御屏障,有引起真菌感染的高危因素存在,考虑有真菌感染可能。建议后腹膜引流液做真菌培养,如果真菌培养阳性可使用抗真菌药。医师认为可能有真菌感染加用抗真菌药卡泊芬净。其后患者的引流液检出热带假丝酵母菌,说明对患者进行抗真菌治疗是及时、合适的。再配合对患者进行腹腔引流管持续冲洗、引流,患者症状好转。
3.2 药品不良反应的监测与防治
患者术后感染使用头孢西丁6 d后,出现肝功能异常。头孢西丁有肝毒性,少数患者用药后可出现肝功能异常(天冬氨酸氨基转移酶、ALT一过性升高)[3]。不排除患者的肝功能变化与使用头孢西丁有关,因此停用头孢西丁,给予异甘草酸镁注射液和注射用还原型谷胱甘肽静脉滴注进行保肝治疗。经过治疗肝功能恢复正常。
万古霉素主要以原型经肾脏排泄,肾毒性发生率约5%[4]。故其不良反应主要为肾损害,主要损害肾小管,早期可有蛋白尿、管型尿,继之出现血尿、少尿等,严重者可出现肾衰竭。本患者在使用万古霉素22 d后,患者的肾功能出现异常。考虑为万古霉素引起的肾损害,停用万古霉素4 d后患者肾功能恢复正常。
患者术后继发腹膜炎使用头孢哌酮/舒巴坦钠进行治疗。由于头孢哌酮分子结构中含N-甲基硫四氮唑侧链,该结构影响机体对维生素K的合成,引起机体内维生素K水平降低而导致凝血功能障碍[5],因此建议同时应用维生素K1预防出血症状。医师采纳临床药师建议,给予患者静脉补充维生素K 140 mg,每天1次。根据多年的临床经验,抗菌药物长期使用极易引起或已经引起胃肠道菌群失调,建议口服双歧三联活菌胶囊和地衣芽孢杆菌胶囊促进肠道微生态环境[6]。使用含有双歧杆菌和/或乳酸杆菌的制剂可有效预防抗菌药物相关性腹泻(AAD)的发生[7]。医师接受建议,给患者服用双歧三联活菌胶囊。患者未出现出血和腹泻等不良反应。
3.3 腹腔感染充分引流至关重要
患者腹腔感染,进行清除病灶和腹腔冲洗引流,可极大减少感染部位(腹腔)细菌的数量。如果不及时进行病灶清除和充分的冲洗和引流,感染部位有大量的病原菌,抗菌治疗效果肯定不佳。8月5日行剖腹探查、腹腔冲洗引流、小肠减压、阑尾切除、大网膜部分切除、后腹膜切开引流术。8月11日考虑患者既往有十二指肠溃疡,此次创伤应激后引起溃疡穿孔,并发后腹膜感染,并考虑存在升结肠坏死穿孔,立即行手术治疗,清除腹腔感染,行胃造口、空肠造口(肠内营养)、回肠造口、后腹膜充分引流术。患者经腹腔持续冲洗和引流,再配合抗感染治疗,症状逐渐减轻。
4 结语
医师在对外科患者的治疗中,除了手术之外,配合药物治疗对患者的早日康复也至关重要。外科医师在手术中可发挥自己的特长,但在患者术后感染药物的选用上需要临床药师给予配合,协助临床医师合理用药。本病例患者病情较复杂,术后切口感染,之后合并阑尾炎和继发腹膜后感染,这给术后抗感染治疗带来较大的困难。临床药师与医师进行较好的沟通,同时对患者的药物治疗进行密切的药学监护,在抗感染药物的种类、用法、用量、药品不良反应的因果分析及防治等方面发挥自己的专业特长。通过积极参与患者的药物治疗,可发挥临床药师在药物治疗中的作用,使患者得到更好的药物治疗,保障患者用药的安全有效。
[1]汝玲.金黄色葡萄球菌和铜绿假单胞菌4年耐药监测分析[J].中国医院药学杂志,2011,31(19):1637.
[2]杨青,危华玲.坏疽穿孔性阑尾炎术后患者的药学监护[J].中国药房,2010,21(42):4032.
[3]国家食品药品监督管理局药品审评中心,四川美康医药软件研究开发公司.临床药物信息参考[M].成都:四川出版集团四川科学技术出版社,2004:89.
[4]孝建华,孙兆荣,武夏明,等.某院万古霉素临床用药合理性分析[J].中国药房,2011,22(8):738.
[5]谭清武,李庆华.头孢哌酮钠舒巴坦钠钠致严重凝血功能障碍[J].药物不良反应杂志,2005,7(3):210.
[6]贾晋生,李树峰,杨大明,等.临床药师协助治疗难治性感染的实践与效果[J].中国药房,2011,22(42):4016.
[7]李瑞军,杨昭徐.微生态制剂在消化系统疾病中的应用进展[J].中国新药杂志,2003,12(6):417.
