托拉塞米与呋塞米治疗慢性心衰的疗效和安全性Meta分析
2013-04-24李广森戴婧李吉孙家忠
李广森,戴婧,李吉,孙家忠
慢性心力衰竭(chronic heart failure,CHF)是由多种病因引起的心脏收缩和/或舒张功能障碍,导致心脏泵血不足,从而产生的一种病理生理状态和临床综合征,也是最常见的心血管病主要致死原因之一。CHF是各种心脏疾病的终末阶段,是由初始的心肌损害,包括心肌细胞数量的减少或心肌应力增加,引起心肌肥厚和心室扩大(心室重塑),继之以心室舒缩功能障碍,逐渐发展而成。
呋塞米是治疗慢性心力衰竭最常用的利尿剂,其功效早已被众多试验证实。托拉塞米为作用于髓袢升支粗段的磺酰脲吡啶类利尿药,多项研究发现其较呋塞米有更少的个体生物利用度变异性和更长的作用时间[1]。最近有研究发现托拉塞米似乎在降低心衰患者全因死亡率方面优于呋塞米[2]。为进一步了解它的疗效和安全性,我们收集有关资料并对其进行系统评价,希望能为临床应用提供参考依据。
1 资料和方法
1.1 文献纳入与排除标准
1.1.1 研究对象 心衰的诊断标准均符合NYHA(1994 AHA)诊断标准,病例不受年龄、性别、病程及种族的限制。
1.1.2 干预及对照措施 试验组:托拉塞米(剂型、剂量不限,疗程大于12周)+常规治疗;对照组:呋塞米(剂型、剂量不限,疗程大于12周)+常规治疗。
1.1.3 结局指标 疗效判定指标包括:①心功能分级(NYHA);②左室射血分数(left ventricular ejection fraction,LVEF);③左心室质量指数(left ventricular mass index ,LVMI);④B型脑钠肽(BNP);⑤血压(BP);⑥体重(Weight);安全性判定指标包括:①任何与药物相关的副作用;②全因死亡。
1.1.4 研究类型 所有随机对照试验(RCT),限定发表语言为英文,无论是否采用盲法。
1.1.5 排除标准 排除标准包括:①无对照组试验;②研究目的不同;③对照组为安慰剂或其他利尿剂;④文献中数据明显有误或不符合要求(无疗效判定指标数据);⑤综述;⑥两组都使用了托拉塞米。
1.2 文献检索 根据Cochrane协作网制定的检索策略进行检索。计算机检索Cochrane图书馆临床对照试验资料库(2013年第5期);MEDLINE(1966.1~2013.5)、EMbase(1980.1~20013.5)有关托拉塞米治疗心衰的所有文献,文献语种为英文。英文数据库检索词为congestive heart failure、heartorcardiac failure、torasemide、torsemide、furosemide、RCT、randomized controlled trial、random,英文词采用不同的写法和形式及运用截词符等。
1.3 资料提取 各临床试验的方法学质量由两位研究者(李广森,戴婧)分别评判,如遇分歧,则通过讨论或征求第三位研究者(孙家忠)的意见解决。
1.4 质量评价 纳入研究的方法学质量采用Cochrane协作网提供的简单方法[3]。对每个试验我们从以下四个方面进行评价:①随机方法是否正确;②是否做到分配隐藏、方法是否正确;③是否采用盲法;④有无失访或退出,在有失访或退出时是否采用意向性治疗分析(ITT)。综上所述,如果所有4条质量评价标准均完全满足,则该研究存在偏倚的可能性最小(A级);如果其中任1条或多条质量评价标准仅为部分满足,则该研究存在偏倚的可能性中等(B级);如果其中任1条或多条质量评价标准完全不满足,则该研究存在偏倚的可能性最高(C级)。
1.5 统计学分析 Meta分析使用Cochrane协作网提供的RevMan5.1软件。计量资料采用加权均数差(WMD)及其95%CI;当测量单位不同时,则选择标准均数差(SMD)及其95%CI。各临床试验的异质性检验采用卡方检验,若无异质性,Meta分析选择固定效应模型,若有异质性,则分析其来源,如各试验间无临床异质性,则选择固定效应模型分析,若系各试验的方法学质量导致的异质性,则按方法学质量等级进行分层分析[4]。
2 结果
2.1 文献检索结果 最初检索到145篇可能符合纳入标准的文献。通过限定文献类型、言语类型等筛选出65篇文献。进一步阅读文题、摘要及全文,有48篇文献因其研究目的或研究方法与本研究纳入标准不符或重复而被排除,剩余17篇文献进一步筛选,最终有9篇[5-13]英文文献,共2099例CHF患者被纳入分析。
2.2 纳入研究的一般特征 所有研究均提及了各组在年龄、性别、病程、体重指数等基线方面无显著差异(P>0.05),具有可比性。纳入的9项研究共包括CHF患者共2099例,其中治疗组1181例,对照组918例,纳入研究均提及两组间基线相似性均较好。托拉塞米剂量为(5~40)mg/d不等,呋塞米剂量为(10~80)mg/d不等,疗程最短6月,最长12月。各研究基本情况见表1。4项研究提及不良反应[5,11-13]。
2.3 纳入研究的质量评价 纳入研究一般情况及方法质量学情况见表2。纳入研究均提及为随机对照试验,除1项研究外,其它研究随机方法均合理;2项研究[5,8]分配隐藏和盲法清楚,其它研究不清楚。总体来看,纳入研究中有2项研究[5,8]质量等级为A级,其余均为B级。
2.4 Meta分析结果
2.4.1 疗效分析结果
2.4.1.1 心功能分级 有7项研究[6-12]比较了托拉塞米治疗对心功能分级的影响,其中一项研究[5]数据不可用,剩余7项研究共纳入CHF患者1669例,托拉塞米组963例,对照组706例。异质性检验显示组问差异无统计学意义(P=0.34,I2=11%)。故采用固定效应模型进行效应量的合并(图1)。结果显示两组差异有统计学意义(WMD=-0.13,95%CI:-0.19~-0.07,P<0.0001),说明在改善CHF患者NYHA分级方面,托拉塞米治疗优于呋塞米。
2.4.1.2 左室射血分数 有5项研究[5,6,8,9,11]比较了托拉塞米治疗对左室射血分数(LVEF)的影响,共纳入CHF患者361例,托拉塞米组151例,对照组150例。异质性检验显示组间差异有统计学意义(P=0.007,I2=72%)。据文献[14]所述方法分析后发现,异质性主要来源于一篇文献(Lopez 2004)[9],但具体原因不清楚。去除该文献后,异质性检验显示组间差异无统计学意义(P=0.84,I2=0%),故采用固定效应模型进行效应量的合并(图2),结果显示两组差异无统计学意义(WMD=0.16,95%CI:-0.08~-0.40,P=0.19),说明在改善慢性心衰患者LVEF分数分级方面,托拉塞米治疗同呋塞米相比无差别。
2.4.1.3 左心室质量指数 有4项研究[6,7,9,10]对托拉塞米治疗对左心室质量指数(LVMI)的影响进行了比较,共纳入CHF患者128例,其中托拉塞米组65例,对照组63例。异质性检验显示组间差异无统计学意义(P=0.12,I2=48%),故采用固定效应模型进行效应量的合并(见图3),结果显示两组差异有统计学意义(WMD=-7.40,95%CI:-12.02~-2.77,P=0.002),说明在改善LVMI方面,托拉塞米治疗同呋噻米相比对LVMI影响更明显。
2.4.1.4 B型脑钠肽 有5项研究[2,3,5-8]比较了托拉塞米治疗对BNP的影响,共纳入CHF患者420例,托拉塞米组209例,对照组211例。异质性检验显示组间差异有统计学意义(P=0.002,I2=67%)。据文献[14]所述分析方法分析后发现,异质性主要来源于一篇文献(Lopez 2004)[9],其原因可能在与其采用的检验方法与其他试验不一致。去除该文献后,异质性检验显示组间差异无统计学意义(P=0.51,I2=0%)。故采用固定效应模型进行效应量的合并(图4)。结果显示两组差异有统计学意义(WMD=-59.86,95%CI:-94.82~24.89,P=0.0008),说明托拉塞米治疗同呋噻米相比更有利于改善BNP。
2.4.1.5 血压 有6项研究[5-7,9,10,15]比较了托拉塞米治疗对血压的影响,共纳入CHF患者307例,托拉塞米组153例,对照组154例。异质性检验显示组间差异有统计学意义(P=0.0005,I2=70%)。据文献[14]分析后发现,异质性主要来源于一篇文献(Lopez 2004)[9],但具体原因不清楚。去除该文献后,异质性检验显示组间差异无统计学意义(P=0.26,I2=21%)。故采用固定效应模型进行效应量的合并(图5)。结果显示两组差异有统计学意义(WMD=2.09,95%CI:0.88~2.84,P=0.06),说明托拉塞米治疗同呋塞米相比对血压的影响更小。
2.4.2 安全性指标分析结果
2.4.2.1 任何与药物相关副作用 有2项研究[5,10]对托拉塞米治疗的副作用进行了比较,共纳入CHF患者626例,托拉塞米组320例,对照组306例。异质性检验显示组间差异无统计学意义(P=0.11,I2=23%)。故采用固定效应模型进行效应量的合并(图6)。结果显示两组差异无统计学意义(RR=1.25,95%CI:0.68~2.32,P=0.47),说明在与药物相关副作用方面,托拉塞米同呋塞米相比无差别。

表1 纳入研究一般情况表
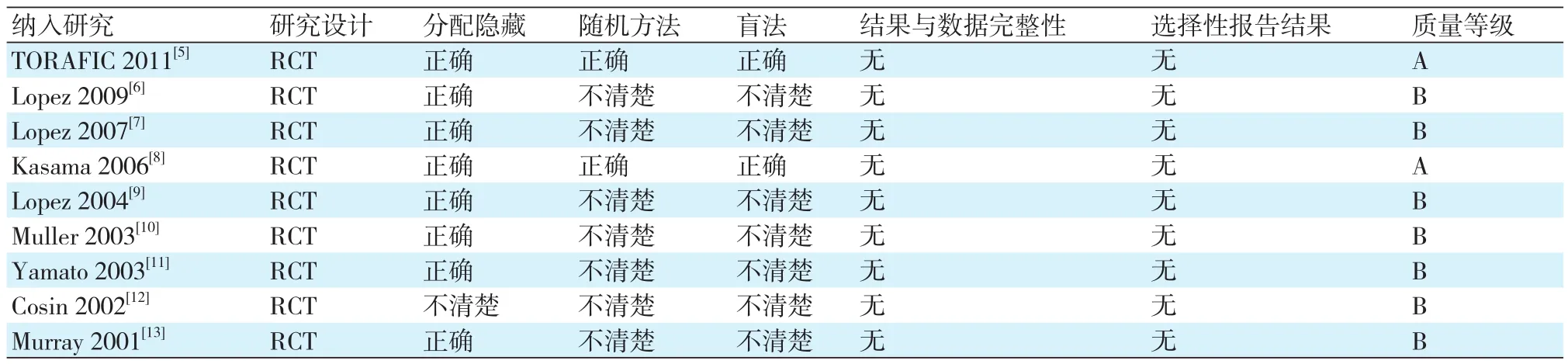
表2 纳入研究质量方法学情况表
2.4.2.2 全因死亡 有3项研究[10,12,13]报道试验中有病例死亡,其中一项研究[12]因对照组中含使用其它利尿剂患者,数据不可用。另2项研究[10,13]包括471例CHF患者,其中托拉塞米组235例,对照组236例。异质性检验显示组间差异无统计学意义(P=0.41,I2=0%)。故采用固定效应模型进行效应量的合并(图7)。结果显示两组差异无统计学意义(RR=0.87,95%CI:0.54~1.41,P=0.57),说明在全因死亡方面,托拉塞米同呋塞米相比无差别。
2.5 发表偏倚评价和敏感性分析 以纳入研究各组性别数据做漏斗图(图8),漏斗图显示纳入文献存在发表偏倚。由于纳入的9篇文献中2篇[5,8]研究方法学质量为A级。其余6篇[6,7,9-13]研究方法学治疗为B级,均存在研究方法学质量问题,6个研究均未描述具体的随机方法,存在随机方法有误或不严谨的可能性;均未提及采用分配隐藏,存在选择性偏倚的可能。

图1 托拉塞米与呋塞米治疗慢性心衰NHYA分级比较森林图

图2 托拉塞米与呋塞米治疗慢性心衰LVEF比较森林图

图3 托拉塞米与呋塞米治疗慢性心衰LVMI比较森林图

图4 托拉塞米与呋塞米治疗慢性心衰血浆BNP比较森林图
3 讨论
3.1 纳入研究的特征及质量 本研究纳入的9个研究共包括CHF患者2099例,其中治疗组1181例,对照组918例,托拉塞米剂量为(5 ~40)mg/d不等,呋塞米剂量为(10~80)mg/d不等,疗程最短6个月,最长12个月。在方法学上,部分纳入的研究质量不高,大部分没有对随机方法进行具体描述,未进行随机分配方案的隐藏,这导致可能存在选择性偏倚;除2项研究提及盲法外,其它试验均未提及盲法,可能导致测量性偏倚;漏斗图该系统评价纳入研究存在发表偏倚;本系统评价所纳入研究的测量指标不一致,这些均可能影响本研究的结果。

图5 托拉塞米与呋塞米治疗慢性心衰血压比较森林图

图6 托拉塞米与呋塞米治疗慢性心衰不良反应比较森林图

图7 托拉塞米与呋塞米治疗慢性心衰全因死亡比较森林图

图8 托拉塞米与呋塞米治疗慢性心衰的漏斗图
3.2 本研究对临床的指导意义 利尿剂、血管紧张素转化酶抑制剂(ACEI)和β受体阻滞剂被认为是治疗CHF的标准药物,目的在于减轻心脏负荷、延缓心肌重构以最大限度改善心功能[2]。而合理使用利尿剂是心衰治疗取得成功的关键因素之一。2007年中国慢性心衰指南将呋塞米和托拉塞米作为多数CHF患者的首选药物[16]。2013年ACCF/AHA指南[17]指出,在治疗CHF时,最常用的利尿剂是呋塞米,但因为托拉塞米有着更好的口服生物利用度,因此部分患者可能效果更明确(证据等级C)。但指南并未推荐何种利尿剂有利,原因在于目前尚无足够的证据来证明二者优劣。我们通过分析发现:①托拉塞米在改善NYHA心功能分级方面明显优于呋塞米;②托拉塞米在改善患者LVEF方面作用同呋塞米相当;③托拉塞米在降低LVMI方面效果较呋塞米显著;④托拉塞米与呋塞米比较能更显著的降低血浆BNP浓度;⑤托拉塞米对慢性心衰患者血压影响较呋塞米小;⑥托拉塞米同呋塞米相比不增加药物相关的副作用和全因死亡率。
NYHA心功能分级反映患者症状的改善,托拉塞米在改善NYHA心功能分级方面明显优于呋塞米,这说明托拉塞米能更明显地缓解患者心衰症状,提高生活质量。LVMI能准确评价左室肥厚程度及其逆转的程度,对预防复杂心律失常的发生、防止和改善心肌病的预后均有重要临床意义[18]。研究显示托拉塞米在降低LVMI方面优于呋塞米,意味着托拉塞米更有利于改善心肌重构。
BNP在心力衰竭的诊断和预后中具有重要作用,BNP水平的升高通常提示患者存在心力衰竭并可能产生不良后果[19]。研究显示托拉塞米在降低BNP方面明显优于呋塞米,与托拉塞米在LVEF和LVMI方面的表现相似。
3.3 本研究的局限性及未来临床研究的方向 尽管本系统评价发现与呋塞米相比,托拉塞米治疗CHF是有效的、安全的,而且在改善患者心衰症状、降低LVMI和BNP方面优于呋塞米。但纳入研究的方法学存在一定问题,并有发表偏倚;另外,本研究所纳入研究均在国外完成,而国内目前尚无好的大样本临床试验,为此,我们认为需谨慎对待该结果。托拉塞米能否在黄种人群取得优于呋塞米的疗效有待于进一步临床试验证实。
[1] Stroupe KT,Forthofer MM,Brater DC,et al. Healthcare costs of patients with heart failure treated with torasemide or furosemide[J]. Pharmacoeconomics,2000,17(5):429-40.
[2] Dinicolantonio JJ. Should torsemide be the loop diuretic of choice in systolic heart failure[J]? Future Cardiol,2012,8(5):707-28.
[3] 刘鸣. 系统评价、Meta-分析设计与实施方法[M]. 北京:人民卫生出版社,2011.
[4] Higgins JPT,Green S(editors). Cochrane Handbook for Systematic Reviews of Interventions Version5.1.0[updated March 2011].The Cochrane Collaboration,2011. Available from www.cochranehandbook.org.
[5] The TIG. Effects of prolonged-release torasemide versus furosemide on myocardial fibrosis in hypertensive patients with chronic heart failure: a randomized, blinded-end point, active-controlled study[J].Clin Ther,2011,33(9):1204-13.
[6] Lopez B,Querejeta R,Gonzalez A,et al. Impact of treatment on myocardial lysyl oxidase expression and collagen cross-linking in patients with heart failure[J]. Hypertension,2009,53(2):236-42.
[7] Lopez B,Gonzalez A,Beaumont J,et al. Identification of a potential cardiac antifibrotic mechanism of torasemide in patients with chronic heart failure[J]. J Am Coll Cardiol,2007,50(9):859-67.
[8] Kasama S,Toyama T,Hatori T,et al. Effects of torasemide on cardiac sympathetic nerve activity and left ventricular remodelling in patients with congestive heart failure[J]. Heart,2006,92(10):1434-40.
[9] Lopez B,Querejeta R,Gonzalez A,et al. Effects of loop diuretics on myocardial fibrosis and collagen type I turnover in chronic heart failure[J]. J Am Coll Cardiol,2004,43(11):2028-35.
[10] Muller K,Gamba G,Jaquet F,et al. Torasemide vs. furosemide in primary care patients with chronic heart failure NYHA II to IV-efficacy and quality of life[J]. Eur J Heart Fail,2003,5(6):793-801.
[11] Yamato M,Sasaki T,Honda K,et al. Effects of torasemide on left ventricular function and neurohumoral factors in patients with chronic heart failure[J]. Circ J,2003,67(5):384-90.
[12] Cosin J,Diez J. Torasemide in chronic heart failure: results of the TORIC study[J]. Eur J Heart Fail,2002,4(4):507-13.
[13] Murray MD,Deer MM,Ferguson JA,et al. Open-label randomized trial of torsemide compared with furosemide therapy for patients with heart failure[J]. Am J Med,2001,111(7):513-20.
[14] 王丹,翟俊霞,牟振云,等. Meta分析中的异质性及其处理方法[J].中国循证医学杂志,2009,9(10):1115-8.
[15] Harada K,Izawa H,Nishizawa T,et al. Beneficial effects of torasemide on systolic wall stress and sympathetic nervous activity in asymptomatic or mildly symptomatic patients with heart failure: comparison with azosemide[J]. J Cardiovasc Pharmacol,2009,53(6):468-73.
[16] 中华医学会心血管病学分会,中华心血管病杂志编辑委员会. 慢性心力衰竭诊断治疗指南[J]. 中华心血管病杂志,2007,35(12):1076-95.
[17] Yancy CW,Jessup M,Bozkurt B,et al. 2013 ACCF/AHA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines[J]. J Am Coll Cardiol,2013,62(16):e147-e239.
[18] Fagard RH,Celis H,Thijs L,et al. Regression of left ventricular mass by antihypertensive treatment: a meta-analysis of randomized comparative studies[J]. Hypertension,2009,54(5):1084-91.
[19] Gluba A,Bielecka-Dabrowa A,Mikhailidis DP,et al. An update on biomarkers of heart failure in hypertensive patients[J]. J Hypertens,2012,30(9):1681-9.
