卡培他滨联合放疗治疗局部进展期直肠癌的疗效观察
2013-04-19帖晓静田永巍刘培杰徐志巧
帖晓静,田永巍,高 岭,李 宁,刘培杰,徐志巧
直肠癌是消化系统高发恶性肿瘤之一,发病率呈逐年上升趋势。术前放化疗逐渐成为局部进展期直肠癌的标准治疗模式,可提高肿瘤局部控制率及手术切除成功率,有助于提升患者生活质量。卡培他滨是一种具有肿瘤选择性的新型口服氟尿嘧啶甲氨酸盐,对直肠癌有显著临床疗效[1]。我院近年应用卡培他滨联合放疗治疗局部进展期直肠癌取得较好疗效,现报道如下。
1 资料与方法
1.1 一般资料 选择我院2007年6月—2010年6月收治的局部进展期直肠癌患者共52例,均经结肠镜、胸腹盆腔CT、组织病理学检查确诊,临床分期为T3/T4期且无远处转移,美国东部肿瘤协作组(ECOG)评分≤2分。将患者按照治疗方法分为对照组25例和观察组27例,两组患者的性别、年龄、临床分期比较,差异均无统计学意义(P>0.05,见表1),具有可比性。治疗前均经患者及家属同意,签署放化疗知情同意书。

表2 两组患者治疗前后CEA水平比较Table 2 Comparison of CEA levels between the two groups before and after treatment

表3 不同临床疗效患者治疗前后CEA水平比较Table 3 Comparison of CEA levels in patients with different efficacy before and after treatment
表1 两组患者一般资料比较
Table1 Comparison of general information between the two groups

组别例数性别(男/女)年龄(x±s,岁)临床分期(T3/T4)对照组2514/1157 4±8 314/11观察组2715/1257 2±7 316/11χ2(t)值0 0010 064∗0 056P值0 9740 9500 812
注:*为t值
1.2 治疗方法 两组患者均进行术前放疗,每周治疗5 d,2 Gy/d,剂量为46~50 Gy/ 4~5 w;观察组患者在此基础上口服卡培他滨1 250 mg/m2,2次/d,餐后0.5 h服用,第1~14天,21 d重复,共化疗2个周期。两组患者均在放化疗结束后复查CT,无手术禁忌证者于6~8周内进行手术治疗,术后进行系统化疗。
1.3 观察指标 (1)临床疗效:治疗后1个月复查盆腔增强CT,按照RECIST标准评价临床疗效,无肿瘤残留为完全缓解(CR);肿瘤浸润深度变浅为部分缓解(PR);肿瘤浸润深度无明显变化为稳定(SD);肿瘤浸润深度加深为进展(PD);计算总体有效率(ORR),ORR=CR率+PR率。(2)毒副作用:根据世界卫生组织(WHO)制定的关于抗癌药物毒副作用评定标准评价观察组患者的毒副作用。(3)治疗前后癌胚抗原(CEA)水平(参考值0~5 μg/L)。(4)随访:对两组患者进行随访,至少随访2年,计算无进展生存期(PFS)、1年及2年生存率。
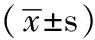
2 结果
2.1 临床疗效 对照组CR 2例,PR 14例,SD 8例,PD 1例,ORR为16/25;观察组CR 4例,PR 20例,SD 2例,PD 1例,ORR为24/27。两组ORR比较,差异有统计学意义(χ2=4.530,P=0.049)。
2.2 毒副作用 观察组出现骨髓抑制5例、腹泻4例、恶心/呕吐3例、皮肤黏膜损害2例、手足综合征2例,患者可耐受,未进行特殊处理,未见4级毒副作用。
2.3 CEA水平 两组治疗前、治疗后CEA水平比较,差异均无统计学意义(P>0.05);对照组治疗前后、观察组治疗前后CEA水平比较,差异均有统计学意义(P<0.05,见表2)。
根据临床疗效将患者进一步分为CR+PR组与SD+PD组,两组治疗前CEA水平比较,差异有统计学意义(P<0.05);治疗后比较,差异无统计学意义(P>0.05)。CR+PR组治疗前后、SD+PD组治疗前后比较,差异均有统计学意义(P<0.05,见表3)。
2.4 随访 对照组PFS为(20.4±1.1)个月,观察组为(27.0±1.4)个月,差异有统计学意义(t=3.795,P<0.05);对照组1年生存率为25/25,观察组为27/27,差异无统计学意义(χ2=0.000,P>0.05);对照组2年生存率为21/25,观察组为25/27,差异有统计学意义(χ2=0.939,P>0.05)。
2.5 相关性分析 Pearson相关分析显示,CEA水平与PFS呈负相关(r=-0.329,P=0.017)、与OS无线性相关性(r=-0.185,P=0.189)。
3 讨论
直肠癌起病隐匿,缺乏特异症状,临床发现时多数已属中晚期;尽管全直肠系膜切除术使其局部复发率明显下降,但仍有10%~15%的患者会出现局部复发[2-3]。一项比较术前单纯放疗与氟尿嘧啶联合亚叶酸钙方案(5-FU/LV方案)同期放化疗辅助手术治疗无远处转移的T3/4直肠癌的研究发现,两组间总体生存率和保肛率无明显差异,但术前同期放化疗组获得了较高的CR率(11.4%与3.6%,P<0.05)和较低的局部复发率(8.1%与16.5%,P<0.05)[4];且此结果在后续多项大型临床研究中得到进一步证实,提示术前同期放化疗与术前单纯放疗相比,可提高肿瘤局部控制率、降低局部复发率。术前新辅助同步放化疗已成为欧美局部进展期直肠癌的标准治疗方案。
卡培他滨是一种全新的靶向性口服化疗药物,能准确识别肿瘤细胞,经肿瘤组织中特有的高浓度的胸苷磷酸化酶转化为活性氟尿嘧啶发挥抗癌作用。最近,两项大型Ⅲ期临床研究(NSABP R-04和德国合作组研究)证实,直肠癌新辅助放化疗中联合卡培他滨的疗效不劣于静脉注射氟尿嘧啶[5]。考虑到患者对持续静脉注射氟尿嘧啶的依从性,不易接受,且增加了感染和血栓形成等风险,因此,本研究采用口服卡培他滨联合放疗治疗局部进展期直肠癌,更为方便安全。
本研究结果显示,观察组ORR高于对照组,PFS长于对照组,主要毒副作用为腹泻和骨髓抑制,患者可耐受,未见4级毒副作用,表明卡培他滨联合放疗治疗局部进展期直肠癌疗效优于单纯放疗,与文献报道结果一致[6]。对所有患者进行为期2年的随访发现,观察组与对照组1年生存率间无明显差异,2年生存率间有明显差异,提示卡培他滨联合放疗治疗局部进展期直肠癌远期疗效较好。Sun等[7]进行的Ⅱ期临床研究中应用西妥昔单抗联合新辅助放化疗治疗直肠癌,结果表明其疗效并不优于联合两种或更多的细胞毒药物。本研究中有2例患者在放化疗后出现远处转移,因而未行手术治疗,继续完成后续全身联合化疗;其余50例于同步放化疗后6~8周行根治性肿瘤切除,术中见直肠周围纤维化明显,术后均未出现吻合口漏,提示卡培他滨联合放疗治疗局部进展期直肠癌并不增加手术难度及手术并发症发生率[8-9]。
CEA水平对消化道肿瘤的诊断及预后判断有良好的临床应用价值[10],术前高水平CEA患者较术前低水平CEA者预后差,PFS及OS短[11]。本研究结果显示,观察组与对照组治疗后CEA水平均明显下降,SD+PD组治疗后CEA水平也较前下降,且CEA水平与PFS呈负相关,而与OS无相关性,提示CEA水平可能为预测卡培他滨联合放疗治疗局部进展期直肠癌疗效的一项指标,与文献报道基本一致[11-12]。但本研究样本量较小,且评价临床疗效的影像学改变有可能晚于血清学改变,有待进一步研究观察;建议术前CEA水平异常增高或术后无明显下降的局部进展期直肠癌患者进行系统性辅助化疗,以减少肿瘤的复发率、转移率。
1 吾甫尔·艾克木,王若峥,王多明.卡培他滨化疗同步放射治疗局部晚期直肠癌的疗效观察[J].中国全科医学,2009,12(15):1426-1427.
2 梁天伟,孙轶,卢永刚,等.两种拖出式超低位直肠癌保肛术疗效分析[J].中国全科医学,2011,14(5):1712.
3 谢雪梅.直肠癌切除术的临床护理[J].实用心脑肺血管病杂志,2011,19(4):672.
4 Sebag-Montefiore D,Stephens RJ,Steele R,et al.Preoperative radiotherapy versus selective postoperative chemoradiotherapy in patients with rectal cancer(MRC CR07 and NCIC-CTG C016):a multicentre,randomised trial[J].Lancet,2009,373(9666):811-820.
5 Chen CF,Huang MY,Huang CJ,et al.A observational study of the efficacy and safety of capecitabine versus bolus infusional 5-fluorouracil in pre-operative chemoradiotherapy for locally advanced rectal cancer [J].Int J Colorectal Dis,2012,27(6):727-736.
6 Hofheinz RD,Wenz F,Post S,et al.Chemoradiotherapy with capecitabine versus fluorouracil for locally advanced rectal cancer:a randomised,multicentre,non-inferiority,phase 3 trial[J].Lancet Oncol,2012,13(6):579-588.
7 Sun PL,Li B,Ye QF.Effect of neoadjuvant cetuximab,capecitabine,and radiotherapy for locally advanced rectal cancer:results of a phase Ⅱ study[J].Int J Colorectal Dis,2012,27(10):1325-1332.
8 蔡钢,章真.直肠癌的辅助放化疗的临床研究[J].中国癌症杂志,2006,16(5):399-402.
9 Rullier E,Goffre B,Bonnel C,et al.Preoperative radiochemotherapy and sphincter-saving resection for T3 carcinomas of the lower third of the rectum[J].Ann Surg,2001,234(5):633-640.
10 李雨升,杨立廷,余云云,等.120例结直肠癌手术前后血清CEA RIA 测定的临床观察[J].标记免疫分析与临床,2003,10(1):9-11.
11 Tarantino I,Warschkow R,Worni M.Elevated preoperative CEA is associated with worse survival in stageⅠ-Ⅲ rectal cancer patients[J].Br J Cancer,2012,107(2):266-274.
12 Kim CW,Yu CS,Yang SS,et al.Clinical significance of pre- to post-chemoradiotherapy s-CEA reduction ratio in rectal cancer patients treated with preoperative chemoradiotherapy and curative resection[J].Ann Surg Oncol,2011,18(12):3271-3277.
