头孢克肟片直压制备工艺的研究*
2013-04-18李纯钢赵婷婷
李纯钢,赵婷婷
(天津医药集团津康制药有限公司,天津 300270)
头孢克肟(cefixime)是日本藤泽药品工业株式会社在上世纪80年代初研发的第3代口服头孢菌素,1985年在日本完成临床试验后投放市场[1]。头孢克肟(cefixime) 为口服的第三代头孢类抗生素, 对链球菌、肺炎球菌、淋球菌、大肠杆菌等有良好的抗菌作用, 对细菌的β-内酰胺酶甚稳定, 临床应用于敏感菌所致的肺炎、支气管炎、泌尿道炎、淋病、胆囊炎、胆管炎、猩红热、中耳炎、副鼻窦炎等[2]。头孢克肟(cefixime)对湿热不稳定, 采用普通湿法制粒工艺, 容易引起头孢克肟(cefixime)效价下降[3]。为此, 采用原料药粉末直接压片法制备头孢克肟(cefixime)片,各项指标均符合《中国药典》要求。
1 材料及仪器
头孢克肟(印度兰花制药总厂);乳糖(Friesland Foods DOMO);微晶纤维素(湖州展望药业有限公司);聚乙二醇6000(湖州展望药业有限公司);交联聚维酮(ISP Technologies, INC);硬脂酸镁(湖州展望药业有限公司);滑石粉(广西龙胜华美滑石开发有限公司);头孢克肟片参比制剂(广州白云山制药总厂)。
GZPL 26C型高速旋转压片机(北京国药龙立科技有限公司);ZRS-8G型智能溶出试验仪(天大天发科技有限公司);高效液相色谱仪15C(日本岛津)。
2 方法与结果
2.1制备工艺按照处方将原辅料过80目筛3次,混合均匀,然后将物料加入到高速压片机中,制得三批头孢克肟片,批号为120501、120502、120503。
2.2粉体学试验与结果
2.2.1物料休止角的测定[4]用固定圆锥底法测定空白辅料、头孢克肟原料药和混粉的休止角, 重复3次,其平均值分别为23°、40°、26°,表明混粉具有优良的流动性。
2.2.2松密度的测定 将待测粉末松缓地转入100 ml量筒中,称量样品的质量m(g),并稍弄平粉末表面,读取待测粉末体积V1(ml),计算:松密度=m/V1。重复3次,取其平均值为0.610 g/ml。
2.2.3紧密度的测定 将上述盛有样品的量筒放在台面上,由2 cm左右的高度自坠到台面上,反复此操作若干次,量得压紧后的粉末体积V2(ml),计算:紧密度=M/V2。重复3次,取其平均值为0.722 g/ml。
2.2.4卡尔系数

松密度、紧密度、卡尔系数反映粉体的可压性和填充性能,压缩度越小,其填充性越强,即粉体越易流动。由上可知,粉体的卡尔系数为18.36%,表明粉体具有良好的填充性。
2.3质量检测
2.3.1片剂重量差异的检验 取本品20片,按《中国药典》2010年版二部附录ⅠA 的方法和标准, 测定头孢克肟片的重量差异, 结果均符合要求, 表明用本工艺压制头孢克肟片时, 物料流动性好, 重量差异符合规定。
2.3.2片剂脆碎度的测定 取本品若干片,使其总重约为6.5 g,按《中国药典》2010年版二部附录Ⅹ G 的方法和标准, 测定头孢克肟片的脆碎度, 120501、120502和120503三批结果分别为0.27%、0.26%和0.27%,均符合要求, 未检出断裂、龟裂及粉碎的片。
2.3.3水分测定 取本品20片,研细,照水分测定法(《中国药典》2010版附录Ⅷ M 第一法A)测定,120501、120502和120503三批结果分别为7.25%、7.28%和7.13%,均符合要求。
2.3.4含量测定 根据《中国药典》2010年版 二部头孢克肟片标准进行含量的定,120501、120502和120503三批结果分别为98.1%、99.6%和101.2%,均符合要求。
2.3.5有关物质测定 取对照溶液20 μl注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的20%,再精密量取供试品溶液和对照溶液各20 μl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的2.5倍,供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积(1.0%),各杂质峰面积的和不得大于对照溶液主峰面积的6倍(6.0%)。试验结果表明,3批样品有关物质均符合要求。见表1。
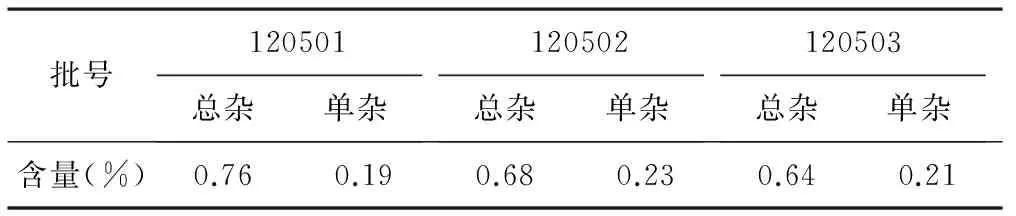
表1 有关物质试验数据
2.3.6溶出度试验取本品,照溶出度测定法(《中国药典》2010版二部附录,Ⅹ C 第一法), 分别以磷酸盐缓冲液(pH 7.2)、磷酸盐缓冲液(pH 6.8)、盐酸+氯化钠(pH 1.2)、水900 ml为溶出介质,转速为100 r/min,依法操作。经5、10、15、20、30、45和60 min时,取溶液适量,滤过,精密量取续滤液适量,用溶出介质定量稀释制成每1 ml中约含头孢克肟10 mg的溶液,照紫外-可见分光光度法(附录Ⅳ A),在288 nm波长处测定吸光度;另精密称取头孢克肟对照品适量,加溶出介质溶解并定量稀释制成每1 ml中约含10 mg的溶液(必要时先用少量甲醇溶解,甲醇量不得超过对照品溶液总体积的0.1%),同法测定。计算每片的溶出量,作溶出曲线,见图1,并与参比制剂做对比。计算磷酸盐缓冲液(pH 7.2)、磷酸盐缓冲液(pH 6.8)、盐酸+氯化钠(pH 1.2)、水4种溶出介质中溶出相似因子f2分别为52.00、50.03、67.32和74.23,由此可知,4种溶出介质中对照片与自制片溶出曲线均相似。
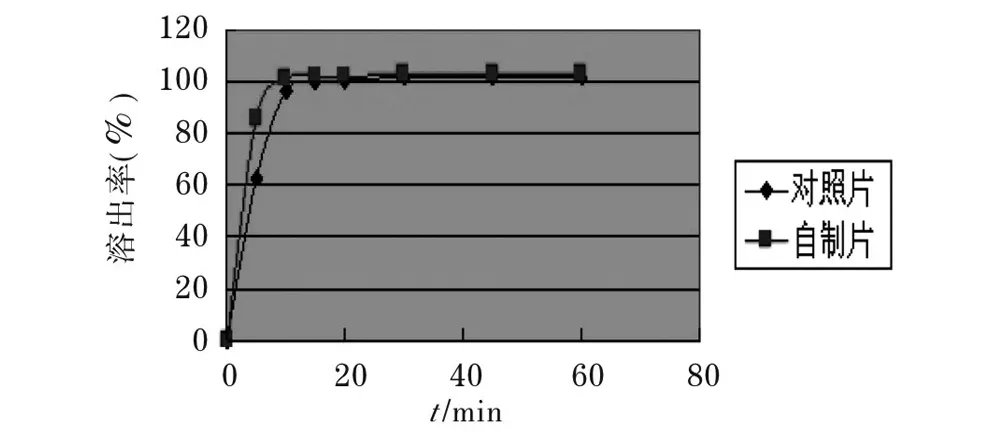
介质1:pH 7.2磷酸盐缓冲液
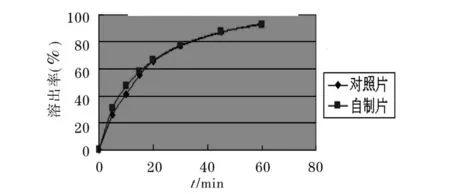
介质2:水

介质3:pH 6.8磷酸盐缓冲液
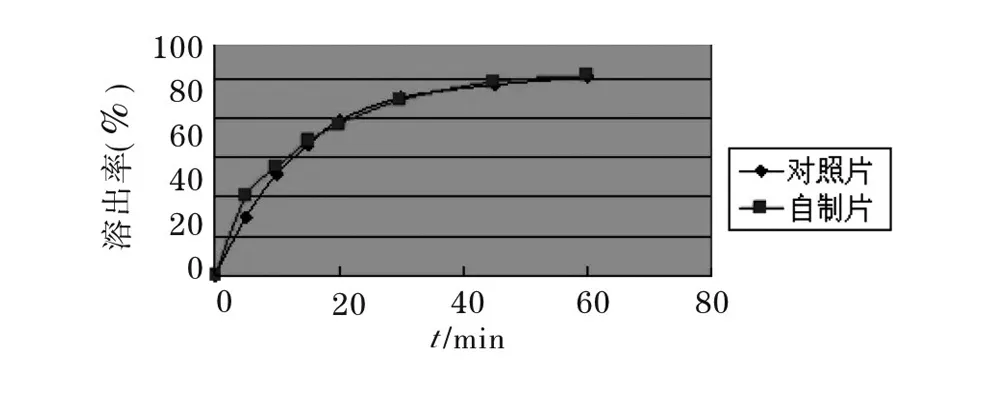
介质4:pH 1.2盐酸+氯化钠溶液
2.4稳定性试验 为了考查头孢克肟片制剂处方、制备工艺的合理性,进行了长期稳定性试验。将头孢克肟片按市售包装,置阴凉条件下储藏6个月,分别于0、3和6月取出测定其含量、溶出度和有关物质,并与参比制剂进行对比。试验结果表明阴凉库放置6个月后,与0月相比,含量、溶出度和有关物质无明显变化,表明本厂制得的头孢克肟片质量稳定、均一。见表2。
3 讨论
3.1头孢克肟对湿热不稳定,若用常规湿法制粒压片,易出现变色、含量下降的问题。为此,本实验采用粉末直接压片技术,可避免头孢克肟受湿热的影响,这样不仅增加了头孢克肟的稳定性,提高了药物溶出度,而且简化了工艺过程,降低了生产成本,适合工业化生产。
3.2采用直接压片法制备头孢克肟片的时候,如果原料药粉太细,在压片过程中有时候会出现流动性不好的现象,所以建议使用晶形较好的原料药。另外,加入适量的直压乳糖可显著改善物料的流动性,可使片剂重量差异符合要求。
1张明发,季珉.国内对头孢克肟的临床研究与评价[J].抗感染药学,2010,7(1):1
2奚念朱.药剂学[M ]. 第三版.北京: 人民卫生出版社, 1995:247,249
3卢丹,尤孝庆.头孢克肟原药粉末直接压片的研究[J].中国医药工业杂志,2000, 31 (11):488
4高春生,单利,崔光华,等.粉末直接压片工艺主要辅料的流动性研究[J].科学技术与工程,2004,4(5):367
