α-二酮的铟促水相烯丙基化研究*
2013-03-26马丽锋陈韶蕊李丽娟马吉海
马丽锋,陈韶蕊,李丽娟,张 静,马吉海
(1.河北化工医药职业技术学院,河北 石家庄 050026;2.河北科技大学 理学院,河北石家庄 050018)
1991年Li[1]首先报道了金属铟引发的卤丙烯与醛及酮在水相中的烯丙基化反应。自此,科学家们对金属铟参与的水相烯丙基化反应进行了大量的研究[2~8]。水相烯丙基化反应适应当前绿色化学的发展趋势,用水作溶剂资源丰富、廉价易得、操作简便安全、不易燃、不易爆、不污染环境,有明显的实用意义[9]。
本课题组曾利用新的方法合成了一系列α-二酮[10,11],并利用其进行了水相烯丙基化反应,得到了一系列α-二酮的水相单烯丙基化产物[12]和双烯丙基化产物[13]。本文在文献[10~13]方法的基础上,利用6,7-十二烷二酮(1)与3-碘-2-碘甲基-1-丙烯(2)的铟促水相烯丙基化反应合成了新型的单烯丙基化产物[7-羟基-7-(2-碘甲基-烯丙基)-十二烷-6-酮(3)]和双烯丙基化产物[4-亚甲基-1,2-二戊基-1,2-环戊二醇(4)];1,2-环烷基二酮(5a~5c)与2的水相烯丙基化反应合成了新型的单烯丙基化产物2-羟基-2-(2-碘甲基-烯丙基)-环烷酮(6a~6c)和新型的双烯丙基化产物2-羟基-2-[2-(1-羟基-2-羰基-环癸基甲基)-烯丙基]-环癸酮(7b)和 2-羟基-2-[2-(1-羟基-2-羰基-环十二基甲基)-烯丙基]-环十二烷酮(7c)(Scheme 1),其结构经1H NMR,IR和HR-MS表征。
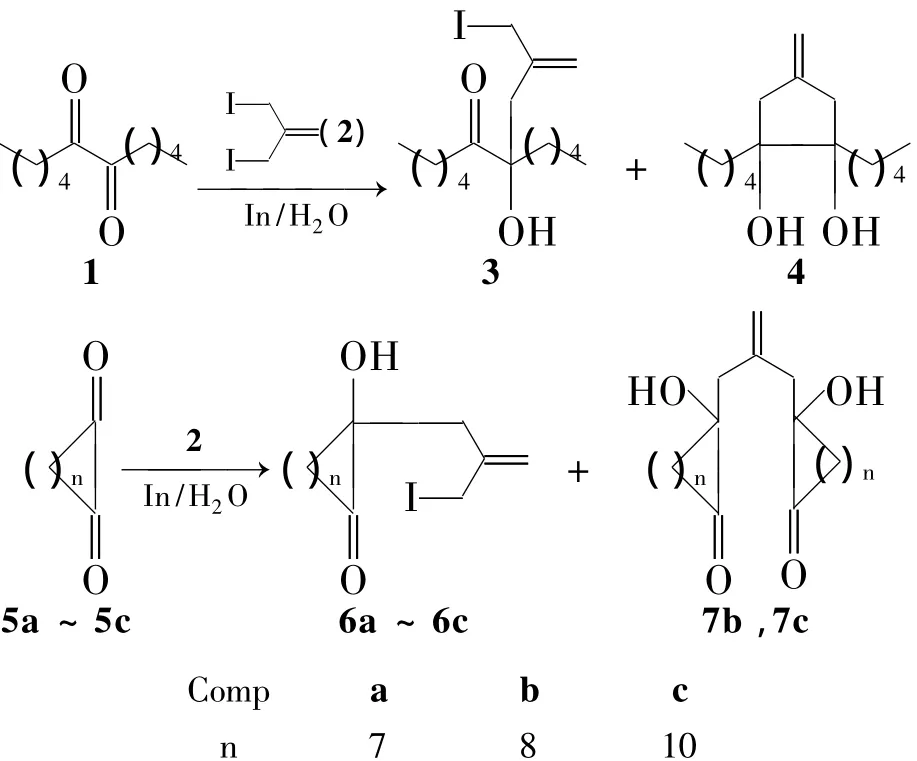
Scheme 1
1 实验部分
1.1 仪器与试剂
X4型数字显示熔点仪(温度未校正);ZF-2型三用紫外仪;AV 400型核磁共振仪(CDCl3为溶剂,TMS为内标);BIO-RAD-FTS-135型傅立叶红外光谱仪(KBr压片)。
1和5a~5c按文献[10]方法制备;其余所用试剂均为化学纯。
1.2 合成
在反应瓶中依次加入1 1.0 g(5.1 mmol),2 1.57 g(5.1 mmol),铟粉 1.76 g(15.3 mmol),混合溶剂[V(THF)∶V(H2O)=4 ∶1]40 mL及AlCl3·6H2O 1.98 g(8.2 mmol),搅拌下于室温避光反应搅拌3 d;于40℃反应9 d。用1 mol·L-1硫酸氢钾调 pH至2~3,用三氯甲烷(3×60 mL)萃取,合并萃取液,用无水硫酸镁干燥,旋蒸除溶得粗品1.23 g,经硅胶柱层析[洗脱剂:A=V(乙酸乙酯)∶V(石油醚)=1 ∶10]纯化得3 0.45 g 和4 0.37 g。
以5a~5c替代1,用类似的方法合成6a~6c,7b 和7c。
3:淡黄色液体,收率 23.4%;1H NMR δ:4.83(s,1H),4.69(s,1H),3.88(s,1H),2.54(m,1H),2.45(s,2H),2.40 ~2.30(m,1H),1.72(s,2H),1.72 ~1.56(m,4H),1.32 ~1.29(m,10H),0.90 ~ 0.85(t,6H);IR ν:3 464(OH),3 079(C -H),1 637(C=C),1 705(C=O)cm-1;HR-MSm/z:Calcd for C16H30O2I{[M+H]+}381.129 1,found 381.129 8。
4:白色固体,收率 29.1%;1H NMR δ:4.95(s,2H),2.67(d,J=15.0 Hz,2.0 Hz,2H),2.34(d,J=17.3 Hz,2H),1.71(m,2H),1.52 ~1.46(m,10H),1.43(s,2H),1.30 ~1.23(m,4H),0.97(t,6H);IR ν:3 465(OH),3 072(C -H),1 658(C=C)cm-1;HR-MSm/z:Calcd for C16H31O2{[M+H]+}255.232 4,found 255.233 2。
6a:淡黄色液体,收率 45.7%;1H NMR δ:4.83(s,1H),4.66(s,1H),4.10(s,1H),2.97(m,1H),2.44(d,1H),2.41(d,1H),2.30 ~2.20(m,1H),2.10 ~ 2.02(m,1H),1.93 ~1.89(m,2H),1.74(m,2H),1.60 ~1.10(m,9H);IR ν:3 471(OH),3 077(C - H),1 644(C=C),1 699(C=O)cm-1;HR-MSm/z:Calcd for C13H22O2I{[M+H]+}337.066 5,found 337.067 0。
6b:无色液体,收率 35.9%;1H NMR δ:4.83(s,1H),4.68(s,1H),4.10(s,1H),3.16(m,1H),2.39(m,2H),2.22 ~1.77(m,3H),1.76(s,2H),1.67 ~ 1.27(m,12H);IR ν:3 475(OH),3 077(C-H),1 647(C=C),1 707(C=O)cm-1;HR-MSm/z:Calcd for C14H24O2I{[M+H]+}351.082 1,found 351.081 2。
6c:无色液体,收率 26.1%;1H NMR δ:4.82(s,1H),4.70(s,1H),3.97(s,1H),2.47(s,2H),2.21(s,2H),1.79(m,2H),1.72(s,2H),1.48 ~1.22(m,16H);IR ν:3 476(OH),3 074(C -H),1 644(C=C),1 703(C=O)cm-1;HR-MSm/z:Calcd.for C16H28O2I{[M+H]+}379.113 4,found 379.114 1。
7b:无色黏状胶体,收率32.9%;1H NMR δ:5.01(s,2H),4.97(s,2H),4.44(s,4H),3.20 ~3.10(m,4H),2.66 ~ 2.50(m,8H),2.30 ~2.00(m,12H),1.70 ~1.60(m,8H),1.60 ~1.30(m,40H);IR ν:3 443(OH),3 075(C -H),1 636(C=C),1 701(C=O)cm-1;HR-MSm/z:Calcd for C24H41O4{[M+H]+}393.300 5,found 393.301 2。
7c:白色固体,收率 39.3%;1H NMR δ:4.90(s,2H),4.21(s,2H),2.94 ~ 2.88(m,2H),2.46 ~ 2.40(m,4H),2.30 ~ 2.22(m,2H),2.07 ~ 2.05(m,2H),1.74 ~ 1.69(m,4H),1.54 ~ 1.45(m,2H),1.40 ~ 0.80(m,26H),0.75 ~0.60(m,2H);IR ν:3438(OH),3 083(C -H),1 634(C=C),1 700(C=O)cm-1;HR-MSm/z:Calcd for C28H49O4{[M+H]+}449.363 1,found 449.364 1。
2 结果与讨论
2.1 2对反应的影响
实验中,我们多次采用1或5与3-氯-2-氯甲基-1-丙烯反应,但反应不发生。可能的原因是由于3-氯-2-氯甲基-1-丙烯的活性太低。实验结果发现,1或5与3-溴-2-溴甲基-1-丙烯只得到单烯丙基化产物;1或5与2发生反应,可以得到单烯丙基化产物和双烯丙基化产物。
2.2 反应条件优化
(1)溶剂
1 5.1 mmol,2 5.1 mmol,其余反应条件同1.2,考察反应溶剂[溶剂 A:V(甲醇)∶V(0.1 mol·L-1HCl)=1 ∶4),溶剂 B:V(THF)∶V(H2O)=4 ∶1),溶剂 C:V(THF)∶V(H2O)=9∶1)及纯水]对反应的影响。TLC检测发现:在溶剂B中反应速度较快,且只有两个主要产物(3和4)生成;在溶剂C中反应速度最快,但产物复杂,副反应较多;采用溶剂A或纯水做溶剂则反应速度较慢。
较佳的反应溶剂为溶剂 B,即V(THF)∶V(H2O)=4 ∶1。
(2)催化剂
以V(THF)∶V(H2O)=4∶1为溶剂,其余反应条件同1.2,考察催化剂对烯丙基化反应的影响,结果见表1。由表1可见,AlCl3·6H2O的催化活性最佳,反应所需时间最短。
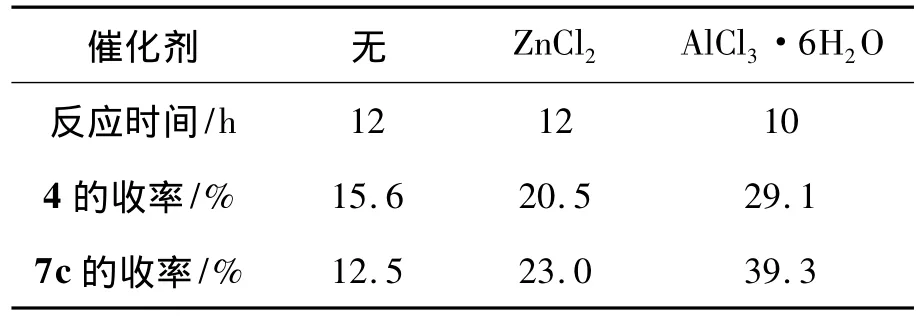
表1 催化剂对烯丙基化反应的影响*Table 1 Effect of catalyst on allylation
(3)反应温度
以V(THF)∶V(H2O)=4 ∶1为溶剂,AlCl3·6H2O为催化剂,其余反应条件同1.2,考察反应温度对烯丙基化反应的影响,结果见表2。从表2可见,单烯丙基化产物(6c)在室温下产率最高,随温度的上升产率不断下降;双烯丙基化产物(7c)在40℃产率最高,在室温和70℃时均有所下降。
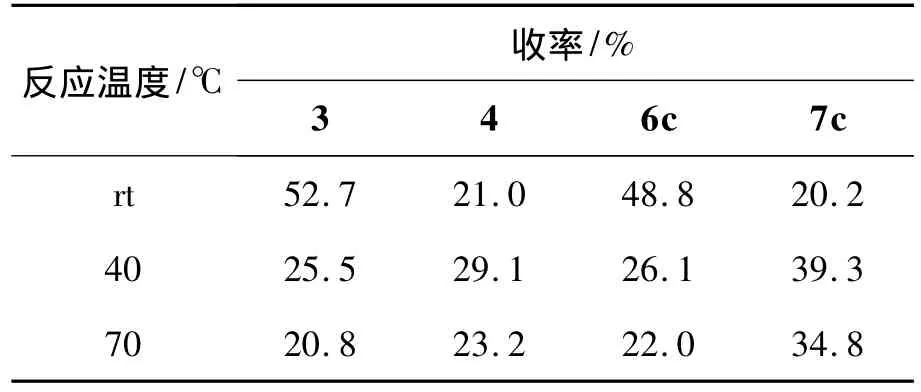
表2 反应温度对烯丙基化反应的影响*Table 2 Effect of reaction temperature on allylation
综上所述,最佳的烯丙基化反应条件为:以V(THF)∶V(H2O)=4 ∶1为溶剂,AlCl3·6H2O 为催化剂,单烯丙基化产物于室温反应12 h,双烯丙基化产物于40℃反应12 h。
[1]Li C J,Chan T H.Organometallic reactions in aqueous media with indium[J].Tetrahedron Lett,1991,32:7017-7019.
[2]谭翔晖,赵晖,侯永泉,等.各种金属参与的水相Barbier-Type反应[J].有机化学,2004,24(9):987 -1003.
[3]Li C J.Aqueous Barbier-Grignard type reaction:Scope mechanism and syntheticapplications[J].Tetrahedron,1996,52(16):5643 -5668.
[4]Petrier C,Luche L J.Allylzinc regeant additions in aqueous media[J].J Org Chem,1985,50:910 -912.
[5]袁耀锋,曹忠,胡爱国.铟试剂在有机合成中的应用[J].有机化学,2000,20(3):269 -281.
[6]Li C J,Chan T H.Organometallics reactions in aqueous media convenient synthesis of methylenetetrahyclrofurans[J].Organometallics,1991,10(8):2548 -2549.
[7]Hachiya I,Kobayashi S.Aqueous reactions with a Lewis acid and an organometallic reagent the scandium trifluoromethanesulfonate-catalyzed allyation reaction of caebonyl compounds with tetraallyltin[J].J Org Chem,1993,58(25):6958 -6960.
[8]Chan T H,Lee M C.Indium-mediated coupling of α-(bromomethyl)acrylic acid with carbonyl compounds in aqueous media concise syntheses of(+)-3-deoxy-D-glycero-D-galacto-nonulosonic acid andN-acetylneuraminic acid[J].J Org Chem,1995,60(13):4228 -4232.
[9]谢斌,冯建申,邹立科,等.金属参与的水相烯丙基化反应[J].化学进展,2007,19(6):920 -931.
[10]陈韶蕊,马吉海,周雪琴,等.合成1,2-环十二二酮的新方法[J].应用化学,2009,26(11):1374 -1376.
[11]Chen S R,Ma J H,Zhou X Q,et al.A rapid and convenient synthesis of diketones[J].Asian Journal of Chemistry,2011,23(1):467 -468.
[12]Nokami J,Otera T,Sudo R O.Allylation of ketones and aldehydes in the presence of water by allylic bromides metallic tin and aluminum[J].Organometallics,1983,2(2):191 -193.
[13]胡丽华,纪顺俊.水相中6-甲基-6-苯基-7-烯-1,5-辛二醇的合成[J].苏州大学学报,2004,20(3):61 -64.
