廉价生物吸附剂的制备及其对刚果红吸附研究
2013-03-20王喜凤宿显瑞杨高举朱大恒
席 宇, 王喜凤, 宿显瑞, 杨高举, 杨 帆, 朱大恒
(1.郑州大学生物工程系 河南郑州450001;2.河南省中原建设有限公司 河南郑州450000)
0 引言
在染料生产和使用过程中,大约10% ~20%的染料随废水排放出去,其中80%是偶氮染料[1],许多染料及其分解产物具有较高毒性,能够引起水生生物的突变或过敏反应,具有潜在的危害[2-3].生物吸附是一种环境友好的廉价方法[4],不会产生有毒的代谢产物,为染料废水处理和染料回收提供一种经济可行的途径.开发廉价的吸附剂用于脱色印染废水已引起许多研究者的关注[5],真菌生物吸附剂具有极大的应用发展潜力[6-10].在烟草加工和烟草废弃物处理过程中常产生大量的TWW,TWW中含有大量有机物质[11-14],在TWW处理前或者处理过程中对其进行资源化利用具有非常重要的意义[15].本试验分离一株能够在TWW中快速生长的青霉菌LY7,其菌丝体对刚果红具有较强的吸附能力[16].实验以TWW为基质培养青霉菌LY7,以灭活菌丝体制备生物吸附剂,研究其对偶氮染料CR的吸附特性,既资源化利用了TWW,又为开发廉价高效生物吸附剂提供新思路.
1 材料与方法
1.1 材料
TWW来源于废弃烟梗固态发酵前的浸泡过程[17].CR购自天津市科密欧化学试剂开发中心,其最大吸收值为495 nm.CR用蒸馏水配成质量浓度为1 000 mg/L溶液备用.染料溶液pH由1 mol/L的HCl和NaOH溶液调节.所有供试试剂均为分析纯.
1.2 菌株及培养基
实验菌株为青霉菌LY7,分离于废弃烟梗固体发酵物中,保藏于郑州大学生物工程系烟草生物工程实验室.TWW于8 000 rpm离心5 min,上清液于121℃灭菌20 min即为TWW培养基,其中固体培养基琼脂含量为2%.菌株的保藏与培养分别采用TWW斜面和液体培养基.
1.3 方法
1.3.1 生物吸附剂的制备 菌株LY7接种到TWW斜面培养基30℃培养3 d,用无菌生理盐水洗脱孢子并计数,制成浓度为1×108个/mL孢子悬液,以1%的接种量加入含200 mL的TWW液体培养基的500 mL的三角瓶中,置摇床150 rpm、30℃培养4 d,形成直径约为2~3 mm的菌丝球,121℃ 灭菌10 min制备灭活菌丝球.去离子水冲洗灭活菌丝球至洗液pH值接近去离子水后,置烘箱内60℃烘干至恒重,研磨过120目标准筛即为真菌生物吸附剂,命名为PLYB.
1.3.2 生物吸附剂的表征 用扫描电子显微镜(JSM-6700F,日本电子公司)观察PLYB的表面特征,用傅立叶变换红外光谱仪(Vector22,美国布鲁)分析PLYB的基团组成.
1.3.3 吸附试验 将一定量的PLYB放入含100 mL的CR溶液的250 mL锥形瓶中,置于恒温摇床180 rpm转速进行吸附试验.为考察不同因素对CR脱色效果的影响,批式试验分别在不同初始染料浓度(50~200 mg/L)、不同pH(4.0~9.0)、不同温度(20~40℃)下进行.实验设置3个平行,所有吸附试验均在180 rpm下进行,定期取样测量脱色率和吸附量,结果取平均值.
1.4 吸附量和脱色率的测定
吸附一定时间后,取脱色液以8 000 rpm离心5 min,用紫外可见分光光度计(UV-2450,日本岛津)在495 nm处测量上清液的吸光度,以不加PLYB的染料溶液为对照,根据吸光度与染料浓度在一定范围内呈线性关系进行染料浓度的测定.脱色率R%=((A0-At)/A0)100%,吸附量q=(C0-Ct)·V/m,式中,A0为不加吸附剂溶液的OD值,At为脱色t时间后溶液的OD值,C0和Ct分别为CR初始浓度和吸附t时间后浓度,单位为mg/L;V为吸附溶液的体积,单位为L;m为PLYB的质量,单位为g;q为吸附量,单位为mg/g.
2 结果与讨论
2.1 生物吸附剂的表征
利用SEM可以清晰观察到吸附剂的外部特征,由图1(A)可以看出,PLYB外表粗糙,具有很多颗粒状突起,且有微孔结构,吸附表面积较大,易于染料颗粒接触其内部和表面,从而有利于染料的吸附.FTIR分析是鉴定物质官能团的一个重要方法.对吸附前后的PLYB进行红外光谱分析,结果如图1(B)所示:3 407 cm-1处的吸收峰表明吸附剂表面存在NH的伸缩振动[6],2 925 cm-1处的吸收峰代表CH2不对称伸缩振动[18],1 629 cm-1和1 653 cm-1处的吸收峰表明=CO伸缩振动,1 472 cm-1和1 482 cm-1处吸收峰表明NH与C—N伸缩振动相互作用,1 041 cm-1和1 080 cm-1处波峰代表=PO伸缩振动[18].吸收峰位置在吸附前后没有明显改变表明吸附过程主要为物理作用.吸附后,在1 230 cm-1处产生新吸收峰,峰宽且有副峰,为=SO伸缩振动[6].CR分子中含有=SO基团,因此1 230 cm-1吸收峰的产生表明CR被吸附剂吸附.
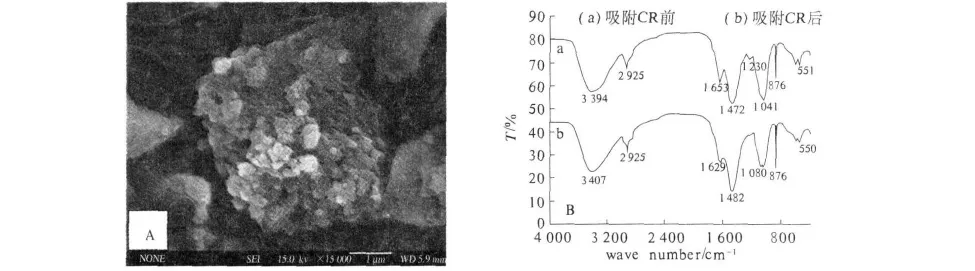
图1 PLYB扫描电子显微镜照片(A)和PLYB的红外光谱(B)Fig.1 SEM photograph of PLYB(A)and FTIR spectra of PLYB(B)
2.2 吸附剂量对吸附效果的影响
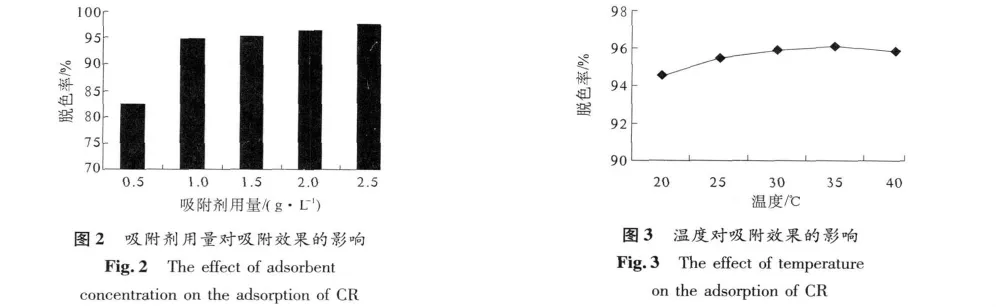
初始浓度为100 mg/L的CR溶液分别置于含不同吸附剂量的锥形瓶中,振荡吸附6 h,考察PLYB用量对吸附效果的影响.由图2可以看出当CR浓度一定时,随着吸附剂量的增加,CR溶液脱色率从82.3%增至97.7%.这表明随着PLYB的增加,吸附表面积和参与吸附的官能团数目均增加.当吸附剂量为1 g/L时,脱色率为94.8%,继续增加吸附剂量CR脱色率增加不大.综合脱色率和PLYB的潜在应用价值等因素,如无特别说明,后续试验均采用1 g/L作为吸附剂量.
2.3 温度和初始pH对吸附效果的影响
由图3可知,吸附过程中温度对脱色率影响显著,20~35℃时,脱色率随温度增加而增加,35℃时脱色率为95.81%,与35℃相比,40℃时脱色率稍微下降,这可能由于40℃时,染料的解吸附能力增加或者吸附剂结构发生变化.
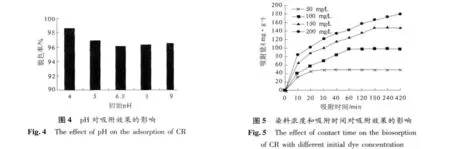
考虑到在实际运用中不会出现极端酸度情况,试验中CR的初始pH设置为4.0~9.0.从图4可以看出初始pH值对CR吸附的影响较小,当pH为4.0时,脱色率为98.1%,脱色效果最好.pH为5.0~9.0时,脱色率变化不大,均在96%以上.CR溶液的自然pH为6.8,因此选用pH 6.8进行其他因素的实验.
2.4 染料浓度和吸附时间对吸附效果的影响
以吸附量为指标,在吸附剂量为1 g/L、初始pH 6.8和30℃条件下,考察了不同初始染料浓度和吸附时间对吸附效果的影响,由图5可以看出,浓度越高,达到平衡所需时间越长,CR浓度为50 mg/L时,20 min即可达到吸附平衡,浓度为100 mg/L时,60 min即可达到吸附平衡,浓度为150 mg/L时,180 min即可达到吸附平衡,浓度为200 mg/L时,实验时间内尚未达到吸附平衡.
2.5 吸附剂对CR的吸附动力学
动力学实验目的是研究吸附的机理和速率控制步骤.准一级反应速率理论和准二级反应速率理论是经常用到的速率理论,其反应理论公式[19-20]分别为:log(qe-qt)=log qt-k1t/2.303,t/qt=1/(k2qe2)+t/qe,式中,t为吸附时间,单位为min.qt为t时PLYB的吸附量,单位为mg/g;qe为达到吸附平衡时的吸附量,单位为mg/g;k1为一级反应吸附速率常数,k2为二级反应吸附速率常数.
表1为两级反应速率公式对吸附数据进行线性拟合后的结果,吸附数据显示使用二级反应速率公式拟合后的相关系数(R22>0.99),理论预测平衡吸附量qe,2与实验值qe非常接近,说明PLYB对染料CR的吸附过程符合二级反应速率理论.一级反应速率公式拟合后相关系数比较低,理论预测平衡吸附量qe,1与实验值qe相差较大,说明吸附过程不符合一级反应速率理论.
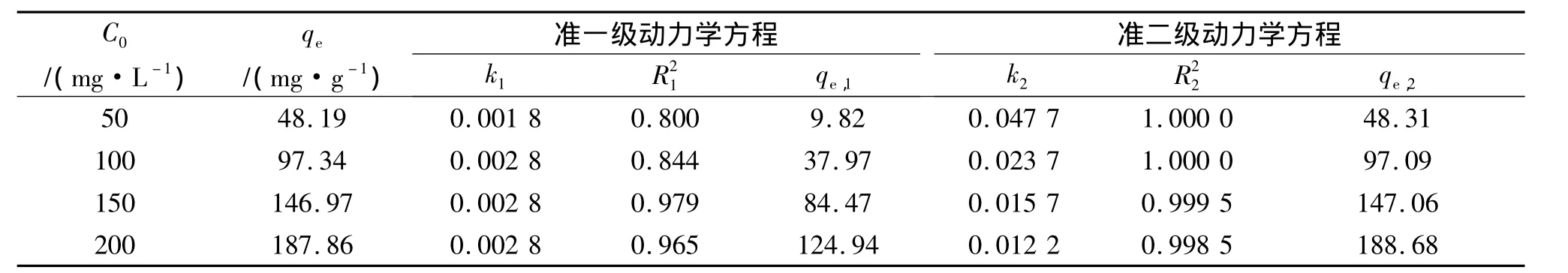
表1 PLYB吸附CR的准一级动力学和准二级动力学方程参数Tab.1 Kinetic parameters of pseudo-first order and pseudo-second order for the biosorption of CR
2.6 吸附等温线
在等温条件下,吸附剂在不同浓度的染料溶液中吸附达到平衡时的吸附量可用来描绘吸附等温线.Langmuir理论和Freundlish理论常用来解释染料吸附平衡数据,其理论公式[18-19]分别为:

其中,qe为达到吸附平衡时的吸附量,单位为mg/g;qm为吸附剂表面达到单分子层吸附时的最大吸附量,单位为mg/g;KL为Langmuir吸附常数;ce为达到吸附平衡时染料溶液的浓度,单位为mg/L;kf为Freundlish吸附系数;n为Freundlish吸附常数.图6和7为Langmuir和Freundlish理论对吸附数据进行线性拟合后的结果,Langmuir理论拟合后吸附数据呈现良好的线性关系,相关系数非常高(R2>0.96),说明PLYB对CR的吸附符合Langmuir吸附理论.而Freundlish理论拟合的相关系数相对较小,不适合用来解释PLYB对CR的吸附过程.根据Langmuir方程,最大吸附量可达到312.5 mg/g,与文献报道相比吸附量较高,PLYB吸附能力较强.

3 结论
1)利用TWW发酵生产青霉菌LY7菌丝体,以灭活菌丝体制备真菌生物吸附剂PLYB,既资源化利用TWW,又可获得廉价生物吸附剂.
2)PLYB对CR的吸附过程符合Langmuir等温线和准二级动力学模型,其最大吸附量可达312.5 mg/g.
3)LY7菌丝体经过高温高压处理,因此PLYB属于环境友好型吸附剂,在偶氮染料的去除中具有潜在的应用价值.
[1] 杨清香,贾振杰,杨敏.微生物染料脱色研究进展[J].微生物学通报,2006,33(4):144-148.
[2] Tatarko M,Bumpus J A.Biodegradation of Congo Red by Phanerochaete chrysosporium[J].Water Research,1998,32(5):1713-1717.
[3] 邹卫华,白红娟,李苛,等.天然沸石对阳离子染料中性红的吸附及机理研究[J].郑州大学学报:理学版,2011,43(4):71-76.
[4] 邹卫华,李苛,白红娟,等.花生壳对水中阳离子染料吸附性能的研究[J].郑州大学学报:工学版,2010,31(6):87-90.
[5] Han Runping,Ding Dandan,Xu Yanfang,et al.Use of rice husk for the adsorption of congo Red from aqueous solution in column mode[J].Bioresource Technology,2008,99(8):2938-2946.
[6] Yang Yuyi,Wang Guan,Wang Bing,et al.Biosorption of acid black 172 and Congo Red from aqueous solution by nonviable Penicillium YW 01:kinetic study,equilibrium isotherm and artificial neural network modeling[J].Bioresource Technology,2011,102(2):828-834.
[7] Yang Yuyi,Jin Danfeng,Wang Guan,et al.Competitive biosorption of Acid Blue 25 and Acid Red 337 onto unmodified and CDAB-modified biomass of Aspergillus oryzae[J].Bioresource Technology,2011,102(16):7429-7436.
[8] Xiong Xiaojing,Meng Xuejiao,Zheng Tianling.Biosorption of C.I.Direct blue 199 from aqueous solution by nonviable Aspergillus niger[J].Journal of Hazardous Materials,2010,175(1/2/3):241-246.
[9] Srinivasan A,Viraraghavan T.Decolorization of dye wastewaters by biosorbents:a review[J].Journal of Environmental Management,2010,91(10):1915-1929.
[10] Kaushik P,Malik A.Fungal dye decolourization:recent advances and future potential[J].Environment International,2009,35(1):127-141.
[11] 陈元彩,陈竹,肖仙英,等.造纸法烟草薄片废水的研究[J].中国造纸,2006,25(9):20-22.
[12] 邱晔,胡群,陈辉敏,等.再造烟叶生产废水处理研究[J].工业水处理,2006,26(3):23-25.
[13] Bejankiwar R S.Electrochemical treatment of cigarette industry wastewater:feasibility study[J].Water Research,2002,36(17):4386-4390.
[14] Wang Meizhen,Yang Guiqin,Min Hang,et al.Bioaugmentation with the nicotine-degrading bacterium pseudomonas sp hf-1 in a sequencing batch reactor treating tobacco wastewater:degradation study and analysis of its mechanisms[J].Water Research,2009,43(17):4187-4196.
[15] 席宇,吉彦龙,李敏睿,等.一株利用烟草废水红酵母的筛选鉴定及发酵性能研究[J].郑州大学学报:理学版,2012,44(3):101-105.
[16] 席宇,高明,郭东衡,等.废弃烟梗发酵生产真菌吸附剂及其脱色作用[J].烟草科技,2012(6):72-75.
[17] 高明,郭灵燕,席宇,等.烟梗生物发酵制造有机肥[J].烟草科技,2010(12):57-60.
[18] Akar T,Tosun I,Kaynak Z,et al.Assessment of the biosorption characteristics of a macro-fungus for the decolorization of Acid Red 44(AR44)dye[J].Journal of Hazardous Materials,2009,171(1/2/3):865-871.
[19] Bhattacharyya K G,Sharma A.Azadirachta indica leaf powder as an effective biosorbent for dyes:a case study with aqueous Congo Red solutions[J].Journal of Environmental Management,2004,71(3):217-229.
[20] Akar S T,Özcan A S,Akar T,et al.Biosorption of a reactive textile dye from aqueous solutions utilizing an agro-waste[J].Desalination,2009,249(2):757-761.
