三氯甲烷在金属有机框架膜上的吸附过程监测
2013-03-14许中石蔡婷婷申大忠
许中石,蔡婷婷,康 琪,申大忠
(山东师范大学化学化工与材料科学学院,山东济南250014)
三氯甲烷在金属有机框架膜上的吸附过程监测
许中石,蔡婷婷,康 琪,申大忠*
(山东师范大学化学化工与材料科学学院,山东济南250014)
采用石英晶体微天平(QCM)技术动态监测三氯甲烷在[Cu(C24H22N4O3)]·CH2Cl2金属有机框架膜(Cu-MOFs)上的吸附动力学,吸附与解吸过程中膜质量的变化由QCM的频率变化实时传感测量,结果表明,吸附过程符合假二级动力学模型,其中在三氯甲烷蒸气压条件下的吸附速率常数为在1.01×105Pa N2存在下速率常数的1.4~2.1倍,半数以上的吸附量相对于气相浓度稀释呈现可逆吸附特征。吸附等温线符合Langmuir等温式,在蒸气压与1.01×105Pa N2存在条件下(25℃),三氯甲烷在厚度为0.337 μm Cu-MOFs上吸附的平衡常数分别为6.47与3.93 L/g,最大吸附量分别为27.2与24.7 μg/cm2。
金属有机框架;挥发性有机物;石英晶体微天平;吸附动力学
0 引言
挥发性有机物(VOCs)现在已经成为空气污染的重要组成部分,如何高效地去除环境中VOCs已经成为一个重要的研究课题[1],目前报道的方法主要包括冷凝法、吸附法、氧化还原法和焚烧法等[2~6]。其中吸附法具有技术成熟、工艺简单,不产生新的污染物的特点,其实际应用取决于高效吸附剂的研发。金属有机框架(MOFs)材料是有机配体与过渡金属离子配合所形成的三维多孔晶体材料,具有巨大的比表面积,因此在存储气体、物质分离、催化、传感及其它方面具有良好应用前景[7~11]。人们合成了各种结构的MOFs,并对其性能进行了较为全面的表征。
石英晶体微天平(QCM)作为一种高灵敏度的质量型传感器,在检测界面传质过程方面具有技术优势[12~14]。采用QCM研究MOFs材料的吸附性能,具有样品用量少,动态过程详细的特点[15~19]。该文采用QCM技术结合阻抗分析法,动态监测 CHCl3在[Cu(C24H22N4O3)]·CH2Cl2(Cu-MOFs)膜上的吸附动力学过程,讨论了吸附方式对吸附量、可逆性、吸附动力学参数的影响,完善了QCM表征MOFs膜吸附特性的分析方法。
1 实验部分
1.1 仪器与试剂
Cu-MOFs样品由山东师范大学董育斌课题组合成,其合成方法参见文献[20]。QCM谐振器(AT切型,直径14 mm,基频5 MHz)购自北京晨晶电子有限公司,以金膜为激励电极。图1为吸附实验装置示意图,检测池由玻璃加工而成,体积为3.9 L,池内温度由恒温水浴控制在(25±1)℃。QCM传感器水平固定在检测池的中央,其谐振频率和动态电阻由阻抗仪(4294A,Agilent)测定。吸附实验中,有机溶剂通过进样口由微量注射器导入检测池,池中加装一小风扇加强对流。脱附实验中,通过真空泵排除池中气体,使膜再生。

图1 QCM监测有机溶剂在MOFs膜表面吸附实验装置示意图(非比例尺)。(1):样品注入口;(2):氮气入口; (3):恒温水浴;(4):微型风扇;(5):MOFs膜修饰QCM传感器;(6):真空泵;(7):阻抗分析仪Fig.1 Schematic drawing of experimental setup employed for the adsorption measurements(not to scale).(1):syringe with organic solvent;(2):inlet for nitrogen gas; (3):thermostatic water bath;(4):mini fan;(5):QCM sensor with MOFs film;(6):vacuum pump;(7):impedance analyzer
1.2 Cu-MOFs膜吸附CHCl3
成膜修饰前先将QCM晶体用丙酮洗涤,用氮气流吹干。用微量注射器移取一定体积浓度为2 mg/mL的Cu-MOFs乙醇悬浊液均匀滴加在QCM金电极上,待乙醇挥发后,金电极表面形成一层Cu-MOFs膜。将成膜后的QCM安放在装置中,在真空条件下进一步去除膜中的溶剂,待QCM频率稳定后,根据成膜前后的频率变化(ΔFf)以Sauerbrey方程确定膜厚度。

式中 F0为 QCM的基频(Hz),ρ(=1.498 g/cm3)为Cu-MOFs晶体的密度[20],在所用实验条件下,ΔFf=-2 856 Hz,对应 Cu-MOFs膜厚度为 h= 0.337μm。

图2 吸附与脱附过程中QCM的频率变化曲线。吸附条件:CHCl3加入量57.7 mg/L,步骤I:CHCl3在低压下吸附;步骤II:N2在大气压下后续吸附;步骤III:去除池中CHCl3后脱附过程;步骤IV:抽真空条件下的脱附过程Fig.2 Frequency shifts of QCM with Cu-MOFs film in adsorption and desorption processes.The amount of CHCl3added was 57.7 mg/L.Stages I to IV corresponds the adsorption of CHCl3under low pressure,subsequent adsorption of air under atmospheric pressure,desorption by replacing CHCl3in cell with N2stream,and desorption under vacuum,respectively
图2为吸附实验中各操作步骤对应QCM的频率变化曲线。在吸附前,先将检测池抽真空,使Cu-MOFs膜中所吸附气体解析,直至获得稳定的基线。步骤I:向检测池中注入一定体积的CHCl3,在真空负压作用下CHCl3被吸入池中并快速气化,而后在Cu-MOFs膜上吸附,对应QCM的频率下降,其频率差ΔF1可用于计算CHCl3的吸附量与动力学参数。步骤II:吸附一定时间后让检测池吸入N2直至其压力与大气压相等,该过程的频率下降量(ΔF2)可用于计算N2的吸附量。步骤III:用N2流驱逐检测池内的CHCl3,后者在大气压下解吸附,QCM频率上升并达到一个稳定值,该频率变化(ΔF3)用来计算CHCl3在MOFs膜中的可逆吸附量。步骤IV:将检测池抽真空,以其频率变化(ΔF4)计算CHCl3在膜内的不可逆吸附量。为扣除N2吸附对计算CHCl3吸附量的影响,测定真空解吸CHCl3后的MOF膜上吸附N2的频率变化(ΔF5),并按所列公式进行校正。
2 结果与讨论
2.1 QCM监测吸附过程及吸附量测定
在所选吸附体系中,以CHCl3和Cu(C24H22N4O3)作为模型VOCs分子和模型MOFs膜,它们相互作用过程中的界面传质动力学可由QCM实时监测。由图2可见,在低压条件下向池中加入CHCl3,它将快速挥发并在Cu-MOFs膜上吸附,QCM的表面质量负载增加其频率下降。在起始吸附阶段,吸附速率较快,在所用实验条件下,在前6 min内,吸附量就能达到总吸附量的90%。随着吸附时间延长,吸附量增幅逐渐下降,但即使吸附60 min后也未达到平衡。
由图3可见,随着CHCl3加入量的增加,QCM频率下降幅度增加,前20 min内频率的变化符合下面的指数衰减模型:
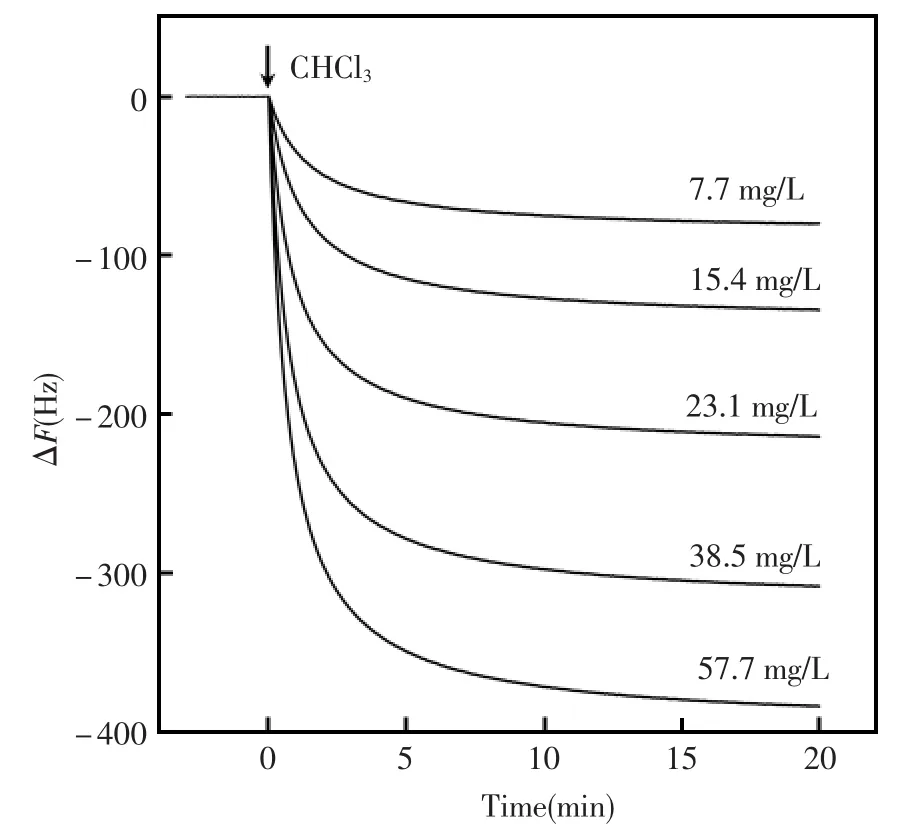
图3 低压条件下Cu-MOFs膜吸附CHCl3过程中QCM的频率变化曲线Fig.3 Frequency shifts of QCM with Cu-MOFs film in adsorption of CHCl3under low pressure.

其中,ΔF10(≈ΔF110+ΔF120)为吸附平衡时的频率差,r1和r2为表观吸附速率常数 (r1>>r2),t是吸附时间。以式(2)为拟合模型,回归所得ΔF10可用于计算CHCl3的平衡吸附量。
根据上述回归方程,该吸附过程至少包括了两个过程。在吸附的初始阶段,CHCl3首先吸附在Cu-MOFs膜表面及浅层中,此时传质阻力较小,因此吸附速率较快,其吸附质量及动力学过程与式(2)中的ΔF110和r1相关。因为MOFs是具有高比表面积的多孔结构材料,吸附在浅层中的CHCl3在浓度梯度的推动下进一步向深层扩散,空出部分先前占据的位点供后续吸附,但向膜内扩散的阻力不断增加,故吸附后期虽然吸附量在缓慢增加,但增幅越来越小,吸附过程需较长的时间才能达到平衡,所对应的吸附量及动力学过程与式(2)中的ΔF120和r2关联。
在实际的变电运维过程中,其复杂性特点决定了设备发生故障和事故的频繁性,从而导致了需要经常对设备进行检修,也即其频繁性。
2.2 CHCl3与N2的竞争吸附
在图3所用吸附实验中,CHCl3浓度低,例如,当加入量为150 μL(1.88 mmol)时,完全挥发后其浓度为0.48 mol/L,根据理想气体状态方程,估算出池中的CHCl3蒸气压约为1 212 Pa,当向检测池中注入N2使最终池中压力达到1.01×105Pa时,由图2可见,N2分子也能在MOFs膜上吸附,因此QCM频率下降(步骤II)。由于N2浓度较高(40.9 mmol/L),吸附速率较快,约5 min即可达到吸附平衡。虽然N2浓度比CHCl3浓度高85倍,但频率变化量仅为-195 Hz,约为CHCl3频率变化量(-383 Hz)的51%,由此可见,Cu-MOFs膜对CHCl3的亲和力远大于N2。
由图4可见,若使Cu-MOFs膜先在1.01×105Pa下吸附N2,吸附速率更快,吸附在2 min内达到平衡,该过程频率变化-231 Hz,当再向池中加入CHCl3时,仍可以观测到QCM频率大幅度下降,表明在大量N2存在下CHCl3仍可以吸附,但与图3相比,吸附速率明显下降,其原因之一是CHCl3在大气压条件下的挥发速率不及近真空的低压条件,另一原因是部分吸附位点已被N2先行占据,CHCl3需通过置换N2而吸附,也导致吸附速率和吸附量减小。Cu-MOFs膜在大量N2存在下仍然保持着对CHCl3的强吸附,这将有利于Cu-MOFs膜在去除有机挥发性气体中的实际应用。
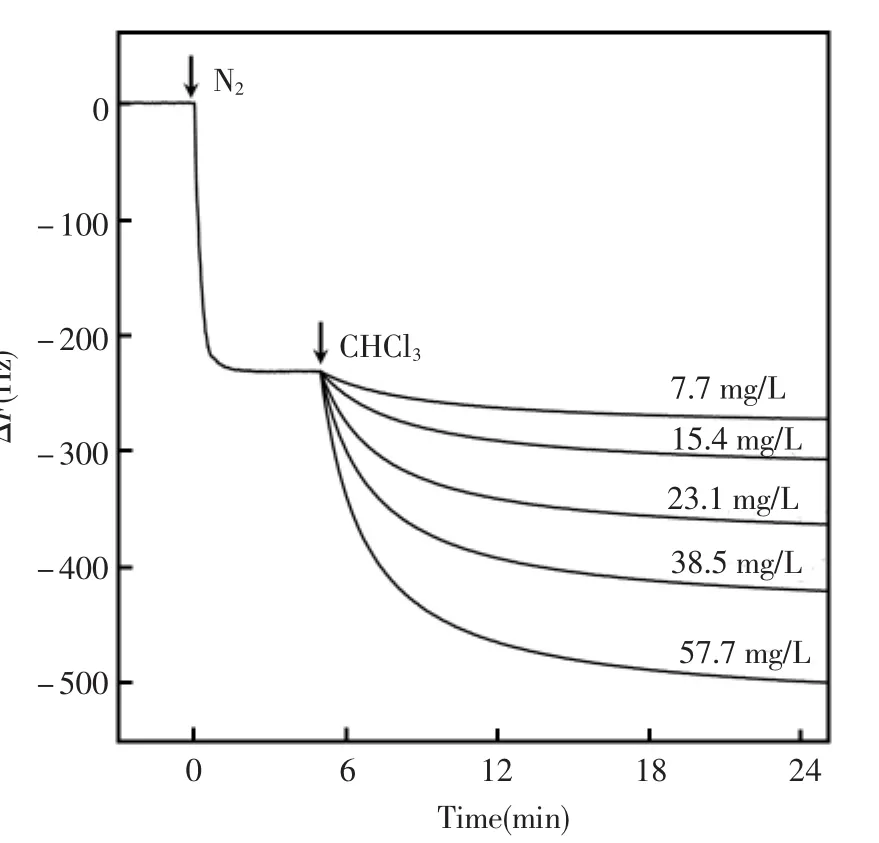
图4 大气压下Cu-MOFs膜先吸附N2再吸附CHCl3过程中QCM的频率变化曲线Fig.4 Frequency shifts of QCM with Cu-MOFs film in subsequent adsorption of N2and CHCl3under atmospheric pressure
2.3 可逆吸附量与不可逆吸附量的计算
根据Sauerbrey方程,在步骤I中单位面积膜上吸附CHCl3的吸附量可由下式计算:
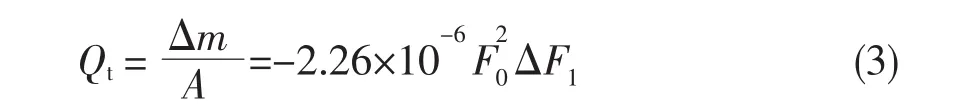
式中,Qt为被吸附分子在吸附过程中的动态吸附量(μg/cm2),Δm为吸附质量(μg),A为QCM的敏感区面积(cm2)。
考虑到Sauerbrey方程仅适用于刚性、均匀的薄膜,为考察膜的刚性,以阻抗法测定了QCM的动态电阻,该参数越小表明QCM在谐振过程中能量损耗越低,膜的刚性度越好,越接近Sauerbrey方程成立的条件。实验结果表明,CHCl3在Cu-MOFs膜上的吸附过程中,QCM的动态电阻随吸附量增加而上升,但变化量较小。图5所示为CHCl3加入量较大(1.8 g/L)时QCM的变化曲线,频率下降与动态电阻上升趋势明显,需要说明的是,电阻与频率变化量之间呈现非线性关系,例如吸附初期QCM的频率从0下降到-1 kHz时,动态电阻仅增加1.1 Ω,而频率从-1 kHz降至-2 kHz时,动态电阻增加8.3 Ω,而后动态电阻随频率下降快速上升,当频率从-2 kHz降至-3 kHz时,动态电阻增加159 Ω,当频率下降到-3.2 kHz时,动态电阻已升高至290 Ω,CHCl3在Cu-MOFs膜上大量吸附而凝结成液膜,此时Sauerbrey方程不成立,需扣除膜粘弹性增加所引起的频率变化。由此可见,在所用实验条件下,当频率下降量低于-2.2 kHz时,QCM的动态电阻值低于50 Ω,可认为吸附CHCl3之后的Cu-MOFs膜虽然增加了QCM谐振时能量耗损,但该膜仍可以视为刚性膜,吸附量可用式(3)计算。
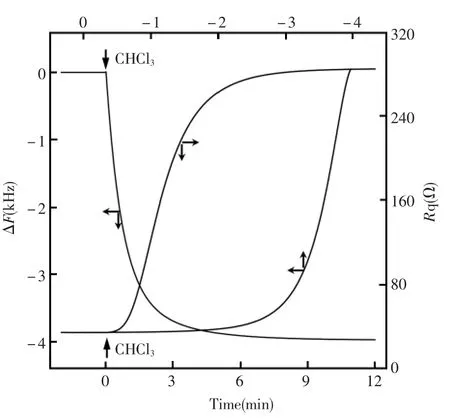
图5 Cu-MOFs膜修饰QCM传感器在吸附CHCl3过程中的频率与动态电阻变化曲线:CHCl3加入量为1.8 g/LFig.5 Changes of frequency and motional resistance of QCM with Cu-MOFs film in adsorption of CHCl3.The amount of CHCl3added was 1.8 g/L

其中,Qe为吸附达到平衡时的吸附量(μg/cm2),ce为CHCl3的平衡浓度(mg/L),图中采用加入量未考虑膜与池壁的吸附损失,Qmax是最大吸附量(μg/cm2),K是吸附平衡常数(L/g)。
在近真空的低压条件下,CHCl3的吸附等温线参数为:Qmax=27.2 μg/cm2K=6.47 L/g,其值略高于在1.01×105Pa N2预吸附后的等温线参数:Qmax=24.7 μg/cm2K=3.93 L/g。结果表明,N2的存在一定程度上阻碍了该膜对CHCl3的吸附,在低浓度曲线中尤为明显,因为气相中N2的浓度远大于CHCl3的浓度,其分子数量上的优势在竞争吸附中显现出来。另外,Qmax=27.2 μg/cm2所对应的吸附质量为膜质量的53.8%。

图6 在低压及N2存在条件下CHCl3在Cu-MOFs膜上的吸附等温线及可逆吸附所占比例Fig.6 Adsorption isotherms and percent of reversible adsorption of CHCl3in Cu-MOF film under low pressure and in the presence of N2at atmospheric pressure
此外,由图2可见,当检测池中CHCl3被N2流带出后,其浓度下降,QCM的频率出现快速上升,表明吸附在Cu-MOFs膜表面的CHCl3发生了解吸,这部分吸附量视为可逆吸附,其大小可由ΔF3表示(步骤III)。因为Cu-MOFs膜对N2也有一定吸附能力,当CHCl3解吸后,所空余出的部分吸附位点又被N2所占据,由此造成的频率下降部分抵消了频率上升值,使ΔF3偏小。当N2在真空脱附后的Cu-MOFs膜上吸附时,其吸附所致频率降为ΔF5=-216 Hz,其绝对值大于图中ΔF2(-195 Hz),差值|ΔF5|-|ΔF2|可近似对应于N2在CHCl3的解吸过程中的新增吸附量,因此可使用下式计算CHCl3的解吸量:

若将不为检测池中CHCl3浓度稀释而解吸的吸附量视为不可逆吸附量,它对应CHCl3分子在膜内层吸附,其值为总吸附量与可逆吸附量之差,即Qir=Qe-Qr。
由图6可见,随检测池中CHCl3浓度增加,总吸附、可逆吸附量、不可逆吸附量均增加,在所用吸附实验条件下,可逆吸附量高于不可逆吸附量,在低浓度区间尤为明显。
需要说明的是,CHCl3在Cu-MOFs膜中相对于气相浓度稀释的不可逆吸附量可以通过真空法去除,但由图2可见,在真空脱附过程中,QCM的频率并未上升到吸附前的起始基线水平(约低23 Hz),表明在膜内仍有部分CHCl3分子在短时间内未完全脱附。为使Cu-MOFs膜中吸附的CHCl3尽快解吸,可重复通N2和抽真空循环3次。
2.4 吸附动力学参数测定
QCM作为一种高灵敏度的质量型传感器,在测定吸附动力学参数方面具有技术优势,在有关吸附动力学研究中,常采用假一级、假二级动力学模型拟合吸附动力学曲线。如前所述,在所用实验条件下,吸附动力学过程可用式(2)的双指数衰减函数拟合,而假一级动力学模型为单指数衰减函数,采用该模型拟合的相关系数较低(0.95~ 0.98),相比之下,由图7可见,采用式(6)所列假二级动力学模型的线性关系式拟合的线性度良好,相关系数在0.993~0.998。
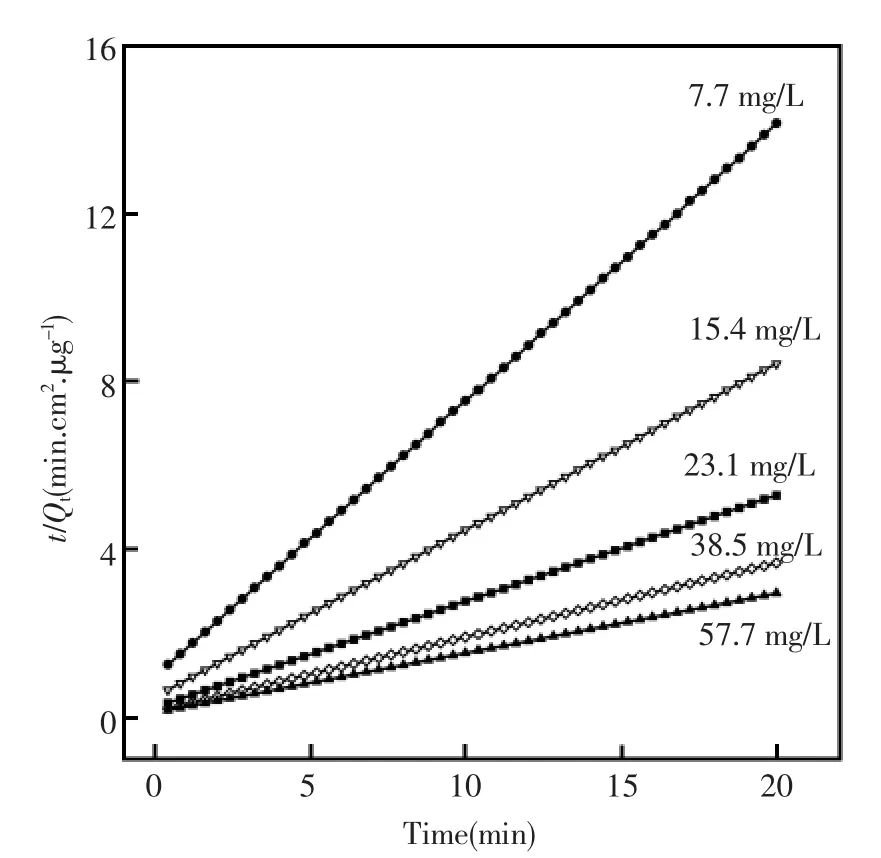
图7 低压条件下CHCl3在Cu-MOFs膜上吸附动力学过程的假二级模型拟合曲线Fig.7 Pseudo-second-order kinetics for CHCl3adsorption onto Cu-MOFs film under low pressure

其中,Qt为t时刻的吸附量(mol/L),k2为假二级吸附的速率常数(min-1·cm2·μg)。根据回归曲线的斜率与截距可以计算出平衡吸附量、吸附速率常数。由图8可见,在低压下的吸附速率常数为在大气压下吸附速率常数的1.4~2.1倍。此外,随着CHCl3浓度增加,假二级吸附速率常数下降。
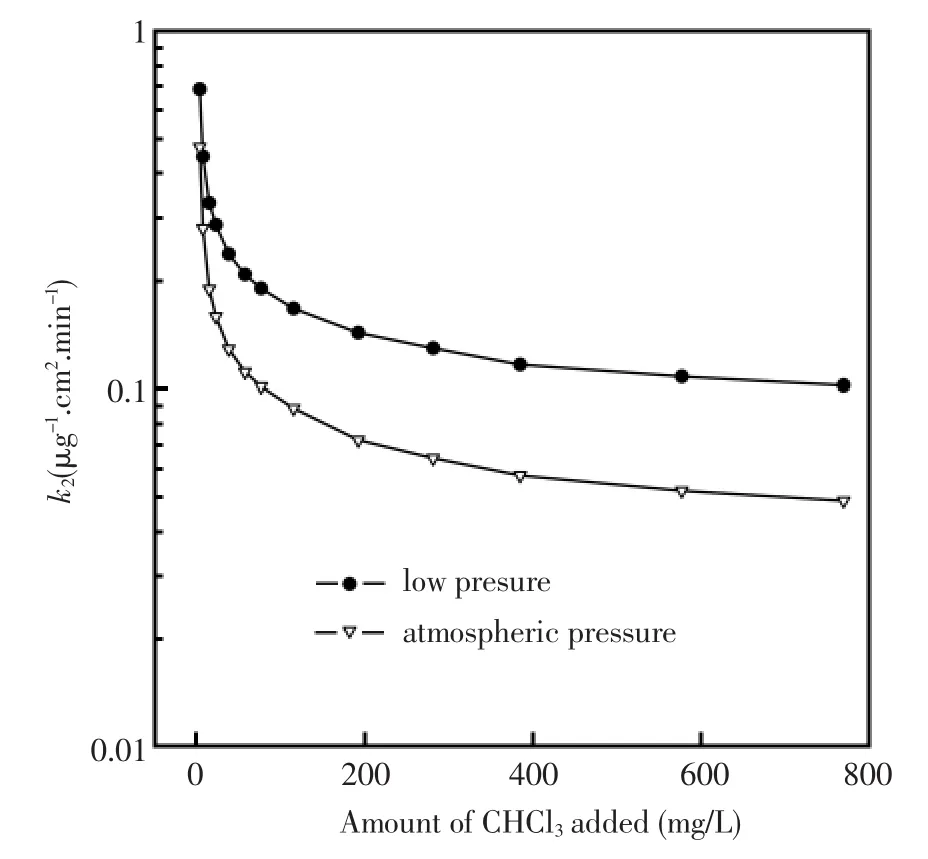
图8 不同气压下CHCl3在Cu-MOFs膜上的假二级吸附速率常数随CHCl3加入量的变化曲线Fig.8 Dependence of the rate constants of the pseudosecond-order model under different vapor pressures on the amount of CHCl3added and the thickness of Cu-MOF film
3 结论
该文建立了一种基于QCM动态表面质量测量传感的膜吸附研究方法,实时监测了所制备的Cu-MOFs膜吸附CHCl3的动力学过程,结果表明,吸附过程包括一个快速的表面吸附过程和一个较缓慢的膜内扩散过程,部分吸附在膜内层的CHCl3相对于气相浓度稀释呈现不可逆吸附特征,Cu-MOFs膜对CHCl3亲和力明显高于N2,在大量N2存在下,CHCl3仍能在Cu-MOFs膜上吸附,但吸附量与吸附速率有所下降。在所用实验条件下,CHCl3在Cu-MOFs膜上的吸附过程符合假二级动力学模型,吸附等温线符合Langmuir吸附等温式。
[1]Guo H,Cheng H R,Ling Z H,et al.Which emission sources are responsible for the volatile organic compounds in the atmosphere of Pearl River Delta[J].J. Hazard.Mater.,2011,188:116~124.
[2]Russo P A,Ribeiro Carrott M M L,Carrott P J M.Trends in the condensation/evaporation and adsorption enthalpies of volatile organic compounds on mesoporous silica materials[J].Microp.Mesop.Mat.,2012,151: 223~230.
[3]Zhong L X,Lee C S,Haghighat F.Adsorption performance of titanium dioxide (TiO2)coated air filters for volatile organic compounds[J].J.Hazard.Mater.,2012, 243:340~349.
[4]Chen J Y,Li G Y,He Z G,et al.Adsorption and degradation of model volatile organic compounds by a combined titania-montmorillonite-silica photocatalyst[J].J. Hazard.Mater.,2011,190:416~423.
[5]Silva B,Figueiredo H,Santos VP,et al.Reutilization of Cr-Y zeolite obtained by biosorption in the catalytic oxidation of volatile organic compounds[J].J.Hazard. Mater.,2011,192:545~553.
[6]Mo J H,Zhang Y P,Xu Q J,et al.Photocatalytic purification of volatile organic compounds in indoor air:A literature review[J].Atmos.Environ.,2009,43:2 229~ 2 246.
[7]Li J R,Sculley J,Zhou H C.Metal-organic frameworks for separations[J].Chem.Rev.,2012,112:869~932.
[8]Stock N,Biswas S.Synthesis of metal-organic frameworks(mofs):routes to various mof topologies,morphologies,and composites[J].Chem.Rev.,2012,112:933~ 969.
[9]Lu G,Hupp J T.Metal-organic frameworks as sensors:A ZIF-8 based Fabry-Pérot device as a selective sensor for chemical vapors and gases[J].J.Am.Chem.Soc.,2010, 132:7 832~7 833.
[10]Keskin S,Kyzylel S.Biomedical applications of metal organic frameworks[J].Ind.Eng.Chem.Res.,2011,50: 1 799~1 812.
[11]Shah M,McCarthy M C,Sachdeva S,et al.Current status of metal-organic framework membranes for gas separations:promises and challenges[J].Ind.Eng.Chem. Res.,2012,51:2 179~2 199.
[12]姚守拙.压电化学与压电传感[M].北京:化学工业出版社,2006.
[13]Ferreira GNM,da-Silva AC,Tomé B.Acoustic wave biosensors:physical models and biological applications of quartz crystal microbalance[J].Trends Biotechnol., 2009,27:689~697.
[14]Xu X M,Cang HW,Li C Z,et al.Quartz crystal microbalance sensor array for the detection of volatile organic compounds[J].Talanta,2009,78:711~716.
[15]Biemmi E,Darga A,Stock N,et al.Direct growth of Cu3(BTC)2(H2O)3·xH2O thin films on modified QCM-gold electrodes-water sorption isotherms[J].Microp.Mesop.Mat.,2008,114:380~386.
[16]Huang C Y,Song M,Gu Z Y,et al.Probing the adsorption characteristic of metal-organic framework MIL-101 for volatile organic compounds by quartz crystal microbalance[J].Environ.Sci.Technol.,2011,45:4 490~ 4 496.
[17]Khoshaman AH,Bahreyni B.Application of metal organic framework crystals for sensing of volatile organic gases [J].Sensor.Actuat.B,2012,162:114~119.
[18]Qian H D,Li S H,Zheng J F,et al.Ultrathin films of organic networks as nanofiltration membranes via solutionbased molecular layer deposition[J].Langmuir,2012, 28:17 803~17 810.
[19]Robinson A L,Stavila V,Zeitler T R,et al.Ultrasensitive humidity detection using metal-organic frameworkcoated microsensors[J].Anal.Chem.,2012,84:7 043~ 7 051.
[20]Dong Y B,Zhang Q,Liu LL,et al.Cu(C24H22N4O3)]· CH2Cl2:A discrete breathing metallamacrocycle showing selective and reversible guest adsorption with retention of single crystallinity[J].J.Am.Chem.Soc.,2007,29: 1 514~1 515.
Monitor the adsorption process of chloroform over a metal-organic framework film
Xu Zhong-shi,Cai Ting-ting,Kang Qi,Shen Da-zhong*
(School of Chemistry,Chemical Engineering and Material Science,Shandong Normal University,Jinan 250014, China)
The adsorption kinetics of chloroform over a metal-organic framework film of[Cu(C24H22N4O3)]·CH2Cl2(Cu-MOFs)was investigated by a quartz crystal microbalance(QCM)technique.The change in the mass of Cu-MOFs film during the adsorption and desorption processes was monitored in real time by the frequency shift of QCM.The adsorption process follows closely the pseudo-second-order kinetic model.The adsorption rates at vapor pressure of chloroform are 1.4~2.1 times of that in the presence of N2at atmospheric pressure.More than half of chloroform adsorbed over Cu-MOFs film is reversible with respect to the dilution of chloroform concentration in gas phase.The adsorption isotherms are fitted well by the Langmuir model.For chloroform adsorbed at its vapor pressure and in N2of 1.01×105Pa over Cu-MOFs film with thickness of 0.337 μm(25℃),the adsorption equilibrium constants are 6.47 and 3.93 L/g,the maximum adsorption capacities are 27.2 and 24.7 μg/cm2.
metal-organic framework;volatile organic compound;quartz crystal microbalance;adsorption kinetics
国家自然科学基金(21175084,21275091)资助项目
*通讯联系人,E-mail:dzshen@sdnu.edu.cn
