局部注射用右旋酮洛芬氨丁三醇温敏凝胶的制备及其体外释药的考察
2013-01-04刘丽君张洁唐丽刘跃黄勇贵阳医学院药学院民族药与中药开发应用教育部工程研究中心贵州贵阳550004贵州省药物制剂重点实验室贵州贵阳550004
刘丽君,张洁,唐丽,刘跃,黄勇, (.贵阳医学院药学院,民族药与中药开发应用教育部工程研究中心,贵州 贵阳550004;.贵州省药物制剂重点实验室,贵州 贵阳550004)
右旋酮洛芬氨丁三醇(dexketoprofen trometamol),是2-芳基丙酸类非甾体抗炎药(non-steroidal anti-inflammatory drugs,NSAIDs),临床主要用于缓解各类疼痛,特别是骨关节病痛,类风湿关节炎等,与酮洛芬相比有更好的吸收及耐受性,为新一代的非甾体抗炎药[1-2]。温度敏感性水凝胶为水溶性或亲水性的高分子材料,通过一定的化学交联或物理交联形成能感知外界环境温度微小变化,并产生相应物理结构和化学性质的变化[3]。壳聚糖-甘油磷酸钠温敏凝胶系统近年来被广泛应用于医药、生物医学工程等领域[4]。该系统在低温低浓度下以液体形式存在,当环境温度达到临界胶凝温度且温度敏感型凝胶基质浓度达到临界胶凝浓度时迅速发生相突变,在给药部位形成半固体凝胶态,达到局部给药后药物在给药部位滞留时间延长的目的[5]。目前市售的右旋酮洛芬氨丁三醇普通制剂,存在半衰期短,给药频繁,胃肠道不良反应大等缺点,基于此笔者研制了通过局部(关节腔或皮下)注射给药,避免胃肠道刺激及减少给药次数的温敏凝胶制剂,并考察其体外释药行为及释药机制,以期为骨关节炎、癌痛患者的临床治疗及药物控缓释制剂的进一步研究奠定基础。
1 材料
UV-2401PC型紫外分光光度计(日本岛津公司);THZ-82型水浴恒温振荡器(金坛市汉康电子有限公司);pHs-3C型酸度计(上海精密科学仪器有限公司);S10-3型恒温磁力搅拌器(上海司乐仪器有限公司);CQ-250A型超声波清洗机(上海跃进医用光学器械厂);CS501A型恒温槽(重庆银河试验仪器有限公司)。
右旋酮洛芬氨丁三醇(纯度:99.8%,武汉远成共创科技有限公司,批号20110301);右旋酮洛芬氨丁三醇片(葵拉兰,湖北安联药业有限公司,批号120703)。壳聚糖(CS,批号20120117,脱乙酰度:95%,青岛海普生物技术有限公司);β-甘油磷酸钠(β-GP,批号 1141M077V,美国 Sigma公司);注射用右旋酮洛芬氨丁三醇温敏凝胶(贵阳医学院药学院贵州省药物制剂重点实验室,批号20121201,20121202,20121203,规格:0.25%);其余试剂均为国产分析纯。
2 方法与结果
2.1 温敏凝胶的制备[6](1)空白凝胶的制备:配制2%CS溶液(0.1 mol·L-1醋酸溶解),真空抽滤,放置于4℃冰箱中待用。配制56% 的β-GP溶液(0.02 mol·L-1氢氧化钠溶解),置超声波清洗机(100功率,6 min)完全溶解后待用。取适量β-GP溶液,缓慢滴加到置于冰浴中的CS溶液内,同时用恒温磁力搅拌器(1 000 r·min-1,10 min)搅拌均匀,即得均匀透明溶液,并密封置于4℃冰箱中冷藏备用。(2)含药凝胶的制备:精密称取一定量的右旋酮洛芬氨丁三醇置量瓶中,注射用水定容至刻度,逐滴加入至已配制并置于冰浴中的β-GP/CS混合溶液内,磁力搅拌器(1 000 r·min-1,10 min)搅拌均匀,用0.02 mol·L-1氢氧化钠溶液调节至pH7.4,放于4℃冰箱中冷藏备用。制得含有右旋酮洛芬氨丁三醇模型药的载药水凝胶。
2.1.1 胶凝过程的测定 采用试管倒装法[7]来判断凝胶的转变。如图1所示,制备的温敏凝胶在低温时,呈均匀、流动的液体状态(A),当温度升高至37℃左右时发生胶凝转变,先在表面形成一层白色薄膜,再逐渐相变为乳白半透明固体凝胶(B)。

图1 温敏性凝胶的胶凝过程Fig 1 The process of gelation of thermosensitive hydrogel
2.1.2 温敏凝胶制剂的处方设计与优化 通过前期预试验,以凝胶化时间、凝胶固化成型性为指标对空白凝胶进行处方初步筛选,并在此基础上以凝胶的体外累积释放度为单因素考察指标。以CS、β-GP为原料制备温敏凝胶载体,对CS脱乙酰度、β-GP/CS溶液配比进行考察,筛选出胶凝温度接近37℃、pH7.4时胶凝时间较短固化成型性较好的方案,即CS脱乙酰度为95%,β-GP/CS溶液配比为1∶2。
2.1.3 温敏凝胶处方筛选 通过“2.1.2”项下单因素考察得知:药物水溶液的浓度(A)、CS用量(B)、β-GP/CS溶液配比(C),对凝胶的体外累积释放度有较大影响。因此,将其作为3个影响因素进行3水平的L9(33)正交试验,以确定最优处方组成。参照中国药典2010年版二部附录XIXD缓控释制剂指导原则[8]的规定,采用综合评分法,设定2 h,4 d,8 d的累积释放度分别以10%,50%,80%为理想值,权重系数定为1,以q2 h,q4 d,q8 d与理想值偏差之和(Y)为评价指标,即Y=|Q2h-10%|×1+|Q4d-50%|×1+|Q8d-80%|×1,以Y值越小越好,表明释放度与所定标准越接近[9]。具体因素水平和结果见表1,表2。
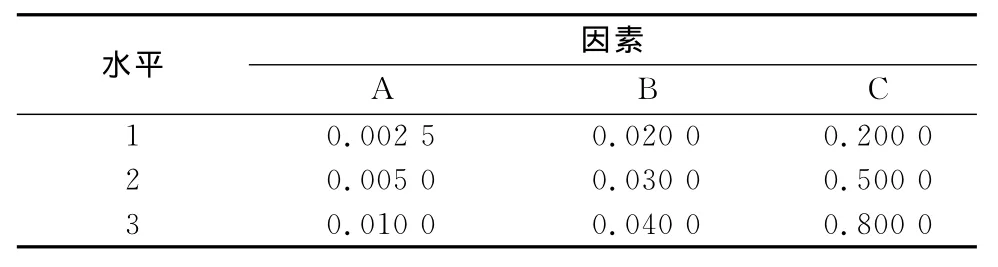
表1 正交因素水平试验表Tab 1 The factors and levels of orthogonal experiment

表2 正交试验结果(n=6)Tab 2 Results of the orthogonal design(n=6)
将上述结果用SPSS统计软件进行分析,结果见表3、表4。
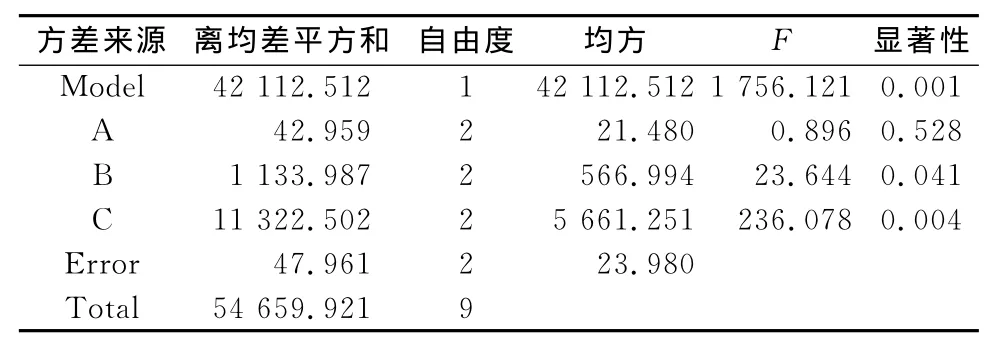
表3 正交试验方差分析结果Tab 3 Results of analysis of variance on orthogonal test
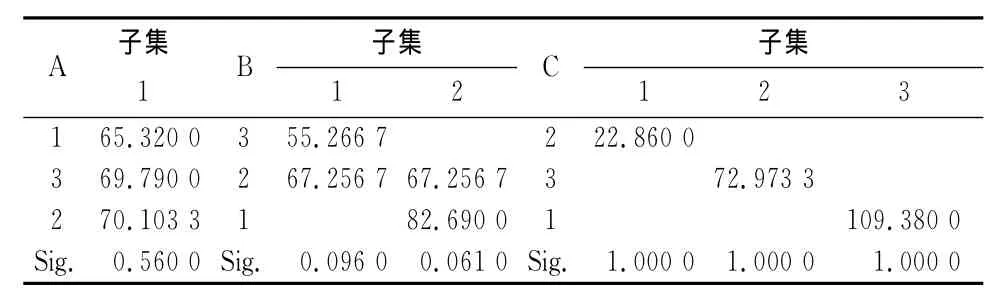
表4 一致性子集表分析结果Tab 4 Results of analysis on consistent subset table
通过上述方差分析得出:B、C两因素具有显著性差异,且各因素对指标影响的大小次序为C>B>A;并结合一致性子集表分析,优选得到的处方组成为:A1B3C2。即药物水溶液浓度为0.002 5 g·mL-1,CS用量为0.04 g,β-GP/CS溶液配比为1∶2。
2.2 体外释放度考察
2.2.1 波长的选择 精密称取右旋酮洛芬氨丁三醇对照品,加纯化水超声溶解,稀释为适当浓度的溶液;按处方比例称取辅料,照上述方法溶解并稀释,超声5 min后,用0.8μm微孔滤膜滤过,取滤液,以纯化水为空白对照,在200~400 nm范围内进行紫外扫描,结果表明本品在260 nm处有最大吸收波长,且辅料在此波长下无干扰。
2.2.2 标准曲线的制备 精密称取右旋酮洛芬氨丁三醇0.021 3 g,置100 mL量瓶中,并用纯化水稀释超声溶解至刻度,作为母液。分别量取母液3,2.5,2,1.5,1,0.5,0.2 mL置25 mL量瓶中,稀释至刻度后,以纯化水为空白对照,在260 nm处测定其吸收度(A),以浓度(C)对吸收度(A)作线性回归,得回归方程式:A=0.043 3C+0.008 4,r=0.999 9,结果表明本品在1.70~25.56μg·mL-1范围内线性关系良好。
2.2.3 精密度试验 取“2.2.2”项下3个浓度的溶液,于260 nm波长处测定其吸收度(A),24 h内重复进样5次,计算其日内精密度;连续测定5 d,计算其日间精密度。
结果表明:该方法的日内、日间精密度良好,所得峰面积RSD均小于2%,符合样品测定要求。
2.2.4 加样回收率试验 按比例加入空白辅料,配制成右旋酮洛芬氨丁三醇浓度分别为完全溶出时的80%,100%,120%的右旋酮洛芬氨丁三醇溶液,测定其吸收度(A),代入标准曲线计算浓度,以测得量对加入量计算回收率。结果表明,本处方辅料不影响右旋酮洛芬氨丁三醇的测定,回收率在99.8%~100.6%之间,RSD<1%,符合测定要求。
2.2.5 释放度的测定方法[6]按“2.1”项下制备3批样品(批号20121201,20121202,20121203,规格:0.25%)放置于玻璃试管内,于水浴恒温振荡器中预热,完全形成凝胶后,加入10 mL的磷酸盐缓冲液(PBS,pH7.4)为溶出介质,转速为100 r·min-1,温度(37±0.5)℃,分别于1,2,4,8,12,24,48,72,96,120,144,168,192,216,240,288 h倾尽溶出介质,以0.8μm的微孔滤膜过滤,精密量取续滤液50μL置5 mL量瓶中,加水稀释并定容,作为供试品溶液;同时补加等温等体积的新鲜PBS溶液。用紫外分光光度法测定吸收度,并计算其累积释放度。
2.3 样品含量测定 取3批温敏凝胶样品,按“2.2”项下的方法测定右旋酮洛芬氨丁三醇的含量。结果,3批样品中右旋酮洛芬氨丁三醇的标示含量分别为98.65%,98.89%,99.90%(n=3),平均标示含量为99.15%。
2.4 温敏凝胶的制备工艺验证 用“2.2.5”项下的3批样品,分别测定其累积释放度。结果见图2。如图所示3批样品各批次间差异较小,工艺重复性良好,含量、溶出较均一。结果显示制备的温敏凝胶在第7天释放量即达到70%以上并可持续释放至12 d以上,证明本品在体外有很好的缓释效果。参照中国药典2010年版二部附录XIXD缓控释制剂指导原则[8]的规定,制定本品的释药范围1,2 h,4,8 d的释放度分别为1%~6%,7%~10%,50%~60%和75%以上,均符合规定。
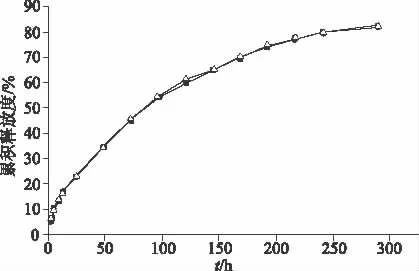
图2 3批样品体外的释放曲线Fig 2 Cumulative release profiles of three batches of dexketoprofen trometamol sustained-release tablets
2.5 温敏凝胶与市售片剂的对比 将优化处方后制得的温敏凝胶与普通市售片剂(葵拉兰)进行体外释药对比,结果见图3。如图所示,温敏凝胶比葵拉兰更具有明显的缓释效果。
2.6 释药机制的研究分析[10]累积释放度按下式计算:F=Q+Mt/M∞,F为0~t时间内右旋酮洛芬氨丁三醇的表观释放率 (%),Q为右旋酮洛芬氨丁三醇的溶出度(%),Mt/M∞为t时间右旋酮洛芬氨丁三醇累积释放百分率(%)[11]。将优化处方分别利用 Higuchi模型、Ritger-Peppas模型、Hixson-Crowell模型、零级方程、一级方程等释药模型对0~12 d的释药行为进行拟合。结果见表5。
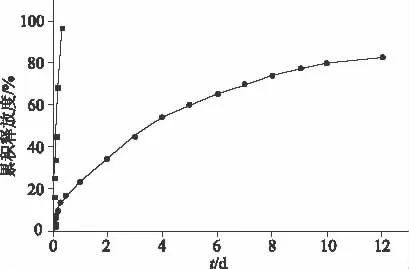
图3 水凝胶与葵拉兰的体外释放曲线Fig 3 Cumulative release profiles of dexketoprofen trometamol hydrogels and dexketoprofen trometamol tablets

表5 右旋酮洛芬氨丁三醇体外释放模型拟合Tab 5 Dexketoprofen tromethamine in vitro released in various models
通过上表的拟合分析结果得知:右旋酮洛芬氨丁三醇温敏凝胶的释药特性用Ritger-Peppas方程拟合较好,并且释放指数n介于0.5~1.0之间,接近0.5,说明该制剂的释药机制为扩散和溶蚀的协同作用,主要以扩散为主[12]。
3 讨论
在实验中,由于CS必须酸化后才能变为阳离子聚合物与带负电的β-GP结合,而CS溶解在不同的酸性物质后又会影响到载药凝胶最终的体外累积释放度。在前期研究中分别考察CS在磷酸、盐酸、醋酸中的载药释放度,发现CS在醋酸中的释放性能较好,在磷酸中稍差。在测定凝胶温度时,升温的速率及搅拌子的大小、转速的快慢、热传导的均匀程度都会影响到结果的重复性,因此实验中所有样品的操作均应在恒定的条件中进行。本研究采用恒温振荡法进行释放度实验时,发现释药的速率会随着振荡频率的加快增加,但彼此间的释药特性基本相同,为了能更好地模拟体内复杂的内环境选用100 r·min-1的频率。
我们以CS、β-GP为凝胶载体,研制了具有缓释性能的可局部注射用的温敏凝胶,采用正交设计优化的处方工艺制备3批温敏凝胶,体外累计释放重复性及均一性均良好,说明本制剂制备工艺稳定、重复性好。并且,释放度的测定符合漏槽条件。本品与市售片剂“葵拉兰”进行体外释药对比研究,证明温敏凝胶更具有缓释的特性。实验累积释放度结果通过数学模型拟合,发现本制剂的释药行为符合Ritger-Peppa方程,为扩散和溶蚀的协同作用,这可能是凝胶基质、原料药及处方工艺对它的影响。
β-GP/CS温敏凝胶体系是一类对环境温度刺激具有较高响应的高分子材料,亦是一种新型的给药传递系统[13]。本实验将右旋酮洛芬氨丁三醇与凝胶均匀混合后制成一种在体外(温度低于36℃)时呈液态,而在体内(温度37±0.5℃)时呈固态的载药凝胶。该制剂不仅可以准确定位于病发部位,使药物通过注射到达人体病变部位,发挥靶向制剂的作用,而且还可维持体内的血药浓度,降低不良反应,减少给药次数和血药浓度的波动,使其发挥缓释和局部起效的作用,尤其是对关节及癌痛部位的给药起到长时间治疗的效果[14-15]。并且,该制剂还具有高效、长效等特点,将拥有广阔的临床应用前景。
[1]Barbanoj MJ,Antonijoan RM,Gich I.Clinical pharmacokinetics of dexketoprofen.[J].Clin Pharmacokinet,2001,40(4):245-262.
[2]杨晓燕,龚培力,沈霖,等.右旋酮洛芬氨丁三醇和酮洛芬双盲对照治疗类风湿关节炎[J].中国新药杂志,2003,12(4)291-295.
[3]郝堂娜,李镇,乔明曦,等.多西他赛皮下注射缓释凝胶的制备及其体外释放行为研究[J].中国药学杂志,2009,44(24):1882-1887.
[4]Chenite A,Chaput C,Wang D,etal.Novel injectable neutral solutions of chitosan from biodegradable gels in situ[J].Biomaterials,2000,21:2155.
[5]章永望,赵会英,张娜.新型可注射温敏水凝胶的制备及其释药性能[J].北京化工大学学报,2007,34(5):535-539.
[6]陈敏燕,吴飞华,潘九英.可注射美洛昔康温敏凝胶的研制[J].中国药房,2010,21(21):1991-1993.
[7]Tang YF,Du M,Hu XW,etal.Rheological characterization of a novel thermosensitive chitosan/poly(vinyl alcohol)blend hydrogel[J].Carbohydrate Polymers,2007,67:491-499.
[8]中国药典.二部[S].2010:附录176.
[9]张洁,石凌云,郑林,等.右旋酮洛芬氨丁三醇速释缓释双层片的研制及其体外释放特性[J].中国医院药学杂志,2013,33(9):680-684.
[10]顼佳音,熊欣,陈燕军.可注射参麦温度敏感型原位凝胶的制剂学评价[J].中国实验方剂学,2012,18(13):60-64.
[11]夏景辉,刘吕孝.固体药物制剂的体外溶出度的统计学评价分析[J].中国药学杂志,2000,35(2):130.
[12]杨辰锴,李万玉,王丽娟,等.盐酸左氧氟沙星用温敏凝胶的制备及滞留性考察[J].中国新药杂志,2011,32(19):1520.
[13]郭启雷.温敏水凝胶在智能给药系统中的应用[J].国外医药(合成药-生化药-制剂)分册,2002,23(1):41-44.
[14]Jones MN.Carbohydrate-mediated liposomal targeting and drug-delivery[J].Adv Drug Deliv-res,1994,3(3):215-249.
[15]Yan,H.Tsujii,K.Potential applieation of Poly(N-isopropylaerylamide)gel eontaining polymeric mieelles to drug delivery systems[J].Colloids and surfaces B:Biointerfaces,2005,46(3):142-146.
