吸附材料处理含Zn2+重金属废水的影响因素
2012-12-28董颖博
林 海,杨 扬,董颖博
(北京科技大学 土木与环境工程学院,北京 100083)
吸附材料处理含Zn2+重金属废水的影响因素
林 海,杨 扬,董颖博
(北京科技大学 土木与环境工程学院,北京 100083)
考察了废水初始pH值、不同阳离子、阴离子、有机物、共存重金属离子、极端条件等因素对吸附Zn2+的影响.结果表明,8 h后吸附接近饱和,废水初始 pH=6时处理效果最好,Zn2+吸附容量为3.98 mg/g,去除率为79.6%;Na+、K+、Mg2+、Ca2+均会抑制Zn2+的吸附,影响顺序从小到大为Na+<K+<Mg2+<Ca2+;Cl-、对吸附Zn2+抑制作用很小,且Cl-的抑制作用小于;COD对吸附Zn2+有促进作用;Pb2+、Cu2+共存时,对Zn2+的吸附有抑制作用,影响顺序为Pb2+单元体系<Cu2+单元体系<Pb2+、Cu2+二元体系;高盐和强酸对Zn2+的吸附有较大影响,但高温基本无影响.饱和吸附材料的后处理试验表明,在550℃马弗炉中热处理6.5 h,烧失率为75.4%,烧渣中Zn2+含量为1.75%,与热处理前相比,富集倍数为4.1倍.本文研究成果为吸附法处理含锌重金属废水并回收废水中的重金属提供了重要依据.
重金属污水处理;锌离子;吸附材料;影响因素;回收重金属
重金属废水已经成为威胁人类发展的重大环境问题之一[1],其主要来源于电镀、矿山、冶金等工业企业。锌是电镀行业使用最多的金属之一,约占50%.含锌废水的危害很大,锌对鱼类和其他水生生物也会造成很大毒性.用含锌废水灌溉农田,会造成小麦出苗不齐,分蘖少,植株矮小,叶片萎黄.过量的锌还会使土壤失去活性,细菌数减少,土壤中的微生物作用减弱[2].目前对重金属废水的主要处理方法有:中和沉淀法、铁氧体法、絮凝沉淀法、离子交换法、膜分离技术等.这些方法存在投资大、运行成本高、操作管理不便、并且会产生二次污染和不能很好地解决金属和水资源再利用等问题.吸附法因其材料易得、成本低、去除效果好且不会产生二次污染,一直受到人们的青睐.近年来科研工作者在这方面的研究主要集中在开发更为廉价、高效的吸附材料[3].本文所用吸附材料具有能吸附多种重金属、适应浓度广泛、可有效回收重金属等优点,主要研究了该吸附材料处理含锌重金属废水的影响因素,分别考察了溶液初始pH值、各种阴阳离子、有机物、共存重金属离子、极端条件等因素对其吸附锌的影响,并研究了饱和吸附材料的后处理,研究成果可为吸附法处理矿山、电镀工业含锌重金属废水提供依据.
1 材料和方法
1.1 主要试剂与仪器
实验试剂主要有:六水合硝酸锌、氯化钠、氯化钾、氯化镁、氯化钙、乙基钠黄药、氢氧化钠、盐酸、硝酸铅、三水合硝酸铜.
实验仪器主要有:HZQ-F160全温振荡培养箱、DELTA 320 pH计、VIS-723N可见分光光度计、AB104-N分析天平、DHG-9053A电热恒温鼓风干燥箱、WRT-2C微机热天平(北京光学仪器厂).
1.2 实验材料
实验所用材料为挪威某公司研发生产的一种新型有机吸附材料(外观如图1所示),它以植物为主要原料,通过一系列工艺加工而成.其性能指标如表1所示.

图1 吸附材料外观照片Fig.1 Picture of the adsorbent material
1.3 实验方法
配制含Zn2+为50 mg/L的废水,取配制好的废水200 mL置于300 mL的锥形瓶中,分别用0.1 mol/L的HCl和0.1 mol/L的NaOH调节废水pH值,称取2 g吸附材料投加其中,放入全温振荡培养箱中振荡24 h,静置后,过滤,取上清液测定Zn2+的浓度,并计算吸附容量.

表1 吸附材料的性能指标Table 1 Performance characteristics of the adsorbent material
1.4 分析方法
重金属Zn2+的测定采用二甲酚橙比色法测定.评价指标为剩余重金属离子含量、吸附容量和吸附容量变化的百分率.
剩余重金属离子含量ρ(mg/L)计算公式为:

式中:m为试样测得含重金属离子质量,μg;V为测定用试样体积,mL.
吸附容量qp(mg/g)按照下式计算:
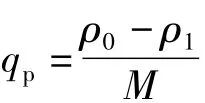
式中:ρ1为吸附平衡重金属离子的质量浓度,mg/L;ρ0为初始重金属离子的质量浓度,mg/L;M为每L废水中吸附材料投加量,g.
吸附容量变化的百分率以C(%)表示,按照下式计算:
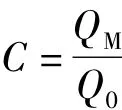
式中:C为吸附量的变化百分率,%;QM为加入干扰离子后的吸附容量,mg/g;Q0为未加入干扰离子的吸附容量,mg/g.
2 结果与讨论
2.1 pH对吸附Zn2+的影响
pH是重金属吸附的主要影响因子.图2为不同pH对吸附Zn2+的影响结果,可以看出,8 h以后,曲线趋于平缓,说明吸附达到了饱和,因此吸附饱和时间可确定为8 h.pH对吸附的影响较为明显,随着pH的升高,吸附容量逐渐增大,这是因为在pH较低时,H+浓度较大,H+会和Zn2+发生竞争吸附,使吸附材料吸附了部分H+,则其对Zn2+的吸附量明显减小[4].pH=6时,吸附容量最大,处理效果最好,吸附容量达到3.98 mg/g,溶液中剩余 Zn2+浓度为10.2 mg/L,去除率达79.6% .pH大于6时,可使Zn2+产生沉淀.

图2 pH对吸附Zn2+的影响Fig.2 pH effect of on adsorption of Zn2+
2.2 不同阴、阳离子对吸附Zn2+的影响
重金属废水中通常含有多种阳离子和阴离子,这些阴阳离子的存在可能会影响吸附处理效果[5],因此研究阴阳离子对吸附材料处理重金属废水的影响具有重要意义.分别配制Na+、K+、Mg2+、Ca2+质量浓度为0~8 000 mg/L的含Zn2+废水进行吸附实验,测定Zn2+浓度,并计算吸附容量.

图3 不同阳离子对吸附Zn2+的影响Fig.3 Effect of different ions on adsorption of Zn2+
图3为不同阳离子对吸附材料吸附Zn2+的影响,结果表明,阳离子的存在均对吸附产生抑制作用,但是不同的离子影响大小不同,4种离子对吸附重金属Zn2+的影响与离子浓度及离子种类有关.随着浓度的增加,4种阳离子对吸附Zn2+的抑制作用增强,且 Na+和 K+的影响要远小于Ca2+和Mg2+的影响.4种阳离子对吸附的影响顺序为Na+<K+<Mg2+<Ca2+.这种影响可能与阳离子的价态有关,二价的阳离子的影响要大于一价的阳离子的影响,这表明价态越高,对吸附的影响越大,这与Deng[6]等的研究结果一致.
图4为不同浓度Cl-、对吸附材料吸附Zn2+的影响结果.可以看出,Cl-和对吸附Zn2+均有抑制作用,但是影响较小,且Cl-的影响小于的影响.

图4 不同阴离子对吸附Zn2+的影响Fig.4 Effect of different anions on adsorption of Zn2+
2.3 有机物对吸附Zn2+的影响
重金属废水中含有有机污染物质(矿山废水中主要由黄药产生)可能会对吸附处理效果有一定的影响[7],因此研究有机物对吸附材料处理重金属废水的影响是十分必要的.试验中COD模拟废水由乙基钠黄药配制而成,图5为不同COD浓度对吸附材料吸附Zn2+的影响结果.
结果表明,随着COD浓度的增加,吸附材料对Zn2+吸附容量逐渐增大,COD浓度由0 mg/L增加到400 mg/L时,吸附容量由3.968增大到4.739,溶液中残留的Zn2+浓度由10.32 mg/L下降到2.61 mg/L,由此说明,乙基钠黄药的存在对吸附Zn2+有促进作用,分析原因可能是由于乙基钠黄药与Zn2+络合,从而使其更容易被吸附.
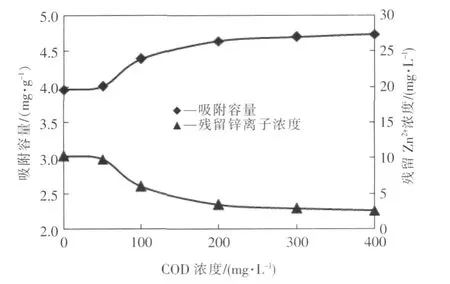
图5 有机物对吸附Zn2+的影响Fig.5 Effect of organic on adsorption of Zn2+
2.4 共存重金属离子对吸附Zn2+的影响
图6是Pb2+单元体系、Cu2+单元体系以及Pb2+、Cu2+二元体系对吸附材料吸附Zn2+的影响曲线.由图可以看出,Cu2+和Pb2+的存在均对吸附Zn2+有抑制作用,影响大小顺序为Pb2+单元体系<Cu2+单元体系<Cu2+、Pb2+二元体系.在单元体系中,Pb2+的影响较Cu2+的影响稍小,原因可能与离子半径有关[5],离子半径越小越容易被吸附,Pb2+、Cu2+的半径分别为121 nm、73 nm[8],Pb2+的半径大于Cu2+的半径,因此影响较小.二元体系的影响要大于单元体系,原因是二元体系中,Cu2+和Pb2+同时与Zn2+竞争吸附,故影响要大于单元体系.

图6 共存重金属离子对吸附Zn2+的影响Fig.6 Effect of coexisting metallic ions on adsorption of Zn2+
2.5 极端条件对吸附Zn2+的影响
实际废水中,通常存在强酸、高温、高盐的极端条件,可能会对吸附处理效果有影响[9,10],因此,研究强酸、高温、高盐对吸附的影响对实际重金属废水的处理意义重大.图7、图8、图9分别为高盐、强酸、高温对吸附材料吸附 Zn2+的影响结果.
由图7可以看出,随着盐度的升高,吸附材料对Zn2+的吸附容量逐渐下降,盐度由20 g/L升高到100 g/L时,吸附容量由3.033 mg/g下降到0.931 mg/g.溶液中残留Zn2+浓度由19.67 mg/L升高到40.69 mg/L,影响较为显著,由此可以得到高盐条件对吸附材料吸附Zn2+有抑制作用,且影响较大,分析原因可能是高浓度的Na+与Zn2+竞争吸附从而使Zn2+的吸附容量降低.
由图8可以看出,当pH=2时,吸附容量为1.471 mg/g,而 pH=0.5时,吸附容量降至0.417 mg/g,溶液中残留Zn2+浓度由35.29 mg/L升高至45.83 mg/L,Zn2+去除率由29.4%降至8.3%,由此可见,强酸对吸附Zn2+的影响极大.pH过低时,溶液中大量的H+会与Zn2+发生竞争吸附,从而使吸附材料对Zn2+的吸附容量显著减小,去除率降低.同时pH过低可能破坏吸附材料的结构从而导致吸附Zn2+的性能降低.
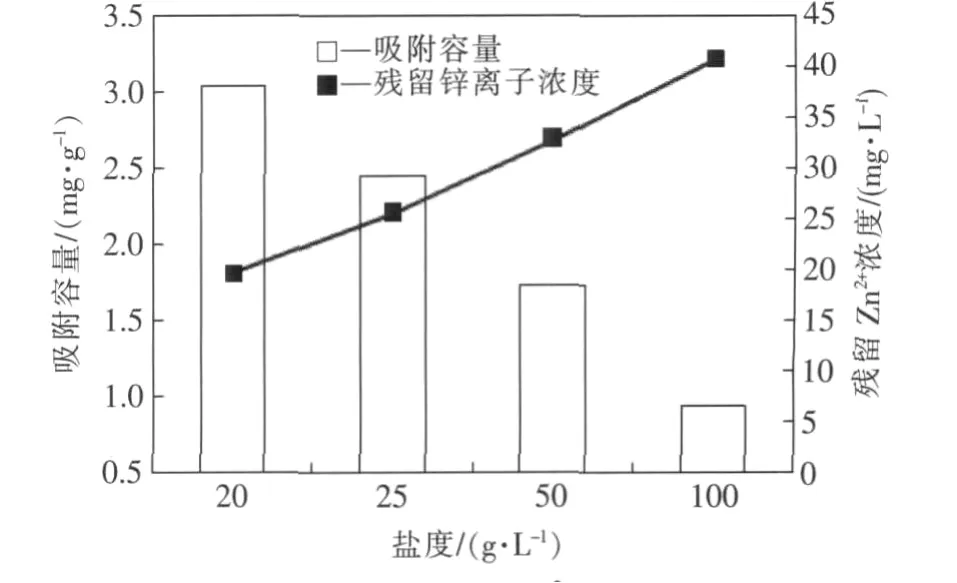
图7 高盐对吸附Zn2+的影响Fig.7 Effect of hyperhaline condition on adsorption of Zn2+
图9的结果表明,随着温度的升高,吸附材料对Zn2+的吸附容量变化很小,溶液中Zn2+浓度基本无变化,均在10.3 mg/L左右,去除率均在79.3%左右,由此可以得出,高温对吸附Zn2+基本无影响,说明该吸附材料耐高温性能比较好.

2.6 热重(TG)分析
分别对吸附Zn2+前后的吸附材料进行热重(TG)分析,结果如图10和图11所示.
图10为吸附前吸附材料在空气中的TG曲线,起始温度为 21℃,材料起始质量约为34.3 mg,在空气中,从21~170℃之间发生一个失重现象,失重量大约占试样初始总质量的10.2%,估计这段主要是脱水失重[11].170~210℃质量基本不变,210~500℃之间是失重的主要阶段,失重量大约占试样初始总量的56.9%,从500℃开始往后,试样质量变化缓慢,从500~1 000℃之间,质量减少为2.7 mg,仅为试样初始总质量的7.8%.
图11为吸附Zn2+后的吸附材料在空气中的TG曲线,由图可以看出,总共有两个阶段的失重过程.起始温度为24℃,材料的起始质量约为67.6 mg,在空气中,在24~150℃之间发生一个明显的失重现象,质量减少大约占试样初始总质量的41.3%,接着是从150~230℃的一个质量量基本不变的平台过程,第一步失重结束后,第二步的失重过程从230℃开始发生,从230~500℃之间,质量减少大约占试样初始总质量的38.8%,从500℃开始,质量基本不变.
综上所述,500℃以后材料质量变化很缓慢,故选择550℃进行饱和吸附材料的后处理实验.取一定量的吸附Zn2+的吸附材料置于坩埚中,在550℃的马弗炉中处理6.5 h,得出吸附Zn2+的饱和吸附材料的烧失率为75.4%.重金属的含量为1.75%,即17.5 mg/g,与热处理之前相比,富集倍数为4.1倍.由此可以说明,该吸附材料处理重金属废水后可以通过焙烧的方式回收重金属.吸附饱和后材料焙烧过程中有机物转化为CO2和H2O以及少量的氮氧化物,所剩残渣主要为吸附材料中所含的少量无机物以及回收的重金属锌的氧化物,这些残渣可通过冶炼回收其中的锌,从而达到回收废水中重金属同时减少对环境危害的目的.

图10 吸附材料的TG曲线Fig.10 TG curve of the adsorbent material
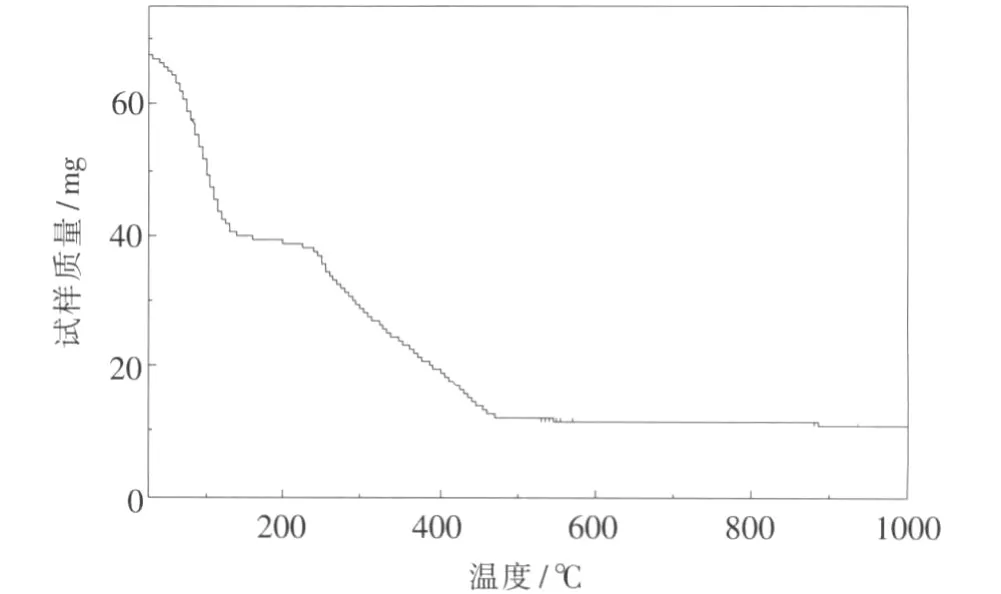
图11 吸附Zn2+后的吸附材料的TG曲线Fig.11 TG curve of the material adsorbing Zn2+
3 结论
(1)吸附材料对Zn2+的吸附容量随pH的增大而增加,吸附的最佳pH为6,吸附容量达到3.98 mg/g,溶液中残留Zn2+浓度为10.2 mg/L,去除率为79.6%.
(2)阳离子的存在对吸附Zn2+有一定的抑制作用,四种阳离子对Zn2+的吸附影响顺序为Na+<K+<Mg2+<Ca2+.与阳离子相比,阴离子的影响较小,影响顺序为Cl-<.
(3)重金属离子共存对Zn2+的吸附存在抑制作用,Cu2+和Pb2+的存在对Zn2+吸附的影响顺序为Pb2+一元体系<Cu2+一元体系<Cu2+、Pb2+二元体系.
(4)强酸和高盐条件对吸附Zn2+的影响非常明显,而高温对吸附基本无影响.
(5)饱和吸附材料的后处理采用热处理方法.吸附Zn2+的材料在马弗炉中热处理6.5 h后的烧失率为75.4%,含量为1.75%,与热处理之前的吸附材料相比,重金属的富集倍数为4.1倍.故该吸附材料处理重金属废水后可以通过焙烧的方式回收重金属.
[1]梅光泉.重金属废水的危害及治理[J].微量元素与健康研究,2004,8(4):54-56.
(Mei Guangquan.Harmfulness and treatment of heavy metal waste waster[J].Studies of Trace Elements and Health,2004,8(4):54-56.)
[2]贾金平,谢少艾,陈虹锦.电镀废水处理技术及工程实例[M].北京:化学工业出版社,2003.
(Jia Jinping, Xie Shaoai, Chen Hongjin. Treatment technologies and project examples of electroplating wastewater[M].Beijing:Chemical Industry Press,2003.)
[3]孙海燕.吸附法在处理重金属废水中的研究进展[J].高校理科研究,100-101.
(Sun Haiyan.Study progress of heavymetal wastewater trement by adsorption method[J].University Science Reserch,100-101.)
[4]王春丽,王中琪.蛭石处理含Cu2+和Zn2+废水的性能研究[J].广东化工,2009,36(3):57-59.
(Wang Chunli,Wang Zhongqi.Study on the treatment of Cu2+and Zn2+wastewater by vermiculite[J].Guang Dong Chemical,2009,36(3):57-59.)
[5]昝逢宇,霍守亮,席北斗,等.啤酒酵母吸附去除水中Cd2+的影响因素[J].化工进展,2010,29(2):365-369.
(Zan Fengyu,Huo Shouliang,Xi Beidou,et al.Influence factors for the biosorption of Cd2+by saccharomyces cerevisiae[J].Chemical industry and engineering progress,2010,29 (2):365-369.)
[6]Deng L P,Zhu X B,Su Y Y,et al.Biosorption and desorption of Cd2+from wastewater by dehydrated shreds of cladophora fascicularis[J].Chinese Journal of Oceanology and Limnology,2008,26(1):45-49.
[7]《电镀行业污染物排放标准》编制组.电镀行业主要污染物情况分析[J].涂料涂装与电镀,2006,8,4(4):42-46.
(The edit group of“The discharge standard for pollutants from electroplating industry.”situation analysis of main pollutants in electroplating industry[J].Coatings painting&electroplating,2006,8,4(4):42-46.)
[8]李梦龙主编.化学数据速查手册[M].北京:化学工业出社,2003:9-12,136-149.
(Li Menglong.Chemical data quick reference[M].Beijing: Chemical Industry Press,2003:9-12,136-149.)
[9]骆昌运.锌冶金废水综合治理实践[J].有色金属,2005,4:10-12.
(Luo Changyun.Plant practice on comprehensive harnessing waster water of zinc hydrometallurgy[J].Nonferrous Metals,2005,4:10-12.)
[10]鞠海燕,黄春文,罗文海,等.金属矿山酸性废水危害及治理技术的现状与对策[J].中国钨业,2008,23(2):1-44.
(Ju Haiyan,Huang Chunwen,Luo Wenhai,et al.The damage and treatmenttechniquesofmetalminesacid wastewater[J].China Tungsten Industry,2008,23(2):1-44.)
[11]施海云,王树荣,方梦祥,等.典型火灾可燃物生物质热失重特性比较研究[J].消防科学与技术,2005,24(1):9-14.
(Shi Haiyun,Wang Shurong,Fang Mengxiang,et al.Comparatively kinetic study on the pyrolysis of fire combustibe biomass[J].Fire Science and Technology,2005,24(1):9-14.)
Influence factors of adsorbent material dealing with Zn2+
LIN Hai,YANG Yang,DONG Ying-bo
(Civil&Environment Engineering School,University of Science&Technology,Beijing 100083,China)
Taking a new adsorbent material as the object of study,some influence factors for adsorption of Zn2+are discussed.Results indicate that the adsorption process approaches to saturation after 8 h.The processing effect is best at pH value of 6.The maximum loading capacity of Zn2+is 3.98 mg/g and the elimination ratio of Zn2+reaches 79.6%.The ions Na+,K+,Mg2+and Ca2+have negative impact on the adsorption of Zn2+.The influence order of cations is Na+<K+<Mg2+<Ca2+.The influence of anions is small and the influence order is Cl->.COD has positive impact on the adsorption.The existence of Cu2+and Pb2+has inhibitory effect on the adsorption.The influence order of heavy mental ions on the adsorption of Zn2+is Pb2+single system<Cu2+single system<Pb2+,Cu2+dual system.The strong acid and high salt environment can extremely affect the adsorption of Zn2+,but high temperature has little impact on the adsorption of Zn2+.In the post-processing experiment,the loss ratio of material weight is 75.4%after 6.5 h heat treatment in the muffle furnace at the temperature of 550℃.The Zn2+content in the cinder is1.75%which is4.1 times higher than that before heat treatment.Results of the present paper provide an important basis for the treatment of heavy metal wastewater including Zn2+by adsorption method and the recovery of heavy metal.
treatment of heavy metal wastewater;Zinc ion;adsorbent material;influence factors;heavy metal recovery
TB 34
A
1671-6620(2012)01-0064-06
2011-09-14.
国家自然科学基金资助项目 (No.51174017).
林海 (1966—),男,北京科技大学教授,E-mail:linhai@ces.ustb.edu.cn.
